La nitrofurantoína es un antimicrobiano utilizado en la profilaxis de las infecciones del tracto urinario. Raramente, puede producir toxicidad pulmonar aguda o crónica y generar una neumonitis intersticial que incluso puede evolucionar a fibrosis, además de poder originar toxicidad hepática y otras manifestaciones.
La toxicidad crónica produce una clínica variable y su presentación radiológica obliga a realizar un exhaustivo diagnóstico diferencial dentro de las neumopatías intersticiales. Como primera medida es preciso retirar el fármaco, lo que suele lograr sin medidas coadyuvantes una evolución favorable.
Se presenta el caso de una mujer de 69años que consulta por expectoración crónica y ruidos torácicos, con el antecedente de cistitis de repetición tratadas con nitrofurantoína. La TAC mostró un infiltrado localizado junto a datos de afectación pulmonar intersticial con engrosamiento septal y bronquiectasias de tracción. Asimismo, se hallaron datos de hepatotoxicidad.
Tras la suspensión del antimicrobiano, la paciente evolucionó favorablemente sin que fuera preciso instaurar tratamiento esteroideo.
Nitrofurantoin is an antibacterial agent used in the management of urinary tract infections. It can rarely induce acute or chronic pulmonary toxicity and generate an interstitial pneumonitis which can turn into fibrosis, besides originating hepatic toxicity and other conditions.
Chronic toxicity has a variable clinical expression, and its radiologic presentation forces to carry out a comprehensive differential diagnosis of interstitial lung conditions. The first measure would be the drug withdrawal, which usually ensures favourable evolution without supporting therapeutic measures.
We present the case of a 69 year-old woman who consulted for chronic productive cough and lung sounds, with a history of recurrent cystitis treated with nitrofurantoin. The CT scan showed localized infiltrates together with interstitial lung disease with septal thickening and traction bronchiectasis. Hepatic toxicity data were also found.
After drug withdrawal patient evolved favourably without the need for steroid treatment.
Mujer de 69años de edad, no fumadora, aquejada de síndrome depresivo en tratamiento psicofarmacológico. Toma omeprazol de forma discontinua por pirosis ocasional, sin antecedentes neumológicos previos de interés.
Realiza tratamiento continuo en los últimos 5 meses y previo hace 5 años sin interrupción durante más de 2 años con nitrofurantoína profiláctica, prescrita en urología como consecuencia de cistitis de repetición que le producen un síndrome miccional.
Acude a nuestra consulta refiriendo un cuadro larvado consistente en la presencia de expectoración verdosa escasa, ruidos torácicos nocturnos, disgeusia con sabor amargo persistente, molestias retroesternales y astenia.
En la exploración física la paciente presenta saturación de oxígeno de 95%, frecuencia cardiaca de 125lpm, auscultación cardiaca anodina, auscultación pulmonar: disminución moderada del murmullo vesicular y crepitantes en ambas bases, campo inferior izquierdo y plano anterior derecho. No presenta alteraciones abdominales, en la piel o faneras ni adenopatías. El resto de la exploración es normal.
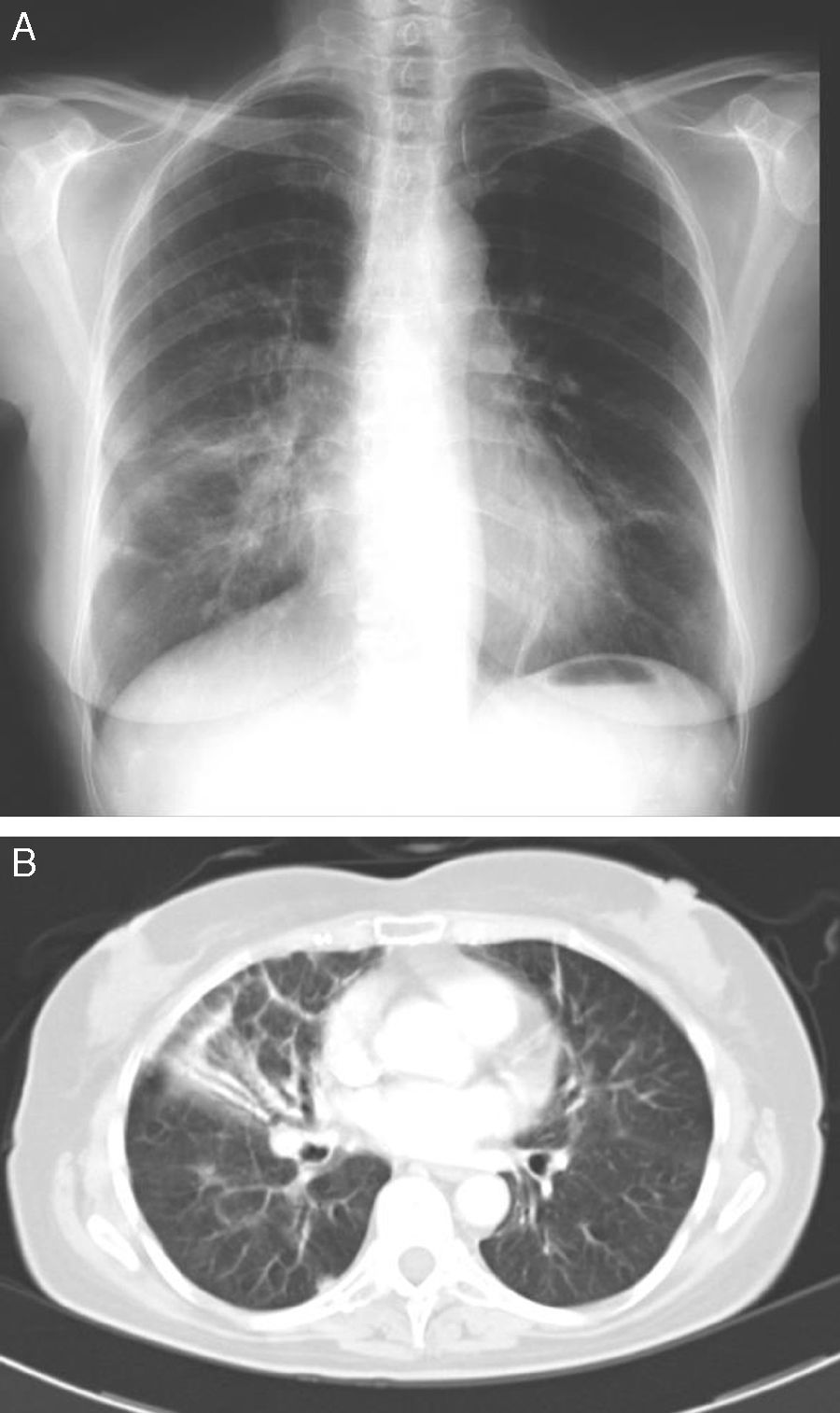
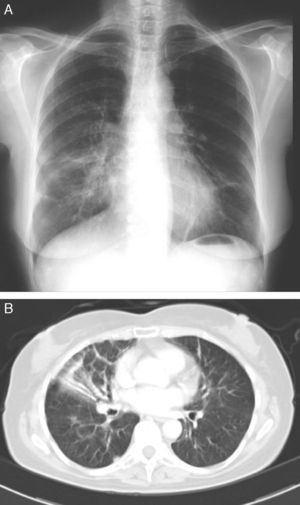
Tras objetivarse en la radiografía de tórax bronquiectasias bilaterales de apariencia cilíndrica, junto con un infiltrado peribronquiectásico en el lóbulo medio (fig. 1A), la paciente ingresa para estudio.
Durante su ingreso a lo largo de 72h se realiza tratamiento broncodilatador mediante anticolinérgicos inhalados y terapia antibiótica con levofloxacino y cefixima, al tiempo que se interrumpe la terapia con nitrofurantoína. Se alcanza la mejoría clínica progresiva durante su hospitalización y después del alta.
Se le practica una TAC torácica (fig. 1B) que demuestra como hallazgo fundamental la presencia de bronquiectasias cilíndricas tanto en el lóbulo medio como en el segmento inferior de la língula, con pérdida de volumen asociada, junto con un infiltrado peribronquiectásico en el primer lóbulo reseñado. Presenta asimismo bronquiectasias de tracción en ambos lóbulos superiores y lóbulo inferior derecho, junto con engrosamiento de los septos interlobulillares en el lóbulo superior derecho y en el lóbulo medio.
En relación con dicha afectación intersticial presente y el síndrome bronquiectásico asociado, la paciente niega historia compatible con reflujo gastroesofágico sintomático persistente, datos de enfermedad inflamatoria intestinal, antecedente de esterilidad, infecciones respiratorias de repetición o sinusitis, artralgias o artropatías; no presenta historia de exposición laboral o ambiental frente a partículas o alergenos ni contacto continuado con animales.
En el estudio funcional pulmonar la paciente sufre una alteración ventilatoria restrictiva leve aparente por espirometría (capacidad vital forzada de 2.110cc, correspondientes a un 74% sobre el teórico).
No hay aislamientos representativos en el cultivo de esputo; solo presenta una determinación positiva para anticuerpos IgG de Mycoplasma pneumoniae en la serología de patógenos respiratorios; la serología para VIH es negativa.
Por último, el estudio de autoinmunidad únicamente mostró un nivel positivo medio (1/320) de anticuerpos antinucleares (ANA) con patrón nucleolar moteado que se atribuye a la antibioterapia crónica, y una discreta elevación del factor reumatoide. No hay alteraciones en la determinación de anti-ADN, ENA, determinación de alfa-1-antitripsina, proteinograma, cuantificación de inmunoglobulinas M, G y A y del complemento. El hemograma muestra una fórmula normal con anemia normocítica leve. La bioquímica muestra datos de citólisis hepática moderada con elevación moderada de la gamma-glutamil-transpeptidasa (aspartato-amino-transferasa 230U/l, alanino-amino-transferasa 245U/l, fosfatasa alcalina 123U/l, gamma-glutamil-transpeptidasa 157U/l).
Tras mantenerse la retirada de la nitrofurantoína y en los controles clínicos practicados a 3 y 6 meses tras el alta, la paciente no vuelve a presentar sintomatología respiratoria, se normalizan las enzimas hepáticas y es reevaluada en Reumatología y Urología. Se descarta la presencia de conectivopatía asociada y se introduce terapia profiláctica con trimetoprim-sulfametoxazol. La tolerancia es adecuada.
Además, se realiza un tránsito gastroesofágico, en el que no se identifica hernia hiatal o reflujo, y una radiografía de senos paranasales que no demuestra alteraciones.
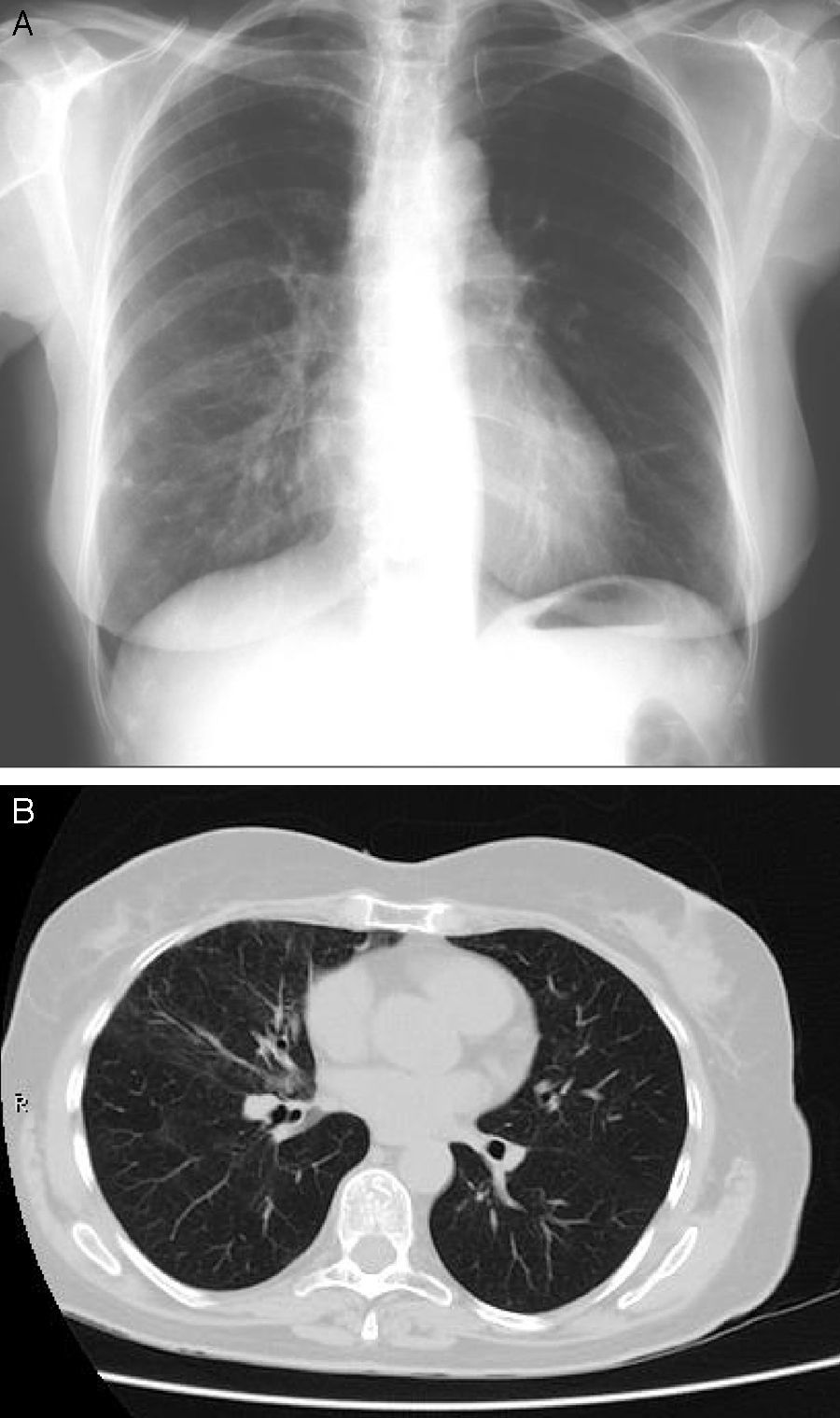
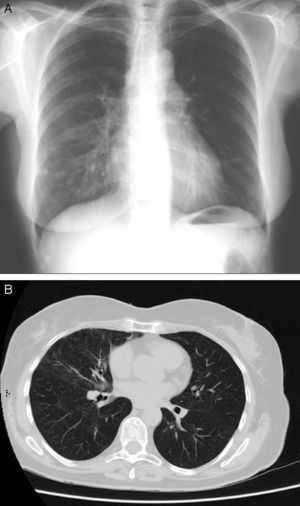
En la radiografía de tórax y en la TAC torácica de alta resolución realizadas a las 6 semanas y al quinto mes de seguimiento sucesivamente (fig. 2) se observa una importante mejoría de la afectación intersticial, con mínimas áreas de vidrio deslustrado y alguna bronquiectasia aislada en el lóbulo medio.
La nitrofurantoína es un antimicrobiano utilizado profusamente en el tratamiento y la profilaxis de las infecciones del tracto urinario recurrentes por su gran eficacia clínica1.
Desde hace años también es conocida la potencial aparición de toxicidad pulmonar aguda2 o crónica3 (con una incidencia menor al 1%) y hepática; la combinación de ambas se considera poco frecuente4. Se ha descrito también la aparición de discrasias sanguíneas y de neuropatía. Estos cuadros presentan un curso generalmente favorable tras la suspensión del fármaco, aunque en algunos casos es obligada la introducción de regímenes de corticoterapia sistémica.
Las manifestaciones pulmonares en la toxicidad por nitrofurantoína son variadas (tabla 1) y pueden aparecer de forma aguda, subaguda o crónica. Sobre todo se presenta como una neumonitis intersticial5. Las formas de afectación pulmonar aguda son más frecuentes y pueden surgir a veces al cabo de pocas horas de la primera exposición al fármaco, aunque normalmente se presentan después de la primera semana. Se genera una afectación por hipersensibilidad y pueden cursar con tos, disnea, fiebre, dolor torácico, taquicardia, artralgias y rash maculopapular.
El estudio radiológico muestra característicamente opacidades reticulares o infiltrados alveolares y puede haber eosinofilia en la sangre o en el lavado broncoalveolar, pero no se considera específica. Puede presentarse también como derrame pleural.
Las pruebas de función pulmonar demuestran un patrón respiratorio restrictivo con disminución de la capacidad de transferencia de monóxido de carbono. Las formas de toxicidad aguda no predisponen a la toxicidad crónica6.
La afectación pulmonar crónica es, sin embargo, menos frecuente; como la aguda, sucede sobre todo en mujeres en la sexta y séptima décadas de la vida. No sigue en su aparición a formas agudas y suele producirse tras cursos de tratamiento de hasta 6 meses e incluso años, como ocurre en nuestro caso. El mecanismo de toxicidad directa es dosis-dependiente. Puede evolucionar hacia una fibrosis pulmonar7. Se suele presentar en forma de tos insidiosa, disnea progresiva y puede asociarse a dolor torácico, pérdida ponderal y mialgias.
Las pruebas de función pulmonar muestran hallazgos similares a los descritos en la forma aguda, compatibles con una afectación intersticial difusa, y en la radiografía de tórax se observa un patrón intersticial bilateral, también ocasionalmente derrame pleural.
La TAC de alta resolución revela la presencia de engrosamiento septal, bronquiectasias de tracción, áreas de vidrio esmerilado e incluso cierto grado de panalización; pueden aparecer también áreas de neumonía organizada.
El hallazgo de eosinofilia es menos frecuente, y no es rara la aparición de una elevación del factor reumatoide, la positividad de anticuerpos antinucleares o la elevación de inmunoglobulinas8. En ocasiones puede llegar a ser necesario recurrir a la realización de biopsia transbronquial o pulmonar para su filiación definitiva.
Por todo ello, los pacientes en tratamiento crónico con nitrofurantoína deben ser monitorizados regularmente en el centro de salud para la detección precoz de una potencial toxicidad por este fármaco, puesto que en algunos casos esta puede llegar a resultar grave y ocasionalmente poner en peligro la vida del paciente, lo que conlleva en muchas ocasiones la necesidad de hospitalización. Es recomendable la realización periódica de radiografía de tórax y analítica, que incluya bioquímica con un perfil hepático.
Como en este caso, deberemos realizar un diagnóstico diferencial para excluir otras causas de afectación intersticial. El fármaco debe ser retirado ante la aparición de tos y/o disnea; su mantenimiento más allá de los 6 meses de tratamiento deber ser cuidadosamente evaluado6.
En los casos en que la suspensión del tratamiento no produzca una mejoría relevante, lo que puede ocurrir más frecuentemente en las formas crónicas, podemos considerar un ciclo de glucocorticoides no prolongado. Con ello se ha reportado una respuesta variable en hasta el 10-30% de los casos; la validez de esta práctica solo es limitada7.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.