de COVID-19, ventilación mecánica invasiva (VMI) y fracaso renal agudo (FRA) con necesidad de terapia continua de reemplazo renal (TCRR) es conocida, pero hay pocos datos publicados sobre el pronóstico a largo plazo de este tipo de FRA.
MétodosEste estudio analiza los resultados a largo plazo de 30 pacientes ingresados en la UCI por neumonía por COVID-19, con VMI y FRA con TCRR en el pico de máxima incidencia. Comparamos las características basales, la evolución clínica y bioquímica y los diferentes filtros usados en la TCRR para identificar los factores de riesgo asociados a la muerte intrahospitalaria. Se analizaron el filtrado glomerular estimado (FGe), la proteinuria y la hematuria a los 6meses de seguimiento de los supervivientes.
ResultadosDe los 30 pacientes, 19 fallecieron y 11 fueron dados de alta. Los pacientes con peor función renal tuvieron mayor mortalidad (p=0,009). Los filtros usados con capacidad adsortiva no ofrecieron beneficios en cuanto a la supervivencia. De los 11 supervivientes, ninguno requirió terapia renal sustitutiva (TRS) una vez superada la infección, pero tuvieron una pérdida importante y mantenida en el tiempo de función renal (FGe de 44ml/min/1,73 m2).
ConclusiónLa mortalidad en pacientes con neumonía por COVID-19 que requieren VMI y TCRR es extremadamente elevada (63%). Los filtros con capacidad adsortiva no modificaron la supervivencia. La función renal basal fue un factor predictor de mortalidad. En este tipo de FRA el deterioro de la función renal no se recupera, objetivándose una reducción importante del FGe a los 6meses.
There are limited data describing the long-term renal outcomes of critically ill COVID-19 patients with acute kidney injury (AKI) and continuous renal replacement therapy (CRRT) and invasive mechanical ventilation.
MethodsIn this retrospective observational study we analyzed the long-term clinical course and outcomes of 30 critically ill patients hospitalized with COVID-19 during the peak of highest incidence in the first wave, with acute respiratory distress syndrome (ARDS) and AKI that required CRRT. Baseline features, clinical course, laboratory data, therapies and filters used in CRRT were compared between survivors and non-survivors to identify risk factors associated with in-hospital death. Renal parameters: glomerular filtration rate, proteinuria and microhematuria were collected at 6months after discharge.
Results19 patients (63%) died and 11 were discharged. Mean time to death was 48days (7-206) after admission. Patients with worse baseline renal function had higher mortality (P=.009). Patients were treated with CRRT for an average of 18.4days. Filters with adsorptive capacity (43%) did not offer survival benefits. Regarding long-term renal outcomes, survivor patients did not receive any additional dialysis, but 9 out of 11 patients had an important loss of renal function (median of eGF of 44 (13-76)ml/min/1.73m2) after 6months.
ConclusionMortality among critically ill hospitalized patients diagnosed with COVID-19 on CRRT is extremely high (63%). Baseline renal function is a predictor factor of mortality. Filters with adsorption capacity did not modify survival. None survivor patients required long-term dialysis, but an important loss of renal function occurred after AKI episode related to COVID-19 infection.
Las primeras notificaciones del síndrome respiratorio agudo grave por coronavirus (SARS-CoV-2) provienen de Wuhan, China, en diciembre del 2019, pero rápidamente se extendió por todo el mundo1,2. SARS-CoV-2 es un virus RNA de cadena simple que afecta fundamentalmente la vía respiratoria de humanos y animales3. Cuando la infección es severa puede producir alteraciones sistémicas. Todavía no se conoce con exactitud la etiología del fracaso renal agudo (FRA) en COVID-194. La estrecha relación entre el fallo respiratorio y el FRA sugieren que pudiera deberse a un mecanismo de necrosis tubular aguda isquémica, lo cual ocurre en situaciones de colapso circulatorio sistémico. Sin embargo, el mecanismo parece ser más complejo, con el desarrollo de lesión renal mediada por una tormenta de citoquinas, activación de la vía angiotensinaII, desregulación de la vía del complemento, hipercoagulación y microangiopatía5. Las terapias de soporte extracorpóreo se han propuesto para la retirada del torrente circulatorio de las citoquinas causantes del daño tisular en pacientes con sepsis y pudieran tener efectos beneficios en los pacientes críticos por COVID-196,7. El objetivo de nuestro estudio fue analizar la evolución clínica: función renal y mortalidad a largo plazo de los pacientes ingresados en la UCI con ventilación mecánica invasiva (VMI) y FRA con terapia continua de reemplazo renal (TCRR) y el papel de los diferentes filtros usados en las terapias de sustitución renal, en un hospital de tercer nivel en Madrid, durante el pico de máxima incidencia en la primera ola de la pandemia.
Material y métodosDiseño del estudioRetrospectivo observacional, analítico, unicéntrico.
Criterios de inclusión- •
Adultos >18años con neumonía por COVID-19, con necesidad de VMI, hospitalizados en la UCI desde el 10 al 31 de marzo del 2020.
- •
FRA con necesidad de TCRR.
Se registraron los datos demográficos, los patrones clínicos, analíticos, radiológicos, los esquemas de tratamiento y la mortalidad.
El método diagnóstico del SARS-CoV-2 fue por proteínaC reactiva (PCR; Thermofisher Multiplex RT-PCR) con muestra de exudado nasofaríngeo al ingreso por urgencias. Los controles analíticos incluyeron hemograma, tiempos de coagulación y bioquímica. Estos parámetros fueron analizados al ingreso, a los 7 y a los 30días al alta o fallecimiento. En los supervivientes, los datos de función renal se recogieron a los 6meses del alta hospitalaria.
Esquema de tratamientoA lo largo del brote, el esquema de tratamiento fue modificado según los protocolos dictados por la comisión del hospital. Así, inicialmente los pacientes fueron tratados con lopinavir/ritonavir más hidroxicloroquina e interferón beta, restringiendo el uso de metilprednisolona o dexametasona para los pacientes que desarrollaban síndrome de distrés respiratorio agudo (SDRA), con PaO2/FiO2<200 o requerimiento de intubación orotraqueal.
Desde el 21 de marzo de 2020 se añadió al esquema anterior también el uso de azitromicina para el paciente ingresado en planta y tocilizumab para pacientes con SDRA y niveles de interleucina6 (IL-6) >40pg/ml.
Los pacientes ingresados en la UCI recibían, además, anticoagulación profiláctica con heparina de bajo peso molecular (enoxaparina) a dosis de 4.000UI/día sc.
El estudio fue aprobado por el Comité ético para la investigación de nuestro hospital.
Definiciones y medidasLa función renal fue medida por filtrado glomerular estimado (FGe), creatinina sérica (Cr) antes del ingreso, al ingreso, pico máximo y a los 30días después del ingreso, al alta hospitalaria o antes del fallecimiento y a los 6meses del alta en aquellos pacientes supervivientes.
El FGe fue calculado usando la ecuación abreviada Modification of Diet in Renal Disease (MDRD-4).
Para el cribado de las alteraciones urinarias en el grupo de los supervivientes se realizó análisis de orina por tira reactiva como estudio inicial de la proteinuria y la hematuria.
Protocolo de TCRRLas indicaciones para la TCRR fueron FRA AKI3 (acute kidney injury) por cifras de creatinina, según las guías KDIGO (The Kidney Disease Improving Global Outcomes)8 o cualquier FRA AKI1 o2 que por sobrecarga de volumen o acidosis metabólica o hiperpotasemia no respondiera al tratamiento inicial conservador, requiriendo posteriormente terapia renal sustitutiva (TRS). En los FRA no oligúricos, definidos como volumen de diuresis >500ml/día, se indicó terapia de hemodiálisis venovenosa continua (HDVVC) y en los FRA oligúricos con volumen de diuresis <500ml/día se usó hemofiltración venovenosa continua (HVVC).
Los filtros denominados estándar para el TCRR fueron: la polisulfona AV600® (Fresenius Medical Care Bad Homburg, Alemania) y el AN69 HF M100® (Baxter, IL, EE.UU.), que es un copolímero de acrilonitrilo y metalil sulfonato de sodio. El filtro usado para TCRR, que además asocia capacidad adsortiva de citoquinas y endotoxinas, se llama oXiris® (Baxter, IL, EE.UU.), que es un AN69 ST modificado que asocia heparina y polietilenimina, injertados en los capilares del filtro que confieren la capacidad adsortiva de esta membrana.
La dosis de depuración inicial estándar fue entre 25-30ml/kg/h, y el balance negativo diario mediante ultrafiltración se determinaba a criterio del médico tratante en función del estado hemodinámico y de las necesidades del paciente. Asociamos perfusión de heparina sódica al 1% administrada prefiltro para la anticoagulación del circuito a dosis de 250-500U/h.
Como vía de acceso central se usaban preferiblemente la vena yugular interna derecha o la vena femoral, priorizándose la colocación del acceso yugular en pacientes con necesidad de pronación.
Análisis estadísticosTodos los análisis estadísticos se realizaron con el software SPSS 21.0 (SPSS; Chicago, IL, EE.UU.). Las variables cualitativas se presentan con su distribución de frecuencia. Las variables cuantitativas, con su media y desviación estándar (DE) o de mediana y rango intercuartil (RIQ) según su distribución. La asociación entre variables cualitativas se ha evaluado con la prueba χ2 (chi cuadrado) o la prueba exacta de Fisher. Las variables cuantitativas se han analizado utilizando la prueba t de Student (en comparaciones de una variable con dos categorías) y/o el análisis de la varianza (prueba ANOVA o Friedman). Utilizando esta técnica, se han evaluado las diferencias medias debidas al efecto individual o principal de cada factor y/o al efecto de sus interacciones. En todos los casos, la distribución de las variables se ha comprobado con los modelos teóricos y se ha probado la hipótesis de homogeneidad de varianza. El análisis de supervivencia (log rank) se utilizó para determinar la influencia de diferentes factores y filtros en la muerte hospitalaria. La significación estadística se consideró como un valor p<0,05
ResultadosDurante el periodo comprendido del 10 al 31 de marzo del 2020, 137 pacientes críticos con necesidad de VMI por COVID-19 fueron hospitalizados en las diferentes estancias habilitadas como UCI (7 en total) en el Hospital General Universitario Gregorio Marañón (HGUGM). Un total de 42 pacientes (30,6%) desarrollaron FRA, con requerimiento de TCRR en 30 de ellos (22%). Los 30 pacientes incluidos tenían una edad media de 62±11años (rango: 31-78), siendo el 70% varones.
La mayoría de los pacientes eran hipertensos (73%), con el 57% en tratamiento con inhibidores del sistema renina angiotensina aldosterona (iSRAA), el 50% tenían dislipemia, el 43% con obesidad y el 20% con diabetes. Los síntomas más frecuentes al ingreso por urgencias fueron la fiebre (83%), la tos (57%) y la astenia (57%). El 33% de los pacientes tuvieron síntomas digestivos.
Al ingreso desde urgencias ya se objetivaba que 15 de los 30 pacientes (50%) tenían una saturación de oxígeno basal <95%, con patrones radiológicos ya patológicos en el 97% de los pacientes, mostrando infiltrados bilaterales periféricos en 21 y unilaterales en 8 de ellos. Solo uno de estos 30 pacientes tenía ausencia de infiltrados en el momento de acudir a urgencias, que hemos definido como radiografía normal.
No había diferencias significativas en los valores clínicos, demográficos ni radiológicos al ingreso entre el grupo de supervivientes y el grupo de fallecidos.
Esquema de tratamientoTodos los pacientes recibieron tratamiento con hidroxicloroquina y lopinavir/ritonavir. Diecinueve (63%) asociaron también azitromicina, 29 (97%) corticoesteroides, 13 (36%) interferónβ y 24 (80%) tocilizumab.
No se encontraron diferencias significativas entre el tratamiento administrado entre los supervivientes y los fallecidos.
Evolución clínica y resultadosSe realizó seguimiento de los pacientes hasta el 30 de diciembre del 2020, con un tiempo medio de 116días (7-262).
Once pacientes fueron dados de alta y 19 pacientes (63%) fallecieron durante la hospitalización.
El tiempo medio de ingreso hasta el fallecimiento fueron 48días (7-206), y la media de tiempo en TCRR fue de 18,4días (1-41).
La media de puntuación del Apache ScoreII al ingreso en la UCI fue de 14,2±4,7, sin diferencias entre el Apache ScoreII de los supervivientes (12,7±5,2) y en los fallecidos (15,3±3,9) (p=0,1).
La mortalidad en la UCI de los pacientes con VMI sin FRA durante el mismo periodo de tiempo fue del 37%, ascendiendo al 43% en el subgrupo de pacientes que desarrollaron un FRA sin necesidad de depuración extrarrenal (creatinina media de 1,37±0,74mg/dl). Ambos grupos tuvieron una puntuación similar en el Apache ScoreII: de 13,74±4,2 y 12,4±3,4, respectivamente.
Durante el ingreso en UCI, la linfopenia, la anemia, el dímeroD y la proteínaC reactiva (PCR) aumentaron progresivamente, pero sin diferencias entre los supervivientes y los fallecidos. Solo el dímeroD y la procalcitonina a los 30días estaban más elevadas en los pacientes que fallecieron (tabla 1).
Valores de laboratorio en la urgencia, a los 7 y a los 30 días (al alta o antes del fallecimiento)
| Basal | Día 7 | Día 30 | |
|---|---|---|---|
| Recuento de linfocitos (×109) | |||
| Total (n = 30) | 0,71±0,31 | 0,46±0,29 | 0,77±0,46 |
| Supervivientes (n = 11) | 0,69±0,23 | 0,51±0,31 | 0,8±0,42 |
| Fallecidos (n = 19) | 0,73±0,38 | 0,43±0,29 | 0,74±0,50 |
| Hemoglobina (g/l) | |||
| Total (n = 30) | 13,8±2,4 | 11,1±2,1 | 8,3±0,5 |
| Supervivientes (n = 11) | 13,8±2,6 | 11,7±2,7 | 8,3±0,5 |
| Fallecidos (n = 19) | 13,8±2,3 | 10,8±1,5 | 8,2±0,8 |
| Dímero D (ng/ml) | |||
| Total (n = 30) | 524 (272-847) | 2.040 (830-3.607) | 2.314 (1.140-3.288) |
| Supervivientes (n = 11) | 376 (252-801) | 996 (473-1.930) | 1.228 (815-1.928) |
| Fallecidos (n = 19) | 601 (307-895) | 3.199 (975-4.823) | 2.825 (975-4.823)p = 0,036 |
| Procalcitonina sérica (μg/l) | |||
| Total (n = 30) | 0,39 (0,17-1,75) | 0,83 (0,29-2,81) | 0,46 (0,17-1,77) |
| Supervivientes (n = 11) | 0,23 (0,09-0,66) | 0,90 (0,42-1,40) | 0,30 (0,42-1,40) |
| Fallecidos (n = 19) | 0,54 (0,20-6,71) | 0,81 (0,24-5,36) | 2,08 (0,36-2,62)p = 0,029 |
| Proteína C reactiva (mg/dl) | |||
| Total (n = 30) | 17,6 (11,3-26,9) | 4,3 (2,2-12,8) | 7,8 (2,4-14,9) |
| Supervivientes (n = 11) | 13,8 (7,4-19,7) | 3,95 (2,7-25,3) | 3,7 (1,3-10) |
| Fallecidos (n = 19) | 18,3 (10-28,1) | 8,0 (5,9-6,4) | 3,7 (1,9-8,6) |
Encontramos infecciones concomitantes en 5 de los supervivientes (3 bacteriemias asociadas al catéter y 2bacteriemias con fungemia) y en 8 de los pacientes fallecidos (1bacteriemia asociada al catéter, 2 fungemias y 5 bacteriemias con fungemia).
El filtro oXiris, con propiedades adsortivas, no mejoró la supervivencia (log Rank=0,945, p=0,833) de nuestros pacientes. Tampoco encontramos ninguna diferencia significativa en cuanto a la mortalidad entre los diferentes esquemas terapéuticos usados.
Función renal y TCRREl FRA se produjo de media en el día 15±8 desde el inicio de los síntomas, con cifras de Cr al ingreso en UCI de 1,6±1,2mg/dl, y Cr pico de 4,1±mg/dl.
El 86,6% de los pacientes se clasificaron por cifra de Cr como AKI3 según las guías KDIGO8, mientras que el 13,4% restante tenían FRA clasificado como AKI2 o AKI1, si bien todos entrarían en categoría AKI3 por la necesidad de TRS, en nuestro caso en modo de terapia continua.
Los pacientes con AKI1 necesitaron TCRR por oliguria y alteraciones iónicas, y aquellos con AKI2 por sobrecarga de volumen refractaria a tratamiento con diuréticos.
Veinticuatro pacientes tuvieron TRS en modo HVVC y 6 pacientes en modo HDVVC.
Catorce de los 19 pacientes que fallecieron necesitaban TCRR en el momento del fallecimiento por ausencia de recuperación de la función renal.
La descripción del TCRR de los supervivientes y de los fallecidos se muestra en la tabla 2.
Parámetros de TCRR
| Supervivientes (n = 11) | Fallecidos(n = 19) | p | |
|---|---|---|---|
| Modalidad TCRR, n (%)HDVVCHVVC | 2 (18%)9 (82%) | 4 (21%)16 (84%) | 1,001,00 |
| Catéter venoso centralVena yugular internaVena femoral | 7 (64%)4 (36%) | 6 (32%)13 (68%) | 0,13 |
| TCRR oXiris, n (%) | 5 (45%) | 8 (42%) | 1,00 |
| oXiris /número de sesiones por pacienteVida Media del filtro, días | 8 (3-13)1,19±0,23 | 10 (7-24)1,33±0,47 | 0,59 |
| TCRR estándar, n (%) | 6 (54%) | 11 (58%) | 1,00 |
| Filtro estándar/número de sesiones por paciente | 21 (8-30) | 18 (8-24) | |
| Vida media del filtro, días | 1,56±0,24 | 1,58±0,47 | 1,00 |
Con respecto a los patrones basales, comorbilidades, Apache ScoreII o tratamientos administrados, tampoco se encontraron diferencias significativas entre el uso del filtro estándar vs oXiris (tabla 3).
Datos demográficos, clínicos, patrones radiológicos y tratamiento administrados entre pacientes con TCRR con filtro estándar vs oXiris
| Filtro estándar(n = 17) | oXiris(n = 13) | p | |
|---|---|---|---|
| Edad, años | 65±7 | 58±14 | 0,11 |
| Varones | 11 (65%) | 10 (77%) | 0,69 |
| Estadio FRA al inicio de TCRRAKI 1AKI 2AKI 3 | 2 (13%)0 (0%)15 (87%) | 0 (0%)2 (18%)11 (82%) | 0,12 |
| Cr pico | 4,3±1,7 | 3,8±1,5 | 0,39 |
| Hipertensión | 12 (71%) | 10 (77%) | 1,00 |
| iSRAA | 7 (41%) | 10 (77%) | 0,07 |
| Diabetes | 3 (18%) | 3 (23%) | 1,00 |
| Enfermedad cardíaca | 1 (6%) | 2 (15%) | 0,38 |
| Dislipidemia | 9 (53%) | 6 (46%) | 0,44 |
| Obesidad | 5 (29%) | 8 (61%) | 0,13 |
| Enfermedad renal crónica previa | 2 (13%) | 5 (33%) | 0,39 |
| Fiebre | 13 (76%) | 12 (92%) | 0,35 |
| Tos | 8 (47%) | 9 (69%) | 0,28 |
| Cansancio | 8 (47%) | 9 (69%) | 0,28 |
| Diarrea, naúseas ó vómitos | 5 (29%) | 5 (38%) | 0,70 |
| Apache Score II | 14,4±5,7 | 13,8±3,1 | 0,07 |
| Tiempo desde la urgencia al ingreso en la UCI, días | 3,2±3,2 | 1,5±1,5 | 0,06 |
| Saturación basal de oxígeno | 85,1±10,9 | 82,1±10,2 | 0,48 |
| Infiltrados bilaterales - vidrio deslustrado | 11 (65%) | 10 (77%) | 0,46 |
| Infiltrado unilateral | 5 (29%) | 3 (23%) | 0,46 |
| Radiografía de tórax normal | 1 (6%) | 0 (0%) | 0,46 |
| TratamientosCorticosteroidesBeta-interferónAzitromicinaTocilizumabHidroxicloroquinaLopinavir/ritonavir | 16 (94%)9 (53%)10 (59%)13 (76%17 (100%)17 (100%) | 13 (100%)8 (61%)9 (69%)11 (84%)13 (100%) 13 (100%) | 1,000,720,700,671,001,00 |
| Mortalidad | 11 (65%) | 8 (61%) | 1,00 |
La evolución de los parámetros de laboratorio entre los pacientes tratados con oXiris vs filtros estándar al ingreso, a los 7 y a los 30días tampoco mostró diferencias significativas (tabla 4).
Hallazgos de laboratorio al ingreso en la urgencia, a los 7 y 30 días tras el debut clínico con los diferentes filtros
| Basal | Día7 | Día 30 | |
|---|---|---|---|
| Recuento linfocitario (×109/l)Filtro estándar (n = 17)Filtro oXiris (n = 13) | 0,73±0,340,68±0,28 | 0,44±0,290,49±0,31 | 0,70±0,600,80±0,32 |
| Hemoglobina (g/l)Filtro estándar (n = 17)Filtro oXiris (n = 13) | 13,8±2,313,7±2,5 | 11,1±1,911,3±2,3 | 8,2±0,88,2±0,7 |
| Dímero D (ng/ml)Filtro estándar (n = 17)Filtro oXiris (n = 13) | 307 (252-756)673 (399-871) | 1.618 (680-7.704)2.040 (844-3.430) | 2.326 (877-4.271)1.788 (1.230-3.205) |
| Procalcitonina sérica (μg/l)Filtro estándar (n = 17)Filtro oXiris (n = 13) | 0,2 (0,1-6,7)0,5 (0,4-1,7) | 0,8 (0,2-1,9)0,9 (0,3-1,6) | 0,4 (0,2-1,9)0,6 (0,2-2,2) |
| Proteína C reactiva (mg/dl)Filtro estándar (n = 17)Filtro oXiris (n = 13) | 14,4 (5,8-24,3)18,8 (13,9-25,8) | 5,3 (3,2-24,6)2,9 (1,6-7,1)p < 0,05 | 8,0 (1,5-16,4)7,8 (2,8-10,4) |
La función renal basal era peor en los fallecidos que en los supervivientes (FGe 66,5±22,4 vs 94,6±31,9ml/min/1,73 m2 (p=0,009), con FGe ≤60ml/min/1,73m2 en 7 de los 30 pacientes.
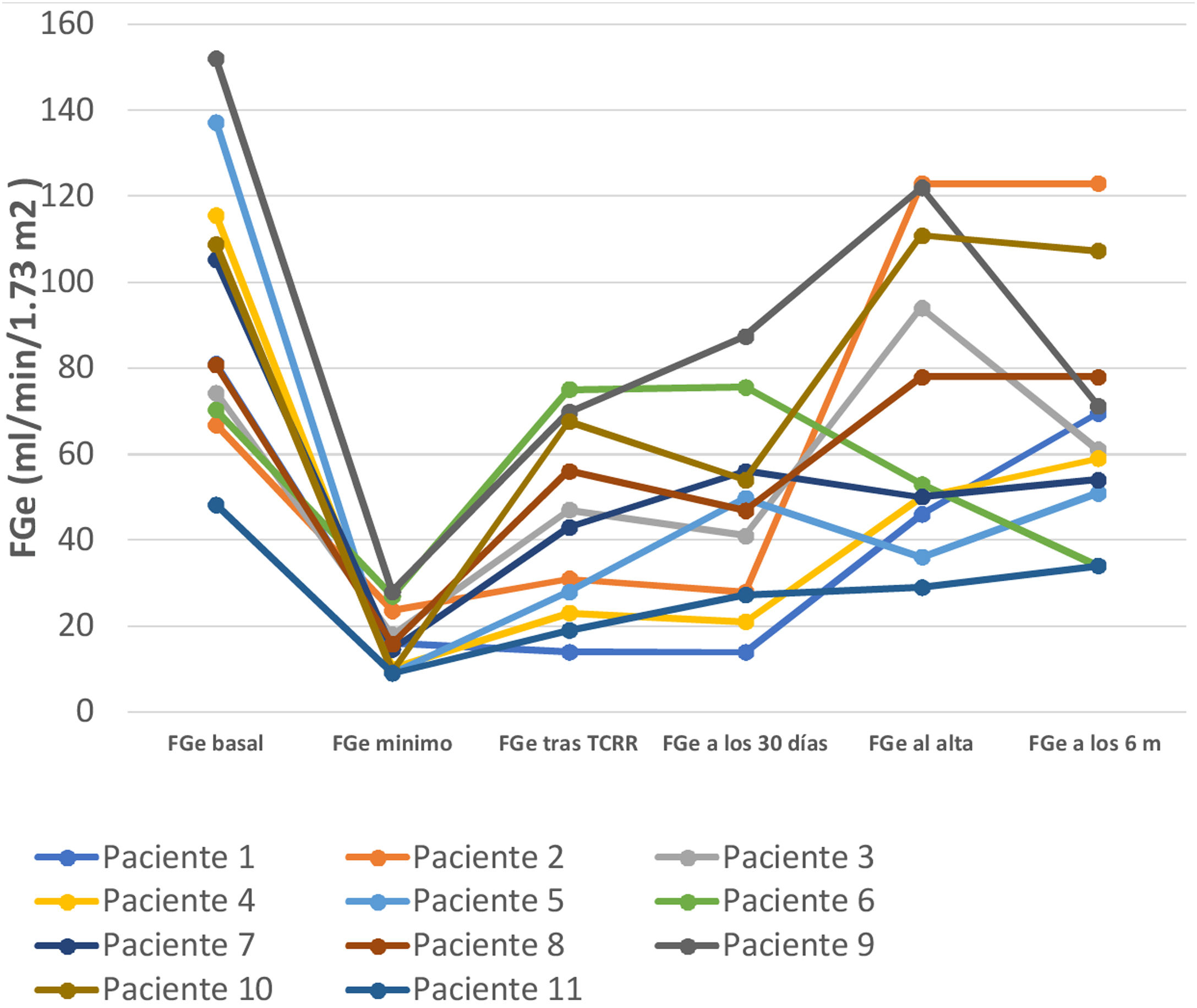
A los 6 meses del alta la función renal había cambiado con respecto a los parámetros basales al ingreso hospitalario: 9 de los 11 supervivientes tuvieron una pérdida media de FGe de 44 (IR 13-76) ml/min/1,73m2 (fig. 1), 1paciente presentaba albuminuria <1g/día y 3 pacientes tenían microhematuria en el análisis urinario.
DiscusiónEl principal objetivo de este estudio fue analizar la evolución clínica: función renal a largo plazo (6meses) y mortalidad en una serie de pacientes hospitalizados en UCI con neumonía por COVID-19 con necesidad de VMI y FRA que requirieron TCRR en el pico de máxima incidencia de la pandemia.
Nuestros principales hallazgos fueron: 1)que la mortalidad de este tipo de pacientes fue extremadamente elevada (63%); 2)que solo la función renal al ingreso se asoció con una mayor mortalidad, no encontrando asociación con otros factores de riesgo generales, como la hipertensión, la obesidad o la diabetes; 3)que los filtros con capacidad adsortiva en nuestra cohorte no modificaron la supervivencia, y 4)que los supervivientes no requirieron TRS a largo plazo, pero tampoco recuperaron por completo su función renal inicial, manteniendo a los 6meses una reducción significativa de la función renal sobre la basal.
El desarrollo de FRA en pacientes críticos con infección por COVID-19 difiere según las series publicadas. En la serie china de Guan et al.9, del 5,5% de los pacientes que acabaron ingresando en la UCI, el 0,5% desarrollaron FRA, pero en series descritas en Estados Unidos y en Europa10,11 la incidencia de FRA en los pacientes críticos por COVID-19 afecta en torno al 20-40%, siendo el desarrollo de FRA un marcador y un factor pronóstico negativo en la supervivencia12. En 5.700 pacientes con COVID-19 en una cohorte de Nueva York el desarrollo de FRA en los hospitalizados en la UCI fue del 36%, muy superior al publicado en China y en otras áreas diferentes (0,5-29%)13,14. En la UCI del HGUGM el porcentaje fue igual que el descrito en la serie de Nueva York, del 36,6%.
El porcentaje de requerimiento de TRS en el paciente crítico por COVID-19 oscila entre el 20% en la serie china con TCRR15 y el 31%, sin especificar si la técnica era continua o intermitente en la cohorte americana16, siendo del 22% en nuestra serie.
Un metaanálisis recientemente publicado17 muestra una elevada prevalencia de alteraciones urinarias y disfunción renal en pacientes con COVID-19: 4,5% FRA, y el 57% de los pacientes con proteinuria durante la hospitalización. Nuestros datos muestran que los pacientes que sobreviven a la infección por COVID-19 mantienen la pérdida de la función renal a largo plazo, a pesar de la normalización del sedimento urinario en la mayoría de ellos: solo un un paciente mantuvo proteinuria y 3 pacientes, microhematuria.
Entre el 5 y el 10% de los pacientes con COVID-19 requieren ingreso en la UCI con VMI debido a la progresión a neumonía severa con SDRA. En estos pacientes la respuesta inmune es excesiva, con el inicio de una «tormenta de citoquinas» que desarrolla un síndrome de respuesta inflamatoria sistémica (SRIS). En ausencia de una terapia eficaz, las indicaciones para la TCRR deben ser las ampliamente aceptadas para el tratamiento con FRA, como restaurar la homeostasis inmune, eliminar los mediadores inflamatorios que causan SRIS, prevenir y corregir la sobrecarga de volumen cuando los diuréticos son ineficaces. En ausencia de opciones de tratamiento establecidas para COVID-19, la justificación fisiopatológica podría apoyar el uso de cartuchos de sorbentes, que podrían eliminar o reducir por mecanismo adsortivo las citoquinas liberadas y, por lo tanto, disminuir el daño pulmonar y renal18. La evidencia de estos tratamientos es limitada en la actualidad. Recientemente se ha publicado una serie de casos retrospectivos de 50 pacientes críticos por COVID-19 tratados con TCRR y cartucho sorbente Cytosorb®19. Estos pacientes mostraron una reducción de los parámetros inflamatorios tras el uso del filtro, pero no se incluyó grupo control para comparar. Otra membrana con capacidad adsortiva es el AN69 ST oXiris, cuya superficie impregnada de heparina y polietilenimina ofrece la posibilidad de adsorber endotoxinas y citoquinas a través de interacciones iónicas. En nuestra serie usamos este tipo de membrana en 13 de los pacientes. Sin embargo, no encontramos diferencias clínicas, ni de laboratorio, ni en la supervivencia, en comparación con los pacientes en los que usamos los filtros estándar; probablemente nuestros pacientes ya se encontraban en una fase avanzada de la enfermedad, con VMI y requerimiento de TCRR.
La opinión actual de expertos es el uso de este tipo de terapias coadyuvantes en situaciones precoces, previas al requerimiento de MVI.
La ausencia de determinaciones seriadas de IL-6 en todos los pacientes, junto con el tratamiento con tocilizumab y la dificultad de interpretación de los niveles de IL-6 una vez es administrado este anticuerpo, no nos permite extraer conclusiones definitivas, en el caso de la infección por COVID-19, sobre la capacidad adsortiva de los filtros, y en concreto del oXiris.
De todos modos, los resultados que obtuvimos modificaron nuestra práctica clínica con respecto a su uso.
Actualmente se están realizando dos ensayos clínicos: NCT 04597034, que compara la eficacia del oXiris frente a AN69 en COVID-19, y NCT 04478539, que estudia dicha membrana como modalidad de tratamiento para COVID-19.
Con respecto a la mortalidad en pacientes intubados por COVID-19 con TCRR, aunque hay pocos y dispares datos publicados, el porcentaje de mortalidad en este tipo de pacientes varía desde el 39% descrito por Eriksson et al.20 hasta el 90,7% en el grupo de Zahid et al.21.
Hirsch et al.5 describieron que, en una serie de 285 pacientes con TCRR, 157 fallecieron y 9 fueron dados de alta; la tasa de mortalidad (55%) fue similar a la de nuestro grupo, pero 118 pacientes permanecían en TRS al final de seguimiento. También la función renal basal fue predictora de mortalidad. Lo que parece claro es que la mortalidad es muchísimo mayor en los pacientes que requieren TRS si lo comparamos con aquellos que desarrollan FRA pero no requieren depuración, como lo muestran los datos de nuestra UCI (43 y 63%, respectivamente), no habiendo diferencias en el Apache ScoreII.
Los hallazgos publicados sobre el impacto de la función renal en cuanto al pronóstico en la infección por COVID-19 son corroborados por los datos publicados en el OpenSAFELY.
El OpenSAFELY analiza los factores asociados con la muerte por COVID-19. Los registros de atención primaria de 17.278.392 adultos se relacionaron con 10.926 muertes relacionadas con COVID-19. El factor más importante asociado a la mortalidad fue la enfermedad renal crónica previa22.
Otros autores, como Cheng et al.23, corroboran que padecer FRA, bien desde el ingreso o desarrollarlo a lo largo del mismo, es factor predictor de mortalidad, ajustado a las comorbilidades habituales como hipertensión arterial, diabetes mellitus o dislipemia. Estos hallazgos son similares a nuestros resultados, en los que la función renal al ingreso se asoció con mayor mortalidad, frente a factores de riesgo clásicos de la población general, como la hipertensión arterial, la diabetes y la obesidad. Aunque también hay que tener en cuenta la limitación del tamaño muestral y la baja prevalencia de estos factores de riesgo en nuestra serie para poder sacar conclusiones.
LimitacionesNuestro estudio tiene limitaciones, entre las que citamos: el número de pacientes, el hecho de ser unicéntrico y de carácter retrospectivo, por lo que nuestros resultados pueden contener sesgos importantes; sin embargo, es novedoso en cuanto a que hay escasa literatura sobre el pronóstico renal a largo plazo de este tipo de FRA en este escenario, y en cuanto al uso de sorbentes tipo oXiris en estos pacientes, y por eso hemos querido describir nuestra experiencia con este filtro, que, además, posterior a nuestro uso, fue autorizado por las autoridades sanitarias (FDA) como tratamiento para la COVID-19.
ConclusionesLa mortalidad de los pacientes ingresados en la UCI que requieren tratamientos de soporte orgánico como la VMI y la TCRR durante la infección por COVID-19 es extremadamente elevada, siendo la función renal basal un factor predictor de mortalidad.
Los filtros con capacidad de adsorción de citoquinas y endotoxinas no modificaron la supervivencia en nuestra serie.
Los pacientes que superan la infección no requieren TRS, pero presentan una reducción significativa del filtrado glomerular a los 6meses de la infección por SARS-COV-2.
Consideraciones éticasLa investigación se llevó a cabo de conformidad con el código de ética de la Asociación Médica Mundial (Declaración de Helsinki). El Comité de Ética local del Hospital General Universitario Gregorio Marañón aprobó el estudio en vista de la naturaleza retrospectiva del mismo y que todos los procedimientos que se estaban realizando formaban parte de la atención rutinaria del servicio.
FinanciaciónNo se ha recibido financiación para el desarrollo de este artículo.
Contribuciones de los autoresRM, AM y MG organizaron y diseñaron el estudio, con pleno acceso a los datos del mismo, y son las responsables de la integridad y la precisión del análisis de los datos. RM y MG adquirieron, analizaron e interpretaron los resultados. El resto de autores revisaron y redactaron el manuscrito.
Conflicto de interesesPRB ha recibido honorarios por conferencia de BAXTER. El resto de autores afirman que no hay conflicto de intereses.
Quiero expresar mi especial agradecimiento a la unidad de enfermería del HGUGM especializada en TCRR, quienes realizaron un trabajo exquisito y ejemplar, en condiciones extremadamente complejas.