El objetivo del estudio fue comparar la prueba de la tuberculina (PT) y el QuantiFERON-TB® Gold In-Tube (QFT) en el diagnóstico de la infección latente tuberculosa (ILT) en una población de contactos de enfermos con tuberculosis pulmonar, y analizar la influencia de distintas variables en la discordancia.
Pacientes y métodoEntre marzo de 2008 y septiembre de 2010, de una población de 300.000 habitantes del País Vasco, se analizaron todos los contactos de pacientes con tuberculosis pulmonar. A todos se les realizó la PT y se midió el valor del QFT. Se analizaron diferentes variables sociodemográficas y la vacunación, analizándose la discordancia entre ambas pruebas.
ResultadosUn total de 704 sujetos fueron incluidos en el estudio, con una edad media de 27 años. De ellos, 397 estaban vacunados, siendo la proporción similar entre autóctonos y extranjeros. El incremento de la edad hasta los 59 años (odds ratio [OR] 10,53; p<0,001), ser extranjero (OR 2,71; p=0,02) y la vacunación (OR 4,22; p<0,001) fueron variables predictoras de la discordancia entre una PT positiva y un QFT negativo.
ConclusionesParece que el QFT, solo o combinado con la PT, es un método seguro para el diagnóstico de la ILT y que su utilización contribuiría a una selección más específica de los individuos que necesitan un tratamiento preventivo.
Our objetive is to compare the tuberculin skin test (TST) and the QuantiFERON-TB® Gold In-Tube (QFT) in the diagnosis of latent tuberculosis infection (LTI) in a population of contacts of patients with pulmonary tuberculosis, and to analyze the influence of different variables in the discordance.
Patients and methodFrom March 2008 to September 2010, among a population of 300,000 inhabitants of the Basque Country, we analyzed all contacts of patients with pulmonary tuberculosis. All patients underwent the TST and the value of QFT was measured. Sociodemographic variables and vaccination were examined and we analyzed the discordance between the 2 tests.
ResultsSeven hundred and four were included in the study, with a mean age of 27 years. Of these, 397 were vaccinated, with similar proportion between native and foreign. Increasing the age to 59 years (odds ratio [OR] 10.53, P<.001), being foreign (OR 2.71, P=.02) and vaccination (OR 4.22, P<.001) were predictors of the discordance between a positive TST and negative QFT.
ConclusionsIt seems that the QFT, alone or combined with the TST, is a safe method for the diagnosis of LTI and its use would contribute to a more specific selection of individuals who would need preventive treatment.
La identificación y el posterior tratamiento de las personas con infección latente tuberculosa (ILT) pertenecientes a grupos de riesgo constituye una estrategia esencial para el control de la tuberculosis1.
Para el diagnóstico de la ILT, los interferon-gamma release assays (IGRA, «pruebas basadas en la liberación del interferón-γ») pueden ser una buena alternativa a la tradicional prueba de la tuberculina (PT). La mayor ventaja de las IGRA respecto a la PT es su mayor especificidad, que resulta de la utilización de antígenos específicos de Mycobacterium tuberculosis (ESAT-6, CFP-10 y TB7.7), mientras que la PT es una mezcla de 200 antígenos no específicos que son compartidos por las micobacterias no tuberculosas y las cepas de Mycobacterium bovis utilizadas para la vacuna con el bacilo Calmette-Guérin (BCG)2–4.
Desde hace algunos años las IGRA han sido incluidas en los protocolos de diagnóstico de la ILT en numerosos países, aunque con estrategias diferentes5–7. Una de las cuestiones controvertidas respecto a su uso es el significado de la discordancia del tipo PT+/IGRA- en los casos no justificados por la vacunación BCG y la infección por micobacterias no tuberculosas, especialmente cuando la discordancia es extrema o se produce en la población infantil.
Por sus diferentes componentes antigénicos y diferencias en la respuesta inmunológica medida por ambos tests, no cabe esperar una concordancia equivalente entre la PT y las IGRA. La PT induce un tipo de reacción de hipersensibilidad retardada que perdura en el tiempo, siendo su declive infrecuente en menores de 55 años8. Las IGRA, sin embargo, detectan la liberación celular de IFN-γ como respuesta a una infección actual. Debido a estas diferencias en la respuesta inmunológica, se ha sugerido que las IGRA son más representativas de una infección reciente y que su sensibilidad para detectar una infección remota es menor frente a la PT9–12. Este hecho puede tener importantes implicaciones clínicas y programáticas, considerando que una infección reciente tiene mayor riesgo de progresar a una enfermedad activa y es, por tanto, una indicación preferente de un tratamiento preventivo.
En este estudio comparamos los resultados de la prueba de la PT y el QuantiFERON®-TB Gold In-Tube (QFT) en el diagnóstico de la ILT en una población de contactos de enfermos con tuberculosis pulmonar y analizamos la influencia de algunas variables demográficas, del grado de contacto con el caso índice y de la vacunación con BCG en la discordancia entre ambas técnicas.
Patients y métodoEl estudio se llevó a cabo en un distrito sanitario del País Vasco (España) con una población de 300.000 habitantes y una tasa de tuberculosis de 14 casos por 100.000 habitantes (año 2008). Participaron en el estudio individuos expuestos recientemente a pacientes con tuberculosis pulmonar (confirmada en cultivo) incluidos consecutivamente entre marzo de 2008 y septiembre de 2010. El estudio se enmarcó dentro de la investigación de contactos que rutinariamente se realiza en nuestra comunidad, siguiendo las recomendaciones establecidas en el Programa de Prevención y Control de la Tuberculosis en la Comunidad Autónoma del País Vasco13. De cada sujeto se recogió información relativa a edad, sexo, país de origen, antecedente de vacunación con BCG (basada en la inspección de la cicatriz característica), la proximidad y el ámbito donde se produjo el contacto.
Fueron excluidas las personas con una historia de tuberculosis activa y aquellas con antecedente conocido de una PT positiva. Se incluyeron en el análisis solamente los contactos con PT y QFT, ambas disponibles.
La PT fue administrada por el método Mantoux, usando 0,1ml (2 unidades de tuberculina) de PPD RT-23 (Statens Serum Institute, Copenhagen, Denmark), y fue leída 48-72h después de su aplicación por enfermeras entrenadas y expertas. Se clasificaron los sujetos en PT+ y PT- utilizando distintos tamaños de induración. Antes de la administración de la PT se obtuvo una muestra de sangre en la que se testó el QFT de acuerdo con las instrucciones del fabricante (Cellestis Ltd, Carnegie, Australia). Para el análisis del QFT se utilizaron rutinariamente el tubo con la mezcla de los antígenos ESAT-6, CFP-10 y TB7-7 (Rv2654) y el tubo de control negativo. En niños menores de 7 años se utilizó además el tubo de control positivo con mitógeno. La prueba se consideró positiva cuando el IFN-γ fue≥0,35IU/ml después de restarle el valor del control negativo. Se interpretó como resultado indeterminado un valor de IFN-γ>0,8IU/ml en el tubo de control negativo.
En contactos con un resultado inicialmente negativo, fuera la PT o el QFT, se repitieron uno o ambos tests 8 a 10 semanas después si no habían transcurrido 6 semanas desde el último contacto con el caso índice. Los resultados fueron considerados positivos si la primera o segunda determinación fue positiva. En sujetos mayores de 50 años con una PT basal negativa se repitió el test una semana después para desenmascarar un posible efecto booster. Se dio como resultado definitivo el obtenido en el segundo intento.
Análisis estadísticoSe ha realizado un análisis exploratorio de los datos de la muestra: frecuencias y porcentajes para variables categóricas, media y desviación estándar para la edad.
Se ha valorado el grado de acuerdo de la positividad establecida por la PT y el QFT, según los diferentes puntos de corte para la PT (5 y 10mm) y estratificado por sexo, edad, procedencia y el estado de vacunación (vacunado, no vacunado, no consta) del contacto. Para ello, se calculó el coeficiente Kappa con su intervalo de confianza del 95% (IC 95%). Un coeficiente Kappa superior a 0,70 se consideró buen acuerdo.
Se evaluó la asociación de los resultados de la PT con los obtenidos con el QFT, estratificado por el estado de vacunación del contacto (vacunado, no vacunado, desconocido). Se usó el test de la ji al cuadrado para la asociación entre ambas variables. A continuación, se determinaron los factores de exposición asociados a una tuberculina positiva para distintos puntos de corte. En primer lugar, se realizó un análisis univariante, usando el test de la ji al cuadrado o el test exacto de Fisher cuando las frecuencias esperadas eran menores de 5. La medida de asociación se estimó mediante la odds ratio (OR) junto con el IC 95%. Finalmente, se realizó un análisis de regresión logística multivariante de predicción de tuberculina positiva (PT>10mm) con aquellas variables cuyo valor de p fue menor que 0,20 en el análisis univariante. Del mismo modo, se realizaron tanto el análisis univariante como el multivariante para la positividad en el QFT.
Se determinaron los factores predictores de la discordancia PT+/QFT- (para diferentes puntos de corte de la PT) mediante el análisis de regresión logística univariante y multivariante para aquellas variables con un valor de p menor a 0,20 en el análisis univariante. Se estimó el poder discriminatorio del modelo mediante el área bajo la curva ROC.
Los análisis estadísticos fueron realizados con el paquete estadístico SAS® System v9.2 y la figura fue realizada con el software R v2.14. Se asumió significación estadística cuando el valor de p fue menor que 0,05.
ResultadosPoblación a estudioEntre marzo de 2008 y septiembre de 2010 se identificaron un total de 762 contactos de 84 pacientes con tuberculosis pulmonar bacteriológicamente confirmada en cultivo. Fueron excluidos 58 (7,6%) contactos: 22 (2,9%) por antecedentes de tuberculosis o de una ILT con PT positiva documentada, otros 31 (4,0%) porque no completaron las pruebas, de los que 10 fueron personas mayores con importante comorbilidad en los que solamente se realizó la radiografía de tórax, y 5 (0,6%) por un resultado indeterminado del QFT (todos ellos mayores de 15 años, 3 con PT≥5mm). Finalmente, la población del estudio quedó conformada por 704 contactos con resultados completos de la PT y QFT disponibles.
La tabla 1 describe las características sociodemográficas y clínicas de los 704 contactos incluidos en el estudio. El promedio del número de contactos por caso índice fue de 8,3; la edad media (DE) fue de 29,7 (17,4) años; 647 habían nacido en España (92%). Un total de 659 (94%) fueron contactos de casos índice con baciloscopia positiva en esputo; 167 fueron contactos íntimos, 106 (64,3%) de ellos en el ámbito domiciliario. Más de la mitad de los contactos, 397(56,3%), estaban vacunados con la BCG, con diferencias significativas en la proporción de vacunados en función de la edad (95, 65, 40 y 25% en los subgrupos de edad de <15, 15-29, 30-44 y 45-59 años, respectivamente, p<0,001). La proporción de vacunados en autóctonos y extranjeros fue similar (52 frente a 49%); en 200 contactos (28,4%) no se registró el antecedente vacunal o la interpretación de la cicatriz característica de la vacuna fue dudosa.
Características sociodemográficas y clínicas
| Variables | Contactos (n=704) |
| Sexo | |
| Varón | 425 (60,37) |
| Mujer | 279 (39,63) |
| Edada, años | 29,75±17,44 |
| Edad, años | |
| <15 | 151 (21,45) |
| 15-29 | 219 (31,11) |
| 30-44 | 176 (25,00) |
| 45-60 | 127 (18,04) |
| ≥60 | 31 (4,40) |
| BK | |
| Positiva | 659 (94,28) |
| Negativa | 40 (5,72) |
| Ámbito contacto | |
| Cerrado | 167 (23,72) |
| No cerrado | 532 (75,56) |
| Procedencia | |
| Autóctono | 647 (91,90) |
| Resto | 57 (8,10) |
| Vacunación con BCG | |
| Sí | 397 (56,39) |
| No | 107 (15,20) |
| Dudosa | 200 (28,41) |
| QFT | |
| Negativo | 493 (70,03) |
| Positivo | 211 (29,97) |
| PT | |
| <5 | 363 (51,56) |
| 5-9 | 52 (7,39) |
| 10-14 | 123 (17,47) |
| ≥15 | 166 (23,58) |
BCG: bacilo Calmette-Guérin; BK: baciloscopia; PT: prueba de la tuberculina; QFT: QuantiFERON® Gold In-Tube.
Datos representados como mediana (intervalo intercuartílico), excepto cuando se indica.
Según el tamaño de la induración de la PT, se detectaron 52 contactos positivos con PT de 5 a 9mm (7,5%), 123 contactos positivos con PT de 10 a 14mm (17,5%) y 166 con PT≥15mm (23,5%). De 341 contactos con PT positiva, 37 (11%) corresponden a conversiones en segunda determinación. El QFT fue positivo en 211 contactos (30%), con 12 (6%) convertores entre ellos.
La mayoría de los contactos con una PT≥15mm fue también QFT positivo (121 de 166; 73%), existiendo diferencias considerables entre los no vacunados (19 de 21; 91%) y los vacunados (29 de 69; 62%). Sin embargo, solo el 56% (69 de 123) y el 21% (11 de 52) de los contactos con una PT de 10 a 14mm y de 5 a 9mm, respectivamente, fueron QFT positivos
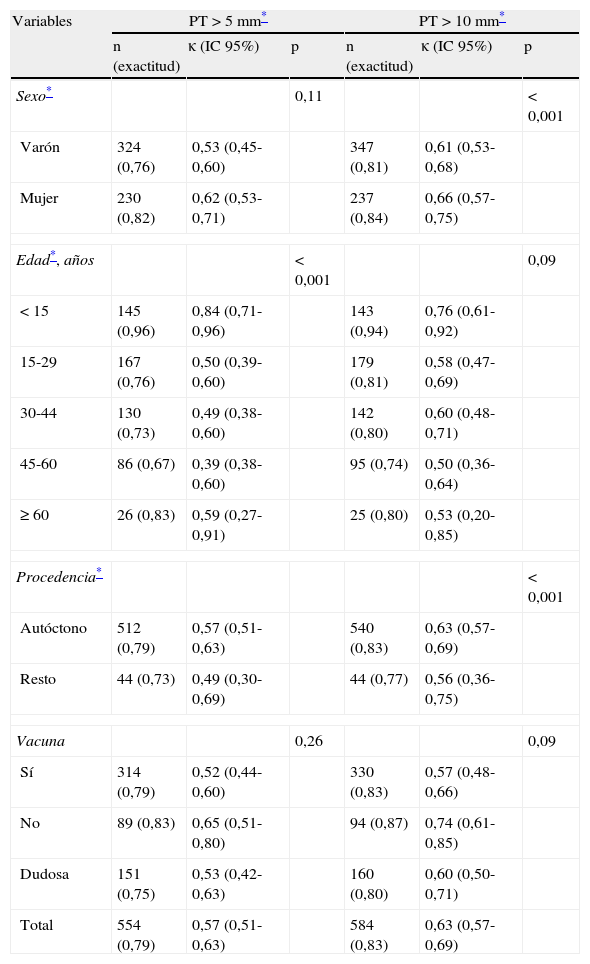
Concordancia entre la prueba de la tuberculina y el QuantiFERON®-TB Gold In-TubeEntre los 704 contactos de la muestra hubo 554 resultados concordantes (79%) entre el QFT y la PT≥5mm, y 150 resultados discordantes (21%) (κ 0,57). De los resultados concordantes, 201 fueron concordantes positivos (36%) y 353 concordantes negativos (64%). De los 150 resultados discordantes, 140 fueron del signo PT+/QFT- (93%) y 10 del signo PT-/QFT+ (7%). Se encontraron diferencias estadísticamente significativas en la concordancia en función del sexo, la edad y la nacionalidad de los participantes. La mejor concordancia se registró en el grupo menor de 15 años (96%, κ 0,84), usando la PT≥5mm como referencia. Hubo una mejor concordancia en el grupo de no vacunados (83%, κ 0,65) respecto al grupo de vacunados (79%, κ 0,52), pero sin diferencias estadísticamente significativas (tabla 2).
Concordancia entre el QuantiFERON®-TB Gold In-Tube y la prueba de la tuberculina (puntos de corte 5 y 10mm), según diferentes variables
| Variables | PT>5mm* | PT>10mm* | ||||
| n (exactitud) | κ (IC 95%) | p | n (exactitud) | κ (IC 95%) | p | |
| Sexo* | 0,11 | <0,001 | ||||
| Varón | 324 (0,76) | 0,53 (0,45-0,60) | 347 (0,81) | 0,61 (0,53-0,68) | ||
| Mujer | 230 (0,82) | 0,62 (0,53-0,71) | 237 (0,84) | 0,66 (0,57-0,75) | ||
| Edad*, años | <0,001 | 0,09 | ||||
| <15 | 145 (0,96) | 0,84 (0,71-0,96) | 143 (0,94) | 0,76 (0,61-0,92) | ||
| 15-29 | 167 (0,76) | 0,50 (0,39-0,60) | 179 (0,81) | 0,58 (0,47-0,69) | ||
| 30-44 | 130 (0,73) | 0,49 (0,38-0,60) | 142 (0,80) | 0,60 (0,48-0,71) | ||
| 45-60 | 86 (0,67) | 0,39 (0,38-0,60) | 95 (0,74) | 0,50 (0,36-0,64) | ||
| ≥60 | 26 (0,83) | 0,59 (0,27-0,91) | 25 (0,80) | 0,53 (0,20-0,85) | ||
| Procedencia* | <0,001 | |||||
| Autóctono | 512 (0,79) | 0,57 (0,51-0,63) | 540 (0,83) | 0,63 (0,57-0,69) | ||
| Resto | 44 (0,73) | 0,49 (0,30-0,69) | 44 (0,77) | 0,56 (0,36-0,75) | ||
| Vacuna | 0,26 | 0,09 | ||||
| Sí | 314 (0,79) | 0,52 (0,44-0,60) | 330 (0,83) | 0,57 (0,48-0,66) | ||
| No | 89 (0,83) | 0,65 (0,51-0,80) | 94 (0,87) | 0,74 (0,61-0,85) | ||
| Dudosa | 151 (0,75) | 0,53 (0,42-0,63) | 160 (0,80) | 0,60 (0,50-0,71) | ||
| Total | 554 (0,79) | 0,57 (0,51-0,63) | 584 (0,83) | 0,63 (0,57-0,69) | ||
Exactitud: coeficiente de exactitud; κ (IC 95%): coeficiente Kappa (intervalo de confianza del 95%); n: contactos con QFT y PT positiva, según los diferentes puntos de corte; PT: prueba de la tuberculina; QFT: QuantiFERON® Gold In-Tube.
La edad media de los contactos con discordancia QFT+/PT- (41,9 años) fue significativamente mayor que la del conjunto (29,7 años), y la media de la respuesta IFN-γ (5,6UI/ml), significativamente menor que la respuesta IFN-γ (1,0UI/ml) en el grupo con QFT+/PT+ (p=0,001).
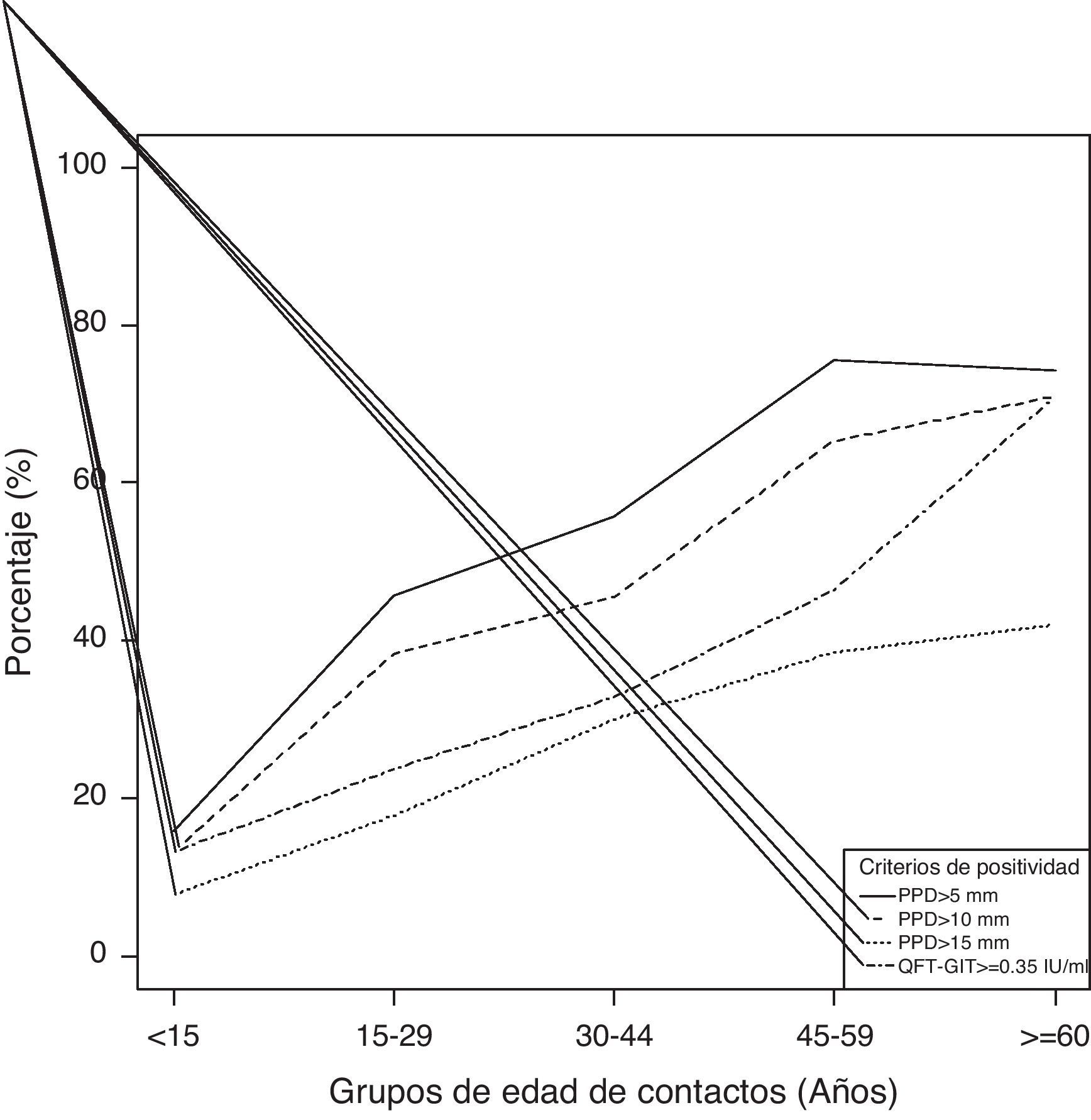
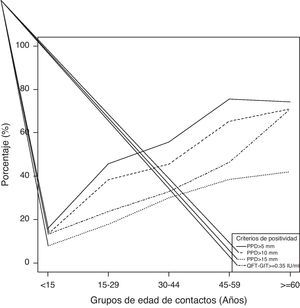
En la figura 1 se muestra el comportamiento de la positividad del QFT y de la PT según la edad. Ambas técnicas mostraron una tendencia ascendente con la edad, pero de intensidad variable según los grupos.
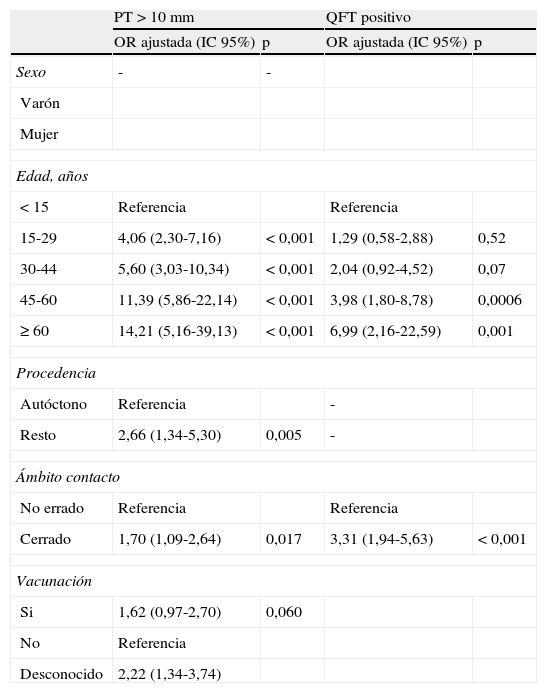
Predictores independientes de la positividad de los tests y de la discordancia prueba de la tuberculina +/QuantiFERON®-TB Gold In-Tube -El análisis multivariante evidenció una asociación significativa de los resultados positivos de la PT y el QFT con el incremento de la edad y la proximidad del contacto. La probabilidad (OR) de tener una PT≥10mm fue incrementada significativamente en cada grupo de edad (p<0,001) y alcanzó el máximo riesgo en mayores de 60 años (OR 14,21). La posibilidad de tener un QFT positivo también aumentó en sucesivos grupos de edad, aunque con diferencias significativas solo en los grupos de 45 a 59 años (OR 3,98, IC 95% 1,80-8,78) y de más de 60 años (OR 6,99, IC 95% 2,16-22,59). Ser extranjero aventajó en más del doble la probabilidad de una PT positiva (OR 2,66). El análisis univariante mostró una asociación negativa de la vacunación con BCG y el QFT (OR 0,38, IC 95% 0,24-0,61) (tabla 3).
Factores predictores para QuantiFERON®-TB Gold In-Tube positivo y prueba de la tuberculina positiva (punto de corte de 10mm)
| PT>10mm | QFT positivo | |||
| OR ajustada (IC 95%) | p | OR ajustada (IC 95%) | p | |
| Sexo | - | - | ||
| Varón | ||||
| Mujer | ||||
| Edad, años | ||||
| <15 | Referencia | Referencia | ||
| 15-29 | 4,06 (2,30-7,16) | <0,001 | 1,29 (0,58-2,88) | 0,52 |
| 30-44 | 5,60 (3,03-10,34) | <0,001 | 2,04 (0,92-4,52) | 0,07 |
| 45-60 | 11,39 (5,86-22,14) | <0,001 | 3,98 (1,80-8,78) | 0,0006 |
| ≥60 | 14,21 (5,16-39,13) | <0,001 | 6,99 (2,16-22,59) | 0,001 |
| Procedencia | ||||
| Autóctono | Referencia | - | ||
| Resto | 2,66 (1,34-5,30) | 0,005 | - | |
| Ámbito contacto | ||||
| No errado | Referencia | Referencia | ||
| Cerrado | 1,70 (1,09-2,64) | 0,017 | 3,31 (1,94-5,63) | <0,001 |
| Vacunación | ||||
| Si | 1,62 (0,97-2,70) | 0,060 | ||
| No | Referencia | |||
| Desconocido | 2,22 (1,34-3,74) | |||
IC 95%: intervalo de confianza del 95%; OR ajustada: odds ratio obtenida en el análisis multivariante; PT: prueba de la tuberculina; QFT: QuantiFERON®-TB Gold In-Tube; -: variable no considerada en el modelo multivariante.
Se consideró significación estadística un valor de p<0,005.
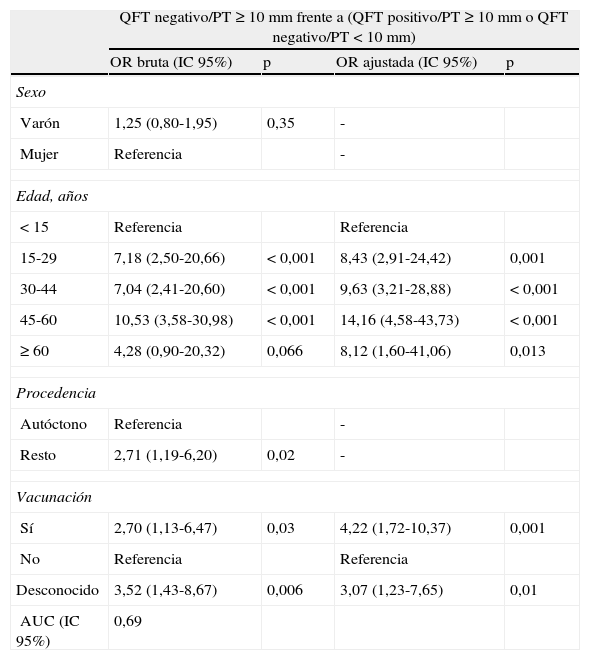
El incremento en la edad (OR 10,53; p<0,001) y la vacunación con BCG (OR 4,22; p=0,001) fueron predictores de la discordancia PT+/QFT- (en todos los puntos de corte de la PT). El ser extranjero se asoció a la discordancia con un punto de corte de 15mm de la PT. La proximidad del contacto y la exposición a enfermos con baciloscopia positiva no se asociaron con la discordancia (tabla 4).
Factores predictores de la discordancia entre la presencia de un QuantiFERON®-TB Gold In-Tube negativo y una prueba de la tuberculina positiva (punto de corte de 10mm)
| QFT negativo/PT≥10mm frente a (QFT positivo/PT≥10mm o QFT negativo/PT<10mm) | ||||
| OR bruta (IC 95%) | p | OR ajustada (IC 95%) | p | |
| Sexo | ||||
| Varón | 1,25 (0,80-1,95) | 0,35 | - | |
| Mujer | Referencia | - | ||
| Edad, años | ||||
| <15 | Referencia | Referencia | ||
| 15-29 | 7,18 (2,50-20,66) | <0,001 | 8,43 (2,91-24,42) | 0,001 |
| 30-44 | 7,04 (2,41-20,60) | <0,001 | 9,63 (3,21-28,88) | <0,001 |
| 45-60 | 10,53 (3,58-30,98) | <0,001 | 14,16 (4,58-43,73) | <0,001 |
| ≥60 | 4,28 (0,90-20,32) | 0,066 | 8,12 (1,60-41,06) | 0,013 |
| Procedencia | ||||
| Autóctono | Referencia | - | ||
| Resto | 2,71 (1,19-6,20) | 0,02 | - | |
| Vacunación | ||||
| Sí | 2,70 (1,13-6,47) | 0,03 | 4,22 (1,72-10,37) | 0,001 |
| No | Referencia | Referencia | ||
| Desconocido | 3,52 (1,43-8,67) | 0,006 | 3,07 (1,23-7,65) | 0,01 |
| AUC (IC 95%) | 0,69 | |||
AUC (IC 95%): area under the curve («área bajo la curva») para el intervalo de confianza del 95%; OR: odds ratio; PT: prueba de la tuberculina; QFT: QuantiFERON®-TB Gold In-Tube.
Análisis de contactos discordantes, definidos por la presencia de un resultado negativo del QFT y un resultado positivo de la PT, para un punto de corte de 10mm, frente a contactos concordantes definidos por la presencia de un resultado positivo del QFT y de la PT o un resultado negativo del QFT y de la PT, para un punto de corte de 10mm.
Este estudio describe una comparación directa entre la PT y el QFT para la detección de la ILT en 704 contactos de enfermos con tuberculosis pulmonar, 94% de ellos contactos de casos índice con baciloscopia positiva. Encontramos una moderada concordancia entre el QFT y la PT (κ=0,57, κ=0,63 y κ=0,51 utilizando una PT≥5, ≥10 y ≥15mm, respectivamente), siendo predictores independientes de la discordancia PT+/QFT- la edad, la nacionalidad de un país de alta endemia tuberculosa y la vacunación con BCG.
No se encontró asociación entre la discordancia PT+/QFT- y factores de exposición como la proximidad o el contacto con casos índice bacilíferos. Este hecho es de gran interés y concuerda con estudios anteriores10,14 que mostraron cómo los IGRA correlacionan mejor el riesgo de infección con el grado de contacto con un enfermo de tuberculosis.
El estudio nos parece relevante habida cuenta de la escasa literatura médica disponible a nivel nacional14–18 y las implicaciones clínicas que pueden derivar de sus resultados.
Nuestra concordancia es consistente con otros estudios19,20, aunque la heterogeneidad en el diseño y las poblaciones dificulta la comparación de los resultados. Por ejemplo, la peor concordancia registrada en un reciente estudio realizado en el País Vasco (κ=0,45)14 puede atribuirse a la mayor representación en nuestra serie de niños (22 frente a 12%), de sujetos vacunados con BCG (56 frente a 44%) y de contactos expuestos a enfermos bacilíferos (94% frente a 70%), teniendo en cuenta que todas ellas favorecieron la concordancia en ambos estudios.
Entre los resultados discordantes (150, 21%), la gran mayoría (140, 93%) fue del signo PT+/QFT-, como corresponde al comparar 2 pruebas de distinta especificidad.
Congruente con su composición antigénica más específica, el QFT no se vio afectado por la vacunación con BCG; incluso es posible un efecto protector dada la asociación de la vacunación con un resultado negativo del QFT constatada en el análisis univariante21.
La evaluación del efecto de la vacunación con BCG sobre la PT ofreció resultados contradictorios. Por un lado, la asociación de la vacunación con la discordancia PT+/QFT- sugeriría un efecto positivo sobre la PT; sin embargo, podría estar también influida por el efecto negativo de la vacuna sobre el QFT. Por otro lado, la menor reactividad a la PT en el grupo de vacunados (39 frente a 46%) y la excelente concordancia observada en los niños vacunados, habitualmente el colectivo más afectado por el efecto de la vacunación, indicarían su escaso impacto en la PT. De hecho, el subgrupo menor de 15 años mostró la mejor concordancia entre las pruebas (κ=0,85) y la menor discordancia PT+/QFT- (3%) de toda la cohorte, a pesar de contar con el mayor número de vacunados entre ellos (96%). Los datos publicados sobre esta cuestión son muy dispares16,22-24 y posiblemente las diferencias estén relacionadas con los diferentes procedimientos de vacunación utilizados en cada caso. La aplicación de la BCG en recién nacidos y en una sola dosis, que es la norma que se sigue en el País Vasco, tendría un débil impacto en la PT según un metaanálisis25, y podría explicar su escasa influencia en nuestros niños. Se estima que la proporción de falsos positivos de la PT inducidos por la BCG en la población de 7 años en nuestra provincia es tan solo del 6,5%26. Por el contrario, cuando la BCG es administrada después del primer año de vida o en varias dosis o en edad adulta, la respuesta inmunológica de la PT sería más intensa, más frecuente y más duradera25. Como esta estrategia vacunal es común en países de alta endemia tuberculosa, la vacunación con BCG podría explicar la mayor proporción de reactores a la PT (en todos los puntos de corte) y la mayor discordancia PT+/QFT- encontrada en nuestros participantes extranjeros, en su inmensa mayoría nacidos en países de esas características.
Teóricamente la discordancia PT+/QFT- podría estar también motivada por infecciones remotas o resueltas detectadas por la PT y no por el QFT. La interpretación de que los IGRA son ante todo representativos de una infección reciente continúa siendo una cuestión controvertida9,27. Nosotros estudiamos indirectamente esta cuestión analizando el comportamiento del QFT y la PT en diferentes subgrupos de edad. Comprobamos que la positividad de la PT y del QFT fue ascendente en todas las franjas de edad, pero con diferencias en su intensidad: de salida, en el grupo más joven, ambas pruebas computaron una proporción similar de resultados positivos (15%), se siguió de un alza de la PT respecto al QFT de hasta el 30% en el tramo de 16-59 años, y a partir de los 60 años el QFT experimentó un notable ascenso mientras que la PT se estancó o descendió (según el punto de corte valorado), confluyendo ambas en un pico máximo de positividad del 71%.
De este comportamiento se pueden extraer 2 interesantes conclusiones. En primer lugar, que el QFT está menos mediatizado por la infección remota que la PT y discrimina mejor la infección reciente, y, en segundo lugar, que en edades más avanzadas, la sensibilidad del QFT para diagnosticar la ILT es superior a la de la PT28,29.
Es improbable que la vacunación con BCG haya podido influir en este comportamiento teniendo en cuenta que la cobertura vacunal fue decreciendo significativamente en cada grupo de edad. Es interesante destacar también que el subgrupo mayor de 60 años contó con una proporción significativamente mayor de contactos de alto riesgo de exposición que el resto (51% de contactos íntimos con enfermo de tuberculosis bacilífera frente a 20%), con el subsiguiente mayor riesgo de haber sido infectados recientemente por ILT. De ahí que el importante repunte del QFT en esa edad, no secundado por la PT, pueda ser indicativo de una mayor sensibilidad del QFT (datos expuestos on-line). Por el contrario, en los otros subgrupos el riesgo de exposición fue de menor intensidad y sin diferencias entre ellos, determinando una curva del QFT de menor incidencia y sin picos.
En ausencia de un estándar oro para el diagnóstico de la ILT no se puede excluir el riesgo de progresión a una tuberculosis activa en contactos con resultados discordantes. En 2 estudios publicados recientemente30,31 ningún paciente con QFT negativo y PT positiva desarrolló enfermedad durante el seguimiento, a pesar de no haber recibido la quimioprofilaxis. Por el contrario, otros estudios han registrado casos de progresión a enfermedad en individuos con discordancia PT+/QFT-32,33. La mejor correlación del QFT con el grado de exposición, la vinculación de la discordancia PT+/QFT- con la infección remota y con la vacunación BCG (particularmente en extranjeros), y un posible efecto negativizador de la BCG sobre el QFT observados en nuestro estudio nos permiten conjeturar que el riesgo de enfermar de tuberculosis activa de los contactos con resultados PT+/QFT- debiera ser pequeño. A todo ello hay que añadir los posibles resultados falsos positivos de la PT inducidos por la sensibilización previa por Mycobacterium avium, de alta prevalencia en nuestra población26.
Nuestros resultados tienen importantes implicaciones clínicas. Asumiendo la positividad del QFT como verdadera infección, la especificidad de la PT fue relativamente baja (363 de 493; 73%) usando el punto de corte≥5mm recomendado en el País Vasco en contactos de alto riesgo. Estos datos respaldarían, por tanto, las recomendaciones del National Institute for Clinical Excellence6 de confirmar con una IGRA las reacciones positivas de la PT antes de ofertar el tratamiento para la ILT. Aplicando esta estrategia, 341 (48%) contactos recibirían tratamiento de la ILT utilizando la PT como referencia y solamente 201 (28%) con el QFT. En un reciente documento de consenso patrocinado por la SEPAR5 se reconoce la utilidad de las IGRA en el diagnóstico de la ILT aunque limitando su uso solamente a pacientes inmunodeprimidos con PT negativa y a los pacientes con PT positiva previamente vacunados con BCG. Según nuestros datos, el papel que se concede a las IGRA en el documento parece demasiado restrictivo considerando que la positividad de la PT está vinculada a otros factores que no conllevan un riesgo de enfermar de tuberculosis además de la BCG. En niños, las 2 técnicas tuvieron resultados equivalentes, con independencia del antecedente vacunal, por lo que el QFT no aportaría ventajas sustanciales respecto a la PT, ni siquiera en los vacunados con BCG.
Asimismo, la escasa discordancia QFT+/PT- en el estudio (10 de 366, 2,7%) valida la buena sensibilidad (97,3%) de la estrategia secuencial para el estudio de contactos, utilizando la PT como test inicial y el QFT como prueba de confirmación cuando la PT es≥5mm. En población de menor riesgo, podría ser incluso factible utilizar de inicio una PT≥10mm, ya que su sensibilidad apenas se vería comprometida. Sin embargo, utilizando un punto de corte≥15mm se perderían un 43% de casos con QFT+.
La opción de reemplazar la PT por IGRA, como proponen los Centers for Disease Control and Prevention (CDC)5, implicaría el enmascaramiento de un 27% (45 de 166) de contactos con PT≥15mm no confirmados con el QFT en nuestro estudio, lo cual puede suscitar dudas sobre la seguridad de esta estrategia dado que reacciones de la PT de esta magnitud se interpretan como verdadera infección al no estar afectadas por la BCG34 o por una infección por micobacterias no tuberculosas17. Sin embargo, en lo que concierne a la vacunación con BCG, esta idea no se sostiene en nuestros datos, ya que la proporción de resultados discordantes PT≥15mm/QFT- en el grupo de vacunados fue mayor que en el de no vacunados (37 frente a 9%).
Por otro lado, la aplicación de la estrategia recomendada por los CDC conllevaría la indicación de quimioprofilaxis en todos los contactos con QFT+, incluyendo aquellos que habrían sido PT-, cuya importancia clínica ha sido cuestionada por el alto porcentaje de reversiones espontáneas del QFT que se producen entre los contactos con discordancia PT-/QFT+35.
Nuestro estudio tiene limitaciones que debemos considerar. Primera, la vacunación con BCG se determinó mediante la constatación de la cicatriz característica, método que, aunque de uso habitual, puede inducir a errores de interpretación. Reseñamos también que en el estudio no se registró el antecedente vacunal en un 29% de los contactos, aunque pensamos que esta limitación no tuvo que influir en los resultados, ya que la gran mayoría de fallos (76%) ocurrió en mayores de 30 años, población potencialmente poco afectada por el impacto de la BCG sobre la PT25.
Segunda, la no utilización sistemática (salvo en niños menores de 7 años) del control positivo (estimulación con mitógeno) pudo conllevar resultados falsos negativos del QFT en contactos con una inmunodepresión grave36,37, aunque es improbable que hubiera un número suficiente de pacientes de esta condición entre los participantes como para influir en los resultados.
En conclusión, nuestros datos sugieren que la discrepancia PT+/QFT- no se debe a una pérdida de sensibilidad del QFT respecto a la PT, sino a factores diversos que no comportan un riesgo de enfermar de tuberculosis. Por tanto, en nuestro contexto, el QFT sería un método seguro para el diagnóstico de la ILT en contactos y su utilización contribuiría a una selección más específica de los individuos que necesitan un tratamiento preventivo, evitando un considerable número de tratamientos innecesarios. Consideraciones económicas y operativas al margen, no habría diferencias clínicas destacables entre el uso del QFT como prueba única o como prueba confirmativa en combinación con la PT, exceptuando la oportunidad que proporcionaría la estrategia combinada de recuperar eventualmente para el tratamiento preventivo casos con induraciones potentes de la PT no confirmadas con el QFT. No obstante, estas conclusiones deben ser validadas por estudios longitudinales a gran escala.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.