Describir las manifestaciones clínicas y hallazgos de laboratorio de una serie de casos febriles agudos con diagnóstico presuntivo de infección por el virus dengue. en Quindío (Colombia).
Materiales y métodosSe realizó un estudio de corte transversal, en pacientes con sospecha clínica de dengue en el periodo comprendido entre enero y agosto de 2013, en algunos centros hospitalarios del departamento del Quindío. Se tomaron muestras de sangre para diagnóstico de dengue, leptospira, malaria, hepatitis B, y rickettsiosis. Como pruebas confirmatorias para dengue se realizó aislamiento viral en células C6/36HT y serotipificación para dengue por RT-PCR; pruebas de función hepática, cuadro hemático y niveles de citocinas.
ResultadosSe caracterizaron 149 casos, de los cuales el 43% presentaron infección por dengue, 4% leptospira, 6,8% rickettsias, un caso de malaria y uno de hepatitis B. En 5 casos se logró el aislamiento del DENV2 y DENV3. Mediante la RT-PCR, se evidenció cocirculación de serotipos 2, 3, 4. Se encontró que las enzimas AST/ALT, el conteo de plaquetas, la erupción y el dolor abdominal fueron marcadores característicos de la infección por dengue, mientras la ictericia y el dolor lumbar se correlacionaron con la leptospirosis. Los valores de citocinas mostraron que la IL-10, TNFα variaron significativamente en casos con dengue frente a otros diagnósticos, y la IL-17α presentó diferencias significativas en individuos con dengue grave.
ConclusionesEl dengue se confirmó como causa etiológica importante de síndrome febril icterohemorrágico en el departamento del Quindío, pero la leptospirosis y la rickettsiosis tienen también una participación importante. Sin embargo, en el 44% de los casos fueron catalogados como síndrome febril indeterminado.
To characterise the clinical and laboratory findings on a series of febrile cases with a presumptive diagnosis of dengue virus infection in Quindío, Colombia.
Materials and methodsThis study was conducted from January to July 2013. Blood samples were obtained from patients suspected of dengue virus infection from Quindío department hospitals. These samples were tested for dengue, leptospira, malaria, hepatitis B and rickettsiosis. To confirm dengue infection, we performed viral isolation in C6/36HT cells and dengue serotyping by RT-PCR; liver function tests, complete blood counts and cytokine levels.
ResultsOf 149 cases, 43% were infected by dengue, 4% leptospira, 6.8% rickettsia, one case of malaria and one case of hepatitis b. We obtained 5 clinical isolates of DENV2 and DENV3 that evidenced co-circulation of serotypes 2, 3, and 4. We found that AST/ALT levels, platelet count, rash and abdominal pain were good markers of infection by dengue, while jaundice and lumbar pain suggested leptospirosis. Cytokine levels revealed that IL-10, TNFα varied significantly in dengue compared with other diagnostics and that IL-17α showed significant differences in individuals with severe dengue.
ConclusionsDengue was confirmed as an important aetiology of acute febrile ictero-haemorrhagic syndrome in Quindío, but leptospirosis and rickettsia also play an important role. However, 44% of the cases were classified as undetermined febrile syndrome.
El síndrome febril agudo es definido como el estado mórbido con inicio repentino de fiebre, de menos de 7 días de evolución, en el cual no se hayan identificado signos o síntomas relacionados con un foco infeccioso1. Dentro de los agentes etiológicos de este síndrome, se deben considerar protozoos parásitos como Plasmodium sp., Babesia sp, bacterias como rickettsia, leptospira entre otras, así como virus de la hepatitis B, HIV, dengue chikungunya hantavirus, entre otros, por lo que se dificulta para el clínico realizar un adecuado diagnóstico etiológico, incurriendo en errores diagnósticos, en el manejo y en los reportes epidemiológicos de cada uno de estos patógenos. El dengue como una infección viral sistémica es causado por el virus dengue (DENV); incluye 5 serotipos denominados DENV1 a DENV5. Este último ha sido descrito recientemente. Produce un espectro de enfermedad que cursa desde una infección asintomática, un cuadro febril sin complicaciones o una enfermedad grave con incremento en la permeabilidad vascular, llevando a complicaciones hemorrágicas, e incluso la muerte del individuo2–5. Su cuadro clínico es similar a otros eventos incluidos en el síndrome febril agudo6–9. La identificación se realiza mediante la cuantificación de anticuerpos IgM específicos contra el virus, el aislamiento viral y técnicas como el RT-PCR6,8,10.
El Quindío es un departamento hiperendémico para esta enfermedad lo cual hace necesario realizar su caracterización y su diferenciación de otros eventos clínicos con sintomatología semejante.
MetodologíaTipo y diseño de estudioSe realizó un estudio descriptivo de corte transversal entre enero y julio de 2013, donde se incluyó a personas que consultaron por cuadro febril agudo, con o sin ictericia, con temperatura superior a 37,5°C y con cualquiera de los siguientes síntomas: dolor osteomuscular, ocular, hemorrágico y con diagnóstico médico presuntivo de infección por DENV, y se excluyó a aquellas con otras enfermedades, además de a aquellas que no aceptaron participar en el estudio. Las muestras se tomaron en varias instituciones de salud de 1.°, 2.° y 3.er nivel de atención del departamento del Quindío previo consentimiento informado. Además se recolectó información clínica de acuerdo con lo reportado tanto por el paciente como por el médico tratante.
ProcedimientosPrevio consentimiento informado, se realizó toma de sangre en tubo Vacutainer® (Becton Dickinson, NJ, USA) seco y con anticoagulante, se obtuvo información clínica-epidemiológica, mediante historia clínica y entrevista con el paciente.
Pruebas diagnósticasA todas las muestras se les realizó cuadro hemático, RT-PCR para serotipificacion del DENV empleando el protocolo descrito por Lanciotti y modificado por Rosario11,12. Se realizaron pruebas de función hepática (transaminasas ALT, AST; bilirrubinas totales y diferenciales) por técnicas enzimáticas y colorimétricas, pruebas rápidas para dengue, leptospira, malaria y hepatitis B de la casa comercial SD BIOLINE®. Para el diagnóstico de rickettsias se utilizó el estuche: IFA IgG Rickettsia, IFA IgM de Focus Diagnostics® (California). Además se realizó aislamiento viral por la técnica de recuento en placa.
Medición de citocinasEn los sueros de los pacientes, se midieron 12 citocinas (IL-1α, IL-2, IL-4, IL-5, IL-6, IL-8, IL-10, IL-12 (p40), IL-17α, TNFα, IFNγ, IFNα2) usando el estuche Milliplex Map Human Cytokine/Chemokine, EMD Millipore®.
Análisis estadísticosSe determinaron los porcentajes o errores estándares de la media (SEM), modelos de regresión logística entre todas las variables clínicas y los hallazgos de laboratorio con el fin de predecir cuál explica mejor determinada enfermedad. La determinación de normalidad se realizó mediante la prueba de D’Agostino-Pearson; a los datos no paramétricos se les realizó el test de Kruskal-Wallis y Mann-Whitney; se consideraron estadísticamente significativas cuando p fue menor a 0,05 con IC del 95% en todas las pruebas.
ResultadosSe captaron un total de 149 individuos con diagnóstico clínico de síndrome febril agudo y con sospecha de dengue. El 60% consultó en los primeros 5 días de inicio de los síntomas, principalmente consistentes en fiebre 97,9%, cefalea 58,1%, mialgias 51,3%, artralgias 47,3% y, con menor frecuencia hematemesis 4,7%, ictericia 4,1% y ascitis 1,41%.
De los 149 casos, 65 (43,6%) fueron positivos para dengue, 3 casos NS1 positivos, 2 casos NS1 e IgM positivos, un caso de IgM positivo, 3 casos de NS1 e IgG positivo, 4 casos de IgG positivo, 33 casos de IgG e IgM positivos, 19 casos de NS1, IgG e IgM positivos. En 17 casos se obtuvo amplificación por RT-PCR, encontrando los serotipos 2, 3 y 4. De los casos positivos para dengue, 43 casos (67,18%) se clasificaron como dengue sin signos de alarma (DESA), 15 casos (23,4%) como dengue con signos de alarma (DCSA) y 6 casos (9,3%) como dengue grave (DG). Además se determinaron 39 casos como infecciones secundarias en los pacientes clasificados como DSSA, 13 casos en los pacientes con DCSA; todos los pacientes con DG presentaron infección secundaria.
El 4,05% de las muestras fueron IgM positivas para Leptospira interrogans, 6,8% de las muestras fueron positivas para IgM contra rickettsias (5,4% contra Rickettsia rickettsii [R. rickettsii] y 0,67% contra R. typhi y un 0,67% de coinfección entre R. rickettsii y R. typhi), además se presentaron 3 casos de coinfección con DENV (IgM) y R. rickettsii y 2 casos de coinfección con DENV y R. typhi. Hubo un caso de malaria (0,67%) y un caso de hepatitis B (0,67%) y un 44,5% de los casos fueron no reactivos para las pruebas diagnósticas utilizadas.
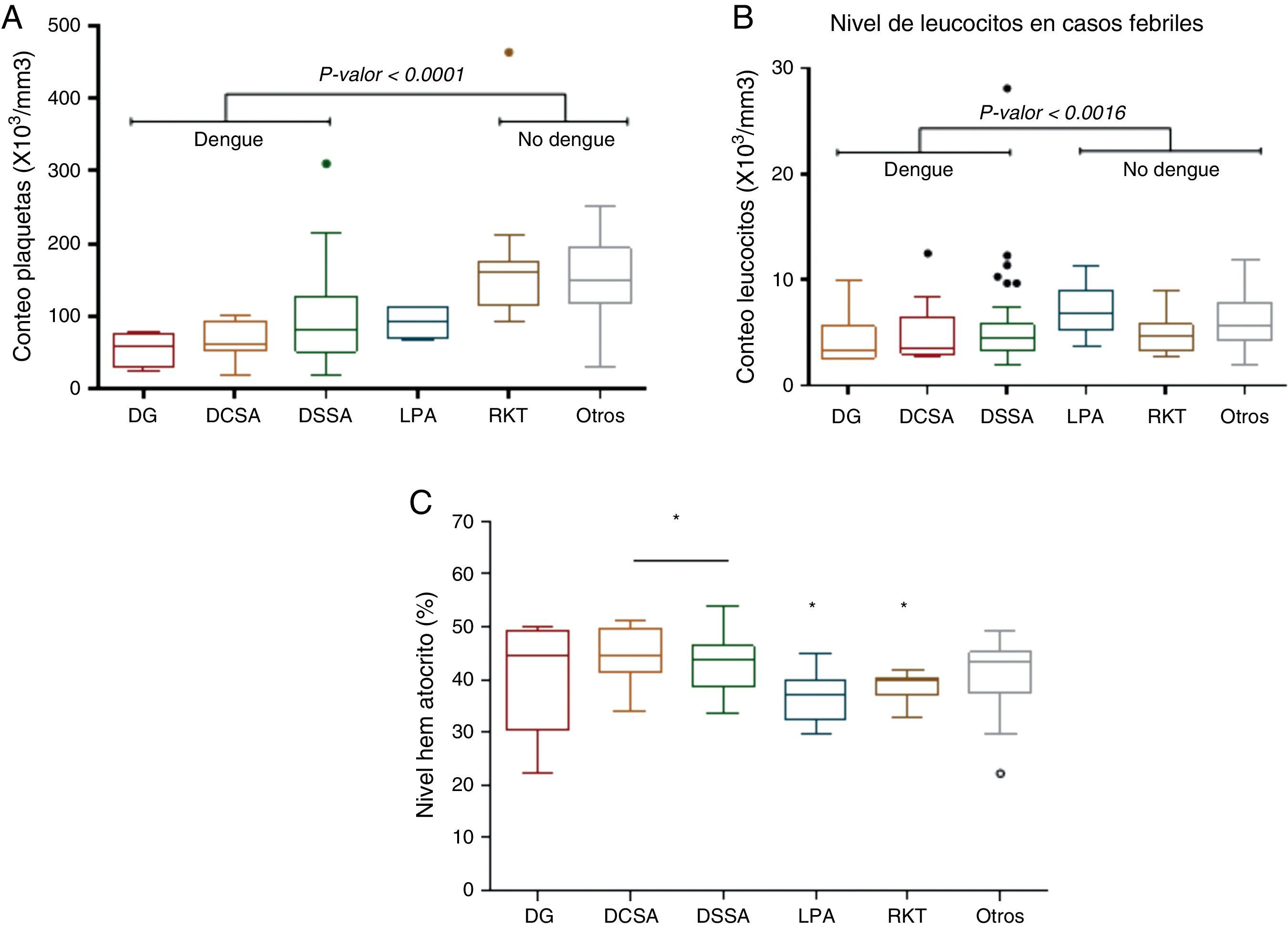
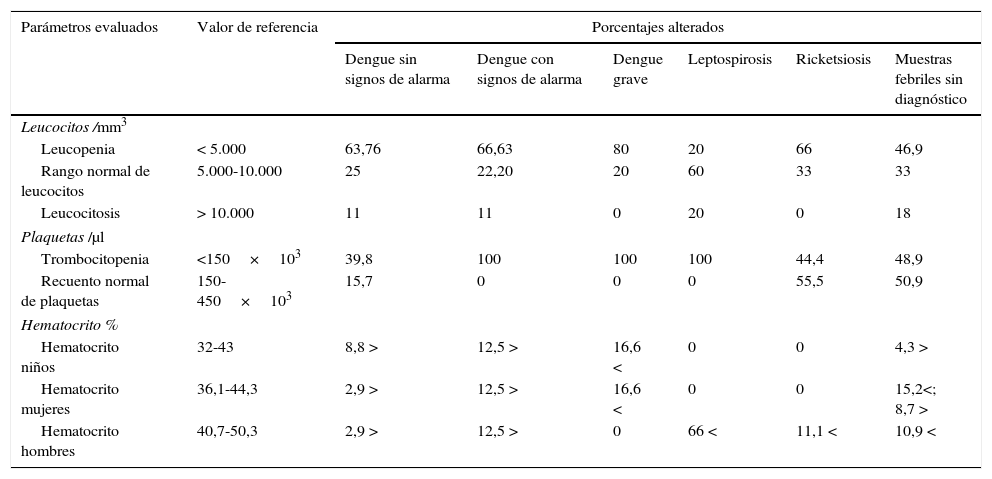
Cuadro hemáticoEn las diferentes formas clínicas de dengue se presentó trombocitopenia, observándose que todos los casos de DCSA (100%) y DG (100%) presentaron disminución de las plaquetas, igual que en los casos de leptospirosis (100%) y solo en un 44% en los casos de rikettsiosis. En los casos febriles negativos para las pruebas realizadas (CFN), el 49,1%, presentó trombocitopenia. La leucopenia se presentó, en el 20% de los casos de leptospirosis, un 66% en los casos de rickettsiosis, un 49% en los casos de CFN, un 63,8% de los casos de DSSA; 66,7% en los casos de DCSA y en un 80% en casos de DG. El aumento del hematocrito se presentó en el 13% de los casos de CFN, en el 14,6% de los casos de DSSA, en el 37,5% en los casos de DCSA y en un 33,2% de los casos de DG. Dos casos de DG presentaron hematocrito bajo, uno de ellos con comorbilidad con leucemia y lupus eritematoso sistémico. No se presentó hemoconcentración en los pacientes con leptospirosis y rickettsiosis (tabla 1).
Hallazgos en el cuadro hemático en pacientes con síndrome febril agudo con diagnóstico presuntivo de infección por el virus dengue. Quindío (Colombia) enero-julio de 2013
| Parámetros evaluados | Valor de referencia | Porcentajes alterados | |||||
|---|---|---|---|---|---|---|---|
| Dengue sin signos de alarma | Dengue con signos de alarma | Dengue grave | Leptospirosis | Ricketsiosis | Muestras febriles sin diagnóstico | ||
| Leucocitos /mm3 | |||||||
| Leucopenia | < 5.000 | 63,76 | 66,63 | 80 | 20 | 66 | 46,9 |
| Rango normal de leucocitos | 5.000-10.000 | 25 | 22,20 | 20 | 60 | 33 | 33 |
| Leucocitosis | > 10.000 | 11 | 11 | 0 | 20 | 0 | 18 |
| Plaquetas /μl | |||||||
| Trombocitopenia | <150×103 | 39,8 | 100 | 100 | 100 | 44,4 | 48,9 |
| Recuento normal de plaquetas | 150-450×103 | 15,7 | 0 | 0 | 0 | 55,5 | 50,9 |
| Hematocrito % | |||||||
| Hematocrito niños | 32-43 | 8,8 > | 12,5 > | 16,6 < | 0 | 0 | 4,3 > |
| Hematocrito mujeres | 36,1-44,3 | 2,9 > | 12,5 > | 16,6 < | 0 | 0 | 15,2<; 8,7 > |
| Hematocrito hombres | 40,7-50,3 | 2,9 > | 12,5 > | 0 | 66 < | 11,1 < | 10,9 < |
<: porcentaje de pacientes que presenta hematocrito menor al valor de referencia; >: porcentaje de pacientes que presenta hematocrito mayor al valor de referencia; 0: personas que no presentan alteración en el resultado (se encuentra en el valor normal).
Los niveles de aspartato-aminotransferasa (AST) presentaron valores alterados en un 90,2% de los casos de DSSA, en el 93,3% de casos de DCSA, en el 100% de los casos de DG, en el 100% de los casos de leptospirosis, en el 70% de los casos de rickettsiosis y en un 57,8% en los CFN. Los niveles de alanina-aminotransferasa (ALT) presentaron valores altos en el 53,6% de los casos de DSSA, en el 86,6% de los casos de DCSA, en un 83,3% en casos de DG, en un 50% en los casos de leptospirosis, un 20% y un 22,2% en los casos de rickettsiosis y CFN, respectivamente. Las bilirrubinas totales resultaron aumentadas en el 39,5% de los DSSA, en el 53,3% en DCSA, en un 83,3% de los casos de DG, además de en un 83,3% en los casos de leptospira, mientras que las infecciones ocurridas por rickettsias presentaron alteración en solo un 30%. Sin embargo, en los CFN un 46,2% de los casos presentó valores por encima del valor normal (VR: ≤ 1mg/dl). La proteína C reactiva (PCR) presentó valores altos en la mayoría de los casos, con porcentajes como el 61% en DSSA; 60% en DCSA; 50% en DG; 83,3% en casos de leptospira; 70% en casos de rickettsiosis y 66,7% en CFN.
El conteo de plaquetas, leucocitos y hematocrito además de las pruebas de función hepática, en los casos con diagnóstico de dengue frente a los casos con diagnóstico diferente a dengue, presentó diferencias estadísticas significativas cuando p fue menor que 0,05.
SintomatologíaLa sintomatología más común que se encontró en el síndrome febril agudo se describe en la tabla 2. Se observó diferencia significativa en cefalea, hiporexia, erupción, astenia, adinamia, epistaxis, dolor abdominal, dolor epigástrico, entre los casos diagnosticados como dengue, frente a las otras enfermedades febriles analizadas (p<0,05). Los casos de leptospirosis positivos muestran una mayor frecuencia de dolor lumbar e ictericia, mientras que en los casos diagnosticados como rickettsiosis no se observó diferencias significativas (p>0,05) en la sintomatología clínica analizada (tabla 3).
Signos y síntomas presentados en los casos con dengue y sin dengue
| Signos y síntomas | Dengue (n=64), n (%) | Sin dengue (n84), n (%) | p |
|---|---|---|---|
| Escalofríos | 11 (17) | 12 (14,2) | 0,6273 |
| Cefalea | 43 (67) | 12 (14) | <0,001 |
| Hiporexia | 22 (34) | 13 (16) | 0,0074 |
| Erupción | 25 (39) | 6 (7) | <0,0001 |
| Emesis | 17 (26,6) | 13 (16) | 0,0965 |
| Astenia | 39 (61) | 19 (23) | <0,0001 |
| Adinamia | 39 (61) | 20 (24) | <0,0001 |
| Dolor epigástrico | 12 (19) | 6 (7) | 0,0323 |
| Mialgias | 33 (52) | 45 (54) | 0,8084 |
| Artralgias | 32 (50) | 40 (48) | 0,774 |
| Dolor ocular | 18 (28) | 20 (24) | 0,5516 |
| Lumbalgia | 7 (11) | 6 (7) | 0,4191 |
| Epistaxis | 12 (19) | 6 (7) | 0,0323 |
| Tos | 5 (8) | 4 (5) | 0,4417 |
| Gingivorragia | 7 (11) | 5 (6) | 0,271 |
| Dolor abdominal | 27 (42) | 11 (13) | <0,0001 |
| Ascitis | 2 (3,1) | 1 (1) | 0,408 |
| Diarrea | 19 (30) | 15 (18) | 0,0901 |
| Melenas | 5 (8) | 5 (6) | 0,6551 |
| Hematemesis | 6 (9) | 1 (1) | 0,0201 |
| Ictericia | 2 (3) | 6 (7) | 0,2842 |
Las comparaciones realizadas fueron hechas por el test de chi-cuadrado, considerando una p < 0,05 como significativa.
Variables de importancia según resultado de la regresión logística (95% IC; p<0,05)
| Diagnósticos | |||
|---|---|---|---|
| Parámetro | Dengue/otras fiebres (p) | Leptospira/otras fiebres (p) | Otros fiebres/dengue y leptospira (p) |
| Erupción | 0,0009 | – | 0,0001 |
| Astenia | 0,0073 | 0,0006 | – |
| Lumbalgia | – | 0,0026 | – |
| Ictericia | – | 0,0194 | – |
| Dolor abdominal | 0,0023 | – | 0,0029 |
| Plaquetas | 0,0000 | – | 0,0001 |
| Hemoglobina | – | – | 0,0193 |
| Hematocrito | – | – | 0,0286 |
| ALT | 0,0023 | – | – |
| AST | – | – | 0,0004 |
| PCR | 0,0118 | – | – |
| Bilirrubinas totales | – | 0,0154 | – |
ALT: alanina aminotransferasa; AST: aspartato transaminasa; PCR: proteína C reactiva.
Se realizó PCR para determinar el serotipo de DENV, encontrando 14 casos de DENV2, 2 casos de DENV3 y un solo caso de DENV4, lo cual demostró cocirculación de 3 de los 4 serotipos de dengue.
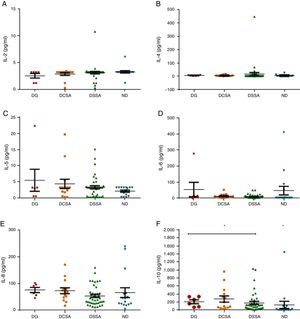
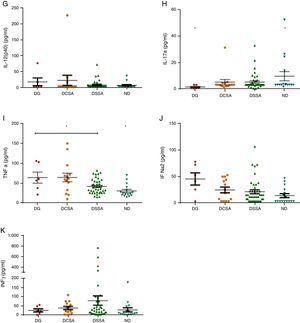
Medición de citocinasSe midieron 12 citocinas (IL-1α, IL-2, IL-4, IL-5, IL-6, IL-8, IL-10, IL-12 (p40), IL-17α, TNFα, IFNϒ, IFN α2), en los sueros de los individuos con diagnóstico de dengue, leptospira y rickettsias. Los niveles de IL-1α, 2, 5 e IL-17α fueron casi indetectables, con valores por debajo de 3,2pg/ml, sin diferencia significativa entre los casos, excepto en la IL-17α que presentó diferencia significativa en los valores en los casos de DG. Mientras que los valores de IL-4, 6, 8, 10, 12, TNFα, IFNα2 e IFNϒ, se incrementaron respecto al valor basal, pero solo se detectó diferencia significativa, entre los casos con diagnóstico de dengue y no dengue, en la IL-10 y TNFα, además, se observó que las IL-4 e IFNϒ se relacionaron con los casos de DSSA.
DiscusiónCuando el paciente consulta con síndrome febril los signos y síntomas que presentan son inespecíficos, por lo que es necesario determinar el agente causal mediante la utilización de diferentes pruebas diagnósticas, dado que muchos de los casos febriles pueden ser diagnosticados como dengue, especialmente en las áreas endémicas para esta enfermedad, lo que genera un aumento en la notificación de casos de dengue y la exclusión del diagnóstico de otros agentes infecciosos asociados al síndrome febril, lo que puede poner en riesgo la vida del paciente. En el presente trabajo, se encontró que la erupción cutánea, el dolor abdominal y la astenia se asociaban significativamente con el diagnóstico de dengue. Entre tanto, la lumbalgia y la ictericia se asociaron con diagnóstico de leptospirosis. Respecto a las enzimas hepáticas (ALT y AST), el valor de las transaminasas resultó hasta 5 veces más elevado con respecto a su valor normal en los casos de DCSA y DG y unas 4 veces en los casos de DSSA, similar a lo reportado por otros autores en diferentes partes del mundo13–15.
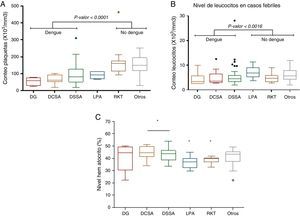
La trombocitopenia no presentó diferencias en las formas clínicas del dengue. Pero sí entre DG y DCSA frente a leptospira (p<0, 0147). Se ha descrito que la leptospirosis produce también una leve trombocitopenia, que es frecuente en las formas graves de la enfermedad, por lo que se debe tener en cuenta en casos de leptospirosis cuando haya recuento bajo16. Cuando se compararon los valores de plaquetas en los casos de dengue (incluidas todas las formas clínicas del dengue) y rickettsias, se observó diferencia significativa (p < 0,0001) al igual que los individuos clasificados como CFN (p < 0,0001). Premaratna et al. en 201117 encontraron que los conteos de plaquetas en infecciones con rickettsias son más bajos de lo normal, con una media de 128.000/mm3; sin embargo, la trombocitopenia no llega a ser marcada. En concordancia con estos datos, la media de plaquetas en los casos de ricketsias tuvo valores promedio de 185.200/mm3 (DE: 109.200), los cuales se encuentran dentro del rango normal y en los CFN fue de 163.200/mm3 (DE: 88.590), siendo la trombocitopenia un buen indicador de infección con dengue. Por otra parte, los valores de los leucocitos presentaron valores por debajo del rango normal en los casos de dengue, similar a lo reportado por Priyadarshini et al. en 201018, pero no se presentaron leucopenias marcadas, como lo propone la OMS/OPS (ver fig. 1).
Según Pizarro et al. (2009)19, la PCR se eleva ligeramente en casos de dengue y sus niveles son más elevados en pacientes con DG. Resultados similares se encontraron en este trabajo, respecto al aumento del valor del PCR en la mayoría de los casos, pero no se observó mayor aumento de esta proteína en los casos de DG como reporta Pizarro.
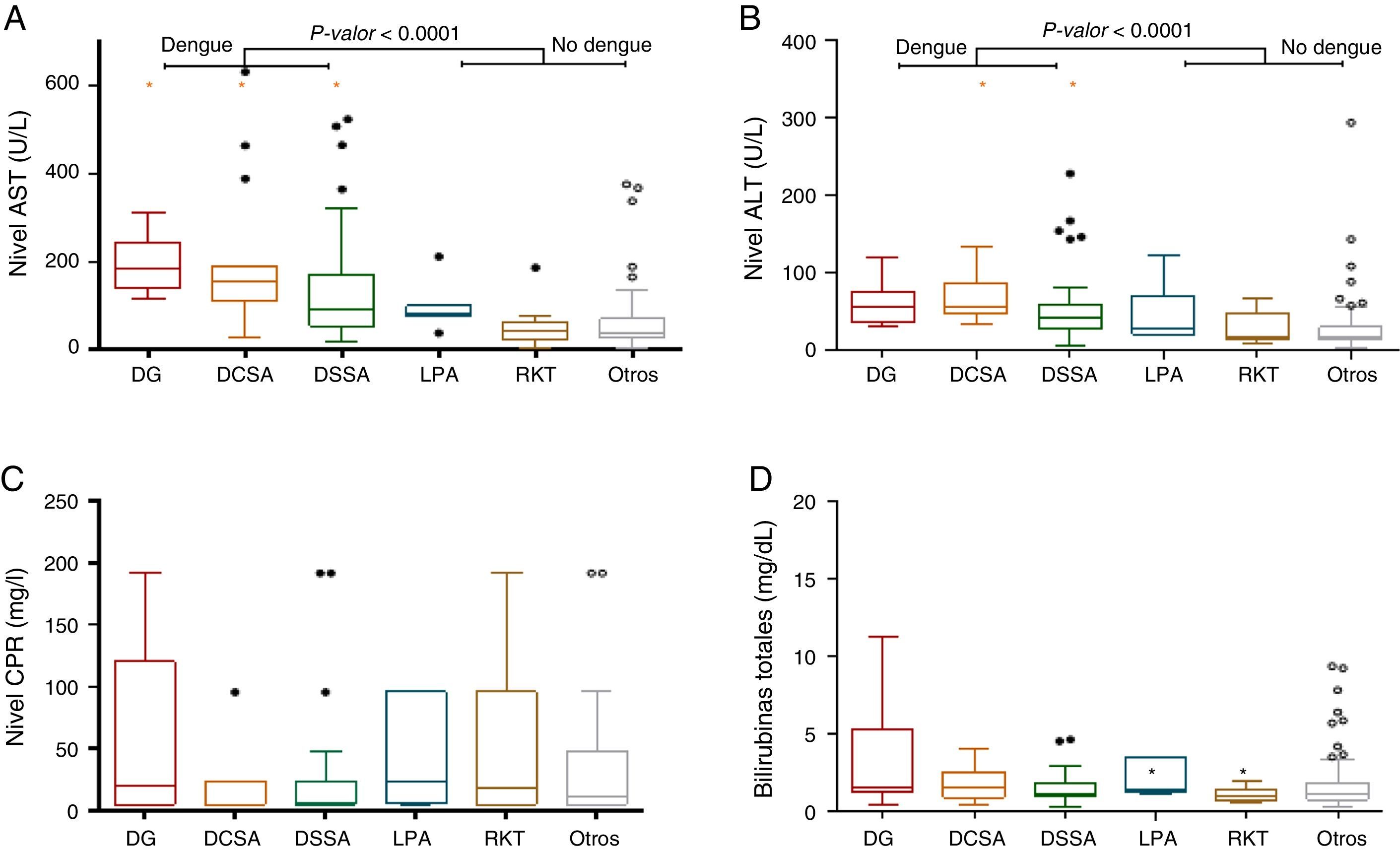
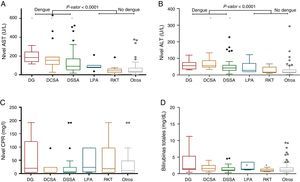
Los niveles de bilirrubina sérica en casos con dengue resultaron por encima de los valores de referencia, diferente a lo mostrado por Larreal et al. en 200520. En este estudio el comportamiento fue similar y muestra que, a medida que los casos se complican, los valores de la bilirrubina tienden a aumentar. Aunque no se encontraron diferencias estadísticas entre los tipos de dengue, sí se encontraron diferencias estadísticamente significativas en los casos con leptospira y rickettsias (p: 0,0136) (ver fig. 2).
Valores en caso de dengue (DCSA, DG y DSSA) y en casos de no dengue (LPA y RKT): A) de aspartato aminotransferasa (AST); B) de alanina aminotransferasa (ALT); C) de proteína C reactiva (PCR); D) de bilirrubinas totales.
DCSA: dengue con signos de alarma; DG: dengue grave; DSSA: dengue sin signos de alarma; LPA: leptospira; RKT: rickettsias y otros.
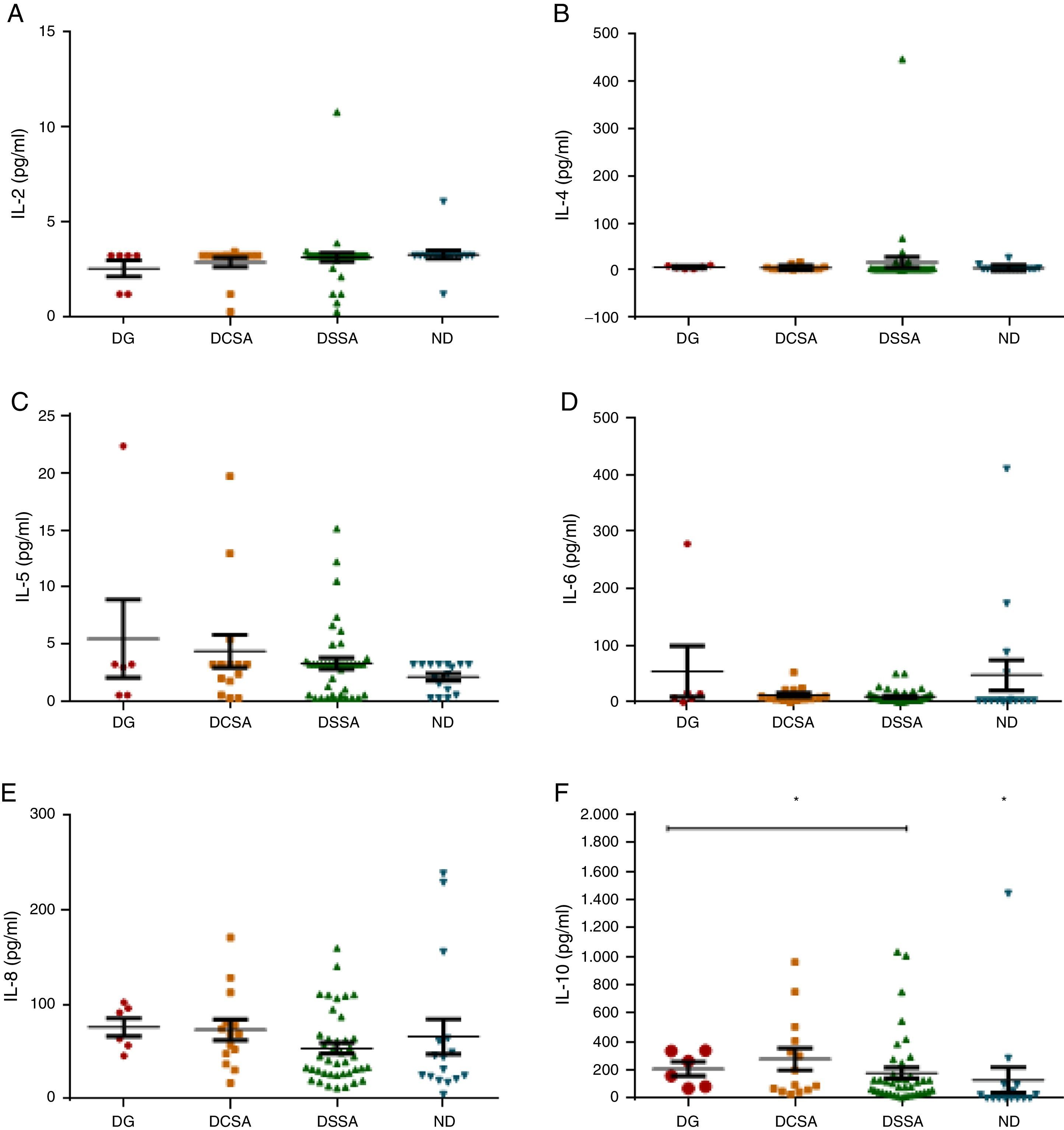
Respecto a las interleucinas, solo se observaron diferencias estadísticas entre los casos clasificados como dengue (DESA, DCSA y DG) y los casos clasificados como CFN en la IL-10 y TNFα, hallazgos que muestran un estado inflamatorio en el paciente, ya que estas son citocinas proinflamatorias que podrían influir en el desenlace grave de la infección por dengue. También se evidenciaron las diferencias estadísticas en la IL-17a, entre el grupo de DG con valores más bajos, frente a DSSA y DCSA y CFN. Contrarios a nuestros datos, Duran et al. en 2013 evidenciaron valores altos de esta interleucina, los cuales se han asociados a una regulación de la respuesta de los neutrófilos durante la infección por DENV21 (ver fig. 3).
Valores en caso de dengue (DCSA, DG y DSSA) y en casos de no dengue (LPA y RKT): A) de IL-2; B) de IL-4; C) de IL-5; D) de IL-6; E) de IL-8; F) de IL-10; G) de IL-12 (p40); H) de IL-17α; I) de TNFα; J) de IFNα2; K) de IFNγ.
DCSA: dengue con signos de alarma; DG: dengue grave; DSSA: dengue sin signos de alarma; IFN: interferón; IL: interleucina; LPA: leptospira; RKT: rickettsias y otros.
Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo.
FinanciaciónColciencias RC 416-2011 código 1115-545-31621.
Conflicto de interesesLos autores declaramos que no existe ningún conflicto de interés.
Al Dr. Juan Carlos Sepúlveda, del grupo de investigación infección e inmunidad, Universidad Tecnológica de Pereira.
A la enfermera jefe Nancy García, coordinadora del Servicio de Urgencias del Hospital San Juan de Dios de Armenia.
Al Hospital San Juan de Dios de Armenia.
Al Hospital del Sur de Armenia.
Al Hospital San Vicente de Paul Quimbaya.