Realizar una revisión sistemática de la literatura sobre la aparición de flebitis en niños, relacionada con catéteres venosos periféricos cortos.
MetodologíaSe buscó en las bases de datos PubMed, Scopus y Scielo, con los términos libres catéter venoso, infección, flebitis y sinónimos, sin límite de idioma, publicados en los últimos 10 años (desde las recomendaciones del CDC).
ResultadosDe un total inicial de 1.486 referencias, se seleccionaron 9 artículos que midieran la frecuencia de flebitis y su relación con el tiempo de permanencia del catéter. Estos fueron realizados en poblaciones heterogéneas, con diferentes definiciones de flebitis, y distintos desenlaces de interés; el tiempo de aparición de flebitis fue un desenlace secundario en todos.
DiscusiónA diferencia de los adultos, en niños no hay estudios encaminados a evaluar el tiempo adecuado de permanencia del catéter venoso periférico corto. Se requiere más investigación en este campo.
To carry out a systematic review of the literature on the occurrence of phlebitis related to short peripheral venous catheters in children.
MethodologyWe searched PubMed, Scopus and Scielo databases using venous catheter, infection, phlebitis and synonyms as free terms, no language restriction, in the last 10 years (since the CDC made its recommendations).
ResultsFrom an initial total of 1486 references, 9 measured the frequency of phlebitis and its relationship to the time of catheter placement. These studies were performed on heterogeneous populations, with varying definitions of phlebitis and various outcomes of interest. The time of occurrence of phlebitis was always a secondary endpoint.
DiscussionUnlike adults, in children there are no studies assessing the appropriate amount of time to maintain a short peripheral venous catheter. More research is needed in this field.
Los accesos más utilizados en la práctica clínica son los catéteres venosos periféricos cortos. Insertar un catéter venoso es un proceso invasivo que genera dolor, incomodidad y complicaciones, una de ellas la flebitis1–3. Aunque la incidencia de flebitis es relativamente baja, la frecuencia y cantidad de catéteres periféricos que son utilizados en la práctica clínica convierten a la flebitis en un problema serio4,5, con serias repercusiones económicas6–9.
En 2001, el CDC de Atlanta estableció que los catéteres venosos periféricos cortos debían ser cambiados entre 48 y 72 h luego de su inserción. Se basaron en un supuesto incremento de flebitis posterior a la hora 7210–12. Sin embargo, al mismo tiempo se publicaban estudios que no encontraron diferencias en la aparición de flebitis posterior a la hora 72. Por este motivo, en el año 2002 el CDC modificó su recomendación, ampliando el intervalo de cambio a entre las 72 y 96 h. Basados en nueva evidencia, en 2011 ratificó que un acceso venoso no se debe cambiar antes de la hora 72 si no está clínicamente indicado13. Se resaltó la falta de evidencia con respecto al riesgo en los niños, por lo que, en ellos, recomendó cambiar un acceso venoso solo cuando estuviera clínicamente indicado4. A diferencia de los adultos, en los niños no se ha demostrado que la duración del acceso venoso incremente el riesgo de flebitis4,14.
A pesar de la recomendación realizada por el CDC en el 2011, donde aplica el primum non nocere (primero no hacer daño) para los niños15, el número limitado de estudios y la falta de evidencia existente4 llevaron a la comunidad clínica a generalizar la práctica de cambio de los accesos venosos a las 72-96 h, tanto en niños como en adultos. En 2010, por ejemplo la Asociación Colombiana de Infectología recomendó cambiar los catéteres venosos periféricos a la hora 72, sin enfatizar en ningún grupo de edad, aunque resaltó que es una recomendación con baja evidencia científica16.
El propósito de este trabajo fue revisar la literatura científica publicada en los últimos 10 años para ver si hay nuevas evidencias sobre el tema.
MetodologíaRevisión de la literaturaSe realizó una revisión sistemática en las bases de datos PubMed, Scielo y Scopus; el tema central de la búsqueda fueron los accesos venosos periféricos y su relación con la flebitis. Los términos utilizados en la búsqueda, realizada en septiembre de 2014, son los siguientes:
- •
PUBMED: venous AND catheter AND infection AND children Limit: 10 years.
- •
Scopus: «venous catheter» AND «infection» AND «children» AND NOT «central catheter», Limit: 10 years
- •
Scielo: (cateter* OR catheter*) AND (flebit* OR phlebitis*).
Dado el propósito de buscar literatura reciente, se usó como límite los últimos 10 años; no se usaron límites de idioma. Dos miembros del equipo de investigación, de forma independiente, revisaron los resultados iniciales de PubMed, Scielo y Scopus (primero el título y el resumen, a continuación el texto completo) para evaluar la relevancia y para la posterior extracción de datos. Los desacuerdos se resolvieron por consenso de todo el equipo.
Criterios de inclusión y exclusiónSe incluyeron todos los estudios clínicos u observacionales, así como las revisiones sistemáticas y metaanálisis para esta síntesis cuantitativa de los datos. Se incluyeron solo trabajos publicados entre 2004 y 2014, realizados en menores de 18 años de edad a quienes se les insertara un catéter venoso periférico corto y se estudiaran las condiciones asociadas a la aparición de flebitis. Las medidas de resultado incluyeron incidencia de flebitis (expresado ya fuera en flebitis por 1.000 h/paciente, o tasa de flebitis por catéter, o por paciente) teniendo en cuenta los criterios utilizados en cada estudio para diagnosticarla, tiempo hasta el evento medido por cambio rutinario o por indicación clínica.
Se excluyeron los estudios en adultos y los relacionados con un tipo de catéter diferente al periférico corto (por ejemplo catéteres centrales); también aquellos cuyos datos no fueran analizables.
Extracción de datosEn primer lugar, 2 de los autores, por separado, realizaron una revisión por título y resumen de los artículos encontrados en cada una de las bases de datos, seleccionando los estudios potencialmente elegibles (o excluyendo los claramente irrelevantes). Las dudas se resolvieron por consenso de los 3 investigadores. Luego se elaboró una lista con los artículos preseleccionados; las referencias fueron revisadas en texto completo para identificar si cumplían los criterios para ser incluidos en el análisis, y se elaboró una planilla de extracción de información en Microsoft Excel. Se dejó explícita la razón para exclusión en esta fase.
Análisis de los datosSe resumieron los datos de análisis, particularmente para edad, tipo de catéter, duración, así como incidencia y definición de flebitis.
Evaluación de riesgo de sesgoSe evaluó de forma independiente la calidad metodológica de los estudios incluidos. Para identificar el riesgo de sesgo se consideró el método de selección de la muestra, intervención si la hubo, metodología, comparabilidad entre grupos, objetivo y resultados. Los desacuerdos se resolvieron por consenso.
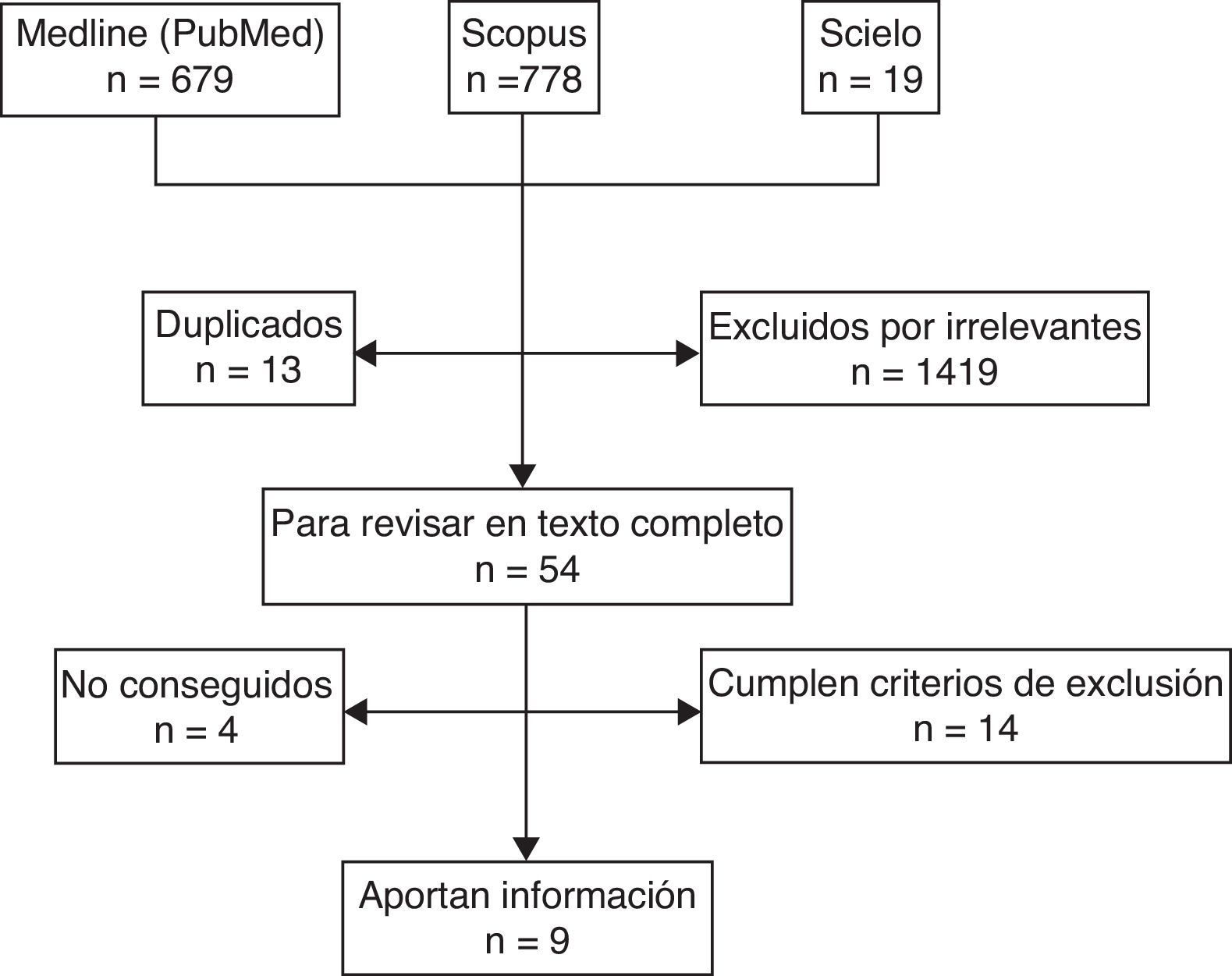
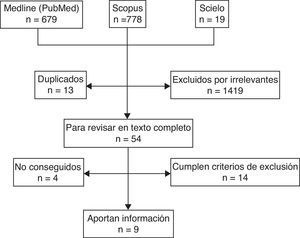
ResultadosDescripción de los estudiosSe identificaron 1.486 referencias a través de la búsqueda de la literatura; 1.419 fueron excluidas a partir del título o el abstract; 50 publicaciones fueron revisadas en texto completo; 41 artículos, excluidos por las siguientes razones: 22 artículos mencionaban un tipo de catéter diferente al periférico corto, 13 artículos tenían datos no analizables (cartas al editor), 6 artículos no especificaban población de estudio; del total de 41 artículos excluidos, 29 correspondían a estudio en adultos; finalmente 9 artículos aportaban información útil para el análisis (fig. 1).
Se identificaron 2 estudios realizados en unidades de cuidado intensivo con recién nacidos17,18; 2 estudios con pacientes entre un día de vida y 12 años de edad14,19; y 5 con pacientes entre 45 días de vida y 18 años de edad20–24. Estos 9 estudios se resumen a continuación.
Tripathi et al.14 realizaron un ensayo clínico aleatorizado, con 88 pacientes en un hospital de India, evaluando la efectividad de la utilización de lavados de heparina comparados con lavados con solución salina en catéteres periféricos, en pediatría. Hallaron que la sobrevida de los catéteres tiene una relación directamente proporcional, estadísticamente significativa (p ≤ 0,001), con la edad de los pacientes. Encontraron mejores resultados en los pacientes a los cuales se les realizó lavado con inyecciones de heparina (p ≤ 0,05). En cuanto a las complicaciones se evidenció una mayor incidencia en los pacientes de menor edad comparados con los de mayor edad. La incidencia de flebitis, a diferencia de los otros desenlaces, fue mayor en los pacientes a quienes se les administró heparina, así como en aquellos en los que se usaron cánulas de menor tamaño.
Barria y Santander17, en Chile, estudiaron 828 catéteres empleados en 75 recién nacidos con una edad gestacional promedio de 31,3±4 semanas, y con un peso de 1.169±849g. La mitad (52%) tuvieron bajo peso al nacer. Su objetivo fue comparar el catéter de vialon de poliuretano 24 G (595 catéteres, y 20.716 h/catéter) con el catéter mariposa de acero inoxidable 27 G (233 catéteres, 6.089 h/catéter). El estudio definió flebitis como la aparición de uno o más de los siguientes: dolor, sensibilidad, eritema, tumefacción, induración y cordón palpable; se reportaron 43 episodios de flebitis (32 con catéter vialon y 11 con mariposa). El remplazo por indicación clínica se llevó a cabo en 61 catéteres, de los cuales 5 presentaron flebitis (vialon 3/53 y mariposa 2/8), mientras el remplazo rutinario a la hora 72 se llevó a cabo en 767 catéteres, de los cuales 38 presentaron flebitis.
Barria et al.18 estudiaron a 74 recién nacidos chilenos de alto riesgo con el objetivo de comparar la efectividad de 2 métodos de acceso vascular. En el grupo de intervención (n=37) se utilizaron catéteres venosos centrales de inserción periférica (conocidos como PICC) con un remplazo rutinario a los 30 días y un total de 14.590 h/catéter. En el grupo control se insertaron catéteres periféricos, ya fuera de vialon o mariposa, con un remplazo rutinario a la hora 72, por un total de 12.749 h/catéter. Este estudio definió flebitis como sensibilidad a la palpación, eritema, tumefacción, o cordón palpable. A partir de esta definición identificaron 29 episodios de flebitis: 6 (10,8%) que correspondieron a catéter PICC y 23 (40,5%) a acceso venoso periférico corto.
El estudio de Nahirya et al.19 fue de corte transversal y fue realizado en 391 niños de uno a 12 años hospitalizados en salas de pediatría en un hospital de Uganda. Su objetivo fue determinar la prevalencia de flebitis, identificar microorganismos causales con su patrón de sensibilidad a los antimicrobianos, así como los factores asociados con las infecciones relacionadas con catéteres venosos periféricos. El estudio no especificaba duración de los catéteres, definición de flebitis o tratamientos recibidos. Solo se concluye que identificaron 77 episodios de flebitis (17%) y que los agentes más comunes fueron Staphylococcus aureus (57%) y Staphylococcus epidermidis (18%).
Boltá y Urreya-Ayal20, en España, estudiaron a 153 pacientes de diferentes servicios de pediatría, con una edad media de 4,6 años, para determinar la incidencia y factores asociados a la aparición de flebitis. La duración media de los catéteres fue de 5,2 (entre uno y 19 días). Se definió flebitis como cordón venoso, dolor local y eritema. Teniendo en cuenta este concepto, identificaron 17 (8,4%) pacientes con flebitis, que apareció, en promedio a los 7,7 días (185 h). El uso de antibióticos intravenosos fue el principal factor asociado con flebitis.
Jacinto et al.21, en Brasil, estudiaron a 338 niños entre un día de vida y 18 años (media 8,7 años) para identificar factores de riesgo para flebitis, relacionados con catéteres venosos periféricos cortos calibre 24 G y 22 G. Se identificó la flebitis mediante la valoración de la escala propuesta por Infusion Nurses Society Brasil (INS Brasil), donde cada categoría define una intensidad de flebitis: 0: no signos clínicos; 1: eritema con o sin dolor; 2: Dolor, eritema y edema; 3: dolor, eritema, edema, endurecimiento o cordón fibroso; 4: todas las anteriores más cordón>1cm con drenaje purulento. Teniendo en cuenta esta escala, identificaron 9 episodios de flebitis; el tiempo de permanencia fue de 32 a 216 h, con una media de 116,8 h. La flebitis se asoció con administración de medicamentos, así como con infusiones hiperosmolares o con pH extremo.
El estudio de Martins et al.22, también en Brasil, fue descriptivo, en niños entre los 45 días de vida y los 18 años, con el objetivo de identificar el perfil «flebitogénico» de diferentes fármacos. La duración promedio del tratamiento fue 7 días (168 h); a 19 pacientes se les identificó flebitis, que se presentó entre los días 3 y 5 de tratamiento. Concluyeron que todos los antimicrobianos estudiados poseen perfil flebitogénico (oxacilina, cefepime, vancomicina, cefuroxima, claritromicina, imipenem, penicilina cristalina, clindamicina, cefazolina).
El estudio de Weise23 es una revisión sistemática de la literatura cuyo objetivo fue evaluar el efecto de los filtros en la aparición de flebitis en los accesos venosos periféricos. Se incluyeron 11 artículos en el análisis, todos publicados antes de 1990, que difieren en las características de la intervención, en el tipo de filtro empleado y en la población objetivo. Los filtros se asociaron con menor riesgo de flebitis, aunque hay dudas sobre la solidez metodológica de los estudios. Solo 6 artículos presentan la duración del acceso venoso periférico y su indicación de cambio o retiro, y solo uno de ellos, publicado en el año 1976, fue en niños.
Una revisión sistemática de Cochrane liderada por Shah24, cuyo objetivo era determinar la efectividad de la heparina comparada con placebo en la duración de los catéteres periféricos en neonatos, identificó 10 estudios. Únicamente 5 de estos valoraron resultados de interés para el objetivo primario: 2 estudios mostraron un incremento estadísticamente significativo en la sobrevida de los catéteres al emplear heparina, 2 no encontraron diferencias significativas y uno evidenció disminución de la sobrevida de los catéteres, con un resultado estadísticamente significativo. Sin embargo, no se encontraron diferencias significativas en incidencia de flebitis o en infiltración. Teniendo en cuenta los resultados de los estudios, se concluyó que no hay evidencia concluyente para dar recomendaciones sobre el uso de heparina.
Con la excepción del estudio de Tripathi et al.14, que fue aleatorizado pero no enmascarado, los demás estudios son observacionales y con sesgos en la inclusión de pacientes. Aunque en los 9 estudios se registró el tiempo desde la inserción del catéter, en ninguno fue este el objetivo principal del estudio.
DiscusiónEl primer hallazgo importante de este trabajo es la escasa cantidad de literatura. En niños hay poca investigación sobre la asociación de flebitis y la duración de un catéter venoso periférico, lo que contrasta con los estudios en adultos, que han estudiado la relación de riesgo entre la duración del acceso venoso periférico y la aparición de flebitis13,25–35. En esta población adulta, los estudios que evalúan el riesgo de aparición de flebitis entre las 72 y las 96 h coinciden en recomendar un cambio por indicación clínica, ya que no encuentran diferencias en la incidencia de flebitis cuando se cambia un acceso ya sea por indicación clínica o por rutina27–29. El cambio rutinario puede ser injustificado y genera vulnerabilidad, costos y riesgos en el paciente6–9.
Las intervenciones realizadas en los niños han estado encaminadas a evaluar diferentes tipos de catéteres, de materiales, de calibres o de tipo de infusiones para evaluar su riesgo en los accesos venosos periféricos cortos. Todas las intervenciones se identifican como un factor de riesgo. El tiempo de duración del catéter, sin embargo, se evalúa como una variable secundaria en estos estudios, por lo que estos no permiten establecer recomendaciones de duración del acceso. Si a esto se agrega la heterogeneidad de las poblaciones estudiadas, las diferencias en tiempo de seguimiento e incluso las diferentes definiciones de flebitis, se incrementa la dificultad para sacar conclusiones.
Al igual que los estudios en adultos36, los aquí analizados coinciden en afirmar que la flebitis es prevenible mediante programas de control y vigilancia15,19,37–42. Algunos desarrollos recientes, como mejores medidas de prevención, vigilancia y control, mejores medios de asepsia y antisepsia, o el desarrollo de nuevos materiales plásticos han generado ahorro directo, así como menores tasas de complicaciones infecciosas (además de mayor comodidad e integridad para los pacientes)27,28,43,44. Ante la ausencia de evidencia, muchas guías recomiendan cambiar los accesos venosos periféricos según tiempos predeterminados (72 a 96 h), en vez de por indicación clínica, en los niños, sin tener en cuenta estos desarrollos y, además, asumiendo resultados obtenidos en estudios de adultos. Una consideración que parece no haberse tenido en cuenta es que el dolor de las venopunciones en los niños no solo es la principal causa de experiencias dolorosas en las hospitalizaciones pediátricas45–50 sino que acarrea consecuencias psicológicas mayores que en el adulto51.
Se plantea la posibilidad de posteriores estudios encaminados a evaluar la duración lineal del catéter venoso periférico en pediatría, más allá de la hora 96 de inserción, para determinar la seguridad en la duración del acceso venoso periférico corto.
En conclusión, la evidencia para responder a la pregunta de cuándo es recomendable cambiar los catéteres venosos en niños es escasa, anticuada, de pobre calidad metodológica o derivada de estudios en adultos. Antes de recomendar el cambio rutinario de un catéter, deben considerarse la edad del paciente, el medicamento que se esté infundiendo, la calidad de las prácticas locales de prevención de infecciones, los factores de riesgo del paciente, así como el sufrimiento que puede acarrear el procedimiento. Se necesitan más estudios, en la población pediátrica, para resolver esta importante inquietud.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.