La bacteremia por Staphylococcus coagulasa negativo (SCN) es una infección que actualmente genera significativa morbimortalidad dado el tipo de pacientes a los que afecta y el cambio en el perfil de susceptibilidad a los antibióticos.
ObjetivoDescribir características de los pacientes con aislamientos de SCN en sangre con CIM para vancomicina ≥2.
MetodologíaEstudio observacional descriptivo en pacientes hospitalizados ≥15años.
ResultadosDe 130 aislamientos, 38 (29,23%) tenían CIM para vancomicina ≥2. La mediana de edad fue de 54años y la razón hombre:mujer, de 1,37:1.
Las especies más frecuentes fueron: S. epidermidis (71,1%), S. haemolyticus (13,2%) y S. hominis (7,9%). El 44,7% tenían antecedentes de inmunosupresión, siendo las más importantes: neoplasias (28,9%), enfermedad reumatológica (5,2%) y VIH (2,6%). El 81,5% tenían accesos vasculares, el 97,3% antecedente de hospitalización previa y el 60,5% habían requerido manejo en la UCI. El 81,4% tuvieron exposición previa a antibióticos, y los más utilizados fueron: betalactámicos (78,9%) y vancomicina (50%). En el 2,6% se documentó endocarditis infecciosa.
De los aislamientos de SCN con CIM para vancomicina ≥2μg/ml, el 26,3% fueron sensibles a meticilina. Los principales tratamientos recibidos fueron: daptomicina (31,5%), vancomicina (21%), linezolid (15,7%) y betalactámicos (10,5%). Se utilizó terapia combinada en el 10,5%. La mortalidad general fue del 15,8%, y la mortalidad atribuible, del 33,3%.
ConclusiónUn porcentaje considerable de aislamientos tenían heterorresistencia para vancomicina. La bacteremia estuvo asociada con accesos vasculares, hospitalizaciones previas, tratamientos en cuidado intensivo y exposición previa a antibióticos. La inmunosupresión es la comorbilidad más importante, y la mortalidad es significativa.
Currently, coagulase-negative Staphylococcus (CNS) bacteremia is an infection that leads to significant morbidity and mortality given the type of patients affected and the recent changes in antimicrobial susceptibility.
ObjectiveTo describe the characteristics of patients with CNS blood isolates with vancomycin MIC≥2.
MethodologyDescriptive observational study on hospitalised patients ≥15years of age.
ResultsOf 130 isolates, 38 (29,23%) contained vancomycin MIC≥2. The median age was 54 years and the male:female ratio was 1.37:1.
The most frequent species were S. epidermidis (71.1%), S. haemolyticus (13.2%) and S. hominis (7.9%). Some 44.7% of patients had a history of immunosuppression, including: neoplasms (28.9%), rheumatologic disease (5.2%) and HIV (2.6%). Some 81,5% had vascular access; 97.3% had previous hospitalisations and 60.5% had required intensive care. A total of 81.4% of the patients had prior exposure to antibiotics and the most commonly used were beta-lactams (78.9%) and vancomycin (50%). Infective endocarditis was documented in 2.6%.
Of the CNS isolates with vancomycin MIC≥2, 26.3% were sensitive to methicillin. The main treatments received were: daptomycin (31.5%), vancomycin (21%), linezolid (15.7%) and beta-lactams (10.5%). Combined therapy was performed in 10.5%. The overall mortality was 15.8% and attributable mortality was 33.3%.
ConclusionA significant proportion of isolates were hetero-resistant to vancomycin. The bacteremia was associated with vascular access, previous hospitalisations, intensive care treatments and prior antibiotic exposure. Immunosuppression is the most important comorbidity and mortality is significant.
En décadas anteriores, los aislamientos microbiológicos de Staphylococcus coagulasa negativo (SCN) no eran centro de atención, pues la gran mayoría de casos eran considerados contaminación. A través del tiempo se les ha reconocido como causa importante de infecciones del torrente sanguíneo, especialmente en poblaciones inmunosuprimidas o pacientes con dispositivos médicos como accesos vasculares y prótesis, entre otros, que alteran las barreras naturales1.
Actualmente en los países desarrollados la gran mayoría de aislamientos microbiológicos intrahospitalarios en sangre son por cocos grampositivos, incluyendo los aislamientos por SCN, que se encuentran en los primeros 10 lugares2-4, y en algunos estudios es la primera causa de bacteremia nosocomial5.
Entre el 70 y el 80% de los aislamientos de SCN son causados por SCN resistentes a meticilina6, por lo cual se considera que el manejo empírico de primera línea sean los glucopéptidos (vancomicina y teicoplanina). Sin embargo, aunque es poco usual, también existen descripciones de surgimiento de SCN resistentes a vancomicina o con concentraciones inhibitorias mínimas (CIM) cada vez más altas, similar a lo descrito para S.aureus, lo que conlleva implícito pérdida de la actividad antibiótica in vivo de los glucopéptidos7. A este respecto, el estudio realizado por Fajardo Olivares et al.8 en unidades de cuidados intensivos (UCI) en España identificó los aislamientos en sangre de SCN, y al hacer análisis de sensibilidad a los diferentes antibióticos encontró que en el 61% de los casos había pérdida de la sensibilidad a vancomicina. De manera similar, Ahlstrand et al.9, en el estudio realizado en Suecia en pacientes con neoplasia hematológica, al realizar el análisis de los aislamientos de SCN durante 3 décadas encontraron que el 28,1% tenían una CIM para vancomicina ≥2mg/l. En Colombia no se encontraron reportes de bacteremias por SCN en adultos.
En nuestra institución, por ser un centro de referencia de alta complejidad, nos enfrentamos cada vez con mayor frecuencia a infecciones por SCN tanto de torrente sanguíneo como de otros sitios, y es ante la necesidad de conocer las características clínicas y microbiológicas en nuestra institución y en nuestro medio que el grupo de investigación GIERI decidió realizar un estudio sobre las características demográficas, microbiológicas, clínicas y los desenlaces de los pacientes con aislamientos en sangre de SCN con CIM para vancomicina ≥2.
MetodologíaTipo de estudioEstudio observacional descriptivo en pacientes hospitalizados ≥15años con aislamiento en sangre de Staphylococcus coagulasa negativo (SCN) en el Hospital Pablo Tobón Uribe (HPTU), en un periodo de tiempo de 26meses.
PoblaciónSe incluyeron pacientes mayores de 15años, sin discriminación de sexo, con primer aislamiento microbiológico en sangre de SCN entre el 1 de enero de 2010 y el 29 de febrero de 2012, atendidos en el HPTU, centro de cuarto nivel localizado en la ciudad de Medellín, Antioquia, Colombia.
Se excluyeron los pacientes con aislamiento de SCN con CIM para vancomicina <2μg/ml o que no tenían en la historia clínica la información de las variables demográficas, clínicas, microbiológicas y desenlaces durante la hospitalización en la cual se realizó el aislamiento.
Recolección de datosLos pacientes con aislamiento microbiológico en sangre de SCN se identificaron en nuestra institución a través de la base de datos del software WHONET10. Se evaluó la historia clínica de cada uno de ellos para identificar las variables (demográficas, clínicas, microbiológicas y desenlaces), se incluyeron en el análisis solo los casos con primer aislamiento en sangre de SCN.
El laboratorio de microbiología del HPTU trabaja con el sistema VITEK®2 de la casa comercial Biomerieux. La metodología utilizada para definir la CIM es microdilución en caldo con las tarjetas AST-P577. Se confirmó la CIM para vancomicina como sensible, intermedia o resistente según el protocolo que sugiere el Clinical and Laboratory Standards Institute (CLSI)11. Los puntos de corte para clasificar la susceptibilidad (resistente, sensible o intermedio) de los SCN según las CIM se definieron acorde a las recomendaciones del CLSI 201211, y se evaluó la susceptibilidad a meticilina, vancomicina, clindamicina, trimetoprim sulfametoxazol, linezolid, rifampicina, tetraciclina, quinupristín, dalfopristín, tetraciclina y quinolonas.
Análisis estadísticoLas variables cuantitativas se expresaran como mediana y rango intercuartílico (RIQ) (P25-75). Las variables cualitativas, como frecuencias absolutas y relativas. Se utilizó el programa Microsoft Office Excel 2010.
La conducción de esta serie de casos fue orientada según las recomendaciones de Dekkers et al.12.
El protocolo de investigación fue aprobado por el Comité de Investigaciones y Ética en Investigaciones del Hospital Pablo Tobón Uribe.
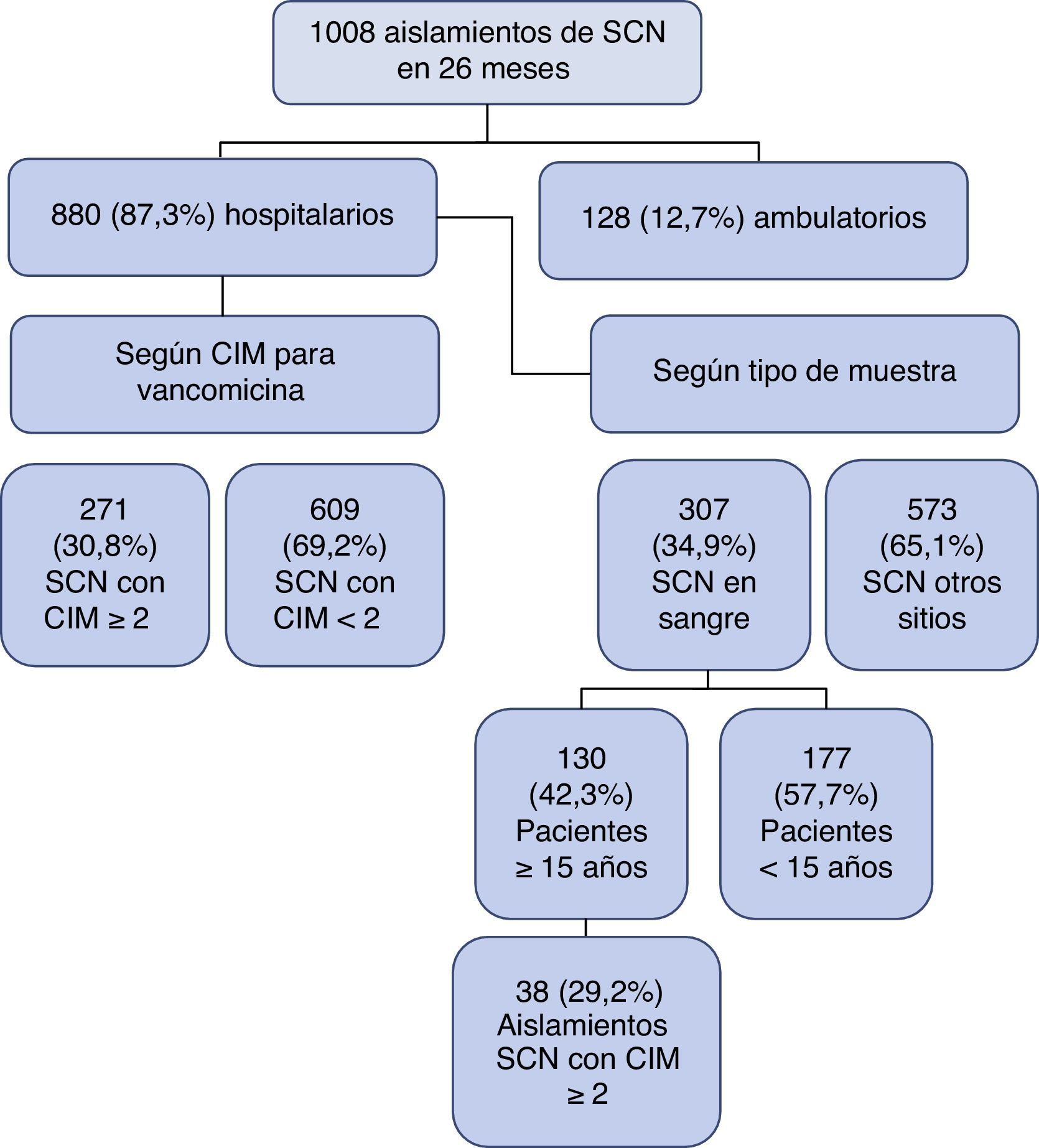
ResultadosOrigen y tipo de aislamientos de Staphylococcus coagulasa negativoEntre el 1 de enero de 2010 y el 29 de febrero de 2012 se identificaron en el HPTU un total de 1.008 aislamientos de SCN en cualquier muestra y cualquier edad (fig. 1), de los cuales las 3 especies más frecuentes fueron Staphylococcus epidermidis (541; 54%), Staphylococcus hominis ss. hominis (145; 14%) y Staphylococcus haemolyticus (103; 10%). De estos 1.008 aislamientos, 880 corresponden a pacientes hospitalizados, de los cuales en 271 (30%) la CIM para vancomicina fue ≥2μg/ml. De estos 271 aislamientos, 266 (98%) tenían CIM de 2μg/ml y 5 (2%) tenían CIM de 4μg/ml
De los 880 aislamientos de pacientes hospitalizados, se identificaron 307 (34,9%) aislamientos en sangre en pacientes de todas las edades; 130 (42,3%) de los aislamientos corresponden a pacientes ≥15años. De los aislamientos en ≥15años, 38 (29,2%) tenían CIM para vancomicina ≥2μg/ml, 100% de los casos con CIM=2μg/ml (fig. 1).
Aislamientos en sangre de Staphylococcus coagulasa negativo en pacientes hospitalizados ≥15añosDe los 130 aislamientos de SCN en sangre, las especies más frecuentes fueron S.epidermidis (68; 52%), S.hominis ss. hominis (30; 23%), S.haemolyticus (17; 13%), S.warneri (3; 2,3%) y S.caprae (2; 1,5%) (tabla 1).
Aislamientos en sangre de Staphylococcus coagulasa negativo en pacientes hospitalizados ≥15años
| Microorganismo | Número de aislamientos | % |
|---|---|---|
| Staphylococcus epidermidis | 68 | 52,3 |
| Staphylococcus hominis ss. hominis | 30 | 23,1 |
| Staphylococcus haemolyticus | 17 | 13,1 |
| Staphylococcus warneri | 3 | 2,3 |
| Staphylococcus caprae | 2 | 1,5 |
| Staphylococcus cohnii ss. urealyticum | 2 | 1,5 |
| Staphylococcus lugdunensis | 2 | 1,5 |
| Staphylococcus saprophyticus ss. saprophytic | 2 | 1,5 |
| Staphylococcus capitis ss. capitis | 1 | 0,8 |
| Staphylococcus cohnii ss. cohnii | 1 | 0,8 |
| Staphylococcus simulans | 1 | 0,8 |
| Staphylococcus coagulasa negativo | 1 | 0,8 |
| Total | 130 | 100 |
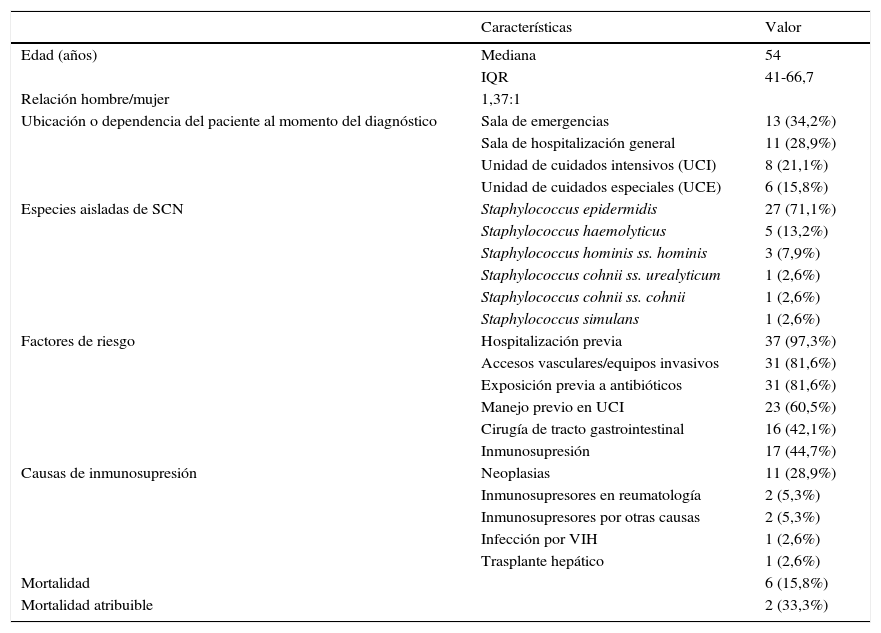
Las características generales de los pacientes con aislamientos de SCN con CIM para vancomicina ≥2μg/ml se muestran en la tabla 2. La mediana de edad fue de 54años RIQ (41 a 66,75), la relación hombre:mujer fue 1,37:1, la dependencia o área en donde el paciente se encontraba a la hora de la toma de la muestra fue: urgencias (13; 34,2%), salas de hospitalización general (11; 28,9%), UCI (8; 21,1%) y UCE (6; 15,8%); las 3 especies de SCN más frecuentes fueron S.epidermidis (27; 71,1%), S.haemolyticus (5; 13,2%) y S.hominis ss. hominis (3; 7,9%).
Características generales de pacientes hospitalizados ≥15años, con aislamientos en sangre de Staphylococcus coagulasa negativo o con CIM para vancomicina ≥2μg/ml (n=38)
| Características | Valor | |
|---|---|---|
| Edad (años) | Mediana | 54 |
| IQR | 41-66,7 | |
| Relación hombre/mujer | 1,37:1 | |
| Ubicación o dependencia del paciente al momento del diagnóstico | Sala de emergencias | 13 (34,2%) |
| Sala de hospitalización general | 11 (28,9%) | |
| Unidad de cuidados intensivos (UCI) | 8 (21,1%) | |
| Unidad de cuidados especiales (UCE) | 6 (15,8%) | |
| Especies aisladas de SCN | Staphylococcus epidermidis | 27 (71,1%) |
| Staphylococcus haemolyticus | 5 (13,2%) | |
| Staphylococcus hominis ss. hominis | 3 (7,9%) | |
| Staphylococcus cohnii ss. urealyticum | 1 (2,6%) | |
| Staphylococcus cohnii ss. cohnii | 1 (2,6%) | |
| Staphylococcus simulans | 1 (2,6%) | |
| Factores de riesgo | Hospitalización previa | 37 (97,3%) |
| Accesos vasculares/equipos invasivos | 31 (81,6%) | |
| Exposición previa a antibióticos | 31 (81,6%) | |
| Manejo previo en UCI | 23 (60,5%) | |
| Cirugía de tracto gastrointestinal | 16 (42,1%) | |
| Inmunosupresión | 17 (44,7%) | |
| Causas de inmunosupresión | Neoplasias | 11 (28,9%) |
| Inmunosupresores en reumatología | 2 (5,3%) | |
| Inmunosupresores por otras causas | 2 (5,3%) | |
| Infección por VIH | 1 (2,6%) | |
| Trasplante hepático | 1 (2,6%) | |
| Mortalidad | 6 (15,8%) | |
| Mortalidad atribuible | 2 (33,3%) |
CIM: concentración inhibitoria mínima; UCE: unidad de cuidados especiales; UCI: unidad de cuidados intensivos; SCN: Staphylococcus coagulasa negativo; VIH: virus de la inmunodeficiencia humana.
Respecto a las comorbilidades, se encontró de manera global que el 44,7% de los pacientes tenían causas de inmunosupresión. Dentro de estas, un paciente con virus de la inmunodeficiencia humana (VIH) (2,6%), un paciente trasplantado hepático (2,6%), 2 pacientes con enfermedad reumatológica en terapia inmunosupresora (5,3%), uso de inmunosupresores por otras causas en 2 (5,3%) y 11 pacientes con neoplasias (28,9%)
El uso de dispositivos o accesos vasculares invasivos (catéter venoso central, catéter central de inserción periférica y catéter arterial) previos o durante el aislamiento se encontró en 31 pacientes (81,6%). Como hallazgo llamativo, encontramos que 16 (42,1%) tenían antecedente de cirugía del tracto gastrointestinal. De los 38 pacientes, 37 (97,3%) tenían antecedente de al menos una hospitalización previa y 23 (60,5%) habían requerido manejo en la unidad de cuidados intensivos. En un paciente (2,6%) se documentó endocarditis infecciosa. La exposición previa a antibióticos se documentó en el 81,6% de los casos, y los antibióticos que con más frecuencia se utilizaron previamente fueron vancomicina (50%) y betalactámicos (78,9%). En el 52,6% de los casos se habían utilizado también otros antibióticos. Solo 7 (18,4%) pacientes no tenían antecedente de uso previo de antibióticos.
Los tratamientos instaurados para bacteremia fueron los siguientes: daptomicina, 31,6% (información de CIM en dos casos 0,94 y 0,125; sensibles acorde a las guías del CLSI); vancomicina, 21%; linezolid, 15,8%; betalactámicos, 10,5% (CIM para oxacilina ≤0,25μg/ml); trimetoprim-sulfametoxazol, 10,5% con CIM ≤10μg/ml, y el 10,5% recibieron terapia combinada con vancomicina más aminoglucósido (5,2%) y vancomicina más clindamicina (5,2%).
La mortalidad general fue del 15,8%, y en solo 2 (33%) fue atribuible a la bacteremia por SCN; estos pacientes venían en tratamiento con vancomicina. Los otros pacientes fallecieron por otras causas; dentro de estas, en el 33% la causa de la muerte fue sepsis por gérmenes gramnegativos. En el 33% de los casos la bacteremia por SCN estaba resuelta al momento de la muerte.
DiscusiónEl surgimiento de SCN como causa importante de infección hospitalaria es una realidad que impacta en la morbimortalidad de los pacientes. Los hallazgos microbiológicos de los países en desarrollo, como los nuestros, difieren significativamente a los de los países desarrollados; en estos últimos predominan las infecciones por gérmenes grampositivos y la resistencia a los antimicrobianos, especialmente a vancomicina, es mucho mayor a la que encontramos generalmente en países como el nuestro1-6. En nuestros países predominan las infecciones por gérmenes gramnegativos, y es en ellos donde tenemos el mayor problema de resistencia bacteriana6.
Del total de los aislamientos en sangre de SCN, identificamos que el 29,2% tenían CIM para vancomicina ≥2μg/ml, a diferencia de otros estudios descritos en la literatura mundial, donde se acerca a valores superiores al 60%8,9.
Las 3 principales especies de SCN con CIM para vancomicina ≥2μg/ml más frecuentes en nuestra serie fueron S.epidermidis (71,1%), S.haemolyticus (13,2%) y S.hominis ss. hominis (7,9%), porcentajes muy similares a los descritos en otros estudios8,13.
Las principales áreas o dependencias donde los pacientes se encontraban hospitalizados al momento del aislamiento microbiológico en nuestro estudio fueron la UCI y la UCE, con el 21,1 y el 15,8% de los casos, respectivamente; cifras inferiores a las reportadas en otros estudios, donde los aislamientos en la UCI son de alrededor del 40% de los casos8,14.
El antecedente de inmunosupresión, la hospitalización en la UCI y la presencia de catéteres han sido previamente descritos como variables relacionadas con aislamiento en sangre de SCN9,13,14, hallazgos similares a lo encontrado en nuestro estudio.
En esta serie encontramos que de los 130 pacientes con primer aislamiento en sangre de SCN, 32 (24,6%) fueron sensibles a meticilina, porcentaje similar para los 38 aislamientos con CIM para vancomicina ≥2μg/ml, donde el 26,3% fueron también sensibles a meticilina. Esto difiere de lo reportado por Cuevas et al.15, estudio español donde la resistencia a meticilina es del 32,5%, pero se asemeja a los reportes actuales en diferentes series y países, donde la resistencia es mayor al 70% y alcanza incluso valores tan altos como 90,2%6,8,16,17.
El porcentaje de aislamientos en sangre con CIM para vancomicina ≥2μg/ml en nuestra serie fue del 29,2%, menor al descrito en otros estudios en la población general5,6 y con mayor diferencia a lo descrito en poblaciones con enfermedad hematológica9.
Respecto a la sensibilidad de otros antibióticos en los aislamientos de SCN con CIM para vancomicina ≥2μg/ml, el 100% eran sensibles a linezolid, el 97,3% a quinupristín/dalfopristín, el 86% a rifampicina, el 55% a clindamicina, el 42% a ciprofloxacino y el 26,3% a meticilina, hallazgos muy similares a los descritos en otros estudios6,8,13,16,18. No se evaluó de rutina la sensibilidad a daptomicina; solo 2 pacientes cuentan con resultados y ambos son sensibles, pues es un antibiótico que recientemente ingresó a nuestro país.
Si tenemos en cuenta que la farmacocinética y la farmacodinamia en el tratamiento de los pacientes con bacteremia por SCN con CIM para vancomicina ≥2 ug/ml, es poco probable que la vancomicina alcance una AUC/MIC adecuada; adicionalmente, el uso de linezolid no se encuentra aprobado para bacteremia, y un 47,8% de los pacientes recibieron un manejo inadecuado.
Como limitantes inherentes a nuestro estudio tenemos varios elementos: a)ausencia de grupo de comparación; b)sesgos de selección; c)sesgos de medida, y d)la posibilidad de datos incompletos o no reportados en la historia clínica. Adicionalmente el número de aislamientos de SCN con CIM para vancomicina ≥2μg/ml fue pequeño. Sin embargo, nuestra serie nos permite aportar datos epidemiológicos al comportamiento de SCN en nuestras instituciones, identificar los factores de riesgo y comorbilidades asociadas, así como las posibilidades de tratamiento. La heterorresistencia o resistencia a vancomicina en nuestra población no es tan alta como la reportada en otras series y países.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran que no tienen conflicto de intereses ni recibieron dinero de ninguna institución. El Hospital Pablo Tobón Uribe ofreció al grupo investigador todo el apoyo logístico necesario para llevar a cabo la recolección de datos, análisis estadístico y elaboración del artículo de investigación.
Especial agradecimiento a los integrantes del Grupo de Investigación en Enfermedades Respiratorias e Infecciosas que participaron en algunas de las fases del estudio: Viviana M. Palacio Castaño, Luz E. Pérez Jaramillo, María A. Monsalve, Humberto Zapata, Melissa Mejía, Natalia Salazar Valderrama, Luisa Guarín H.