Entre las ventajas de la mamografía digital se destacan el amplio rango dinámico y la posibilidad de elaboración, elementos que permiten mayor precisión diagnóstica y reducción relativa de dosis. Sin embargo, el manejo posproceso esconde perlas y trampas relacionadas con la densidad mamaria: con este estudio se quisieron estimar las variables que condicionan el resultado final.
The wide dynamic range, as well the opportunity for image processing, are some of the major advantages of digital mammography, which leads to greater diagnostic precision and relative dose reduction. Nevertheless, posprocess handling hides pearls and pitfalls related to breast density. This study is aimed at estimating the variables that determine the outcome of posprocessing.
El contraste intrínseco en mamografía es muy bajo a causa de las limitadas variaciones de atenuación de la mama, que producen escaso número de niveles de gris. Incrementar el contraste significa incrementar el número de niveles de gris y mejorar la representación de las diferentes estructuras anatómicas. Viene en nuestra ayuda la tecnología digital con su amplio rango dinámico y la posibilidad de manipulación de la imagen por medio de algoritmos de proceso, características que, especialmente en el estudio de mamas densas, caracterizadas por una menor sensibilidad1 y especificidad2, se traducen en mayor precisión diagnóstica, además de en reducción relativa de las dosis.
El recurso al posprocesamiento puede tener sus efectos adversos, más evidentes a medida que se va «estresando» el método.
ObjetivosLa realización del presente estudio tuvo como objetivo la evaluación de los efectos de la manipulación posproceso y la definición de un umbral de confianza, necesario para evitar que el exceso de elaboración origine el deterioro de la imagen e incremente el riesgo de falsos negativos.
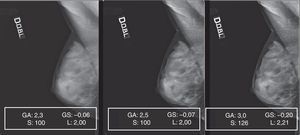
Materiales y métodoSe ha utilizado una consola de posproceso FUJI FCR (sw APL-B v5.1) con ajustes preestablecidos para una visualización optimizada, de acuerdo con los criterios de preferencia del centro. De los algoritmos de lectura disponibles se eligió la modalidad «fix», pues en esta condición el algoritmo define la conversión (lineal) entre el logaritmo de dosis y la escala de grises, dependiente de 2 parámetros determinables de forma manual: el parámetro latitud (L), determinante del intervalo de dosis (en mR) muestreado por el sistema en 4.096 niveles de gris (GL) (12 bit), y el parámetro sensibilidad (S), determinante del valor de dosis al cual corresponde un GL equivalente a 2.0483,4. Por lo tanto, para controlar el contraste y la densidad es necesario intervenir adecuadamente sobre los parámetros de exposición (kV y mAs)4,5. Para todas las exposiciones se fijó el valor L en 200.
En el sistema digital utilizado la curva densidad-exposición se puede variar arbitrariamente, dependiendo de los detalles anatómicos que se quieren evidenciar, y se caracteriza por 4 parámetros:
- -
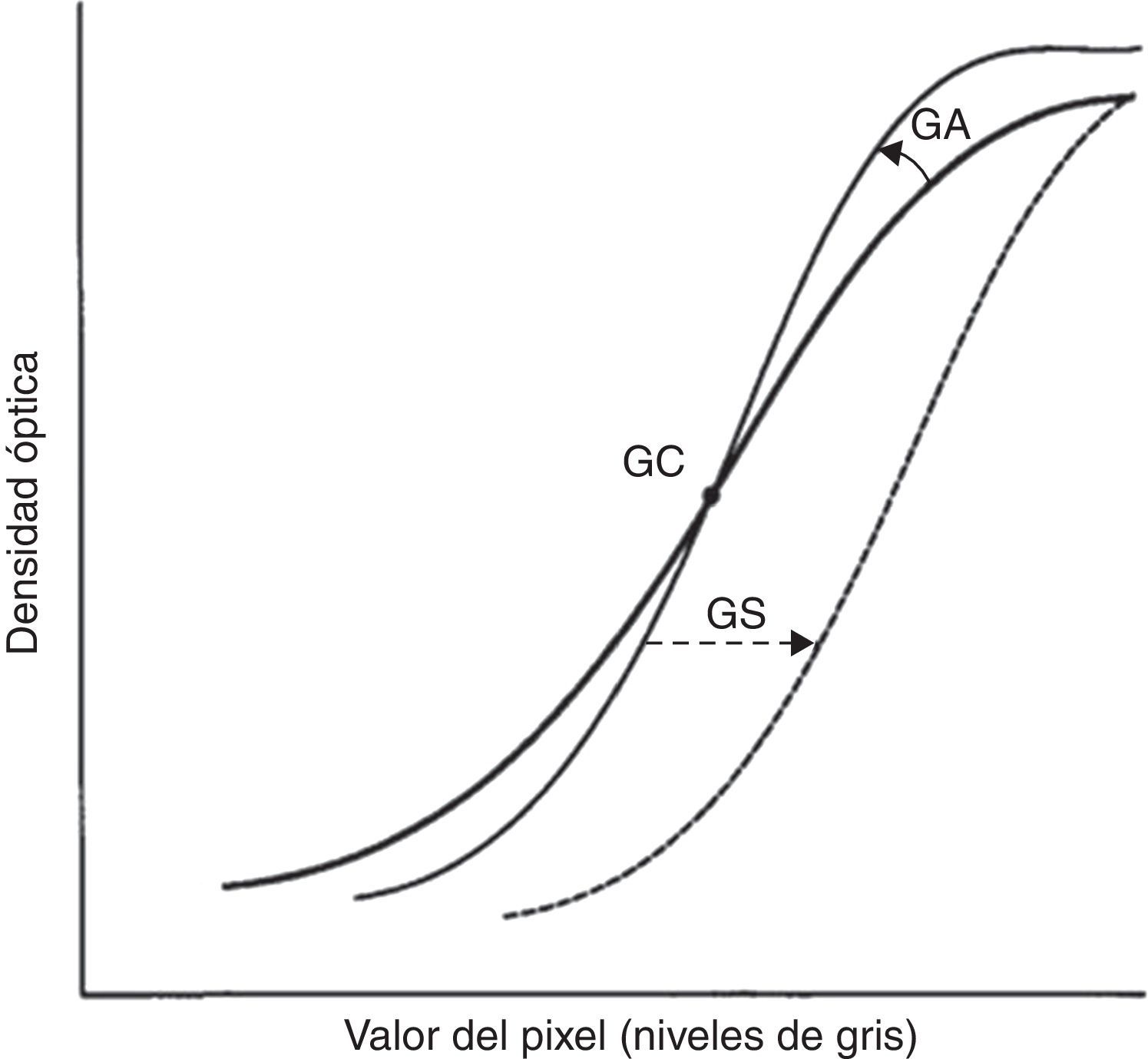
GT, que indica la forma de la curva seleccionada (fig. 1).
- -
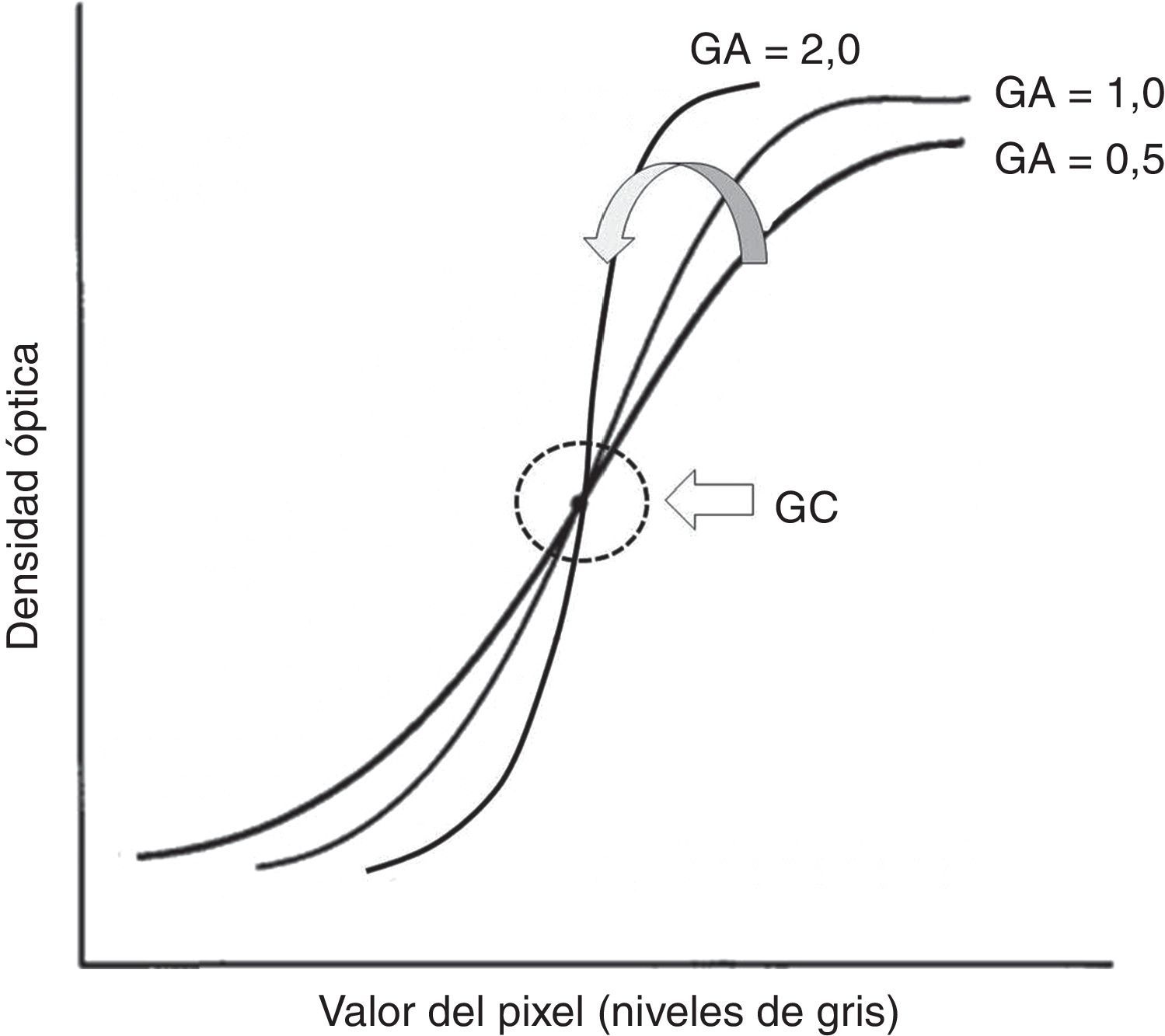
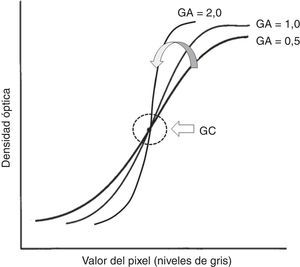
GC y GA, que controlan la pendiente de la curva de conversión GT elegida: GA define el grado de rotación con respecto a la curva elegida y GC determina el centro de la rotación. Al aumentar el GA, aumenta la pendiente de la curva y, por consiguiente, el contraste (fig. 2).
- -
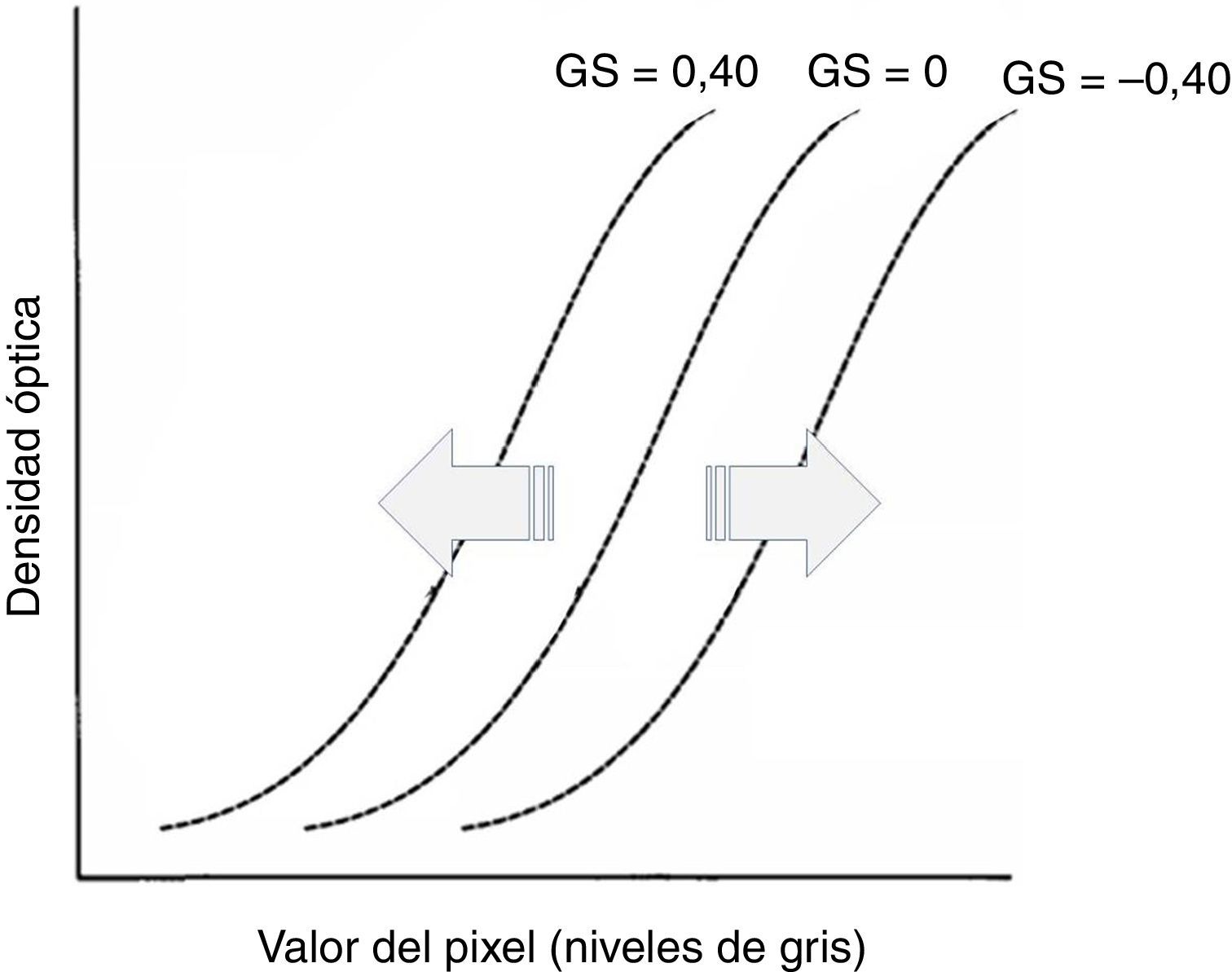
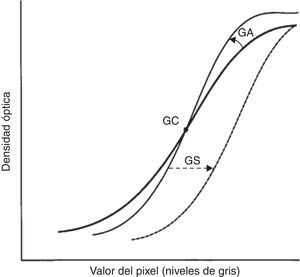
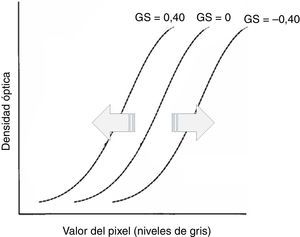
GS, que determina el desplazamiento de la curva GT a lo largo del eje de entrada de la señal. Su manejo (fig. 3) comporta un cambio global en la densidad de visualización de la imagen3.
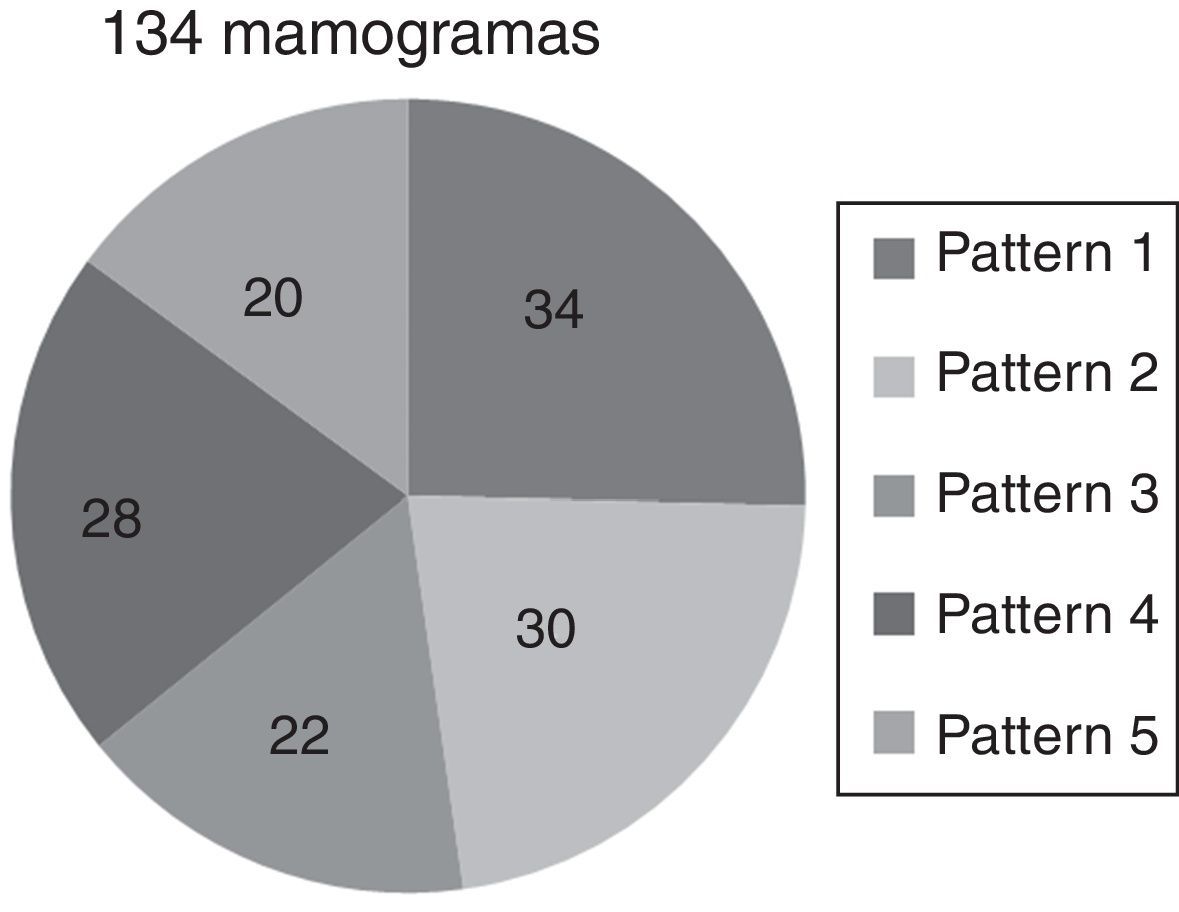
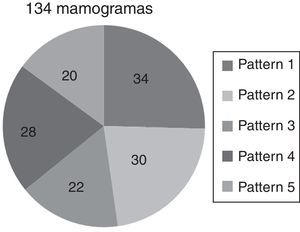
Se ha seleccionado un grupo de 134 mamogramas en proyección oblicua, distribuidos en 5 subgrupos de diferentes patrones parenquimales de acuerdo con la clasificación de Tabár6 (fig. 4), basada en la proporción de 4 elementos básicos que componen la anatomía normal de la mama (nodular, lineal, homogénea y radiolúcida), donde la mayoría de las densidades nodulares corresponden a las unidades terminales ductolobulillares (TDLU), las densidades lineales corresponden a ductos, vasos y tejido fibroso, las áreas radiolúcidas están relacionadas con el tejido adiposo, mientras las densidades homogéneas corresponden a tejido fibroso y aparecen como áreas de alta densidad que pueden ocultar estructuras subyacentes como las TDLU y los ductos con sus modificaciones6.
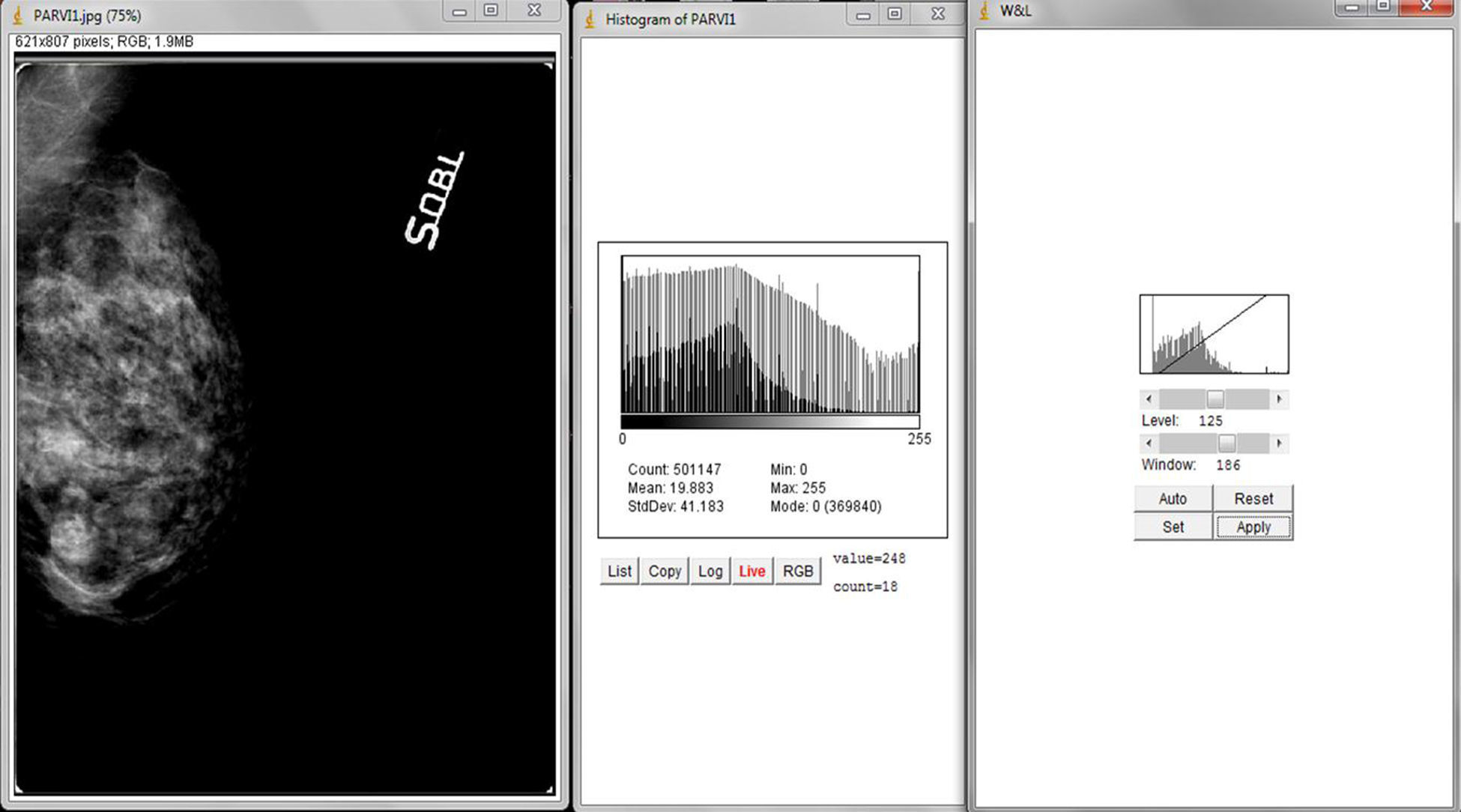
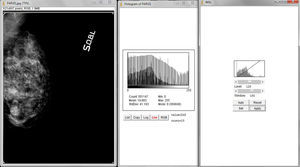
Tras haber efectuado pruebas de calidad de pantalla y de impresión utilizando el patrón SMPTE, se ha procesado cada mamograma mediante la aplicación de algoritmos apropiados y la corrección de curvas. Por último, utilizando el software ImageJ, se analizaron los histogramas pre- y posproceso para exceptuar pérdidas ocultas de informaciones anatómicas y de diagnóstico causadas por el efecto adverso del sobreprocesado.
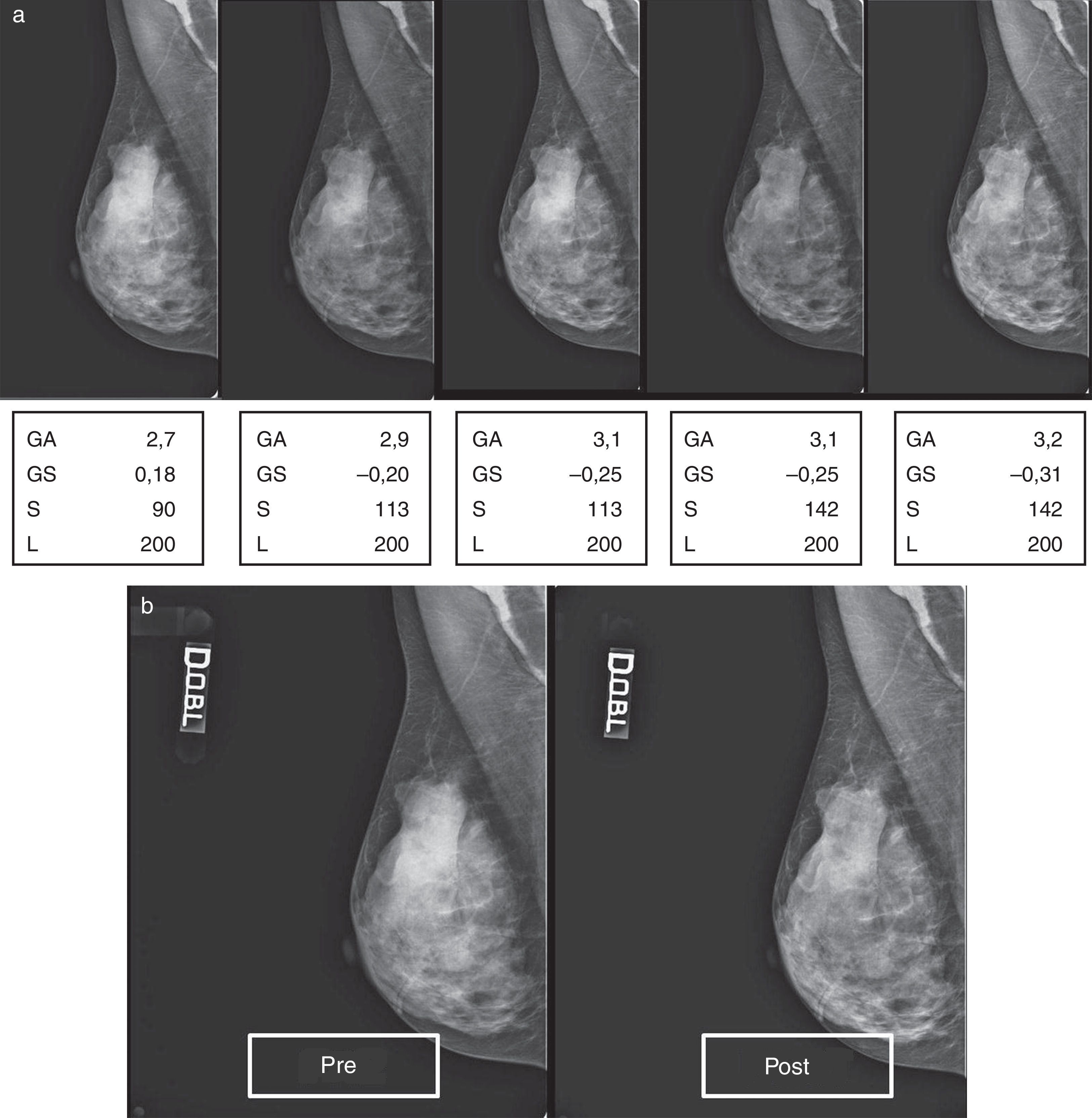
ResultadosPatrón 1: mama con densidad heterogénea; proporción equilibrada entre todos los componentes6Este patrón representa las mamas compuestas de tejido fibroglandular por un 50%. Eso quiere decir que el volumen está relleno por una mezcla de tejido adiposo y glandular, aunque solo una pequeña parte del volumen fibroglandular represente tejido mamario completamente opaco.
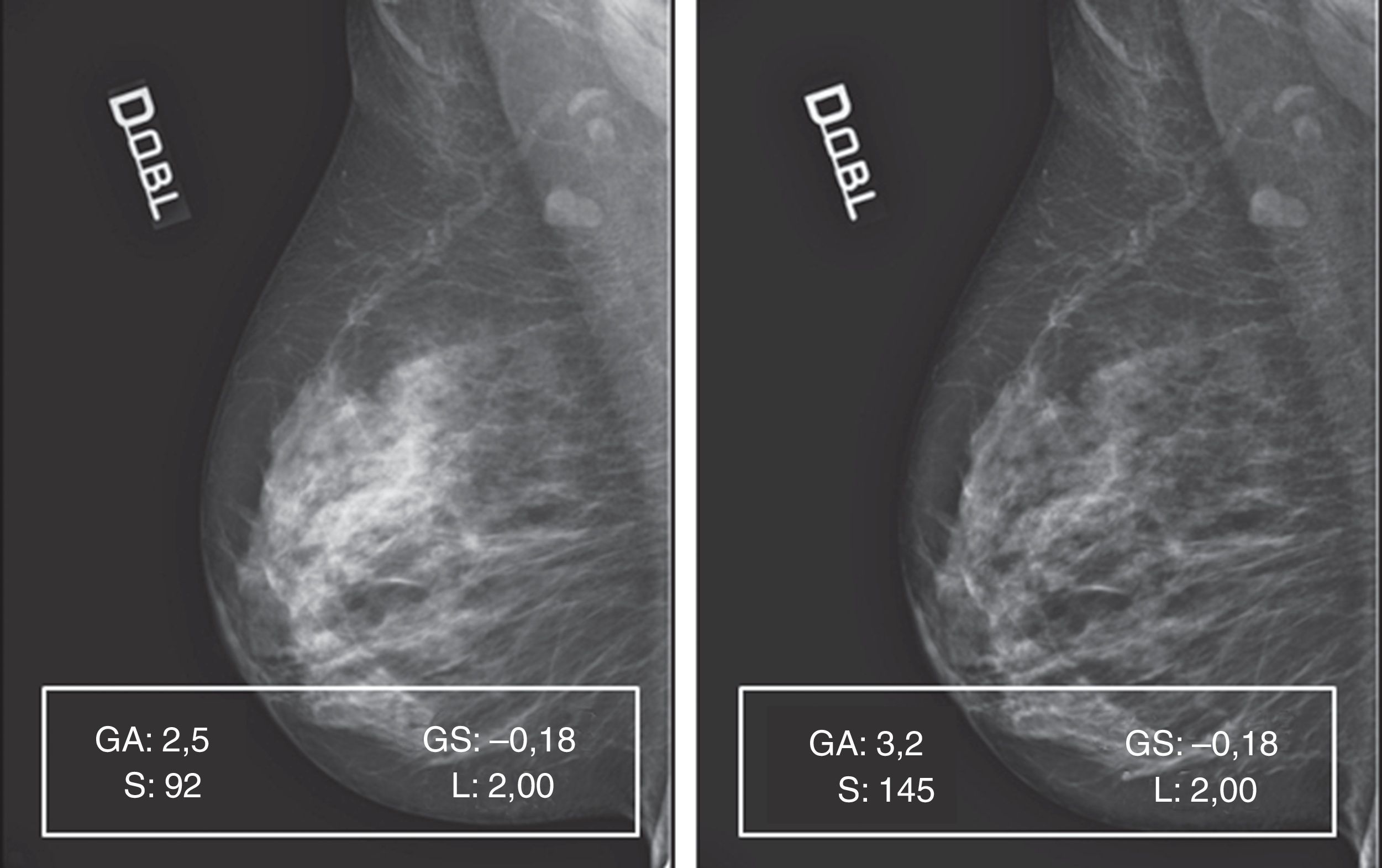
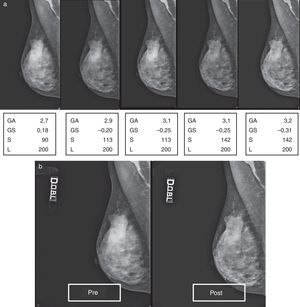
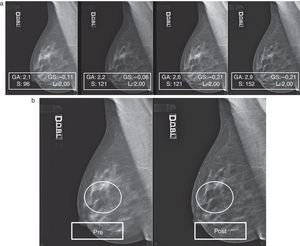
En la figura 5A está representada una secuencia de elaboraciones aplicadas a un mamograma con patrón 1, a partir de los valores de captura, que nos demuestra como, simplemente incrementando el valor de S y aportando oportunas correcciones de GA/GS, se supera gradualmente el límite puesto por la densidad, llegando a ver a través de ella (fig. 5B, pre- y posproceso) y, por tanto, mejorando la calidad.
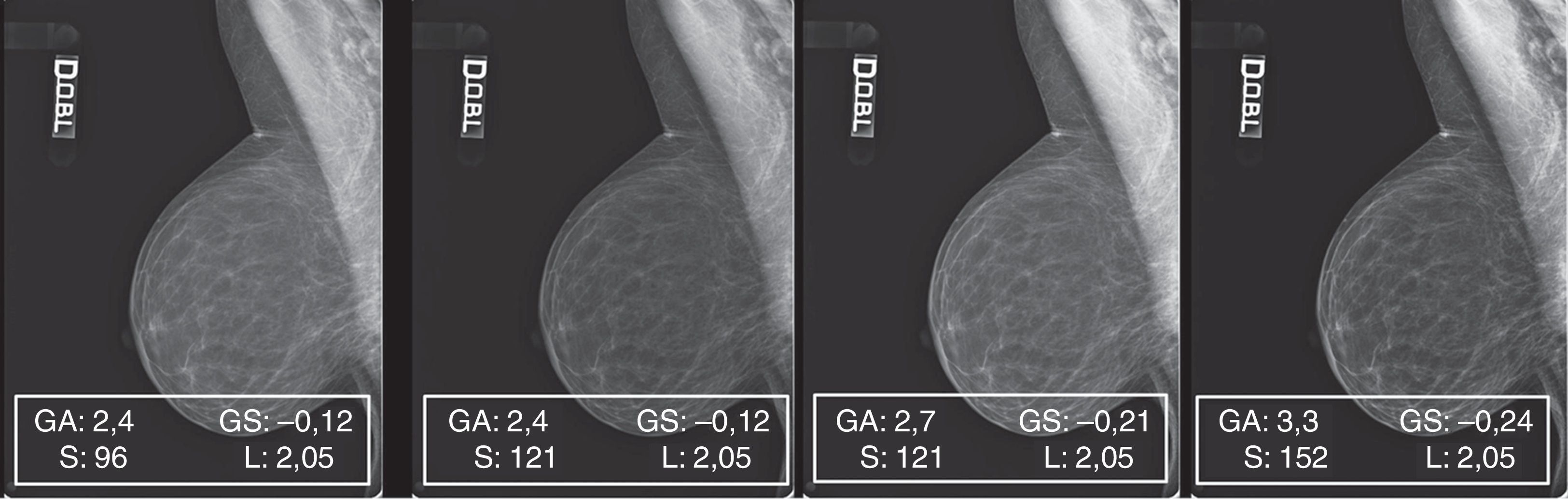
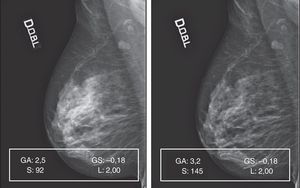
Patrón 2: mama fibroadiposa; preponderancia de tejido adiposo6Aunque con este patrón resulte más fácil la identificación de lesiones sospechosas, es muy importante que su representación en la pantalla tenga adecuado contraste, pues con un fondo adiposo los bajos contrastes pueden pasar desapercibidos, ya que la piel y las líneas trabeculares resultan ser relativamente brillantes7.
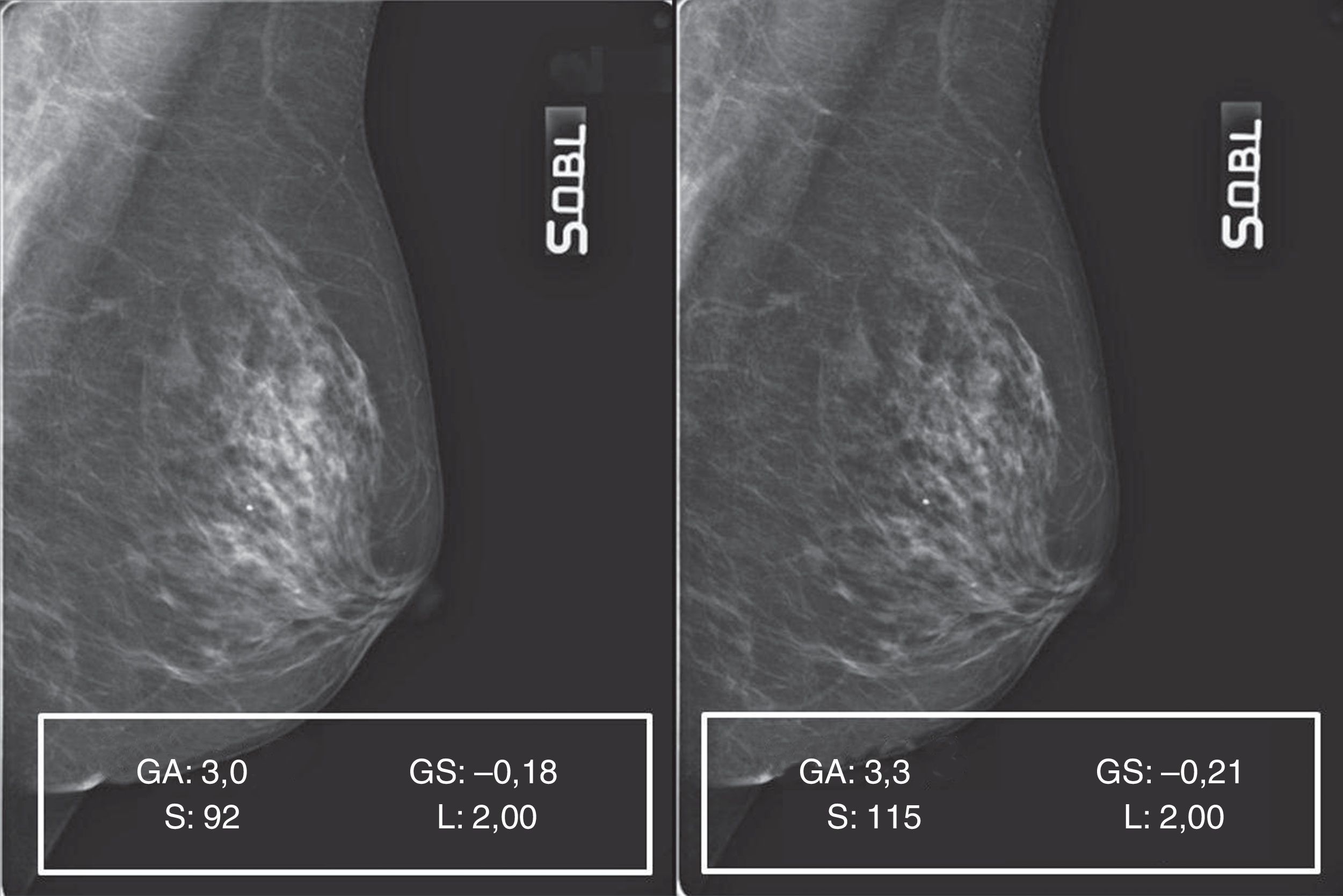
La elaboración de los 30 mamogramas representativos de este patrón siempre proporcionó buenos resultados (fig. 6).
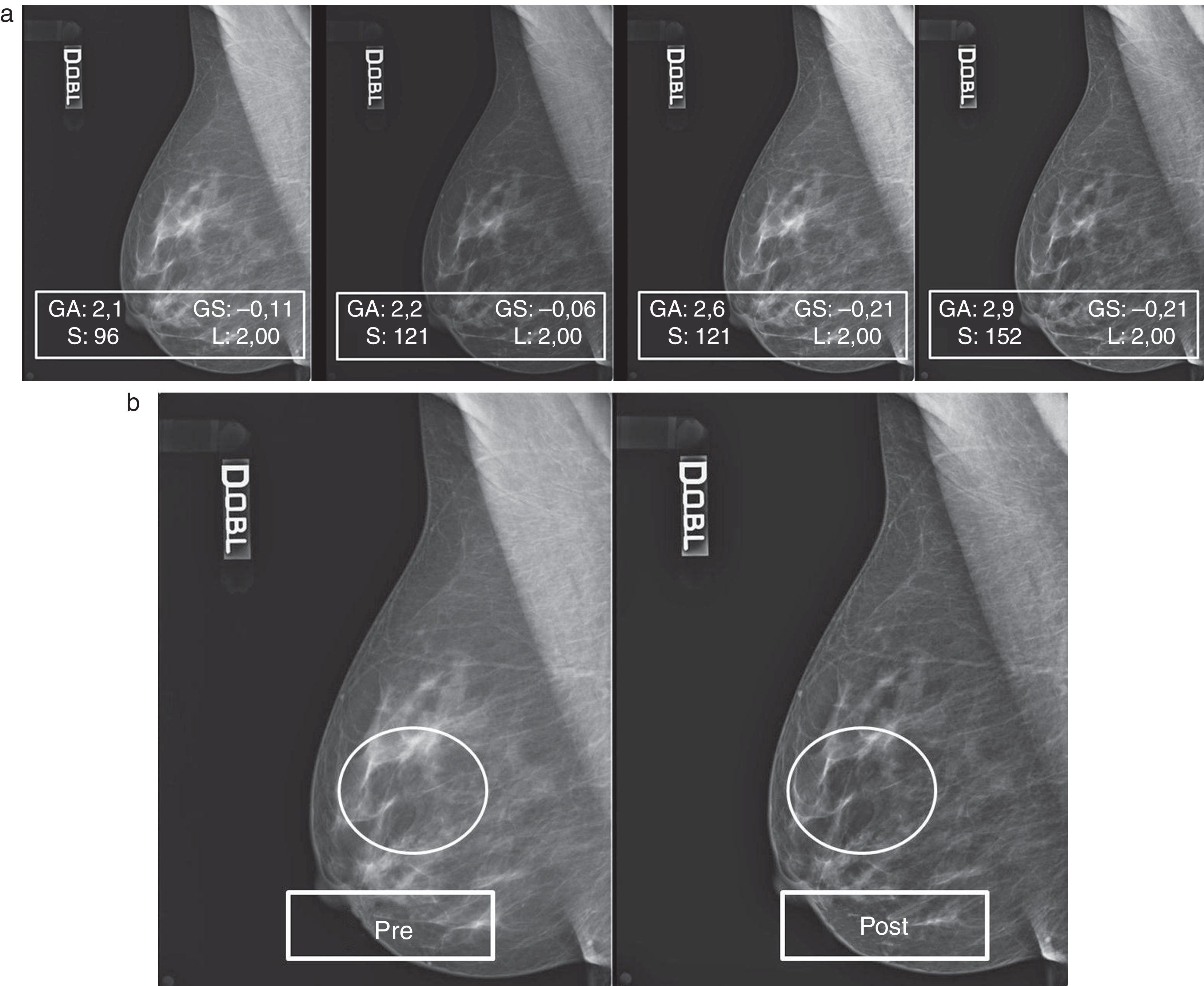
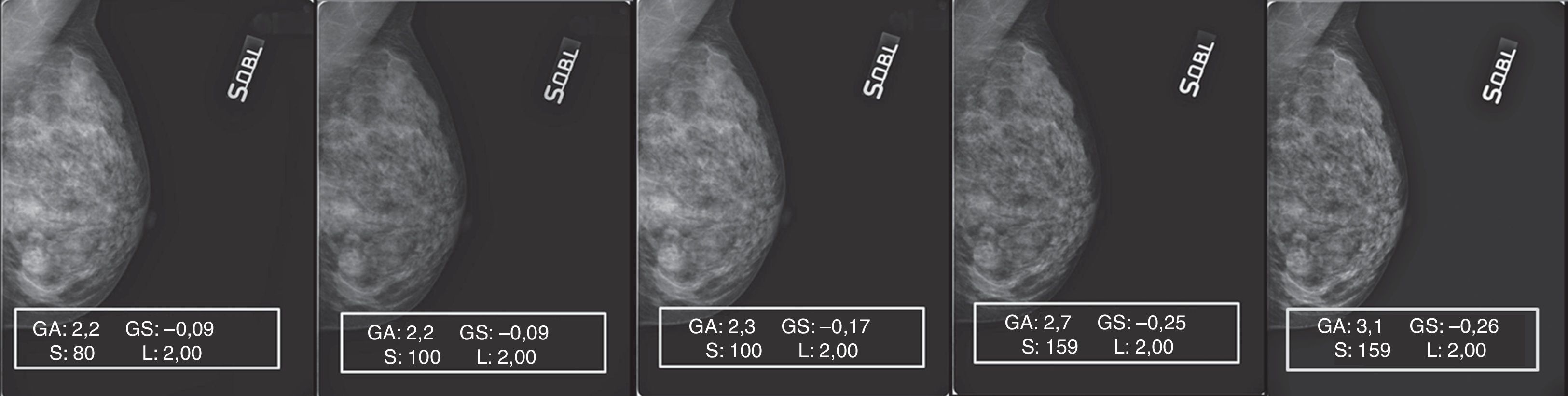
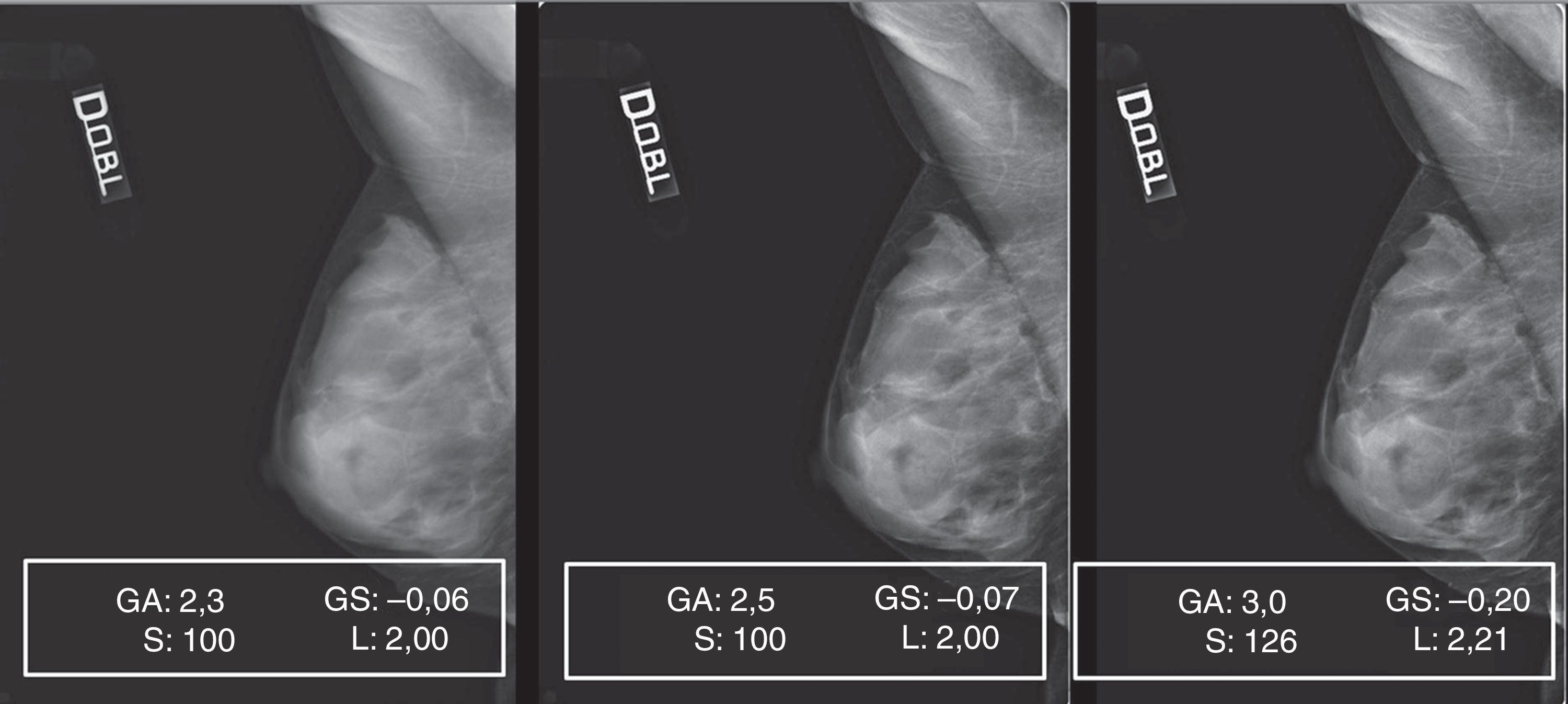
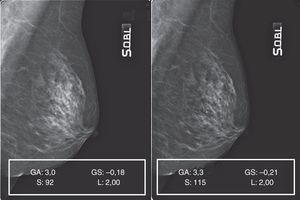
Patrón 3: mama fibroadiposa con parénquima residual6Este patrón, caracterizado por la difusión, o bien la concentración, de áreas de parénquima residual, planteó algunas dificultades de gestión del posproceso. De hecho, aunque el ajuste del valor de S y de GA/GS siempre fue gradual, paso a paso (fig. 7A), se encontraron a menudo repentinas pérdidas de detalles en los residuos glandulares superpuestos a las islas de tejido adiposo de sustitución. Aunque en este caso concreto el mamograma elaborado (fig. 7B) presente una calidad general mejor que el original y siga conservando su calidad diagnóstica, durante las elaboraciones se hicieron necesarias continuas correcciones de GA, GS y S para evitar el detrimento de la calidad integral y la pérdida de detalles anatómicos (figs. 8 y 9).
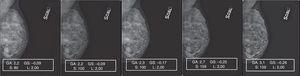
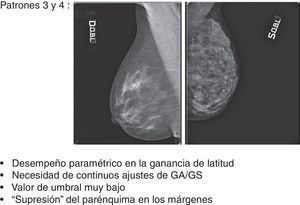
También la elaboración de los mamogramas de patrón 4 resultó muy difícil, a causa de la alternancia de múltiples pequeñas áreas de elevada densidad y de grasa, típica de la mama micronodular (fig. 10). En este caso, el incremento de los parámetros de elaboración lleva a la asignación de valores de gris próximos a 0 a los píxeles que representan las pequeñas lagunas adiposas («efecto sobrexposición» de la grasa) con el consecuente «efecto supresión» de los márgenes de los micronódulos, enfatizado con la aplicación del filtro edge enhancement (artefacto de blooming)8,9.
Patrón 5: mama densa6Inesperadamente, la gestión del posproceso de los patrones 5, gracias a la escasa presencia de tejido adiposo infraparenquimal (fig. 11), ha resultado ser la que más permitió la alteración de parámetros de elaboración dentro de un rango muy amplio, sin riesgo de perder información, consintiendo la visualización de estructuras ocultadas por la elevada densidad parenquimal.
Este es un importante resultado, ya que está ampliamente aceptada la relación entre riesgo de cáncer y densidad del tejido mamario10–13 y además está probada la escasa contribución de la segmentación automatizada en la detección de lesiones en mamas densas14,15. Cabe destacar que la elevada densidad disminuye la visibilidad de las lesiones y el retraso en el diagnóstico de cáncer de mama se mantiene entre los principales errores en las reclamaciones por mala práctica radiológica16. De estas, en EE. UU., casi el 70% se refieren a mujeres con menos de 50 años de edad, que representan el 78% del total de las indemnizaciones17.
Observando los valores preproceso de todos los mamogramas elaborados, se nota que el factor recurrente, concomitante con la aparición de efectos adversos relacionados con el cambio de valores de GA/GS, es un valor de S muy elevado.
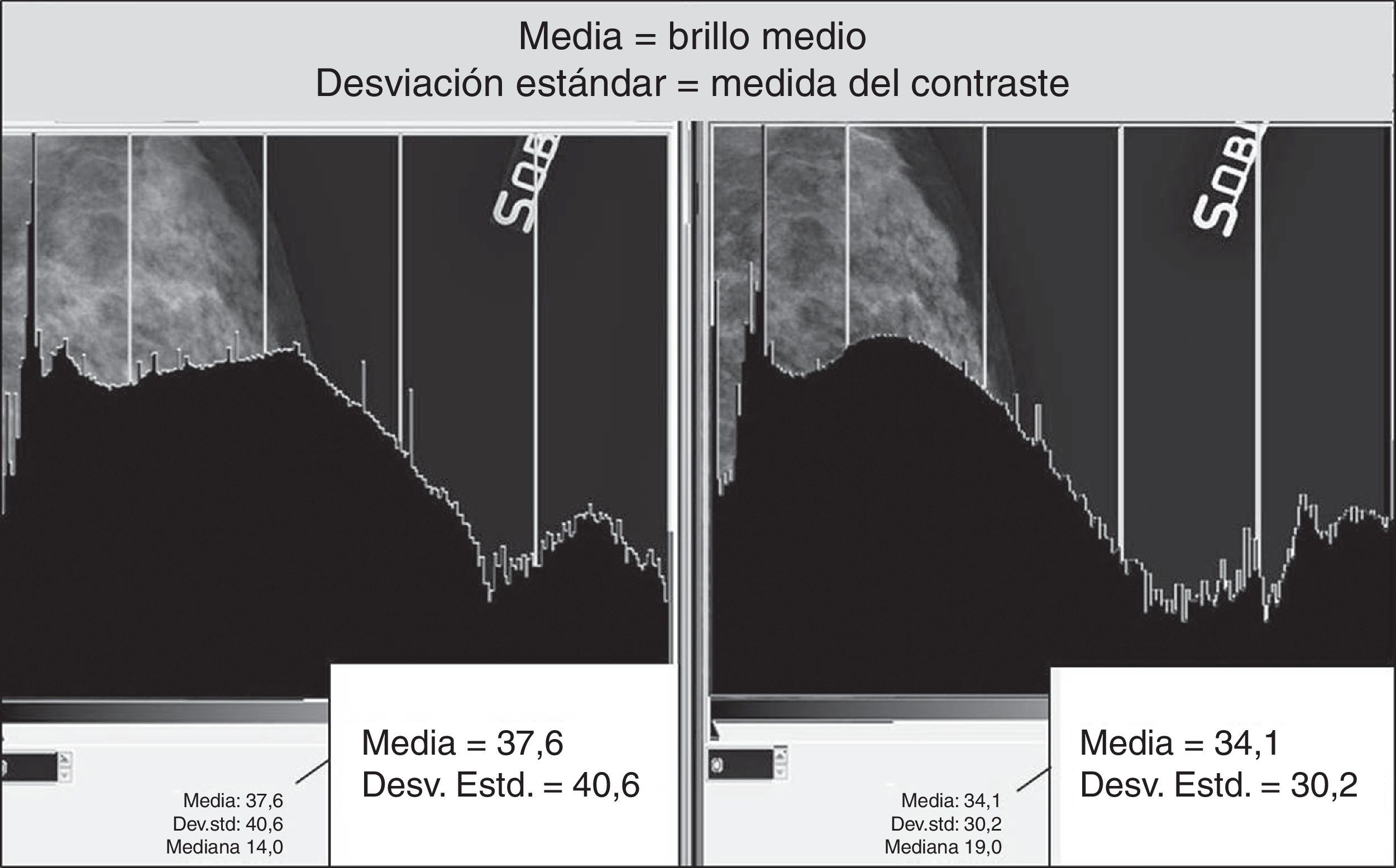
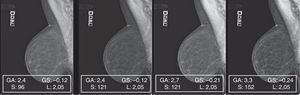
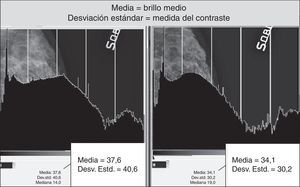
La secuencia de pantallas representadas en la figura 10 nos demuestra los efectos negativos en la calidad de la imagen cuando actuamos modificando GA y GS en presencia de elevados valores de S, obteniendo un realce de contraste excesivo, como queda demostrado por la fuerte expansión de la dinámica de los niveles de gris y la fuerte pendiente de la curva tonal representadas en los 2 histogramas (fig. 12).
En la evaluación comparativa de los histogramas inherentes a diferentes variaciones del valor de S del mismo mamograma, se nota que antes de sobrepasar el valor máximo de umbral de elaboración, ellos presentan una leve variación de distribución de los grises medianos, conservando la misma amplitud de la escala de grises (fig. 13).
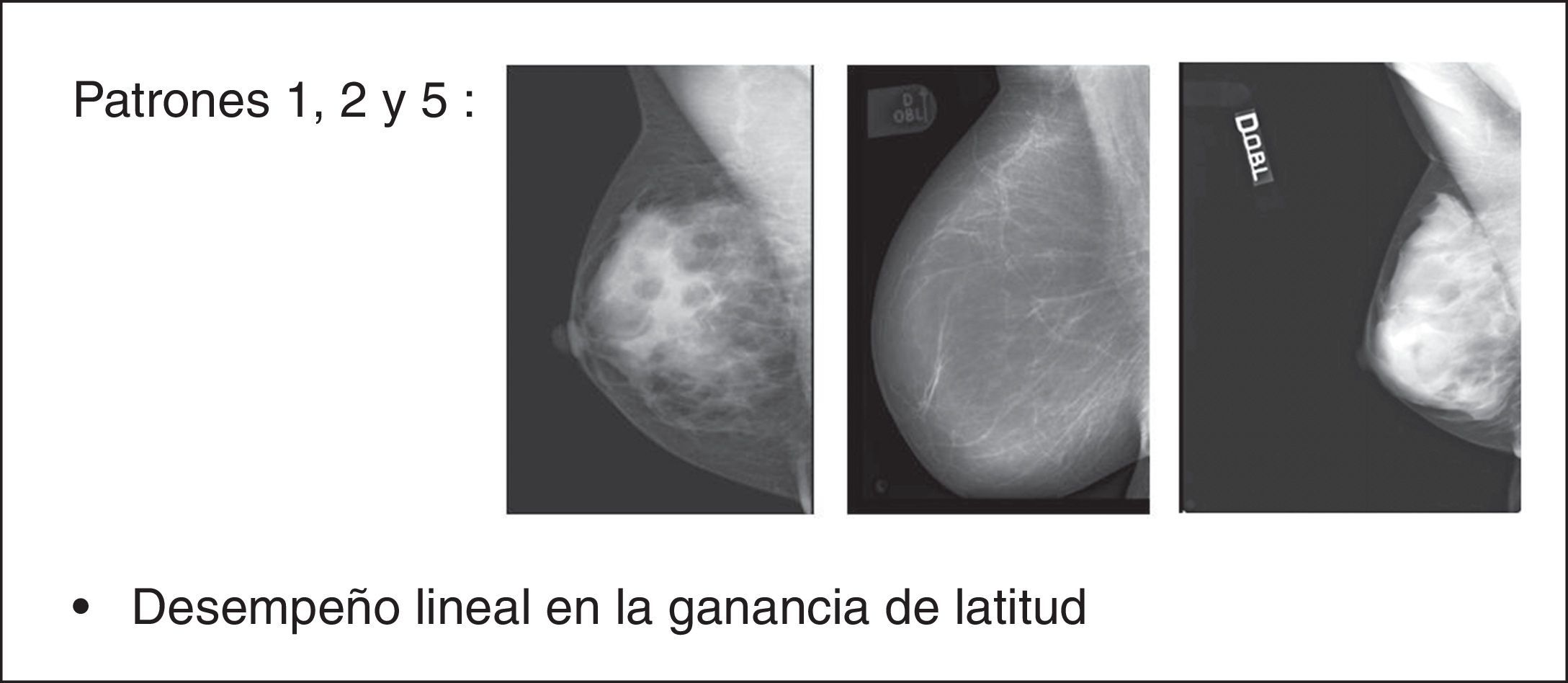
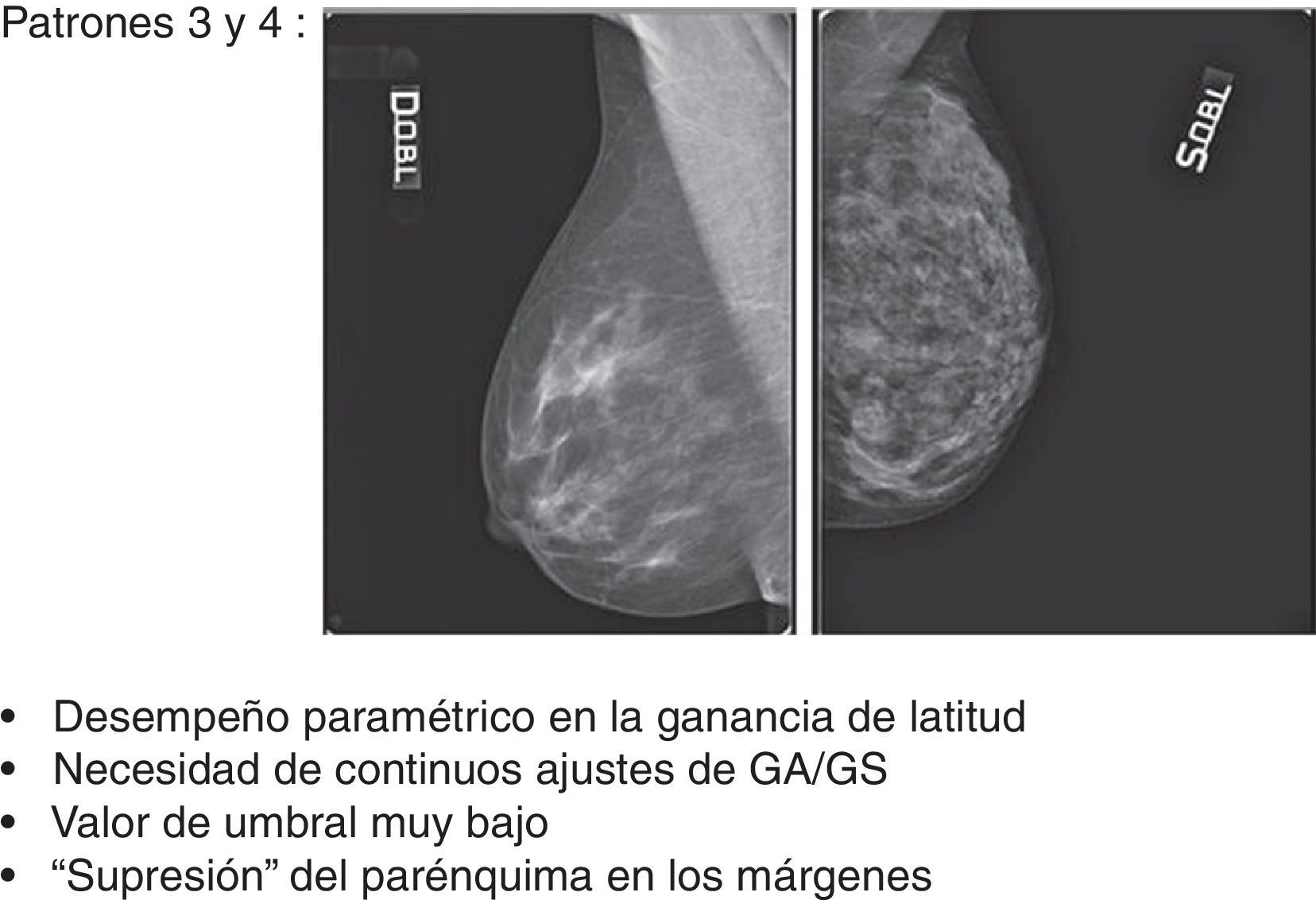
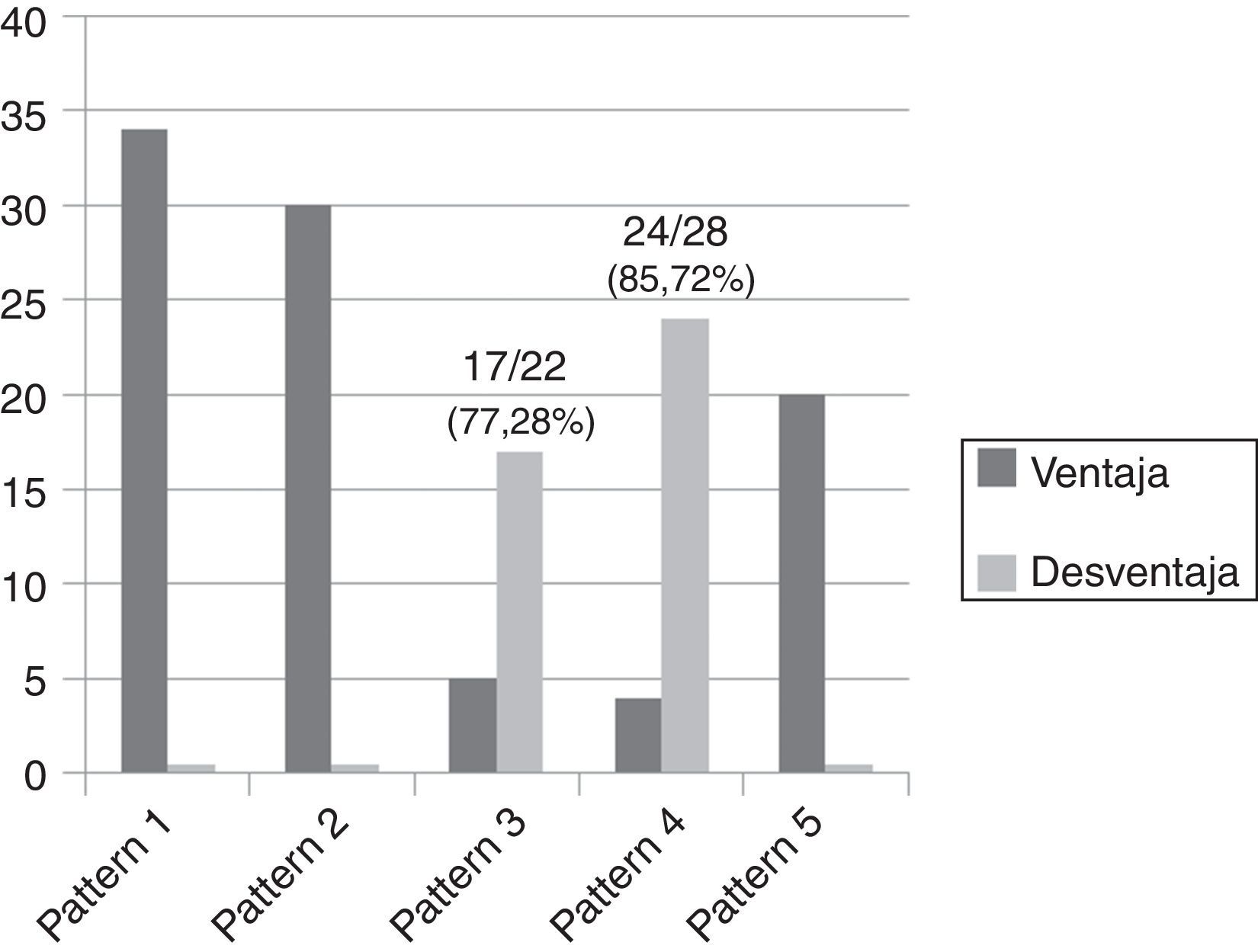
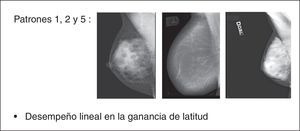
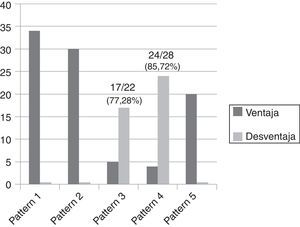
Como resultado del estudio se ha observado que los patrones 1, 2 y 5 siempre han respondido con un desempeño lineal en la ganancia de latitud, beneficiando el posproceso sin exhibir problemas de sobretratamiento (fig. 14), a diferencia de los patrones 3 y 4 que han respondido con un desempeño paramétrico que necesitaba continuos ajustes de GA/GS para evitar sobrepasar el valor máximo de umbral, con consecuente efecto repentino de «supresión» del parénquima en las regiones fronterizas con el tejido adiposo (fig. 15). El número de mamogramas que tras el posproceso presentaron desventajas en términos de efectos adversos fue respectivamente de 17/22 (77,28%) para el patrón 3 y de 24/28 (85,72%) para el patrón 4 (fig. 16).
Número de mamogramas que se han beneficiado del posproceso (en gris oscuro) para cada patrón frente al número de mamogramas que no se han beneficiado (en gris claro), dentro de los cuales se destacan los patrones 3 y 4, con un número de desventajas (en términos de efectos adversos) de 17/22 (77,28%) y de 24/28 (85,72%), respectivamente.
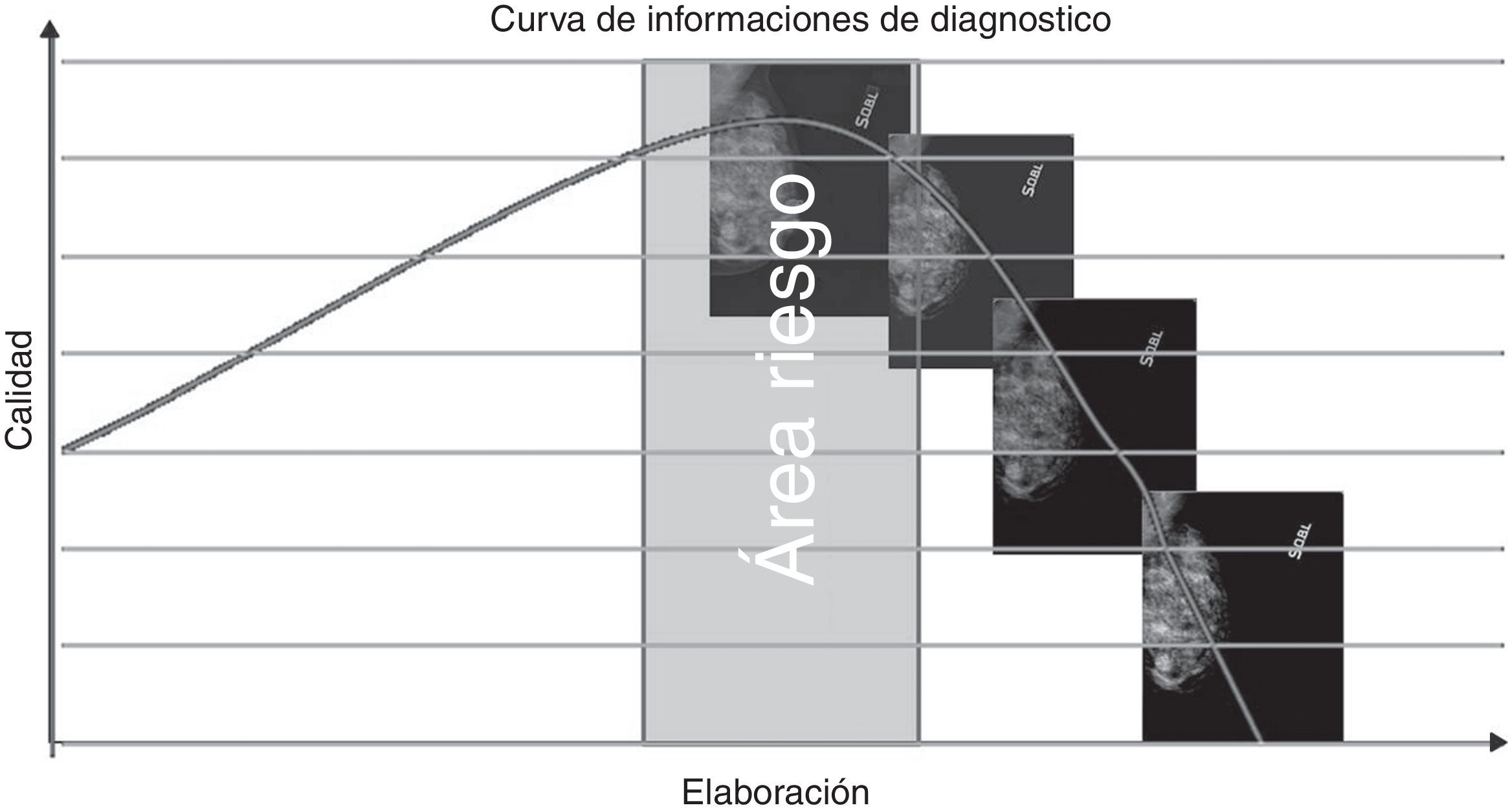
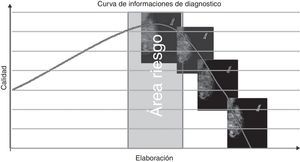
El estudio ha evidenciado que, cuando se intentan elaborar patrones micronodulares o de parénquima residual, nos movemos peligrosamente dentro de un área de riesgo (fig. 17), cuya variabilidad depende de las características intrínsecas del parénquima (aunque siempre relacionada con la presencia de pequeñas áreas de elevada densidad). La explicación de esta respuesta negativa se encuentra en el artefacto de blooming, que se produce cuando el filtro edge enhancement se ajusta a valores altos y se manifiesta en forma de halo oscuro alrededor de las zonas con mayor densidad, particularmente evidente en las interfaces entre el tejido glandular y adiposo9,18, enmascarando la presencia de lesiones en las «zonas muertas»8.
La curvas obtenidas pueden ser memorizadas en preajustes por cada usuario. Sin embargo, puesto que no es posible reducir a un modelo anatómico todas las variables que se pueden encontrar entre los diferentes tipos de mama, es en todo caso necesaria la intervención manual para el ajuste fino de los parámetros de procesamiento.
ConclusionesEl posproceso en mamografía digital permite mejorar la calidad de imagen y aumentar la precisión diagnóstica, especialmente en mamas densas, aunque su uso impropio o excesivo puede volverse un arma de 2 filos, al sustraer importante información anatómica y aumentar, de paso, el número de falsos negativos. Por lo tanto, resulta imprescindible que el manejo del posproceso lo realicen profesionales con mucha experiencia, que los cambios sean reversibles y que siempre se conserve la imagen original16.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.