Este artículo revisa la técnica actual en los estudios de perfusión en cuerpo por tomografía computarizada multidetector (TCMD), las recomendaciones para obtener la información en imágenes de manera más efectiva y los resultados ofrecidos, así como el futuro tecnológico próximo para este tipo de estudios.
Material y métodosLightSpeed VCT, GE Healthcare. Advantage Workstation 4.4, GE Healthcare.
ConclusionesEl estudio de perfusión de cuerpo por TCMD es una modalidad en constante crecimiento, con cada vez menos limitaciones técnicas y que se consolida como una de las técnicas prioritarias para la valoración de imagen funcional en el área oncológica. La finalidad de esta técnica es conseguir un estudio con la máxima resolución temporal posible.
This article reviews the current technique for body perfusion studies in multidetector computed tomography (MDCT), recommendations on the most effective way to obtain the information in the images, the results, and the technological developments likely in the near future for this type of studies.
Material and methodsWe used a LightSpeed VCT with an Advantage Workstation 4.4, both from GE Healthcare.
ConclusionsBody perfusion MDCT is a constantly expanding modality. The limitations to the technique are being overcome and it is becoming established as one of the priority techniques for functional imaging in oncologic patients. The aim of this technique is to achieve the maximum temporal resolution possible.
Hasta el momento actual, los principales avances en el campo de la imagen diagnóstica, en concreto en tomografía computarizada multidetector (TCMD), se han centrado tanto en mejorar la resolución espacial y la velocidad de adquisición de los datos como en la introducción de nuevas técnicas y medios de contraste, que se acompañan de novedosos software para el tratamiento de la imagen.
Los radiólogos han conseguido, de este modo, una excelente resolución anatómica y de contraste debido en buena parte a la aparición de equipos de última generación con tiempos de rotación cada vez más rápidos, con resoluciones isotrópicas que ofrecen la máxima calidad de imagen en cualquier plano de estudio (axial, sagital, coronal, oblicuo), así como diferentes tipos de imágenes (2D, 3D y 4D), todos estos son elementos muy importantes en el estudio de tumores, pero aun así, a la hora de interpretar, el radiólogo que debe trabajar con este tipo de enfermedades continúa encontrándose grandes lagunas en la estadificación tumoral y, por supuesto, en las características de estas lesiones tumorales, esto es: imagen funcional tumoral.
Por lo tanto, las técnicas de imagen funcional están en continuo auge, la industria se centra en mejorar e investigar en este tipo de exámenes que consigue estudiar en tiempo real los procesos fisiológicos de los tejidos y los tumores. Perfusión TCMD, resonancia magnética (RM) de perfusión tumoral (perfusión: llevar oxígeno y nutrientes a un tejido por medio de la sangre), tomografía por emisión de positrones (PET), espectro-RM, PET-TC, etc., son modalidades que nos ofrecen características del entorno tumoral para unirlo como un valor añadido al diagnóstico, estadificación, planificación terapéutica y control, los cuales son puntos esenciales para la solución multidisciplinaria de una lesión tumoral.
Existen amplios conocimiento y experiencia en los estudios de perfusión TCMD neurovascular en los servicios de radiología que hayan establecido un protocolo de actuación “código ictus”, donde este examen se convierte en estudio sistemático para el diagnóstico de regiones infartadas o de penumbra y su respectiva área. Por otro lado, no hay tanta facilidad en llevar a cabo estudios de la misma modalidad TCMD en lesiones tumorales de cuerpo.
En este artículo revisaremos la técnica de perfusión de cuerpo TCMD, su adquisición y posprocesamiento en uno de los equipos más utilizados en los servicios de radiología de hoy en día.
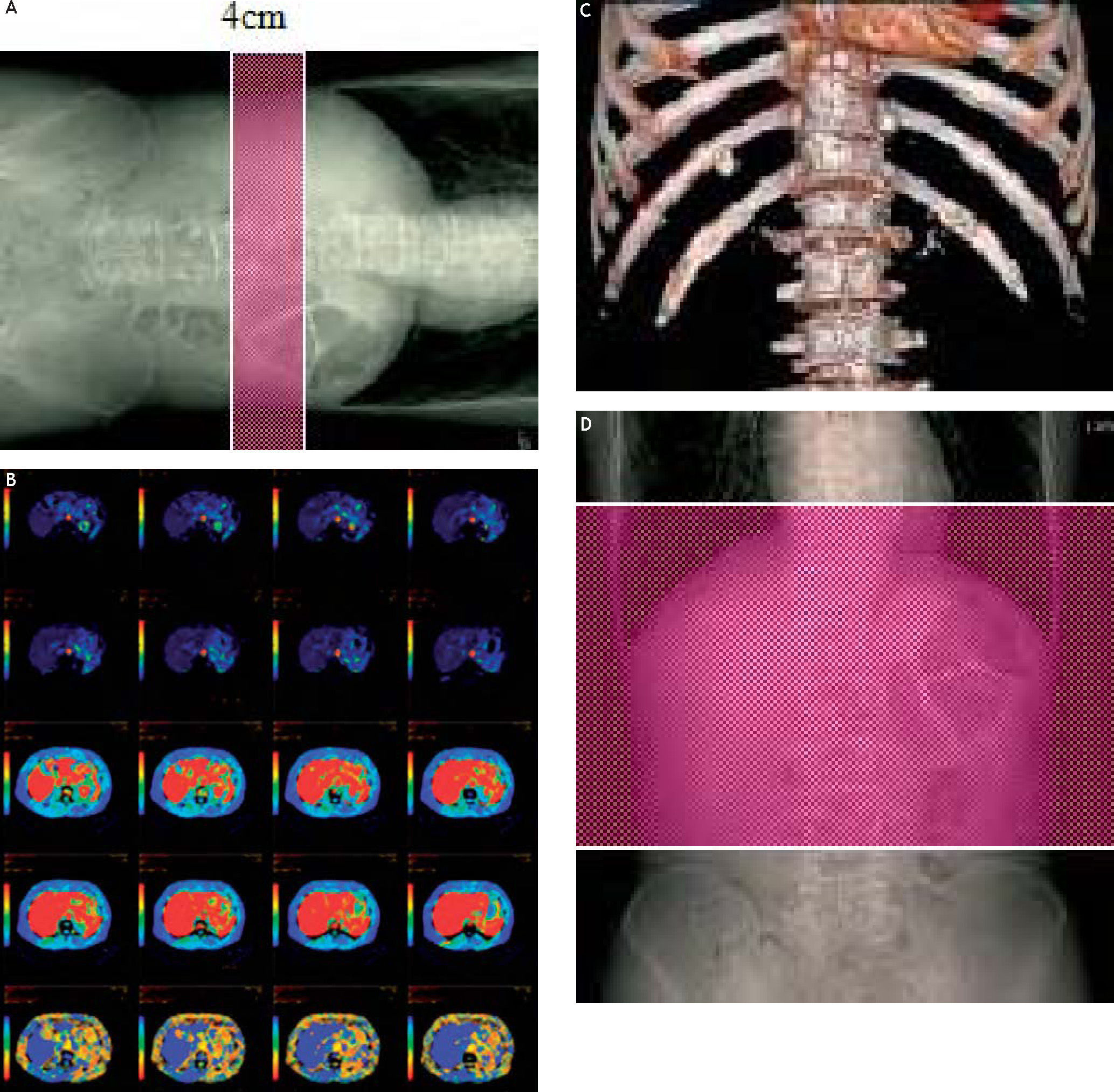
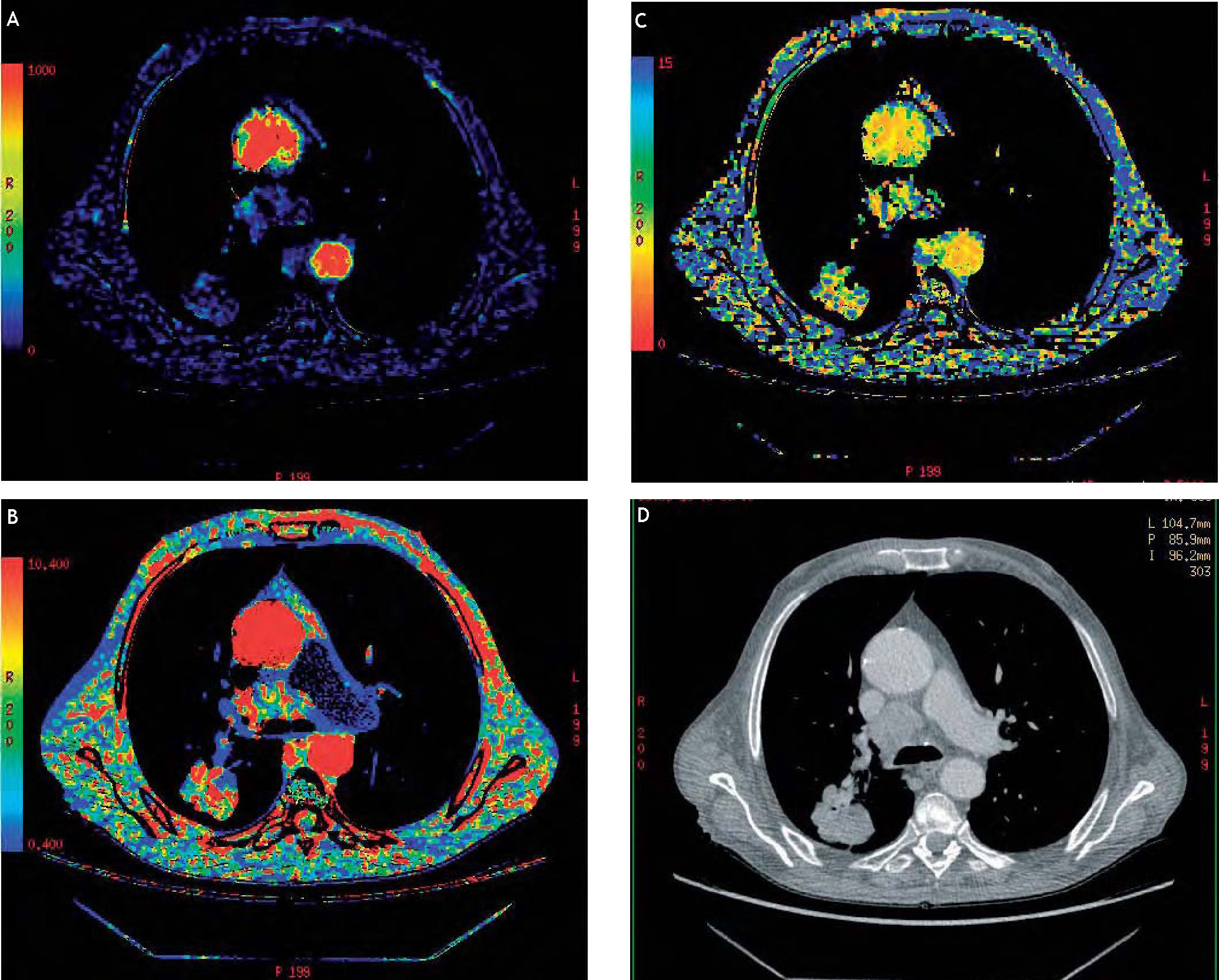
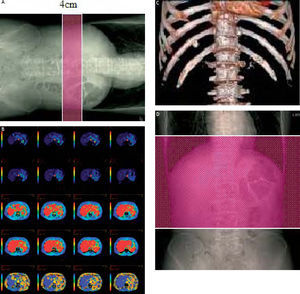
Material y métodosHemos utilizado como equipo de referencia para este artículo un TCMD LightSpeed VCT, GE Healthcare (fig. 1) que, en su configuración simple, consigue una cobertura de 4cm en eje Z (eje longitudinal) y muestra 8 localizaciones o, lo que es lo mismo, 8 imágenes de 5 mm cada una en plano axial con sus respectivos mapas de resultados (fig. 2A-B).
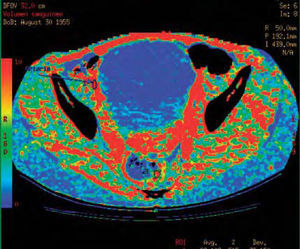
A: cobertura de 4cm, en eje z superpuesta en imagen localizadora. B: ejemplo de mapas funcionales en una perfusión abdominal, que muestra las ocho localizaciones sobre el nivel de 4cm seleccionado. C y D: cobertura en eje z utilizando la técnica Volume Helical Suttle; se observa que se abarca un abdomen de tamaño medio en su totalidad, desde el final del tórax hasta las crestas ilíacas.
Para el proceso ulterior, en el que manejaremos un gran número de imágenes, hemos utilizado una estación de trabajo Advantage Workstation AW4.4 GE Healthcare con software de Perfusión 4 Multiorgan.
La manera de adquirir será tipo cine, no habrá movimiento de camilla, efectuaremos un escaneado continuo, con lo que estudiaremos una determinada región en un determinado tiempo al paso del producto de contraste; para completar el estudio, realizaremos una adquisición secuencial, con un intervalo de 5 s entre imagen e imagen.
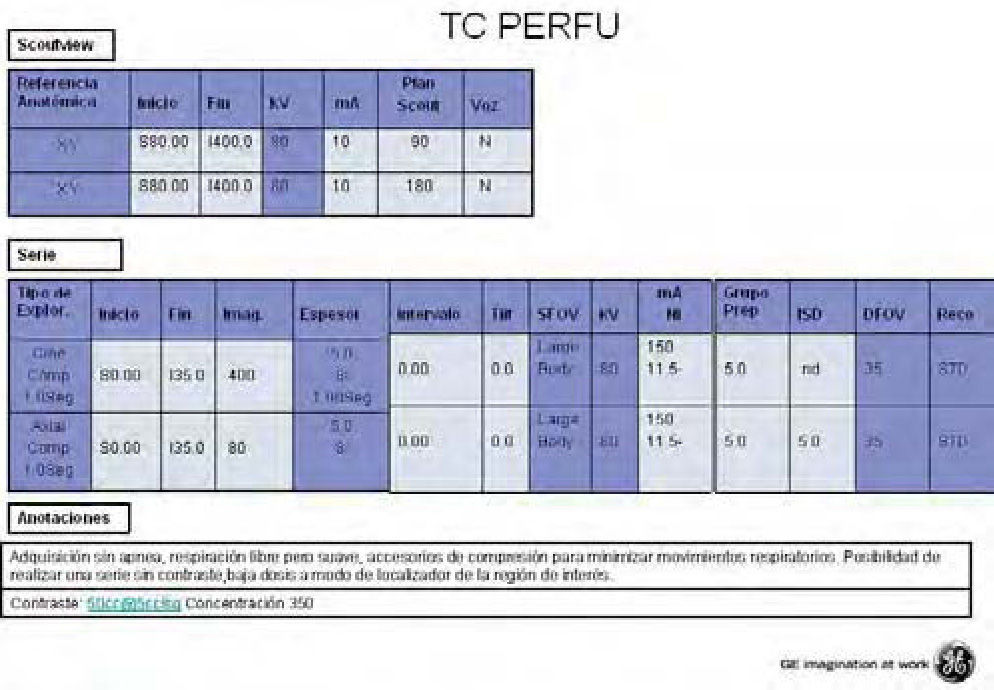
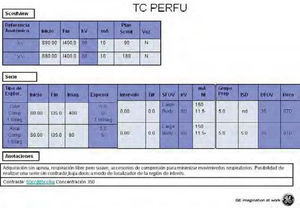
La prioridad es conseguir una adquisición que sea mayor de 2 min de duración; este tiempo variará en función del órgano en estudio, siempre debemos tener en cuenta que serán necesarias imágenes previas a la llegada del producto de contraste en la zona de estudio para que los mapas obtenidos se puedan computar de manera correcta; para ello el inicio de nuestro escaneado coincidirá con el inicio de la inyección de contraste. En la figura 3 se ofrece un protocolo “tipo” para un estudio de recto; como se puede observar, configuramos el equipo con dos tipos diferentes de adquisición, una cine y una secuencial, la intención es minimizar el índice de dosis de TC (CTDi) final del estudio.
El CTDi es el indicador de dosis para una rotación completa de tubo, el equipo muestra este dato tanto prospectivamente como retrospectivamente. Una adquisición tipo cine, con los parámetros del protocolo antes mencionado, equivale a 192 mGy, mientras que en el mismo estudio la adquisición tipo secuencial no supera los 53 mGy. La gran diferencia entre ambos tipos de adquisiciones para este tipo de estudios recala en la resolución temporal. La adquisición secuencial no tiene la resolución temporal necesaria para los primeros 50 s de estudio, es por este motivo que utilizamos el modo cine. Por otro lado, la mayor dosis emitida en el grupo cine nos obliga a utilizar el modo secuencial en la segunda parte del estudio, la pérdida de resolución temporal en esta fase no es apreciable en los resultados finales y el paciente se beneficia de una significativa reducción de dosis.
En pacientes obesos, deberemos utilizar 100 kV, tanto en el grupo cine como en el grupo secuencial, si no queremos encontrarnos mapas funcionales con excesivo ruido, esta misma consideración la tendremos en pacientes que no puedan posicionar los brazos fuera de la zona estudiada.
Valoraremos la opción de realizar una primera adquisición de baja dosis sin contraste, que nos sirva como localizador de la región de interés. Todo el estudio se deberá realizar en respiración libre pero suave, con accesorios de compresión para intentar minimizar los artefactos producidos por el movimiento del paciente.
En cuanto a la inyección intravenosa de producto de contraste, será necesario realizarla con un flujo de 5ml/s y un volumen de 50ml para un paciente medio de 80kg de peso y finalizar la inyección con un flash de suero para compactar el bolo administrado y ayudar a la limpieza de la vía utilizada.
Desde principios de 2009 ya está disponible en el mercado LightSpeed VCT XTe, GE Healthcare; con sus actuales configuraciones de última generación, para estudios de perfusión consigue con la máxima resolución temporal hasta 14cm en eje Z (cobertura suficiente para la mayor parte de las lesiones en estudio) y hasta 31,25cm para exámenes angiográficos dinámicos 4D por técnica VolumeHelical Suttle (fig. 2C-D).
La nueva generación de equipos TCMD de alta definición, disponibles desde finales de 2009, con capacidad para trabajar a diferentes energías (imágenes monocromáticas) con un único tubo de rayos X, Discovery CT750 HD, GE Healthcare, con FOV de visualización completo y que reduce la dosis que recibe el paciente será la nueva estrategia para caracterizar, cualificar y cuantificar lesiones tumorales. Este tipo de equipos es el futuro próximo en cuanto a estudios radiológicos de imagen funcional tumoral.
ResultadosLa TCMD perfusión se basa en el cambio temporal de la atenuación de los tejidos tras la administración de contraste yodado intravenoso. En el estudio podemos distinguir dos fases, una primera que dura alrededor de 1 min en la que necesitamos una alta resolución temporal (cine), como máximo 1 s por imagen, y una segunda fase que dura entre 2 y 5 min por lo que realizamos una adquisición más espaciada (secuencial).
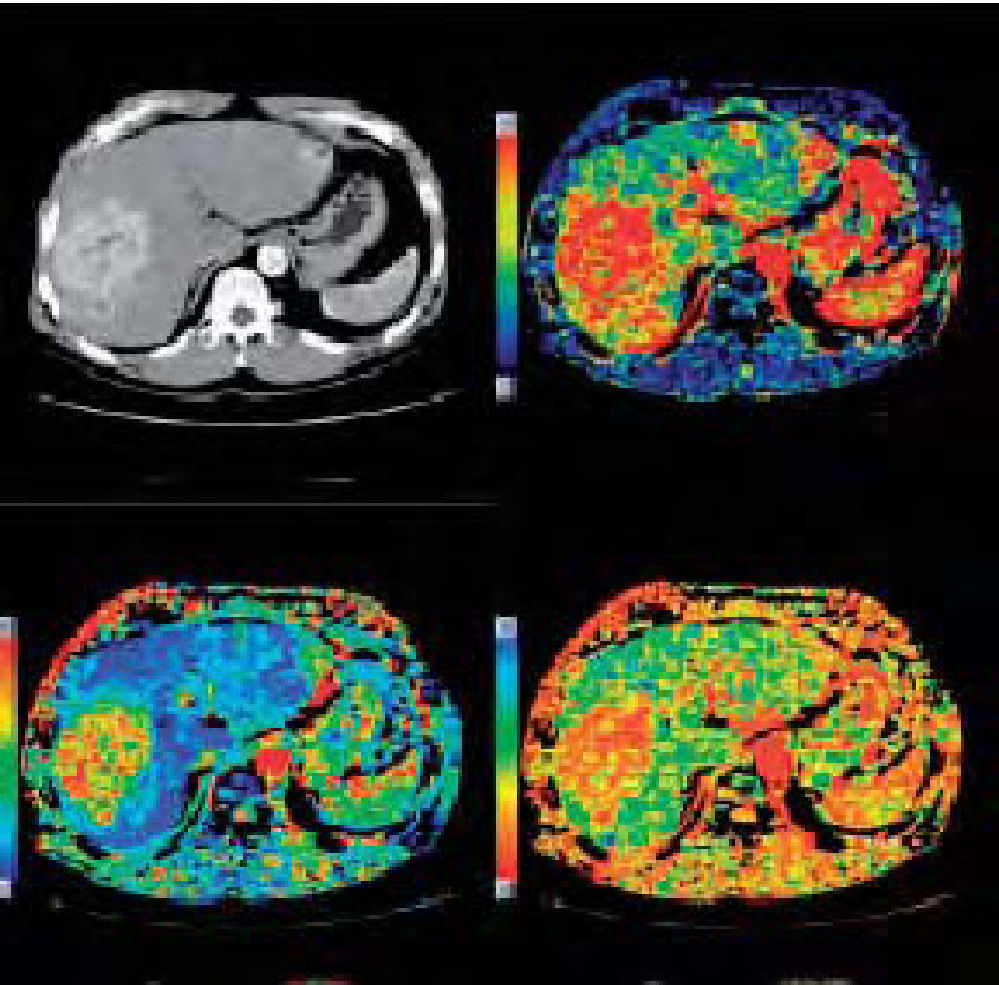
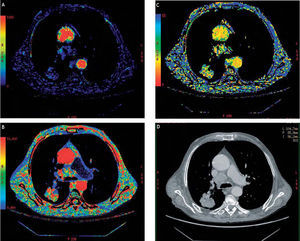
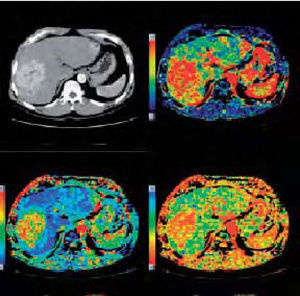
En la estación de trabajo AW4.4, después de reconocer por medio de ROI una arteria y una vena, el software nos mostrará simultáneamente varios mapas resultantes, que se verán representados por una escala de colores frente a UH, esa escala puede optimizarse para establecer una correcta relación entre ruido en la imagen y color, estos mapas nos facilitarán la identificación de la angiogénesis tumoral (angiogénesis: formación de una red de nuevos capilares, elemento clave en el desarrollo y la diseminación metastásica de un tumor maligno). En la figura 4A-D se pueden observar los diferentes mapas obtenidos en un estudio de perfusión torácica. Básicamente se interpretarán los resultados con los mapas de volumen sanguíneo, flujo sanguíneo y tiempo de tránsito medio.
Flujo sanguíneo: se calcula y visualiza en ml por 100g de tejido húmedo/min.
Volumen sanguíneo: representa la parte intravascular del espacio sanguíneo. Se calcula y visualiza en ml por cada 100g de tejido húmedo, se define como el producto de flujo sanguíneo y el tiempo de tránsito medio.
Tiempo de tránsito medio: representa el tiempo de tránsito medio de la parte intravascular de la respuesta.
Producto de la superficie de permeabilidad: se calcula y visualiza en ml por 100 g de tejido húmedo/min.
Fracción arterial hepática: se calcula y visualiza como una fracción. Utilizada en oncología, representa la fracción de la entrada de la sangre al hígado que se puede atribuir a la arteria hepática.
Tiempo de llegada: se calcula y visualiza en segundos. Representa el momento en que el agente de contraste llega a una ubicación determinada.
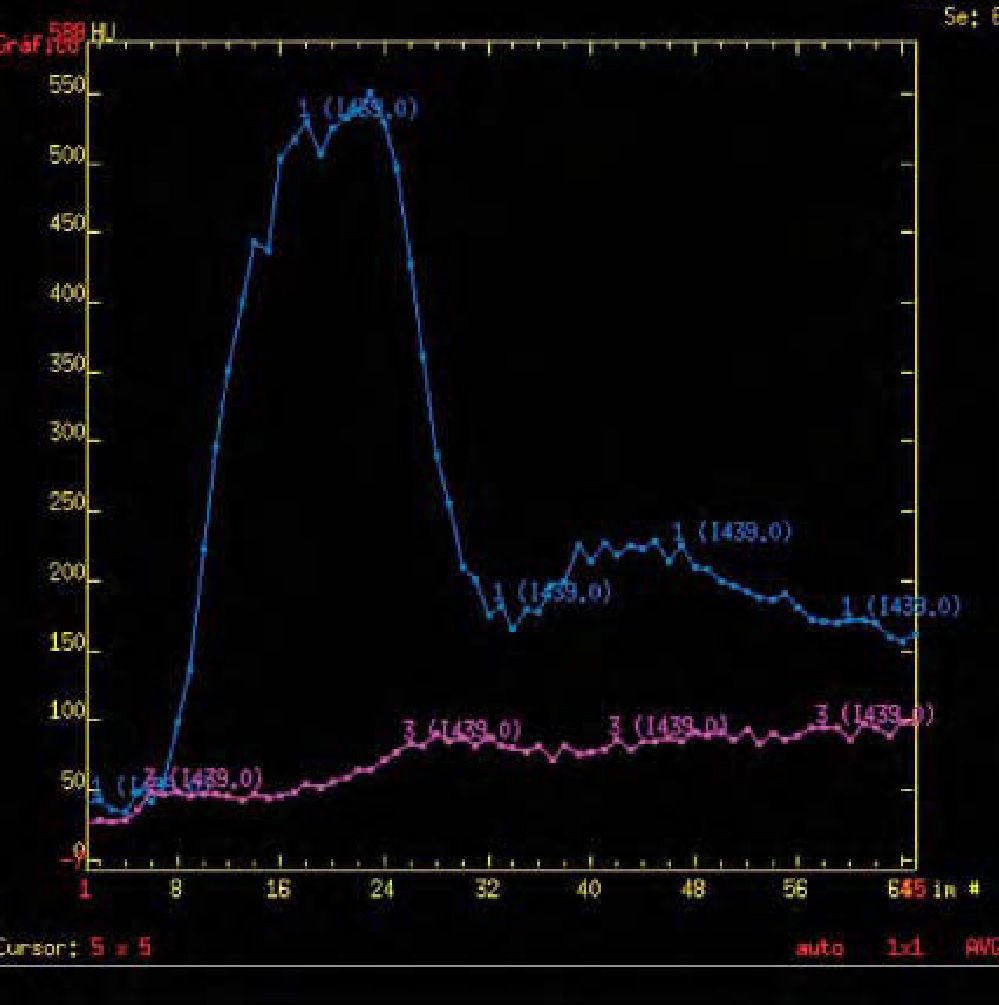
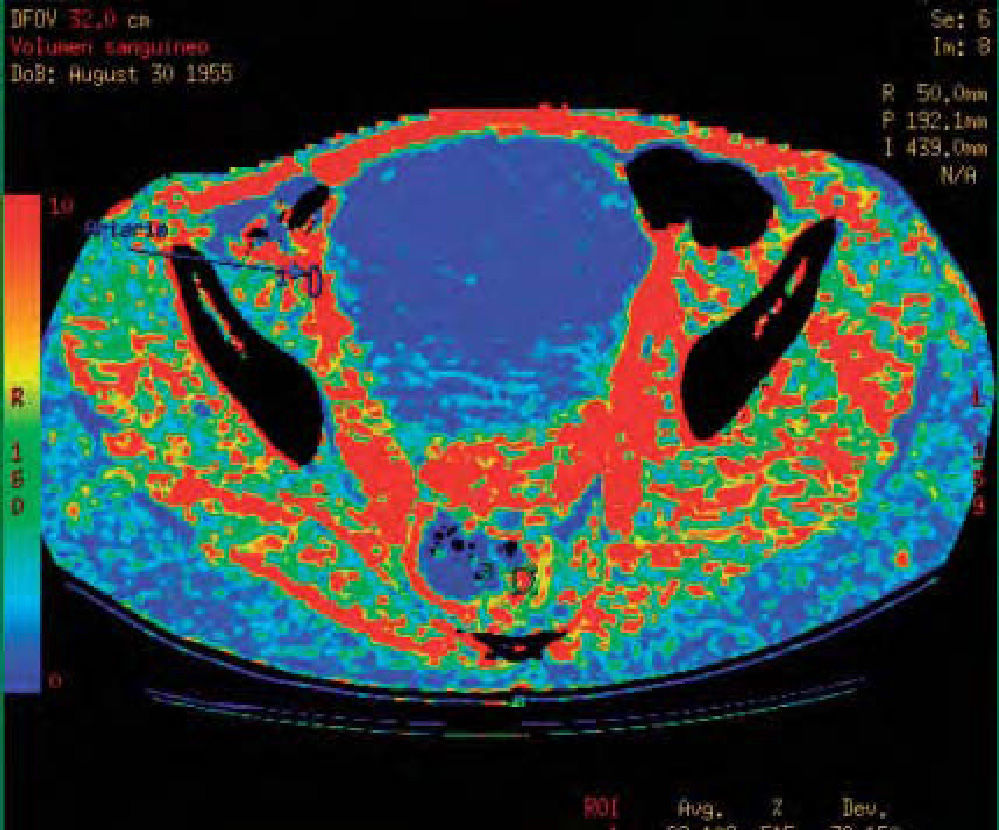
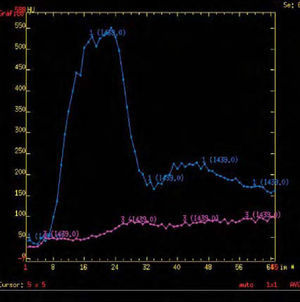
El análisis de todos estos mapas puede ser de tres maneras: cualitativo, semicuantitativo o cuantitativo. El análisis cualitativo se centra en el estudio del perfil de la curva en el gráfico obtenido después de reconocer arteria y vena (fig. 5); en el análisis semicuantitativo, se utiliza la intensidad de señal en los diferentes mapas (interpretación visual contra mapas) (fig. 6); por último, el análisis cuantitativo se realizará utilizando regiones de interés en las zonas de estudio, que nos ofrecerán valores numéricos (fig. 7).
Las desventajas de esta técnica en los equipos convencionales (no HD) podemos resumirlas en sus niveles de radiación (CTDi > 190 mGy para adquisición cine, > 56 mGy para adquisición secuencial), también en su resolución espacial, que se ve reducida debido a que en este tipo de estudios se prioriza la resolución temporal, y en la cobertura de estudio, que dependerá básicamente del equipo que utilicemos. Mientras que, por otro lado, la alta disponibilidad de TCMD y la evolución de la industria, al aumentar la cobertura de estudio y minimizar los índices dosimétricos, así como la rapidez de lectura en las estaciones de trabajo que proporcionan los mapas de resultados prácticamente de manera automática, hacen que esta técnica se convierta en el examen radiológico prioritario en los estudios oncológicos de imagen funcional.
Otro de los motivos que hacen cada vez más robusta esta modalidad es la facilidad en términos técnicos. Siempre y cuando el equipo que utilicemos tenga capacidad de cobertura en eje Z acorde con el tipo de lesión que queremos estudiar, podremos llevar a cabo con plenas garantías este tipo de adquisición, únicamente se debe recordar no utilizar tiempos de espera con respecto a la inyección de contraste intravenoso.
Las aplicaciones clínicas de esta modalidad que hemos nombrado antes (diagnóstico, estadificación, planificación y control) de nada servirán si no se consigue realizar un trabajo multigrupo/multiservicios, donde se lleve a cabo una labor en equipo entre radiología, oncología, radioterapia, etc.