El estudio muestra las ventajas de la resonancia magnética de bajo campo en investigación preclínica frente a otra técnica de diagnóstico como la ecografía. Con la ayuda de un modelo experimental en rata, exponemos la valoración «in vivo» de una de las patologías cardiacas más prevalentes como es el infarto agudo de miocardio frente a la isquemia-reperfusión, simulando un procedimiento de angioplastia primaria tras el infarto. El análisis comparativo de las imágenes mediante las 2 técnicas demostró las diferencias estructurales y funcionales entre los modelos de infarto e isquemia-reperfusión sin la necesidad de grandes infraestructuras.
The study shows the advantages of low-field magnetic resonance imaging in pre-clinical research compared to other diagnostic techniques, such as echocardiography. Using an experimental rat model, we present an “in vivo” evaluation of one of the most prevalent heart diseases, such as acute myocardial infarction and ischaemia-reperfusion, simulating a primary angioplasty procedure after infarction. The analysis of the images demonstrated both structural and functional differences between models of infarction and ischaemia-reperfusion without needing a major infrastructure.
Las cardiopatías de origen isquémico son actualmente la principal causa de muerte en los países desarrollados, a pesar de todos los avances tanto farmacológicos como quirúrgicos para combatir la enfermedad coronaria1. La principal expresión clínica de la cardiopatía isquémica es el infarto agudo de miocardio (IAM) y surge tras la interrupción del flujo sanguíneo en alguna de las arterias que irrigan el corazón, lo que provoca la reducción del aporte de oxígeno y nutrientes a las células del músculo cardiaco. Como consecuencia de ello, estas células mueren por necrosis si el flujo de sangre no se reestablece a tiempo, produciéndose una cicatriz fibrosa e irreversible del tejido, como ocurre en el infarto. Si, por el contrario, ese flujo coronario se reestableciera a tiempo mediante un tratamiento de reperfusión (como la realización de angioplastia primaria en pacientes con infarto), permitiría un posible tratamiento para minimizar los daños producidos tanto por la oclusión coronaria no reversible, como por la isquemia-reperfusión2.
Tradicionalmente, para el estudio de la cardiopatía isquémica se han utilizado herramientas diagnósticas como el cateterismo cardiaco o la gammagrafía de perfusión. Lamentablemente, estas técnicas son invasivas y emisoras de radiación ionizante. La ecografía cardiaca desempeña un papel muy importante, pero en los últimos años se ha desarrollado el uso de la resonancia magnética (RM) dada su capacidad de valorar tanto la morfología como la función cardiaca3. Basándose en un fenómeno físico de excitación nuclear de los átomos de H+ tras absorber energía electromagnética y su posterior relajación, bajo un potente campo magnético, permite formar así las imágenes por RM. Las distintas secuencias o protocolos utilizados mediante esta técnica y la posibilidad de incorporar medios de contraste como el gadolinio facilitan la distinción de los diferentes tejidos con mayor claridad, haciendo de la RM el patrón oro en la valoración de muchas de las patologías cardiacas que concurren en la actualidad4.
Para el estudio preclínico de la cardiopatía isquémica se utilizan modelos experimentales en roedores (ratas y ratones)5, a pesar de que los protocolos utilizados en clínica no sean totalmente transferibles debido al pequeño tamaño del corazón y a su alta frecuencia cardiaca. Por este motivo, la gran mayoría de los estudios de RM con roedores se han realizado en equipos de alto campo (≥ 4,7T) con características diferentes a los resonadores clínicos de 1,5T.
El principal objetivo de este artículo es dar a conocer la utilidad de la RM preclínica de bajo campo (1T) en un modelo experimental en rata de IAM e isquemia-reperfusión, en comparación con otras técnicas más operador-dependientes como la ecocardiografía.
Presentación de casosSe realizó el modelo experimental en 6 ratas macho Wistar de 200-250 g, cumpliendo la normativa según el Real Decreto 53/2013 de acuerdo con la directiva 2010/63/EU del Parlamento Europeo y aprobada por el comité ético local de investigación del Hospital Universitario Virgen del Rocío de Sevilla, así como por el comité de investigación animal de la Universidad de Sevilla.
Todos los animales fueron anestesiados con una dosis de xilacina (10mg/kg)+ketamina (80mg/kg) por vía intraperitoneal. Posteriormente, se les realizó una intubación endotraqueal con el objetivo de permitir la ventilación mecánica utilizando el equipo para pequeños animales Harvard Apparatus Model 683 (Harvard Apparatus, Massachusetts, NC). Previa toracotomía, se llevaron a cabo 2 procedimientos: la ligadura irreversible de la arteria coronaria descendente anterior con la interrupción total del flujo sanguíneo (n=2) provocando un IAM y en el resto de los animales (n = 4), se ligó dicha arteria durante un tiempo de 40 min de isquemia, tras el cual se procedió a la reperfusión del flujo de sangre, realizando así el modelo de isquemia-reperfusión (I/R). Estos procesos fueron confirmados mediante la observación de la elevación del segmento ST en el electrocardiograma. En el postoperatorio se administró a los animales un analgésico cada 12 h hasta su sacrifico pasado una semana del procedimiento.
Cada rata fue sometida a un estudio basal de imagen cardiaca mediante ecocardiografía transtorácica antes de los protocolos descritos anteriormente (IAM e I/R) y tras una semana de la cirugía. Los animales fueron sedados mediante anestesia inhalatoria con sevoflurano (inducción al 4% y mantenimiento al 2%) y monitorizados por medio de electrocardiograma y termómetro rectal, comprobando la existencia y el mantenimiento de condiciones fisiológicas y hemodinámicas adecuadas (frecuencia cardiaca entre 400 y 500 latidos por minuto, frecuencia respiratoria superior entre 60-100 respiraciones por minuto y temperatura corporal superior a 35°C).
El estudio ecocardiográfico se llevó a cabo mediante el sistema de imagen Vevo2100 (Visualsonics; Ámsterdam, Holanda) con un transductor para pequeños animales de 13-24MHz (Visualsonics; Ámsterdam, Holanda). Se realizaron los planos paraesternal eje largo y paraesternal eje corto a nivel valvular, de músculos papilares y apical. A través de dichos planos, se valoraron cualitativamente las alteraciones de la contractilidad del ventrículo izquierdo. Se obtuvieron medidas de las dimensiones y derivación de los volúmenes diastólico y sistólico del ventrículo izquierdo mediante el método de Simpson6.
Se realizó un estudio de imagen cardiovascular por RM a cada animal previo a la cirugía y una semana después. Los animales fueron sedados y monitorizados del mismo modo utilizado para el estudio ecocardiográfico, anteriormente descrito.
El estudio por RM se llevó a cabo empleando el sistema de imagen ICON 1T (Bruker; Ettlingen, Alemania), utilizando una antena de radiofrecuencia para imagen de cuerpo de rata. Se evaluó la función cardiaca y la cuantificación del área isquémica.
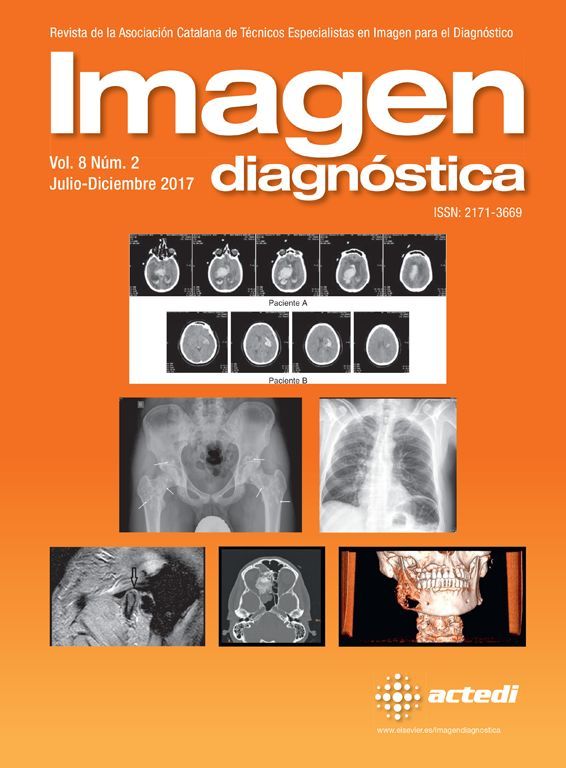
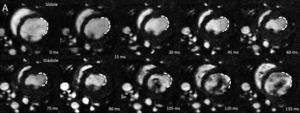
Para la evaluación de la función cardiaca, se realizaron secuencias rápidas eco de gradiente (FLASH) en modo cine potenciadas en T1 y sincronizadas con el electrocardiograma (tiempo de repetición 15 ms, tiempo de eco 2 ms, resolución en plano 0,234×0,234 mm, grosor de corte 1,250 mm, ángulo de giro 40°, 3 cortes con 10 fases cardiacas cada uno) en plano eje corto a nivel basal, medio ventricular y apical. Estas secuencias de cine se adquirieron con el objetivo de cuantificar los volúmenes telesistólico (VS) y telediastólico (VD) y la fracción de eyección (FE) del ventrículo izquierdo, todo ello con el software de procesado de imágenes VIRTUE (Diagnosoft; Durham, NC).
Posteriormente, para la cuantificación del área isquémica, se realizaron secuencias eco de gradiente potenciadas en T1 y sincronizadas con el electrocardiograma (tiempo de repetición 100 ms, tiempo de eco 2,5 ms, resolución en plano 0,234×0,234 mm, grosor de corte 1,250 mm, ángulo de giro 75 o 90°, 3 cortes con la misma geometría que las secuencias de cine previas) a los 15 min aproximadamente tras la introducción de un medio de contraste basado en gadolinio cuyo objetivo es la visualización de los segmentos del ventrículo izquierdo donde existe fibrosis.
El análisis de los resultados obtenidos en el contexto de un modelo experimental de I/R por cardiorresonancia permite estudiar la función y la estructura del corazón, y con ello comprobar la eficacia de fármacos o sistemas de revascularización para su traslación a la clínica.
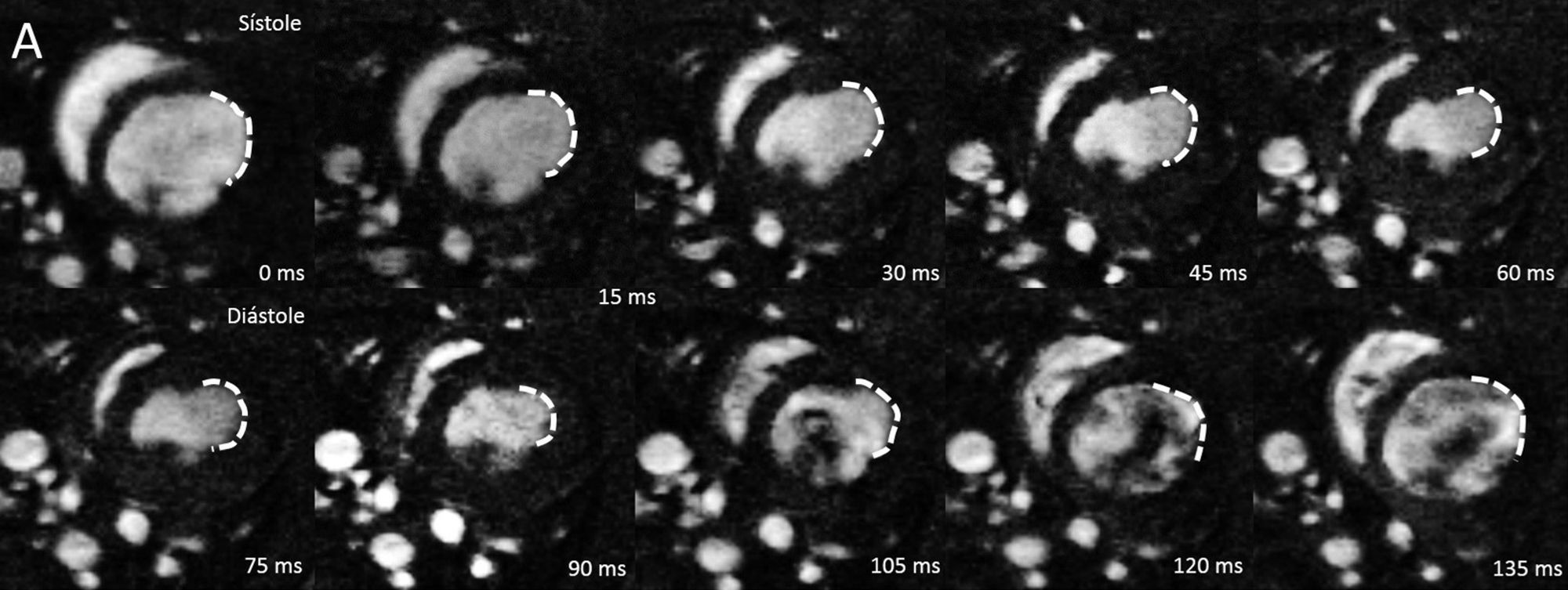
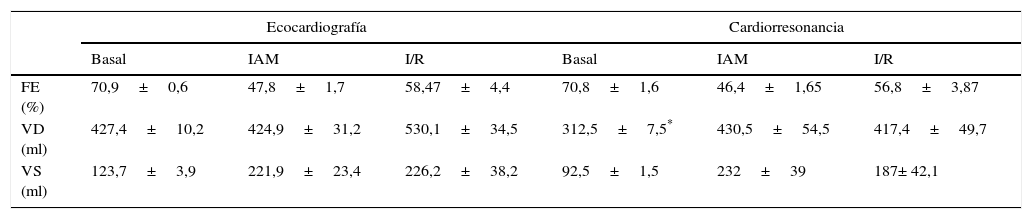
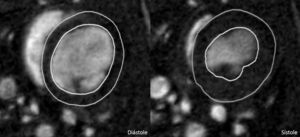
Utilizamos secuencias de cine por RM en el plano eje corto a nivel de músculos papilares para observar defectos de contractilidad en la zona antero-lateral del ventrículo izquierdo, área irrigada por la arteria ocluida (fig. 1). Delimitamos los bordes endocárdico y epicárdico del ventrículo izquierdo en todos los cortes, como se observa en la figura 2; con ello obtuvimos los volúmenes sistólicos y diastólicos y la FE, para cuantificar el daño miocárdico y remodelado tras la isquemia. En la tabla 1 se expone una comparación entre los datos obtenidos por ecocardiografía y por RM cardiaca en nuestros modelos experimentales, viendo solo una diferencia significativa entre los valores basales de volumen diastólico en ambos métodos (p<0,05), habiendo en el resto de valores de FE y volúmenes una importante concordancia entre las 2 modalidades de imagen estudiadas (FE basal p=0,954; FE IAM p=0,656; FE I/R p=0,798; VD IAM p=0,934; VS IAM p=0,846; VS I/R p=0,510) o poca concordancia (VD I/R p=0,09; VS basal p=0,115).
Función cardiaca por ecocardiografía y cardiorresonancia
| Ecocardiografía | Cardiorresonancia | |||||
|---|---|---|---|---|---|---|
| Basal | IAM | I/R | Basal | IAM | I/R | |
| FE (%) | 70,9±0,6 | 47,8±1,7 | 58,47±4,4 | 70,8±1,6 | 46,4±1,65 | 56,8±3,87 |
| VD (ml) | 427,4±10,2 | 424,9±31,2 | 530,1±34,5 | 312,5±7,5* | 430,5±54,5 | 417,4±49,7 |
| VS (ml) | 123,7±3,9 | 221,9±23,4 | 226,2±38,2 | 92,5±1,5 | 232±39 | 187± 42,1 |
Media±error estándar de los valores de fracción de eyección (FE, %), volumen diastólico (VD, ml) y volumen sistólico (VS, ml) de toda la muestra, medidos por ecocardiografía y resonancia magnética en un momento basal y en los modelos de IAM e I/R.
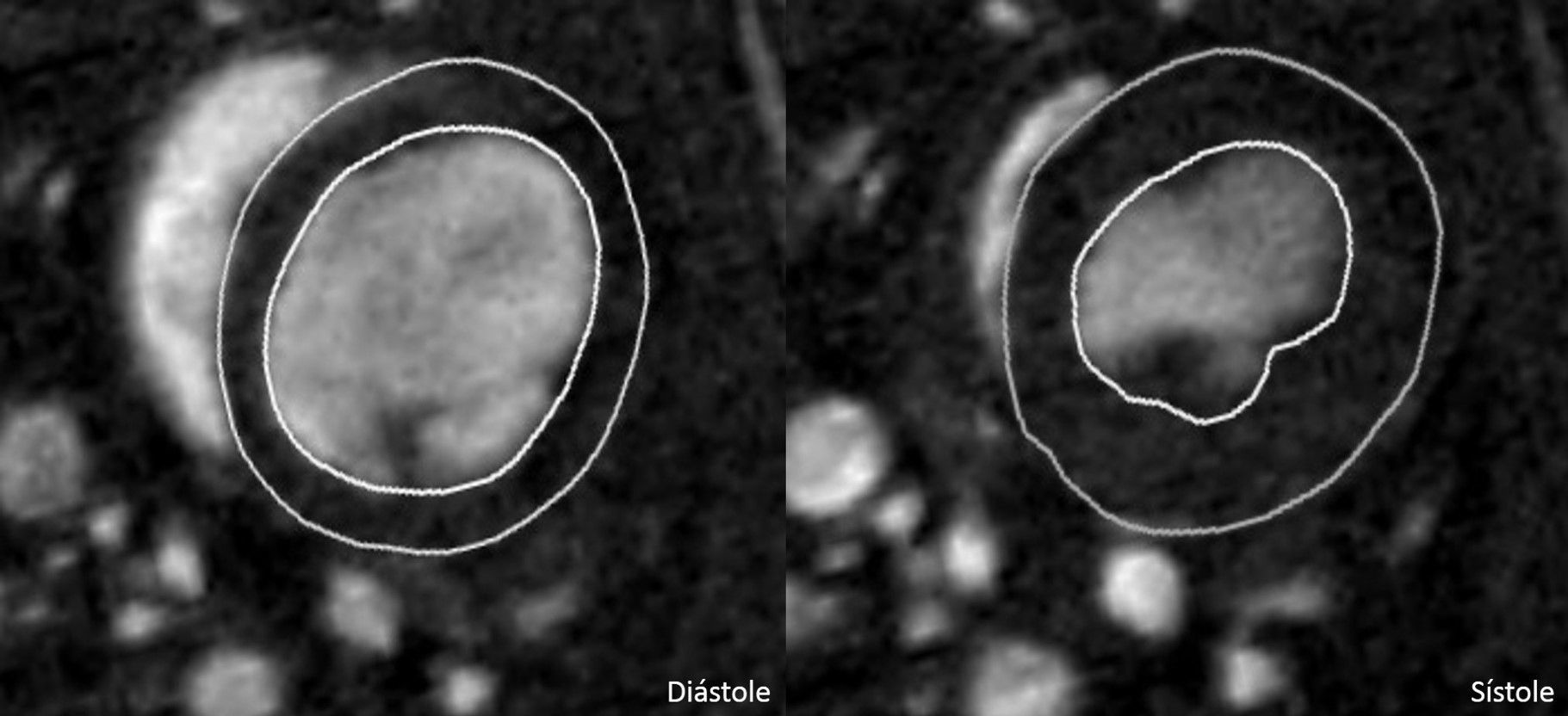
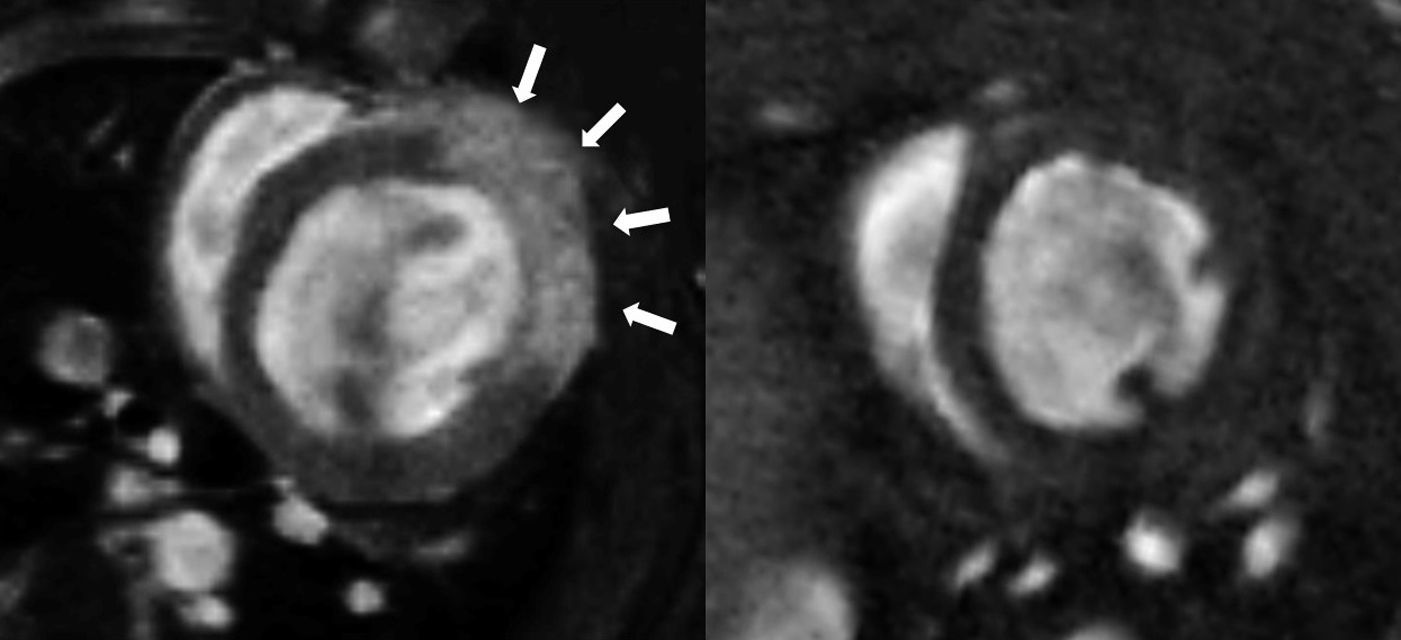
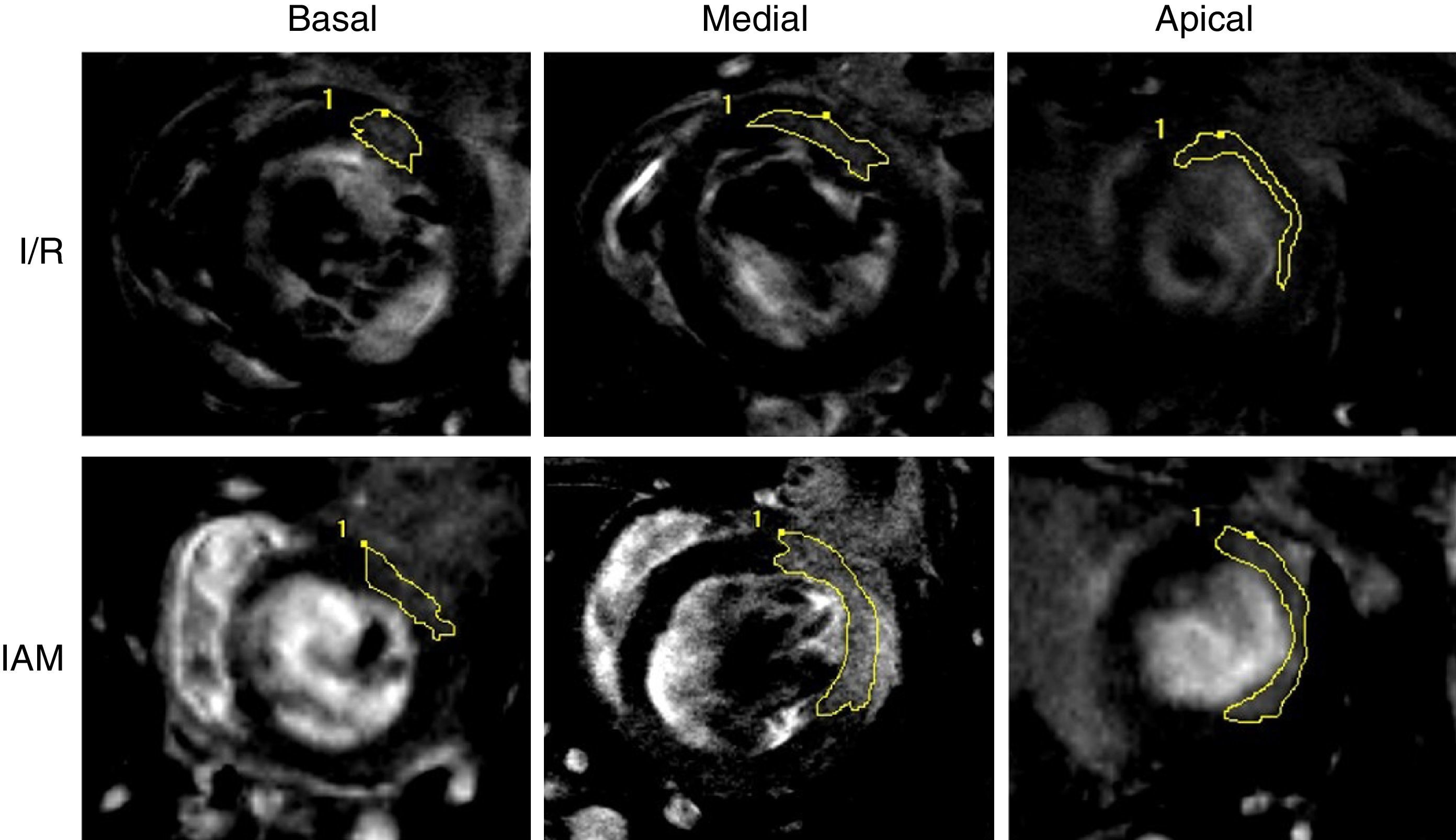
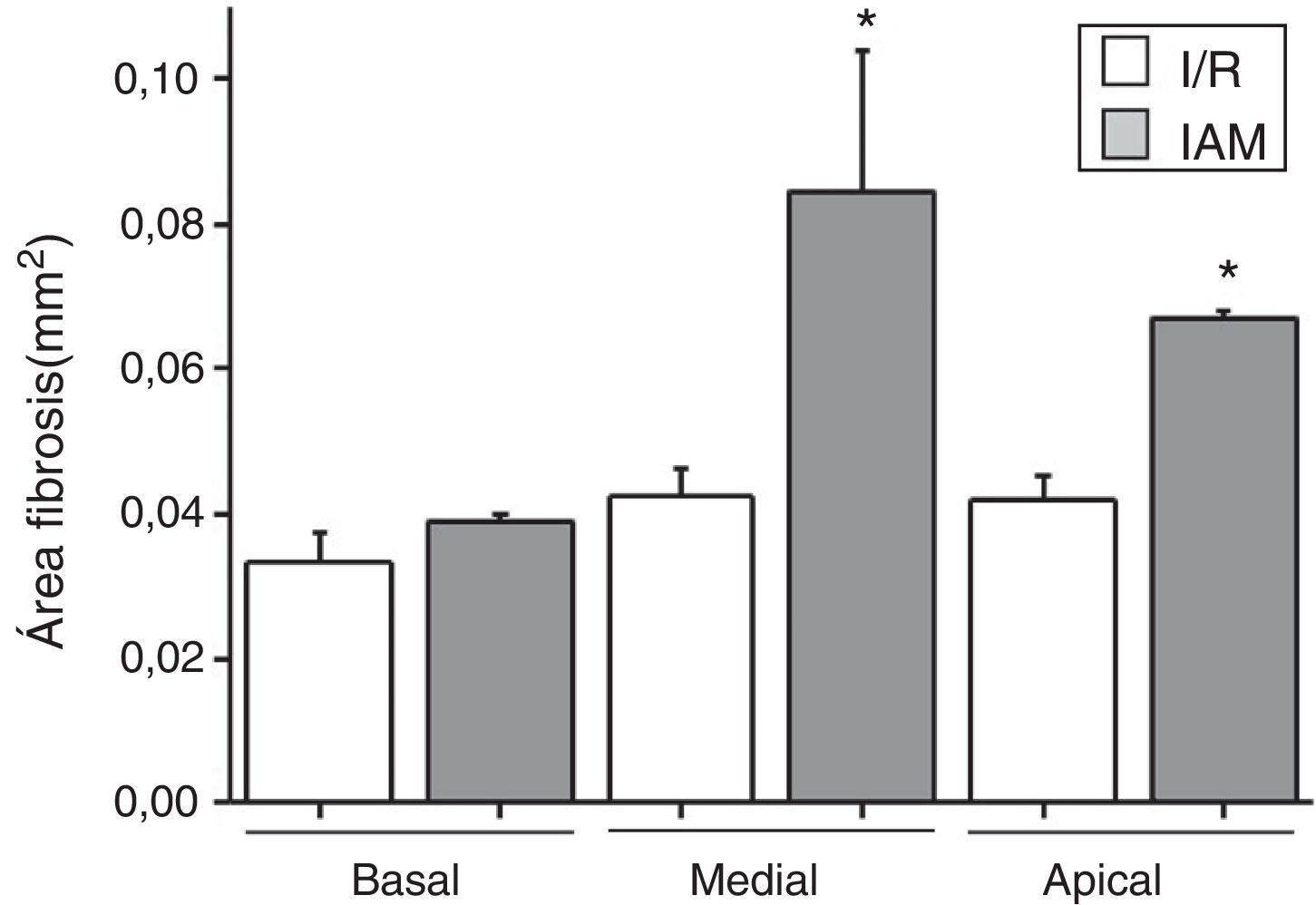
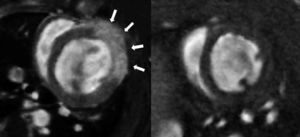
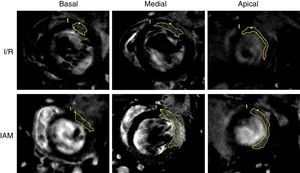
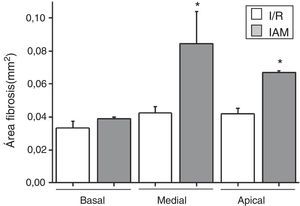
Posteriormente, en las secuencias realizadas con gadolinio en el equipo de RM, se observó un realce miocárdico en los segmentos con fibrosis, en comparación con las secuencias previas a la cirugía (fig. 3), en las que no existe tejido cicatricial. Trazando la zona realzada en los cortes adquiridos a lo largo de todo el corazón, conseguimos definir el área y la cuantificación del daño por fibrosis. En la figura 4 se expone la forma en la que se obtuvieron las áreas realzadas en los 3 cortes de ambos modelos (basal a nivel de válvula mitral, medial a nivel de músculos papilares y en la zona apical del ventrículo izquierdo). Se observa la existencia de fibrosis en los 3 niveles estudiados, con un aumento del área realzada por el contraste en los niveles medial y apical con respecto al basal, viendo también diferencias significativas entre IAM e I/R en los niveles medial y apical (p<0,05) (fig. 5).
Realce miocárdico en un modelo de infarto frente al estudio basal. En la imagen de izquierda, secuencia de realce tardío con gadolinio de un modelo de infarto. Las flechas blancas indican el área del ventrículo izquierdo donde existe fibrosis. A la derecha, la misma secuencia en un estudio basal.
Método de cuantificación de las áreas miocárdicas realzadas a 3 niveles en los modelos de infarto e isquemia-reperfusión. Imágenes de realce tardío realizadas mediante RM en 3 niveles (basal, medial y apical) y en los 2 modelos experimentales (infarto e isquemia-reperfusión). La zona anterior realzada por la fibrosis miocárdica se encuentra delimitada para calcular así el área de fibrosis en cada corte y modelo.
La cardiorresonancia preclínica, siendo una herramienta de diagnóstico no invasiva, nos permite la obtención de imágenes de calidad para el estudio de las enfermedades cardiovasculares más prevalentes, como es la cardiopatía isquémica.
La cuantificación del daño miocárdico por fibrosis y la viabilidad del tejido cardiaco afectado in vivo están entre las ventajas que diferencian a la RM de otras técnicas muy utilizadas en este campo, como es la ecocardiografía, que solo permite una estimación operador-dependiente del daño producido tras la oclusión coronaria7.
Como muestran los resultados de este artículo, existe una gran concordancia entre los valores de FE medidos por RM y los obtenidos por ecocardiografía. Sin embargo, es más notable la disparidad entre los datos de VD y VS, sobre todo en el momento basal. La mayor diferencia entre las 2 técnicas es que mediante los resonadores se accede a una valoración de la patología isquémica más allá de la función miocárdica, pudiendo cuantificar la viabilidad del tejido dañado, un dato relevante en el pronóstico terapéutico de la enfermedad8.
En conclusión, a pesar de que la RM es una técnica que precisa más recursos económicos, gran experiencia técnica y mayor inversión de tiempo, la gran concordancia en la mayoría de los datos obtenidos referentes a la función cardiaca entre la ecocardiografía y la RM de bajo campo hace de esta última una muy buena opción para la investigación preclínica en modelos animales de infarto e isquemia-reperfusión.
FinanciaciónEste estudio fue financiado por el Ministerio español de Economía y Competitividad (BFU2013-45564-C2-2-P); Instituto Carlos III y Red Cardiovascular «RIC» (RD12/0042/0041; PI12/00941), y por la Junta de Andalucía (PI-0108-2012; P10-CVI-6095); ESRP está contratada a cargo del proyecto Improving translational research potential at the Institute of Biomedicine of Seville (ITRIBiS).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.