La formación de pseudoaneurisma de arterias viscerales (PSAV), como una complicación vascular de la pancreatitis, es un fenómeno muy poco frecuente. Aún más excepcional resulta la formación de pseudoaneurismas localizados en la arteria mesentérica superior (AMS).
Reportamos el caso de una paciente de 58 años con antecedentes de enolismo crónico, hipertensión, diabetes mellitus, cirrosis hepática enólica y una pancreatitis crónica enólica con un pseudoquiste pancreático de 32×43mm, según último TAC realizado en mayo de 2011. No antecedentes quirúrgicos.
La paciente acude a urgencias por unas 6h de evolución de dolor intenso en el epigastrio, que irradia a ambos hipocondrios, y se acompaña de náuseas y vómitos. No refiere fiebre ni otra clínica acompañante. Se cursa una analítica en la que destaca amilasemia de 2.215U/l, AST/ALT 32/18U/l, bilirrubina total 2,7mg/dl, leucocitos 21.910mm3 (91%N, 4%L), Hb 15,1g/dl, Hto 42,9% e INR 1,32. Se orienta inicialmente como una pancreatitis crónica reagudizada, y se decide el ingreso en el servicio de digestivo para iniciar tratamiento y seguimiento evolutivo.
A las 24h de su llegada, la paciente permanece hemodinámicamente estable, aunque persiste el dolor intenso en abdomen. En la analítica de control destaca anemización aguda con Hb 10,7g/dl y Hto 29,9%. Se realiza una angio-TAC donde se evidencian signos de pancreatitis crónica, hepatopatía crónica, ascitis difusa (perihepática, periesplénica, entre asas y en pelvis) y una colección hemática heterogénea en varios estadios de evolución con signos de sangrado reciente que engloba la AMS, que sugiere una rotura contenida de pseudoaneurisma de la arteria mesentérica superior (PSAMS) (fig. 1).
Se consulta el caso al servicio de cirugía vascular, y se decide realizar una arteriografía con intención de tratamiento endovascular (TEV) para la exclusión del PSAMS.
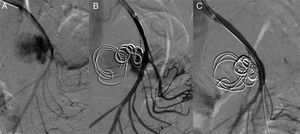
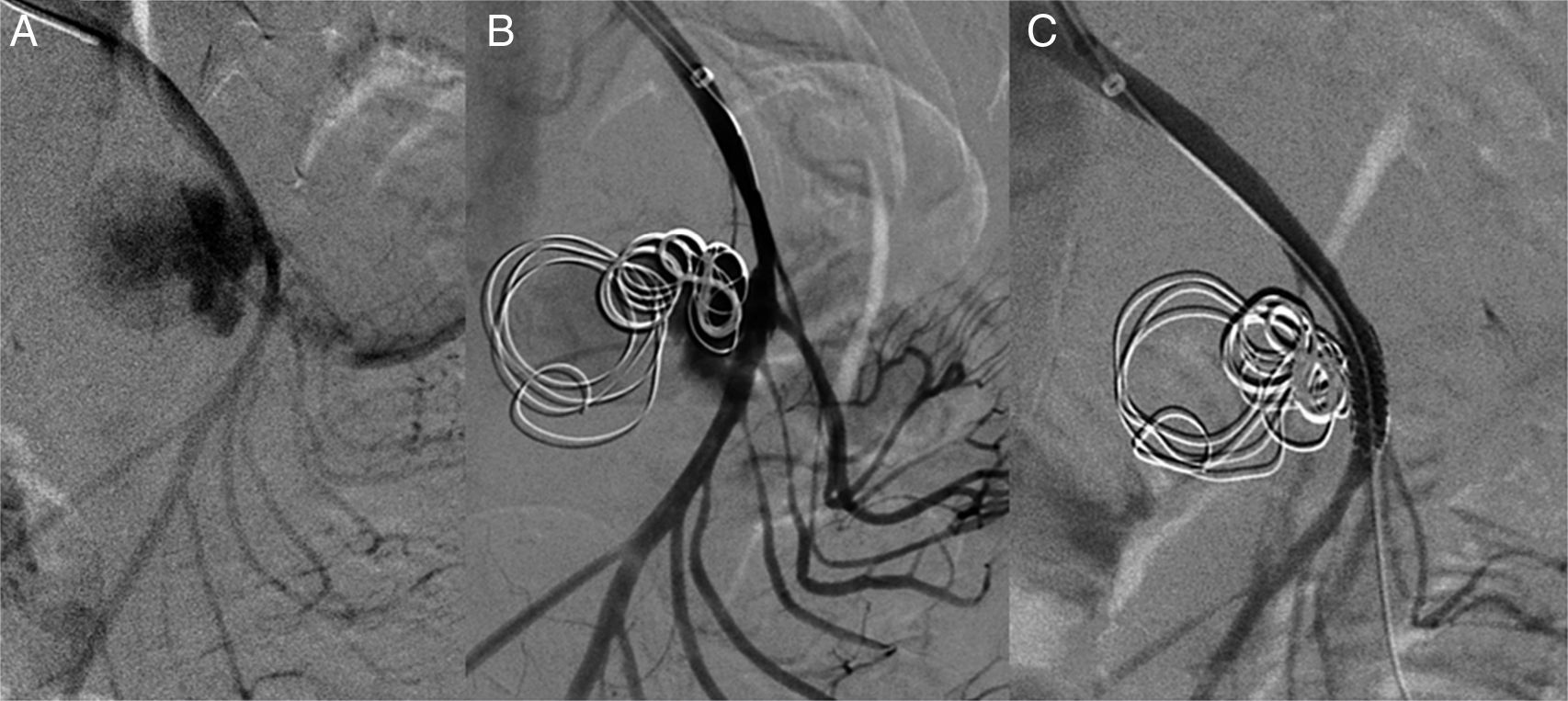
Mediante un acceso humeral izquierdo, se cateteriza la AMS mediante un catéter multipropósito (COOK®), y se coloca un introductor de 6F en el origen de la AMS. Se realiza una arteriografía selectiva, visualizando un gran pseudoaneurisma con cuello ancho y con una luz verdadera irregular de aproximadamente unos 25mm. Mediante una técnica telescópica se cateteriza el saco aneurismático con un microcatéter Progreat® (Terumo), que se posiciona en el interior del pseudoaneurisma. Para evitar que los coils migren a la AMS se utiliza una técnica de andamiaje del saco, embolizando inicialmente con dos microcoils de liberación controlada en J de 25×25mm y 20×50mm tipo DCS (COOK®) creando una «jaula» y, posteriormente, rellenando el saco en forma de ovillo con microcoils DCS espiral de 15×8mm y 10×8mm. Se realiza una angiografía de control, y se aprecia una imagen de contraste remanente a la entrada del saco aneurismático. Se valora continuar con esta técnica, aunque debido al alto riesgo de invasión de la luz arterial por algún coil se decide dejar el microcatéter Progreat® dentro del saco del pseudoanerisma, y colocar un stent cubierto de 5×28mm (BeGraft®) en la AMS, posteriormente se emboliza con un nuevo coil DCS espiral de 10×8mm para acabar de excluir el pseudoaneurisma.
En la comprobación de la arteriografía, se observa la exclusión completa del saco aneurismático con permeabilidad de la AMS, y con la colateralidad preservada excepto en la zona de la colocación del stent donde no hay contrastación de varias ramas yeyunales (fig. 2).
Durante su ingreso hospitalario, la paciente no presentó complicaciones relacionadas con enfermedad vascular, y no tubo nueva anemización. Fue dada de alta a los 20 días posteriores al TEV.
Fue controlada posteriormente en consultas externas mediante la realización de angio-TAC al mes y a los 3 meses de la intervención. No se observó crecimiento ni fugas en la cavidad aneurismática, el stent se mantiene permeable y sin presencia de estenosis. La paciente permanece clínicamente asintomática.
A la vista del caso anterior, podemos destacar que la incidencia de pseudoaneurismas como complicación posterior a pancreatitis es baja y no está bien establecida. Algunas series de casos reportados establecen un rango de incidencia del 1,2-14%1, con una incidencia del 1-6% en las pancreatitis agudas y una incidencia mayor del 7-10% en las pancreatitis crónicas debido a su frecuente asociación con pseudoquistes pancreáticos2.
Diferentes mecanismos han sido sugeridos para explicar la formación de pseudoaneurismas, las 2 teorías más aceptadas se relacionan con: la presencia de un pseudoquiste que erosiona y debilita la pared de una arteria adyacente al páncreas, llevando a la formación de un pseudoaneurisma, y la activación de las enzimas proteolíticas dentro del tejido pancreático, lo que produce la autodigestión del tejido pancreático y de las estructuras adyacentes3,4.
En este sentido, las arterias más afectadas por proximidad al páncreas son la arteria esplénica (50%), seguida de la arteria gastroduodenal (20-50%) y las arterias pancreaticoduodenales (20-30%). El resto de arterias viscerales suele afectarse sobre el 10% de los casos1,5.
Algunos de los factores que aumentan el riesgo de complicaciones vasculares incluyen la pancreatitis necrosante, insuficiencia multiorgánica, sepsis, abscesos, pseudoquistes o necrosis pancreática y tratamiento anticoagulante2,6.
A diferencia de los aneurismas verdaderos, la mayoría de los PSAV son sintomáticos. Es habitual que presenten clínica de dolor abdominal y, en caso de rotura, diferentes tipos de sangrado como pueden ser: hemosuccus pancreático, hemorragia digestiva a retroperitoneo y cavidad abdominal, entre otras6. En relación con el diagnóstico y estudio de los PSAV, la angio-TAC es la prueba de primera elección, si bien la prueba gold standard en estos casos sería la arteriografía, que permite realizar un tratamiento endovascular en el mismo acto7,8.
Los PSAV siempre requieren tratamiento, independientemente de su tamaño y de los síntomas. El tratamiento conservador no es recomendable debido a la alta tasa de rotura y una mortalidad de hasta el 90% de los casos no tratados. El objetivo principal del tratamiento es la exclusión del saco aneurismático9. El tratamiento clásico comprende la cirugía reconstructiva o ligadura, pero debido a su elevada morbimortalidad (50-100%) ha sido remplazada en la mayoría de los casos por el tratamiento endovascular, ya que se relaciona con un bajo riesgo de complicaciones y menor mortalidad (13-50%)3.
El objetivo del TEV es la exclusión del saco aneurismático mediante la embolización y/o la colocación de un stent en la arteria afectada9. El éxito técnico global es alto, del 79-100%, aunque en el 6-55% de los casos se precisa más de un procedimiento para lograr la exclusión completa del pseudoaneurisma3.





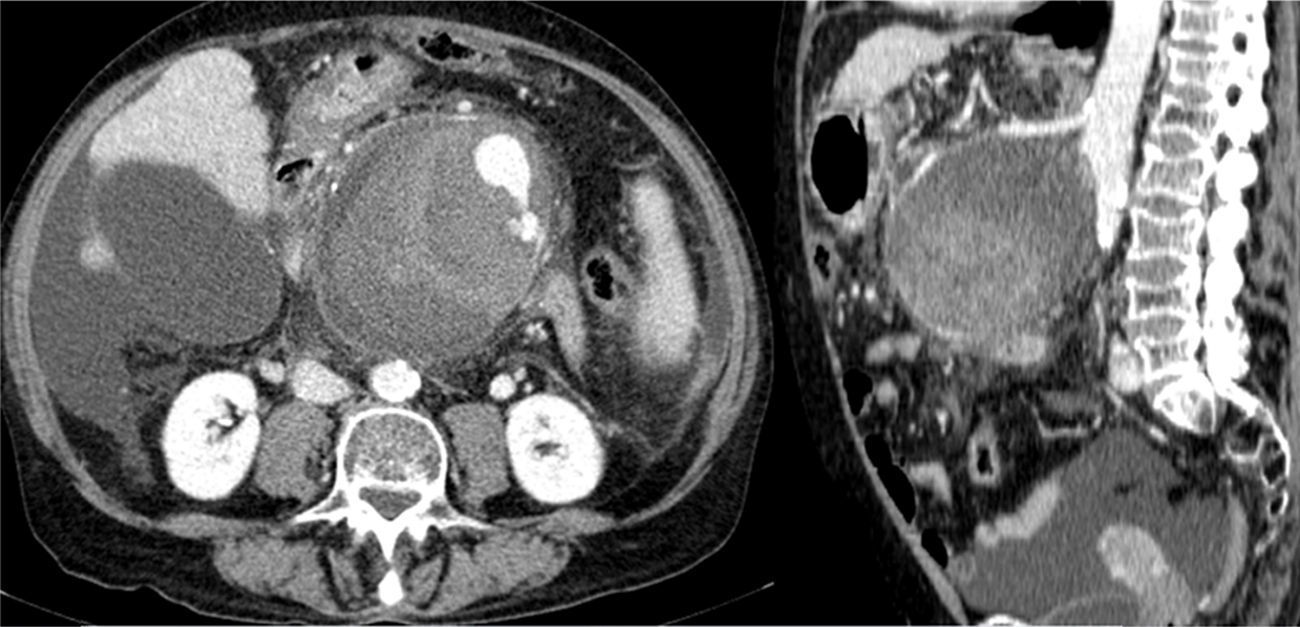
![Angio-TAC de abdomen: muestra el PSAMS (102×98×103mm [AP×LL×CC]). Angio-TAC de abdomen: muestra el PSAMS (102×98×103mm [AP×LL×CC]).](https://static.elsevier.es/multimedia/02105705/0000004000000008/v1_201709230034/S0210570516300966/v1_201709230034/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)