La inmunodeficiencia común variable (IDCV) es poco frecuente, estimándose que afecta a uno de cada 25.000 individuos. Cursa con déficit en la producción de anticuerpos y presenta una gran variedad de manifestaciones clínicas1. Según el mayor registro europeo realizado, las principales afecciones presentadas fueron neumonía (32%), autoinmunidad (29%), esplenomegalia (26%) y bronquiectasias (23%)2.
Presentamos el caso de una paciente con IDCV, que presentó una infección oportunista por citomegalovirus (CMV) que evolucionó de manera satisfactoria tras realizar tratamiento con ganciclovir y un anti-TNF.
Mujer de 37 años, diagnosticada 8 años antes de IDCV a raíz de infecciones respiratorias de repetición. Se encontraba en tratamiento con inmunoglobulinas y B12, en seguimiento por digestivo por presentar diarrea crónica, que en el contexto de un proceso de inmune y descartada causa infecciosa, fue tratada con corticoides con respuesta positiva.
Ingresa por incremento de la diarrea, 6-8 deposiciones/día, sin productos patológicos y asociada a pérdida de peso de 10kg. A la exploración, destaca: IMC de 17, abdomen distendido, doloroso a la palpación, sin peritonismo con ruidos normales.
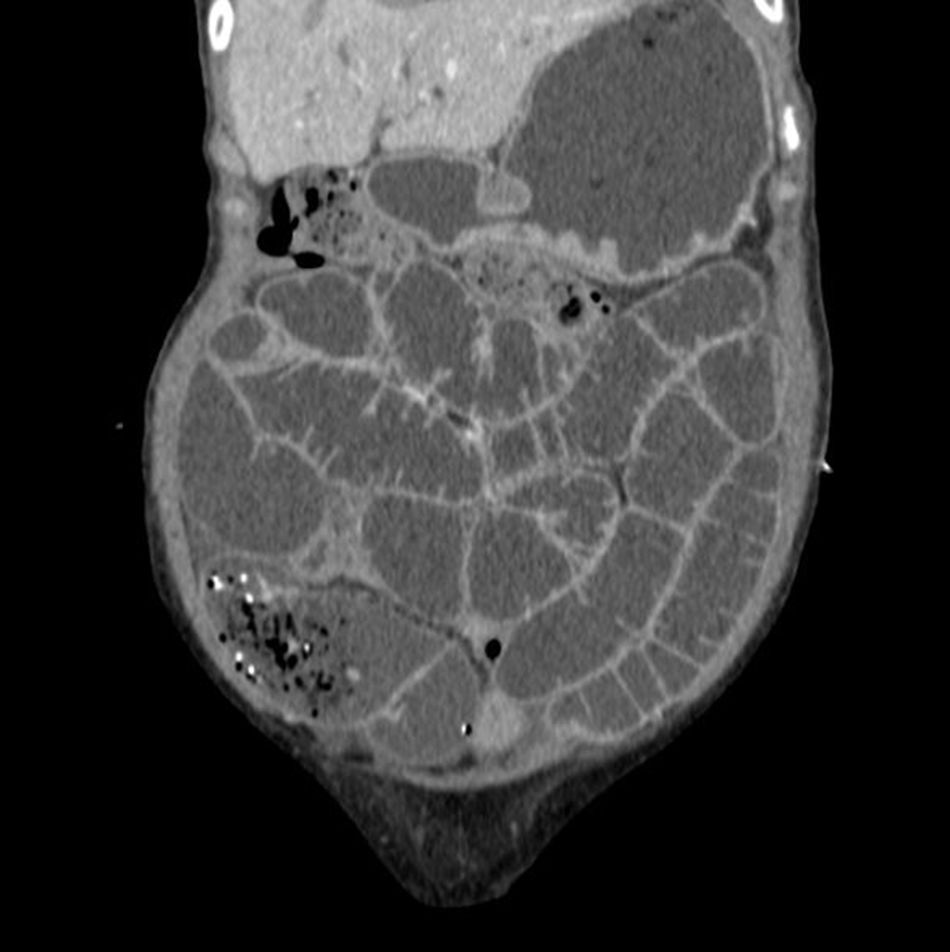
El estudio mediante coprocultivos (×3), parásitos en heces (×3), toxina C. difficile (×3), tinción de auramina en heces, cultivo de micobacterias, Tropheryma whipplei PCR en saliva y heces, fueron negativos. Gastroscopia y colonoscopia sin alteraciones endoscópicas; en cambio, en la biopsia duodenal y en las biopsias aleatorias del colon se objetivó edema e infiltrado linfoplasmocitario en la lámina propia. Se realiza TAC abdomino-pélvica, evidenciándose hepatomegalia homogénea, esplenomegalia y adenopatías retroperitoneales y mesentéricas, hipodensas mayores de un centímetro (fig. 1).
Ante la tórpida evolución clínica, persistencia de la diarrea y el hallazgo de adenopatías retroperitoneales y hepato-esplenomegalia, nos planteamos el diagnóstico diferencial con linfoma, como entidad responsable de la de las manifestaciones clínicas de la paciente.
Dada la falta de acceso a las adenopatías por ecoendoscopia, optamos por resección con laparoscopia de una adenopatía mesentérica. El estudio histológico, mediante tinción de hematoxilina-eosina demostró inclusiones intranucleares eosinofílicas rodeadas de un halo que corresponden a la típica imagen en ojo de búho. Esto es compatible con infección invasiva por CMV.
Previa a infusión rutinaria de inmunoglobulinas, la paciente presentaba hipoalbuminemia e hipogammaglobulinemia con albúmina de 2,90g/dl, gammaglobulinas de 0,46g/dl (IgG: 594, IgA<20 e IgM<17mg/dl) y una carga sérica positiva para CMV, 2.895 copias/ml, analizado mediante PCR en sangre periférica.
Con los hallazgos descritos se inicia tratamiento para la infección por CMV con ganciclovir durante 5 días y posteriormente con valganciclovir hasta completar 21 días. La paciente presentó mejoría clínica, por lo que se procedió al alta.
Dos semanas más tarde, reingresa con 4-5 deposiciones/día y distensión abdominal. De nuevo el estudio de heces (coprocultivos, parásitos y C. difficile) fue negativo y los niveles de gammaglobulinas séricas no mostraban cambios significativos. La carga del CMV había disminuido a 220copias/m. Se decide comenzar tratamiento con infliximab a dosis de 5mg/kg con la pauta de inducción (0/2/6 semanas) y posteriormente dosis de mantenimiento cada 8 semanas.
Al alta, la paciente continua seguimiento en consulta, objetivándose una respuesta clínica favorable, con una deposición/día y un aumento de 5kg de peso a las 8 semanas de iniciar el tratamiento.
La IDCV es la inmunodeficiencia primaria más frecuente, después del déficit selectivo de IgA. Las manifestaciones clínicas comienzan en la segunda y tercera década, sin diferencia de sexo. Se caracteriza por presentar infecciones recurrentes que afectan principalmente al tracto respiratorio3. Las manifestaciones digestivas aparecen más tarde, siendo la diarrea la más frecuente, junto con malabsorción, giardiasis, déficit de B12, hepatomegalia y esplenomegalia. Además, en la mayoría de los casos para llegar al diagnóstico se precisa realizar una endoscopia para tomar biopsias. Las alteraciones de histología duodenal en estos pacientes son complicadas de evaluar por el frecuente asociado sobrecrecimiento bacteriano4.
Presenta una disfunción en la diferenciación de linfocitos B a células plasmáticas, afectando también a los linfocitos T. Debido a la disregulación del sistema inmune estos pacientes son más susceptibles a padecer linfoma no Hodgkin, neoplasias gastrointestinales, enfermedades autoinmunes, infecciones oportunistas y enfermedad inflamatoria intestinal5. La colitis ulcerosa y la enfermedad de Crohn que se observan en la IDCV tienen características distintas que las definen como «like». La diferencia fundamental es la ausencia de células plasmáticas y de granulomas de células gigantes6.
Descartado el origen infeccioso, el tratamiento de la enteropatía grave en IDCV, resistente a corticoides, no se encuentra bien establecido. Se han descrito algunos casos que han respondido favorablemente al tratamiento con anti-TNF obteniendo ganancia ponderal y mejoría en la calidad de vida7,8.
En casos excepcionales, como el que presentamos, el tratamiento con anti-TNF se justifica por la severidad clínica en ausencia de otros hallazgos patológicos. La eficacia del fármaco, podría estar en relación con niveles elevados de TNF-α en el suero y tejidos descritos en algunos pacientes con IDCV. También se ha observado que el TNF-α aumenta la replicación de CMV in vitro9, lo que presupone que infliximab, como anti-TNF, podría inhibir la reactivación de CMV in vivo. Todo ello, podría explicar la respuesta favorable al tratamiento con infliximab que ha presentado nuestra paciente.