La incorporación de los antivirales de acción directa al tratamiento de la hepatitis C crónica permite simplificar el diagnóstico y seguimiento del paciente, optimizando los recursos asistenciales (consultas y pruebas) dedicados al abordaje de la enfermedad. El objetivo fue estimar el impacto económico derivado de esta simplificación. La optimización de recursos asistenciales se estimó, mediante el método Delphi, a partir de un panel de 36 expertos clínicos españoles, y de las guías de práctica clínica. Los costes unitarios (€ en 2017) de los recursos sanitarios considerados se obtuvieron de fuentes españolas. La simplificación del proceso, así como la coordinación entre el médico especialista, enfermería y el servicio de farmacia, generarían unos ahorros por paciente de 591,17 €. Asimismo, se estima que la duración media de las consultas sería inferior con regímenes diarios de 1 solo comprimido que con regímenes de más de 1 comprimido al día.
Información sobre el suplemento: este artículo forma parte del suplemento titulado “El valor de la simplicidad en el tratamiento de la hepatitis C”, que ha sido patrocinado por Gilead.
© 2019 Elsevier España, S.L.U. Todos los derechos reservados.
TThe incorporation of direct-acting antiviral agents to the treatment of chronic hepatitis C infection has simplified diagnosis and follow-up, allowing optimisation of health resources (consultations and tests) dedicated to the management of the disease. The aim of this study was to estimate the economic impact of this simplification. Health resource optimisation was estimated through the Delphi method, based on a panel of 36 experts, consisting of Spanish clinicians, and on clinical practice guidelines. The unit costs (€ in 2017) of the health resources included were obtained from Spanish sources. Simplification of the process, as well as liaison between the medical specialist, nurses and the pharmacy service, would generate savings of €591.17 per patient. Likewise, the mean length of consultations would be shorter with regimens of only 1 tablet daily compared with regimens of more than 1 tablet daily.
Supplement information: This article is part of a supplement entitled “The value of simplicity in hepatitis C treatment”, which is sponsored by Gilead.
© 2019 Elsevier España, S.L.U. All rights reserved.
La prevalencia de anticuerpos del virus de la hepatitis C (VHC) en España se estima en el 1,11% (0,7-1,5%) de la población adulta1. Según estimaciones del año 2006, en España se producirían anualmente entre 3.873 y 4.464 defunciones por hepatitis C (HC), lo que supondría el 1-1,2% de la mortalidad en España por todas las causas2. De acuerdo con el documento del Plan Estratégico para el abordaje de la HC (PEAHC) en el Sistema Nacional de Salud (SNS)2, los nuevos fármacos antivirales de acción directa (AAD) simplifican el tratamiento, reducen las necesidades de seguimiento, aumentan las tasas de curación de la infección y evitan en gran medida la aparición de las complicaciones tardías y graves de la enfermedad. Con los AAD se obtienen elevadas tasas de respuesta viral sostenida (RVS), superiores al 90%3, motivo por el que la Organización Mundial de la Salud considera un objetivo alcanzable la eliminación mundial de la HC en el año 20304. Además, la alta tasa de eficacia de los AAD se trasladaría al ámbito clínico como una reducción de la incidencia del desarrollo de cirrosis, hepatocarcinomas y de indicación de trasplantes hepáticos por HC5,6 y, por tanto, de la mortalidad relacionada con estos eventos, por lo que se generaría una ganancia de años de vida adicionales en los pacientes con y sin HC candidatos a trasplante hepático7. Según un estudio español reciente8,9, en el que se evaluó el tratamiento con AAD en el marco del PEAHC tras 2 años de su implementación, el tratamiento basado en AAD conllevaría una reducción del 82% de las muertes por causa hepática, así como una disminución significativa de la morbilidad hepática (un 87% de los casos de cirrosis descompensada, un 74% de los casos de carcinoma hepatocelular y un 84% de los trasplantes hepáticos), así como del coste asociado al manejo de estas complicaciones. Dicho estudio muestra que el tratamiento con AAD representa un uso eficiente de los recursos en comparación con la estrategia anterior a la introducción de dichos fármacos, con un coste por año de vida ganado por calidad muy inferior a los umbrales de eficiencia generalmente utilizados en España.
Por otro lado, el tratamiento de la HC con los AAD tendría un impacto económico derivado de la reducción del absentismo y presentismo laboral, y se ha estimado un ahorro laboral por el uso de los AAD en España de entre 97 y 211 millones de euros anuales10,11. Además de las ventajas indicadas, la incorporación de los AAD al tratamiento farmacológico de la HC permite simplificar el seguimiento del paciente2, con la optimización del número de recursos asistenciales (principalmente consultas y pruebas) dedicados al manejo de la enfermedad. El objetivo de este estudio fue estimar el impacto económico derivado de la optimización o simplificación de los recursos asistenciales en el seguimiento del paciente con HC tratado con AAD, desde la perspectiva del SNS.
MétodosLa optimización de recursos asistenciales en el paciente con HC tratado con AAD se estimó a partir de un panel de expertos clínicos, siguiendo la metodología Delphi12 y de las guías de práctica clínica13-16. Se diseñó un cuestionario, validado por un comité científico, que incluyó distintos profesionales sanitarios involucrados en el manejo de pacientes con HC crónica y que se cumplimentó por 36 expertos españoles (23 hepatólogos o infectólogos, 1 médico de atención primaria, 1 médico de prisiones, 1 médico de centro de adicciones, 7 farmacéuticos hospitalarios, 2 enfermeros y 1 microbiólogo). Dicho cuestionario recogía diferentes aspectos sobre el uso de recursos asistenciales para las siguientes etapas: a) diagnóstico; b) basal; c) semana 4; d) semana 8; e) finalización del tratamiento; f) evaluación de la RVS en la semana 12, y g) evaluación de la RVS en las semanas 24 o 4812. Los recursos analizados fueron las consultas al médico especialista, las consultas a enfermería, las consultas al servicio de farmacia, así como las pruebas de diagnóstico y/o seguimiento de la enfermedad (carga viral, genotipado y subgenotipado del VHC, función hepática, fibroscan y ecografía)12. En primer lugar, el panel hizo una estimación del consumo actual de recursos sanitarios según el seguimiento más habitual de los pacientes que reciben un tratamiento de 12 semanas. En segundo lugar, se pidió a los expertos que valorasen, de acuerdo con las actuales guías de práctica clínica y con su propia experiencia, de qué manera podría simplificarse u optimizarse el uso de recursos sanitarios (reducción en el número de consultas o pruebas) en dichos pacientes tratados con AAD. Estas estimaciones se realizaron para regímenes de 12 y 8 semanas de tratamiento. El análisis cubrió el período comprendido entre el diagnóstico de la enfermedad y la evaluación de la RVS en las semanas 24 o 48. Se utilizó un cuestionario de 44 ítems y se realizaron 2 rondas de respuestas. La primera ronda se subdividió en 2 fases de análisis. En la primera fase, el experto manifestó su grado de acuerdo mediante una escala de tipo Likert valorada de 1 a 5, indicando con el valor 1 un total desacuerdo y con el valor 5 un acuerdo total con la afirmación. Una vez obtenidas las respuestas para los 44 ítems y realizado un análisis descriptivo de los datos, que mostraron la frecuencia de respuestas para cada una de las cuestiones planteadas, se procedió a realizar la segunda fase del estudio. En esta fase se seleccionaron las cuestiones con menos de un 75% de acuerdo mediante las siguientes categorías de respuesta: 1 o 2, en desacuerdo; 3, neutro; 4 o 5, de acuerdo. En esta segunda fase del estudio, se propuso una respuesta dicotómica (acuerdo sí/acuerdo no), para obtener así un grado de consenso más elevado. Respecto al uso de recursos sanitarios (consultas y pruebas) se recogió la opinión de los miembros del panel de manera cuantitativa. De esa manera, se recogió el número de consultas y el número de pruebas con las pautas actuales de tratamiento y en el caso de que se pudieran simplificar. La cuantificación se realizó para las diferentes etapas del tratamiento y seguimiento (diagnóstico, basal, semana 4, semana 8, semana 12, final del tratamiento, RVS semana 12, RVS semana 24, RVS semana 48, seguimiento a 1 año). Estos datos cuantitativos se utilizaron en el modelo económico para estimar los costes, con o sin la simplificación del proceso respecto al número de consultas y pruebas.
Los resultados obtenidos del panel de expertos sobre el uso actual de recursos y su previsible simplificación se incluyeron en un modelo de costes realizado en Microsoft Excel. El número de recursos estimado por el panel se multiplicó por sus correspondientes costes unitarios (expresados en euros [€] del año 2017), que se obtuvieron de fuentes españolas17 (tabla 1).
Costes unitarios españoles del diagnóstico y seguimiento del paciente con hepatitis C (€ 2017)17
| Recurso sanitario | Coste (€) |
|---|---|
| Seguimiento del paciente | |
| Consulta al médico especialista (primera) | 142,94 |
| Consulta al médico especialista (siguiente) | 87,11 |
| Consulta de enfermería (primera) | 48,47 |
| Consulta de enfermería (siguiente) | 26,73 |
| Estudio de interacciones (servicio de farmacia) (primero) | 120,39 |
| Estudio de interacciones (servicio de farmacia) (siguiente) | 70,07 |
| Diagnóstico de la enfermedad | |
| Consulta al médico especialista | 142,94 |
| Carga viral | 137,42 |
| Genotipado/subgenotipado | 176,07 |
| Función hepática | 32,14 |
| Fibroscan | 73,70 |
| Ecografía | 97,70 |
Se realizaron análisis de costes determinísticos, con valores fijos de las variables (costes por paciente del diagnóstico de la HC, de la valoración basal del paciente, del seguimiento en las semanas 4 y 8, al final del tratamiento y en la evaluación de la RVS en las semanas 12 y 24/48), así como de los resultados. También se efectuaron análisis probabilísticos mediante simulaciones de Monte Carlo de segundo orden en una cohorte hipotética de 1.000 pacientes. Los costes utilizados en el análisis probabilístico se ajustaron a distribuciones gamma18,19.
Los resultados se presentan del modo siguiente: a) simplificación del abordaje (uso de recursos sanitarios) del paciente con HC según el panel de expertos; b) coste por paciente según el tipo de abordaje (actual o simplificado) y las etapas del manejo del paciente (diagnóstico, basal, semana 4, etc.). Finalmente, también se presenta la estimación del panel de expertos respecto al tiempo medio dedicado por los diferentes profesionales sanitarios (médico especialista, enfermera, farmacéutico) para el tratamiento farmacológico del paciente con HC, según el número de comprimidos del régimen farmacológico.
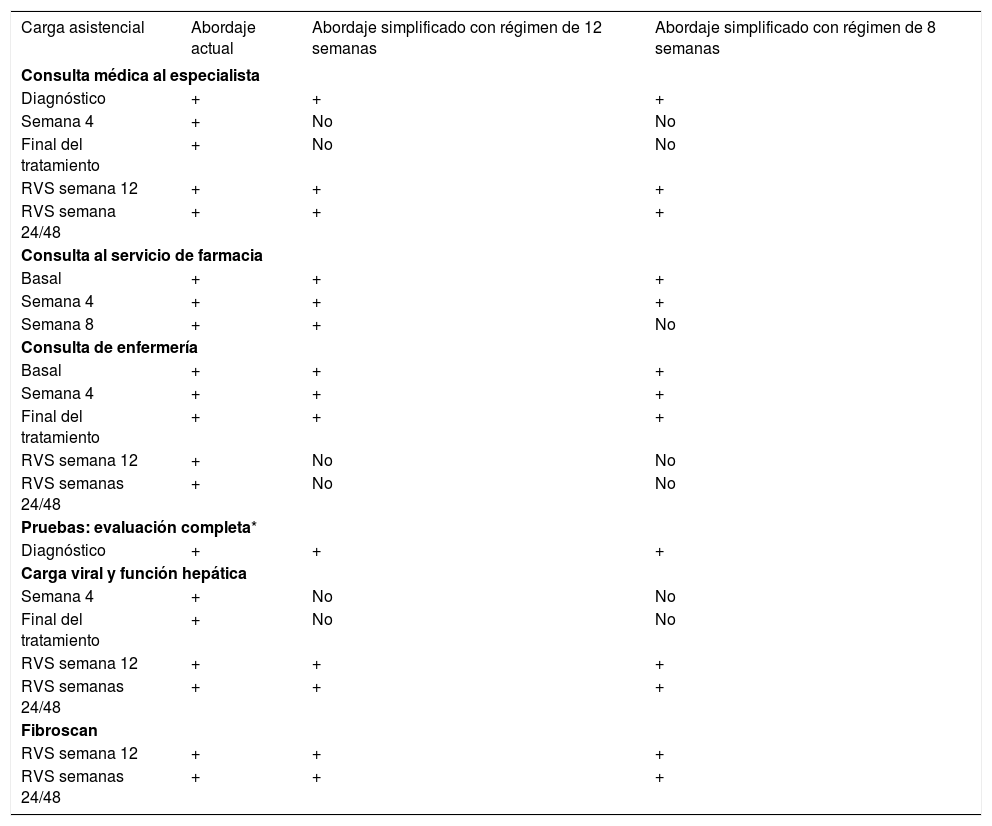
ResultadosConsumo de recursos derivados del abordaje del paciente con hepatitis C según el panel de expertosSegún el panel de expertos, para un tratamiento de 12 semanas, el 54% de los clínicos indicaron que los pacientes con HC acudirían a 5 consultas médicas con el especialista (gastroenterólogo, hepatólogo, infectólogo). El 57% de los farmacéuticos indicó un promedio de 3 consultas al servicio de farmacia y en el 100% de las consultas de enfermería habría un promedio de 5 consultas. En estos pacientes, se aplicaría una batería de pruebas para el diagnóstico que incluiría la determinación de la carga viral, el genotipado/subgenotipado del VHC, analítica de perfil hepático, una elastografía (fibroscan) y una ecografía12. En seguimientos posteriores del paciente se repetirían en 4 ocasiones la determinación de la carga viral y la analítica de perfil hepático y en 2 la elastografía (fibroscan). En la tabla 2 se presenta de manera esquemática las consultas y pruebas que se podrían simplificar en el manejo del paciente.
Simplificación del abordaje del paciente con hepatitis C según el panel de expertos
| Carga asistencial | Abordaje actual | Abordaje simplificado con régimen de 12 semanas | Abordaje simplificado con régimen de 8 semanas |
|---|---|---|---|
| Consulta médica al especialista | |||
| Diagnóstico | + | + | + |
| Semana 4 | + | No | No |
| Final del tratamiento | + | No | No |
| RVS semana 12 | + | + | + |
| RVS semana 24/48 | + | + | + |
| Consulta al servicio de farmacia | |||
| Basal | + | + | + |
| Semana 4 | + | + | + |
| Semana 8 | + | + | No |
| Consulta de enfermería | |||
| Basal | + | + | + |
| Semana 4 | + | + | + |
| Final del tratamiento | + | + | + |
| RVS semana 12 | + | No | No |
| RVS semanas 24/48 | + | No | No |
| Pruebas: evaluación completa* | |||
| Diagnóstico | + | + | + |
| Carga viral y función hepática | |||
| Semana 4 | + | No | No |
| Final del tratamiento | + | No | No |
| RVS semana 12 | + | + | + |
| RVS semanas 24/48 | + | + | + |
| Fibroscan | |||
| RVS semana 12 | + | + | + |
| RVS semanas 24/48 | + | + | + |
RVS: respuesta viral sostenida.
Según el panel de expertos12, en el abordaje simplificado del paciente se contempla la posibilidad de eliminar algunas consultas al especialista, de enfermería y del servicio de farmacia en el caso de optar por determinados tratamientos que no requieran monitorización, bien por reacciones adversas, por anomalías de laboratorio o bien por interacciones farmacológicas. En concreto, se considera que podrían obviarse las consultas al médico especialista en la semana 4 y al final del tratamiento, así como las consultas de enfermería en la evaluación de la RVS en las semanas 12 y 24/4812 (tabla 2).
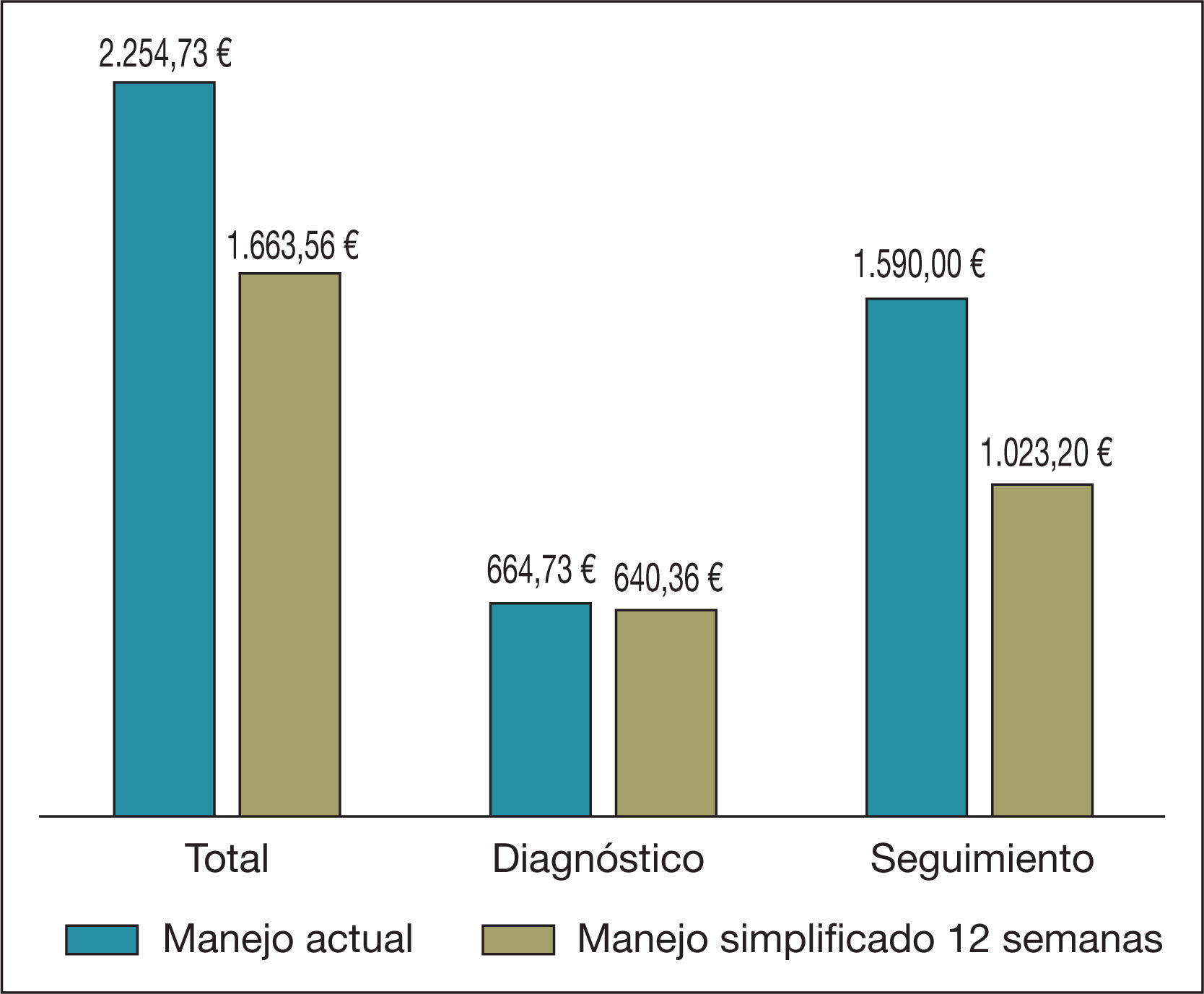
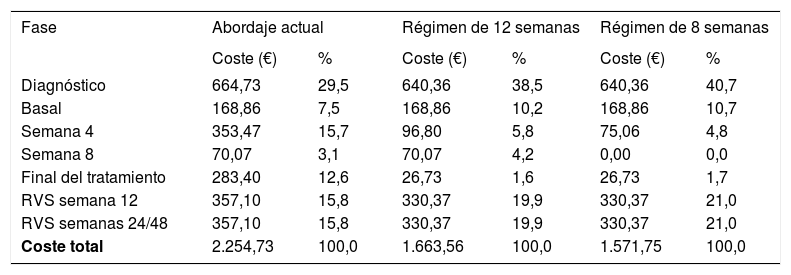
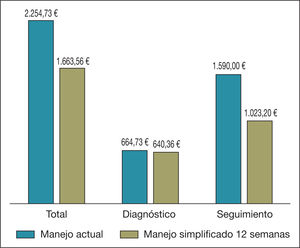
Ahorro por paciente según la etapa de abordaje de la hepatitis CComo puede observarse en la tabla 3 y en la figura 1, en el análisis determinístico el coste de un paciente con HC sería de 2.254,73 € con el abordaje actual y de 1.663,56 € con el simplificado, para un régimen de 12 semanas; por tanto, el coste asociado a la estrategia de optimización de los recursos es un 26,2% inferior al coste de la estrategia actual, lo que genera un ahorro por paciente de 591,17 €. En el caso de que se adoptara un régimen de 8 semanas, el ahorro que se obtendría sería de 682,98 €.
Coste por paciente según las etapas y el tipo de abordaje de la hepatitis C con un régimen de 12 u 8 semanas
| Fase | Abordaje actual | Régimen de 12 semanas | Régimen de 8 semanas | |||
|---|---|---|---|---|---|---|
| Coste (€) | % | Coste (€) | % | Coste (€) | % | |
| Diagnóstico | 664,73 | 29,5 | 640,36 | 38,5 | 640,36 | 40,7 |
| Basal | 168,86 | 7,5 | 168,86 | 10,2 | 168,86 | 10,7 |
| Semana 4 | 353,47 | 15,7 | 96,80 | 5,8 | 75,06 | 4,8 |
| Semana 8 | 70,07 | 3,1 | 70,07 | 4,2 | 0,00 | 0,0 |
| Final del tratamiento | 283,40 | 12,6 | 26,73 | 1,6 | 26,73 | 1,7 |
| RVS semana 12 | 357,10 | 15,8 | 330,37 | 19,9 | 330,37 | 21,0 |
| RVS semanas 24/48 | 357,10 | 15,8 | 330,37 | 19,9 | 330,37 | 21,0 |
| Coste total | 2.254,73 | 100,0 | 1.663,56 | 100,0 | 1.571,75 | 100,0 |
RVS: respuesta viral sostenida.
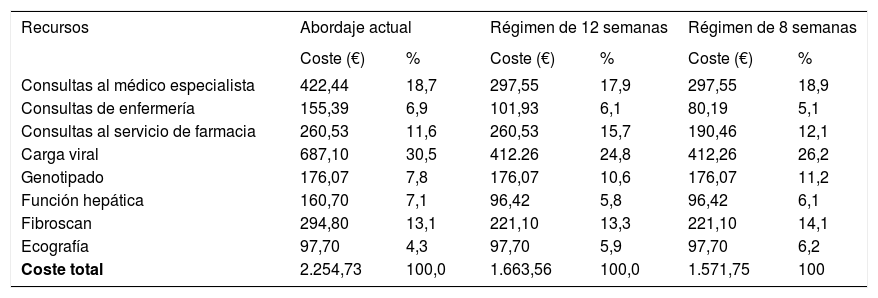
El ahorro a consecuencia de la simplificación u optimización del uso de recursos sanitarios en el paciente con HC se produciría por la reducción en el número de evaluaciones de la carga viral (274,84 € para 12 y 8 semanas de tratamiento), consultas al médico especialista (124,89 €), fibroscan (73,70 €), pruebas de la función hepática (64,28 €), consultas de enfermería (53,46 y 75,20 € para 12 y 8 semanas de tratamiento, respectivamente) y de farmacia (70,7 € con la pauta de 8 semanas de tratamiento) (tabla 4).
Coste estimado por paciente de los recursos sanitarios utilizados en el abordaje de la hepatitis C con un régimen de 12 u 8 semanas
| Recursos | Abordaje actual | Régimen de 12 semanas | Régimen de 8 semanas | |||
|---|---|---|---|---|---|---|
| Coste (€) | % | Coste (€) | % | Coste (€) | % | |
| Consultas al médico especialista | 422,44 | 18,7 | 297,55 | 17,9 | 297,55 | 18,9 |
| Consultas de enfermería | 155,39 | 6,9 | 101,93 | 6,1 | 80,19 | 5,1 |
| Consultas al servicio de farmacia | 260,53 | 11,6 | 260,53 | 15,7 | 190,46 | 12,1 |
| Carga viral | 687,10 | 30,5 | 412.26 | 24,8 | 412,26 | 26,2 |
| Genotipado | 176,07 | 7,8 | 176,07 | 10,6 | 176,07 | 11,2 |
| Función hepática | 160,70 | 7,1 | 96,42 | 5,8 | 96,42 | 6,1 |
| Fibroscan | 294,80 | 13,1 | 221,10 | 13,3 | 221,10 | 14,1 |
| Ecografía | 97,70 | 4,3 | 97,70 | 5,9 | 97,70 | 6,2 |
| Coste total | 2.254,73 | 100,0 | 1.663,56 | 100,0 | 1.571,75 | 100 |
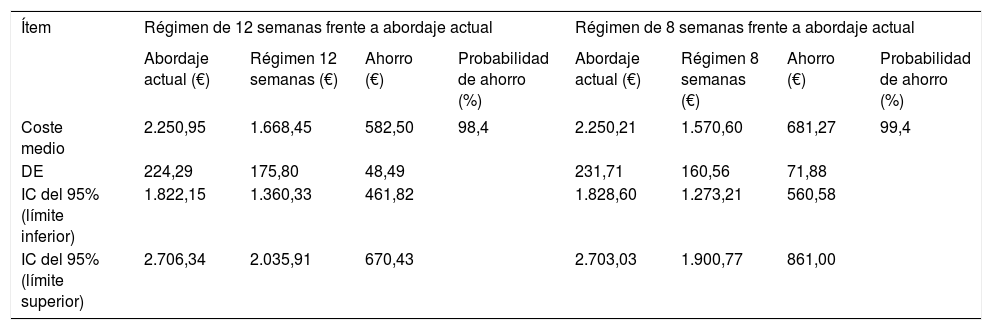
La optimización de los recursos generaría un ahorro por paciente de 582,50 ± 48,49 € y de 679,62 ± 71,15 € con el régimen de 12 y 8 semanas, respectivamente, con una probabilidad de ahorro con el abordaje simplificado en comparación con el abordaje actual del 98,4 y del 99,4%, respectivamente (tabla 5).
Coste por paciente según el análisis probabilístico con un régimen de 12 u 8 semanas
| Ítem | Régimen de 12 semanas frente a abordaje actual | Régimen de 8 semanas frente a abordaje actual | ||||||
|---|---|---|---|---|---|---|---|---|
| Abordaje actual (€) | Régimen 12 semanas (€) | Ahorro (€) | Probabilidad de ahorro (%) | Abordaje actual (€) | Régimen 8 semanas (€) | Ahorro (€) | Probabilidad de ahorro (%) | |
| Coste medio | 2.250,95 | 1.668,45 | 582,50 | 98,4 | 2.250,21 | 1.570,60 | 681,27 | 99,4 |
| DE | 224,29 | 175,80 | 48,49 | 231,71 | 160,56 | 71,88 | ||
| IC del 95% (límite inferior) | 1.822,15 | 1.360,33 | 461,82 | 1.828,60 | 1.273,21 | 560,58 | ||
| IC del 95% (límite superior) | 2.706,34 | 2.035,91 | 670,43 | 2.703,03 | 1.900,77 | 861,00 | ||
DE: desviación estándar; IC: intervalo de confianza.
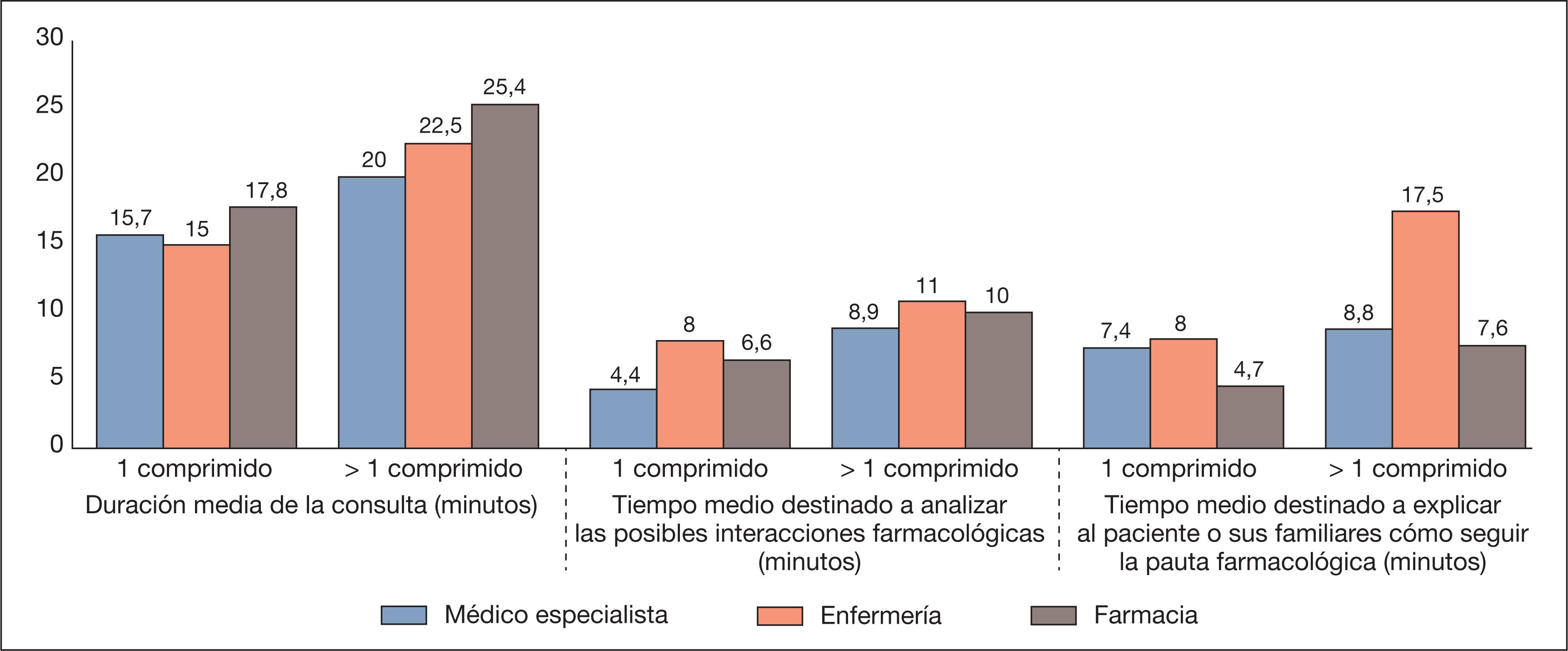
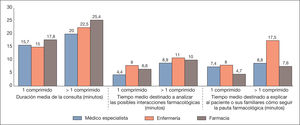
Como se observa en la figura 2, se estima que la duración media de las consultas y del tiempo medio destinado a analizar las posibles interacciones farmacológicas, así como el dedicado a explicar al paciente o a sus familiares cómo tomar el medicamento, serían inferiores en todos los casos (médico, enfermera, farmacéutico) con regímenes diarios de tratamiento con 1 solo comprimido que con regímenes con más de 1 comprimido al día.
DiscusiónLa introducción de los regímenes antivirales orales basados en AAD para tratar la HC ha cambiado radicalmente el pronóstico de esta enfermedad al permitir obtener tasas de curación (RVS) superiores al 95%. Además de su eficacia, su excelente perfil de seguridad y la simplicidad posológica permiten extender los beneficios de estos regímenes a la totalidad del proceso terapéutico, que puede simplificarse respecto a estándares de tratamiento previos y reducir el consumo global de recursos sanitarios. El presente estudio evalúa el impacto de un modelo simplificado de tratamiento de pacientes con HC en nuestro medio sobre el consumo de recursos sanitarios directos. Los resultados demuestran que el tratamiento de la HC con determinados regímenes de AAD podría generar un ahorro significativo de recursos para el SNS. Estos ahorros serían adicionales a los que se estima que podrían producirse en el contexto de la enfermedad a nivel poblacional como consecuencia de la elevada efectividad de estos nuevos tratamientos farmacológicos20-22.
El análisis de los costes del tratamiento de la HC se ha estudiado ampliamente, tanto desde la perspectiva individual como de coste-efectividad y coste-utilidad para los sistemas de salud, teniendo en cuenta fundamentalmente los costes farmacológicos y el ahorro generados por la curación de la infección sobre los costes futuros del abordaje de la progresión de la enfermedad hepática. El análisis de la monitorización del tratamiento, sus costes asociados y potenciales áreas de optimización de los recursos ha recibido una atención marginal. Sin embargo se trata de un área relevante, ya que nuestros resultados muestran un ahorro potencial promedio por paciente tratado del 26,2%. Desde una perspectiva del SNS, esta estrategia se ajusta al principio de coste de oportunidad, es decir, el valor de lo que se podría hacer y no se hace porque se hacen cosas menos adecuadas23. Precisamente, el análisis económico trata de asegurar que la eficiencia conseguida al seleccionar una opción sea mayor que la que se habría obtenido con otras. En el contexto del presente estudio, el coste de oportunidad corresponde al coste del abordaje simplificado del paciente con HC, que realmente supondría un ahorro en comparación con el manejo actual del paciente. Este ahorro monetario tendría además un impacto sobre el uso de recursos que, al reducirse, posibilitaría dedicarlos al cuidado de otros pacientes con o sin HC.
Es importante tener en cuenta que la simplificación del abordaje del paciente con HC no es posible realizarla con todos los regímenes de tratamiento. Es el caso, por ejemplo, de los regímenes que requieran la utilización de ribavirina, pues se recomienda la monitorización de la hemoglobina y el recuento de leucocitos, o del esquema con grazoprevir/elbasvir administrado durante 12 semanas, ya que se debe realizar un análisis de la función hepática antes de iniciar el tratamiento, en la semana 8 de tratamiento y cuando esté clínicamente indicado24. Tampoco puede simplificarse en pacientes que requieran un seguimiento más estrecho, como pueden ser los pacientes polimedicados en los que puedan existir interacciones potenciales que precisen monitorización, ni en el caso de los regímenes que por efectos adversos o anomalías de laboratorio requieran visitas adicionales del clínico o de enfermería, o de farmacia. Aunque no se puede cuantificar el número de pacientes que, debido a la presencia de comorbilidades o a polimedicación, precisarán un seguimiento más estrecho durante el tratamiento antiviral, probablemente se trata de un grupo con una baja prevalencia en la actualidad atendiendo a los datos recientemente publicados en España25.
El abordaje simplificado de la HC también beneficiaría al paciente por 2 motivos: en primer lugar, porque no perdería un tiempo dedicado actualmente a consultas y pruebas que pueden ser innecesarias y, en segundo lugar, porque se reducirían tanto los gastos directos no sanitarios que recaen sobre el paciente (p. ej., los gastos del transporte para acudir a consultas o pruebas) como los costes indirectos (por pérdida de jornadas laborales).
La reducción en el número de comprimidos, conseguida con los nuevos AAD, además de favorecer la adherencia al tratamiento26, reduciría el tiempo de consulta del médico especialista, la enfermera y el farmacéutico, conforme al panel de expertos consultado. Esto redundaría en un beneficio para los pacientes con HC, ya que dichos profesionales sanitarios podrían dedicar el tiempo liberado a una mejor gestión y atención global de la enfermedad.
En la valoración de los resultados del estudio hay que tener en cuenta sus posibles limitaciones. En primer lugar, se trata de un modelo teórico que es, por definición, una simulación simplificada de la realidad y que tanto la valoración del abordaje actual del paciente con HC como su previsible simplificación, no se obtuvieron de un estudio de práctica clínica ad-hoc, sino que se realizó por un panel de 36 expertos clínicos españoles, con amplia experiencia en el tratamiento de la enfermedad y en consonancia con las actuales recomendaciones de optimización de los recursos destinados al abordaje de la enfermedad e incluyendo a las distintas especialidades involucradas (médico especialista, farmacia, enfermería)12-15. En segundo lugar, se desconoce el porcentaje de pacientes en los que no se podría aplicar un modelo de seguimiento simplificado y que englobaría principalmente a aquellos con cirrosis hepática, algunas comorbilidades graves o con potenciales interacciones farmacológicas, que sin ser incompatibles con los regímenes antivirales podrían requerir una monitorización adicional25. Sin embargo, en el escenario de tratamiento actual en España, con un predominio de pacientes naïve y sin fibrosis avanzada estimamos que la mayoría de los pacientes que recibe un régimen antiviral en nuestro medio son candidatos potenciales a este abordaje simplificado. En tercer lugar, el estudio se ha realizado desde la perspectiva del SNS y no desde la perspectiva social, por tanto, no se ha considerado la pérdida de productividad en pacientes con HC ni el potencial ahorro sobre esta, derivados de un abordaje simplificado. La inclusión de la perspectiva social en el modelo previsiblemente incrementaría el ahorro promedio por paciente, aunque sería necesario un estudio específicamente diseñado desde la perspectiva social para obtener una estimación precisa. En cuarto lugar, siguiendo el marco del panel Delphi, en el análisis económico no se abordó el uso de recursos en los escasos fracasos virológicos que deberían estimarse a partir de la bibliografía, lo que desvirtuaría la coherencia de los datos obtenidos a partir del panel Delphi.
A pesar de las limitaciones descritas, los resultados del análisis probabilístico ratifican los obtenidos en el caso base determinístico27,28, con una probabilidad del 98,4 y del 99,4% de que la estrategia de simplificación del uso de recursos genere ahorro para el SNS con regímenes de tratamiento de 12 y 8 semanas, respectivamente.
Es de prever que, en un futuro próximo, con la simplificación de los sistemas informáticos de prescripción de los AAD, se pueda simplificar aún más el manejo de la HC, eliminando el genotipado e incluso el fibroscan en una amplia proporción de pacientes, sustituyéndolos por marcadores serológicos.
Según este modelo económico, la optimización de los recursos asistenciales en el abordaje del paciente con HC tratado con determinados AAD, que permiten simplificar en gran medida las necesidades de monitorización, podría generar ahorro para el SNS de España.
Conflicto de interesesJuan Turnes ha recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto. Ha realizado labores de asesoramiento y participado como ponente en conferencias con Abbvie, Gilead y MSD. Ha recibido ayudas para el desarrollo de proyectos de investigación de Gilead.
Federico García ha recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto. Ha realizado labores de asesoramiento para ViiV, Gilead, Abbvie, Roche y Hologic. Ha recibido honorarios en concepto de ponencias de ViiV, Gilead, Abbvie, MSD, Janssen, Roche, Biomerieux, Hologic y Qiagen. Ha recibido ayudas para proyectos de investigación de Gilead y Roche.
Moisés Diago ha recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto. Ha realizado labores de asesoramiento para Abbvie, Gilead y Janssen. Ha recibido honorarios en concepto de ponencias de Abbvie, Gilead y MSD.
Raúl Andrade ha recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto. Ha realizado labores de asesoramiento y participado como ponente en conferencias con Abbvie, Gilead y MSD.
Pilar Díaz ha recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto. Ha realizado labores de asesoramiento para ViiV y Gilead. Ha recibido honorarios en concepto de ponencias de Gilead, Janssen y Roche.
Darío Rubio-Rodríguez y Carlos Rubio-Terrés han recibido una financiación no condicionada a resultados de Gilead Sciences para el desarrollo del proyecto.
Información sobre el suplementoEste artículo forma parte del suplemento titulado “El valor de la simplicidad en el tratamiento de la hepatitis C”, que ha sido patrocinado por Gilead.