INTRODUCCIÓN
La pancreatitis crónica se asocia al desarrollo progresivo de cambios histopatológicos y morfológicos, tanto ductales como parenquimatosos, que conllevan la alteración de las funciones exocrina y endocrina de la glándula. Clásicamente se ha considerado que la pancreatitis crónica es una lesión irreversible, que persiste, e incluso progresa, a pesar de eliminar el factor etiológico primario. No obstante, el conocimiento más profundo de la enfermedad, sobre todo de sus distintas etiologías, obliga a aceptar la posibilidad de reversibilidad del proceso en determinados casos con la aplicación de las medidas terapéuticas oportunas. Los ejemplos más claros en este sentido son la pancreatitis crónica autoinmune, cuyas lesiones pueden mejorar e incluso desaparecer con el tratamiento esteroideo, y la pancreatitis crónica obstructiva, que puede mejorar tras el tratamiento de la obstrucción del conducto pancreático. Desde el punto de vista histológico, la pancreatitis crónica se caracteriza por la aparición de un infiltrado inflamatorio crónico asociado a la pérdida del epitelio exocrino y la transdiferenciación de las células acinares en células ductales. Estos cambios regresivos celulares se asocian al desarrollo de fibrosis y al incremento de las estructuras nerviosas, tanto en número como en tamaño. A pesar de que se conocen estas características histopatológicas, la toma de biopsia pancreática para el diagnóstico de pancreatitis crónica no se ha impuesto en la práctica clínica. Algunos aspectos, como la difícil accesibilidad anatómica del páncreas, el patrón probablemente parcheado de la enfermedad y la morbilidad asociada a la punción pancreática (hemorragia, pancreatitis aguda) han limitado el papel de la histología en el diagnóstico de la pancreatitis crónica. Por ello, y aunque el advenimiento y el desarrollo de la ecografía endoscópica y la punción guiada por ésta pueden y deben cambiar esta situación, el diagnóstico de la pancreatitis crónica sigue basándose en la demostración de los cambios morfológicos y/o funcionales que son consecuencia de las lesiones histológicas. Este hecho limita el diagnóstico de la pancreatitis crónica a estadios en los que las lesiones son ya evidentes.
FUNCIÓN PANCREÁTICA EXOCRINA EN LA PANCREATITIS CRÓNICA: BASE FISIOPATOLÓGICALa función pancreática exocrina se altera en pancreatitis crónica de forma progresiva a medida que avanza la enfermedad. Su mecanismo patogénico básico lo constituye la pérdida de parénquima pancreático. En este sentido, como se ha comentado, el desarrollo de la enfermedad se asocia a la diferenciación de las células acinares en células ductales y a la pérdida del tejido exocrino. Por otra parte, es conocida la evolución hacia fibrosis del parénquima pancreático en sustitución del parénquima funcional, y la atrofia glandular en estadios avanzados de la enfermedad. La cantidad de enzimas segregada por el tejido acinar sano es aproximadamente 10 veces superior a la cantidad necesaria para asegurar una digestión normal. Por tanto, esta gran capacidad funcional del páncreas exocrino hace que la función digestiva se mantenga hasta que se ha perdido al menos el 90% de la secreción de enzimas1 . El momento en el que la secreción pancreática no es suficiente para mantener una función digestiva normal es el que define la insuficiencia pancreática exocrina. Estadios previos definen una hipofunción pancreática exocrina, que puede detectarse por distintos métodos de exploración funcional del páncreas y cuyo grado es variable, desde una hipofunción leve inicial a una moderada y, finalmente, a una grave. Como concepto, hipofunción pancreática grave e insuficiencia pancreática exocrina son términos sinónimos. La evolución de la función pancreática exocrina depende de la etiología de la pancreatitis crónica2 . En este sentido, y como término medio, los pacientes con pancreatitis crónica alcohólica desarrollan insuficiencia pancreática exocrina tras unos 13 años desde el inicio de la enfermedad, mientras que este período es más prolongado (de 17 a 28 años) en los que presentan pancreatitis crónica idiopática. Hasta ese momento, la demostración de una hipofunción pancreática puede ser de utilidad diagnóstica pero carece de implicaciones terapéuticas. En sujetos con insuficiencia pancreática exocrina, la digestión de las grasas está más alterada que la de hidratos de carbono y proteínas. Esto se debe a una serie de factores que se resumen en la tabla I:
–A medida que la función pancreática exocrina se va de-teriorando con la evolución de la pancreatitis crónica, la secreción de lipasa disminuye de forma más temprana y marcada que la del resto de enzimas.–La lipasa se inactiva a lo largo del tránsito intestinal de-bido a la acción de las proteasas pancreáticas; esta inactivación se produce en tramos más proximales que la degradación de la amilasa o las propias proteasas 3 .
–La lipasa es más sensible a pH ácidos que otras enzimaspancreáticas; con un pH < 4 se produce la inactivación irreversible de la enzima 4 .
–La reducida secreción pancreática de bicarbonato enpancreatitis crónica hace que el pH duodenal de estos pacientes sea ácido; de esta forma se produce tanto la inactivación de la lipasa secretada como la precipitación de las sales biliares, lo cual afecta gravemente a la digestión grasa 5 .
–La pérdida de capacidad del páncreas para digerir pro-teínas y carbohidratos es más fácilmente compensada por mecanismos extrapancreáticos (amilasa salival, proteasas y peptidasas intestinales) que la pérdida de secreción de lipasa, que es pobremente compensada por la secreción de lipasa lingual o gástrica 6 .
La consecuencia de la suma de todos estos factores es que la mala digestión grasa es la principal manifestación y el principal problema clínico en pacientes con insuficiencia pancreática exocrina. Este hecho es clave tanto para la aplicación de pruebas funcionales para el diagnóstico de la insuficiencia pancreática exocrina como para su enfoque terapéutico.
PRUEBAS DE FUNCIÓN PANCREÁTICA EN PANCREATITIS CRÓNICAEn el contexto de la pancreatitis crónica, la evaluación funcional del páncreas exocrino adquiere relevancia básicamente en 5 situaciones clínicas:
–Confirmación del diagnóstico de pancreatitis crónica encaso de hallazgo no concluyente de los métodos de imagen.–Diagnóstico inicial de enfermedad pancreática en pa-cientes con sospecha clínica de pancreatitis crónica.
–Diagnóstico de insuficiencia pancreática exocrina.
–Control de la eficacia del tratamiento de insuficienciapancreática exocrina.
–Control del cumplimiento terapéutico de insuficienciapancreática exocrina.
TABLA I. Factores que justifican una más temprana y marcada alteración de la digestión grasa que de la digestión de hidratos de carbono y proteínas en pacientes con insuficiencia pancreática exocrina secundaria a pancreatitis crónica
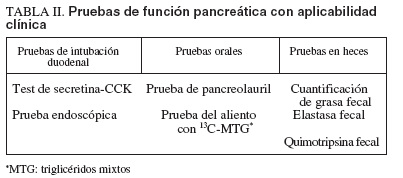
TABLA II. Pruebas de función pancreática con aplicabilidad clínica
En cada una de estas situaciones se debe emplear una prueba funcional determinada, en función de parámetros como la eficacia diagnóstica de cada prueba, su aplicabilidad y disponibilidad clínica y el coste económico. Las distintas pruebas de función pancreática se dividen básicamente en pruebas de intubación duodenal, pruebas orales y pruebas en heces (tabla II). La eficacia diagnóstica de estas pruebas es muy variable, desde las que permiten detectar disminuciones leves de la secreción pancreática de enzimas y/o bicarbonato (test de secretina-CCK) en pacientes con pancreatitis crónica leve, a pruebas cuyo objetivo es detectar mala digestión grasa (cuantificación de grasa fecal, prueba del aliento con 13 C-triglicéridos) en pacientes con pancreatitis crónica avanzada. Las pruebas directas de intubación duodenal, básicamente el test de secretina-CCK o ceruleína, se consideran el método de referencia para la evaluación de la función pancreática exocrina. Sin embargo, estas pruebas son invasivas, laboriosas, de duración prolongada y elevado coste, por lo que su uso está limitado a algunos centros especializados. Las pruebas orales y fecales son más fácilmente aplicables en la práctica clínica y, por tanto, más ampliamente empleadas. La eficacia diagnóstica de estas pruebas es, sin embargo, variable y en cualquier caso menor que la de las pruebas de intubación duodenal. La información aportada por cada prueba es diferente y, por tanto, es importante seleccionar la prueba óptima para realizar en cada situación clínica. En pacientes con sospecha clínica de pancreatitis crónica y hallazgos no concluyentes en los métodos de imagen, sólo el test de secreti-na-CCK o ceruleína es el único lo suficientemente sensible para apoyar el diagnóstico. El desarrollo de la ecografía endoscópica, que muestra una muy elevada sensibilidad para el diagnóstico de pancreatitis crónica, ha limitado aún más la utilidad clínica de las pruebas de intubación duodenal. En el extremo contrario, el diagnóstico de insuficiencia pancreática exocrina, así como la indicación de tratamiento enzimático sustitutivo y su control requiere de una prueba capaz de detectar mala digestión grasa y, por tanto, con una baja sensibilidad para la detección de hipofunción leve o moderada. Entre ambas situaciones clínicas, pruebas con una sensibilidad alta pero fundamentalmente no invasivas y fácilmente aplicables a la práctica clínica son de elección en el diagnóstico inicial de la enfermedad pancreática en pacientes con sospecha clínica de pancreatitis crónica.
Pruebas de intubación duodenalSe basan en la cuantificación de la secreción pancreática de enzimas y bicarbonato en muestras de jugo duodenal obtenidas mediante intubación duodenal durante la estimulación submáxima del páncreas con secretina y/o CCK o ceruleína. El test clásico de secretina-CCK es la prueba de función más eficaz para el diagnóstico de la pancreatitis crónica, con cifras de sensibilidad y especificidad que alcanzan el 95%7 . No obstante, esta prueba tiene como inconvenientes su invasividad (requiere la colocación de una sonda nasoduodenal), complejidad, elevado coste y falta de estandarización, que hacen que se realice sólo en determinados centros de referencia que dispongan de unidades especializadas en enfermedades del páncreas. Una de las limitaciones básicas del test de secretina-CCK es la rápida inactivación de las enzimas pancreáticas en jugo duodenal, lo cual se intenta limitar parcialmente mediante el enfriamiento inmediato de las muestras obtenidas y mediante la adición de antiproteasas a éstas. Una alternativa adecuada es la cuantificación única de cinc en las muestras de jugo duodenal en sustitución de la cuantificación de enzimas y bicarbonato8 . El cinc es secretado por el páncreas como parte de metaloproteasas, de forma que la secreción de cinc es proporcional a la de enzimas. La gran ventaja del cinc es su estabilidad en el jugo duodenal, incluso a temperatura ambiente, y su fácil cuantificación en laboratorios clínicos. El test de secretina-CCK permite la clasificación del grado de hipofunción exocrina en leve, moderada y grave, según el porcentaje de reducción de la secreción pancreática7,8 . Más recientemente se ha desarrollado la denominada prueba endoscópica de función pancreática que, a diferencia del test clásico de secretina-CCK, obtiene el jugo pancreático mediante aspiración del contenido duodenal tras estimulación de la secreción pancreática con secretina o CCK durante la realización de una endoscopia digestiva alta9,10 . Su objetivo es evitar los inconvenientes de la intubación nasoduodenal, la duración y la limitada aplicabilidad clínica del test de secretina-CCK. No obstante, esta prueba es al menos tan invasiva como la prueba clásica de intubación, ya que requiere mantener el endoscopio en segunda porción duodenal durante 60 min. Además, no cuantifica flujo de secreción pancreática (secreción por unidad de tiempo) sino concentración de enzimas o bicarbonato, que es un parámetro menos sensible en el diagnóstico de pancreatitis crónica. Por ello, hoy por hoy, no puede recomendarse su uso en la práctica clínica.
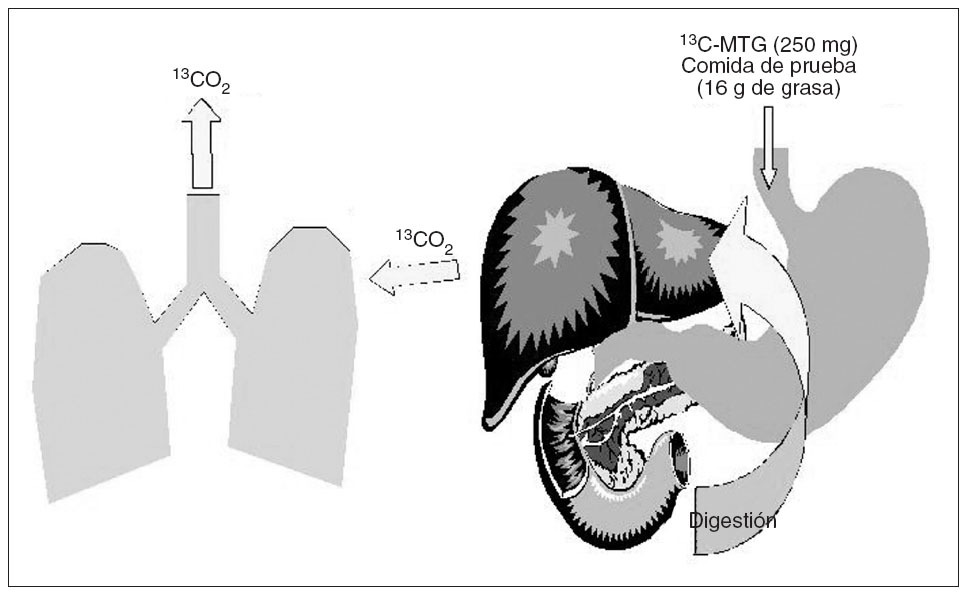
Pruebas oralesLas pruebas orales de función pancreática son pruebas indirectas que evalúan la capacidad de digestión de determinados sustratos administrados junto a una comida de prueba. Entre las distintas pruebas evaluadas, en la actualidad mantienen su utilidad clínica la prueba del pancreolauril y, más recientemente, la del aliento con mezcla de 13 C-triglicéridos (13 C-MTG). La prueba del pancreolauril consiste en la medición en suero de la concentración de fluoresceína en distintos intervalos tras la administración de una comida de prueba con dilaurato de fluoresceína. Este sustrato es hidrolizado por una colesterol-éster hidrolasa pancreática liberando fluoresceína. Por tanto, la concentración de fluoresceína sérica es un índice indirecto de la función pancreática exocrina (normal si el pico de concentración durante 4 h > 4,5 µg/ml)11 . La prueba clásica del pancreolauril en orina carece de utilidad clínica por su baja eficacia diagnóstica. Por otra parte, la administración de un bolo intravenoso de se-cretina antes de la realización de la prueba permite elevar su sensibilidad para el diagnóstico de pancreatitis crónica, y llega a detectar hasta el 75% de los casos en estadios iniciales y el 100% de los pacientes en fases moderadas y avanzadas12 . Esta prueba, por tanto, puede considerarse adecuada como primera exploración en pacientes con sospecha de pancreatitis crónica, aunque requiere una unidad de exploraciones funcionales adecuadamente dotada. La prueba del aliento con 13 C-MTG persigue detectar mala digestión grasa y, por tanto, detectar insuficiencia pancreática exocrina en pacientes con pancreatitis crónica conocida13 . En esta prueba, el sustrato (13 C-MTG) se administra por vía oral junto a una comida de prueba. Tras hidrólisis duodenal por la acción de la lipasa pancreática, los metabolitos marcados se absorben y son metabolizados en el hígado. Como consecuencia de ese metabolismo hepático se libera 13 CO2 , que es eliminado en el aire espirado (fig. 1). La cantidad de 13 CO2 en muestras de aliento, que refleja de forma indirecta la función pancreática exocrina, se cuantifica mediante espectrometría de masas. El resultado de la prueba se expresa en porcentaje de 13 CO2 recuperado en aire espirado, que es proporcional a la cantidad de grasa digerida (normal > 57% a las 6 h)14 . Esta prueba es simple, no invasiva y muy eficaz en el diagnóstico de mala digestión grasa, con cifras de sensibilidad y especificidad superiores al 90%, por lo que permite reemplazar a la cuantificación de grasa fecal en la práctica clínica. Su utilidad se extiende, además, al control de la eficacia del tratamiento enzimático sustitutivo15 .
Pruebas en hecesLa cuantificación de grasa fecal (prueba clásica de Van opinión, cualquier paciente con insuficiencia pancreática exocrina (mala digestión) requiere tratamiento enzimático sustitutivo independientemente de sus manifestaciones clínicas. La base de esta actuación es múltiple y puede re-sumirse en los siguientes puntos:
–La esteatorrea clínicamente evidente es infrecuente enla pancreatitis crónica, ya que su instauración progresiva durante años hace que el paciente adapte su dieta y limite la ingesta de grasas. Así, no es raro encontrar pacientes con mala digestión grasa y estreñimiento.–La pérdida de peso como manifestación de insuficienciapancreática exocrina es un signo demasiado tardío.
–Es frecuente la presencia de datos bioquímicos de mal-nutrición, básicamente concentraciones séricas disminuidas de vitaminas liposolubles, por mala digestión en pacientes por otra parte asintomáticos y con valores de esteatorrea inferiores a 15 g/día 18 .
–La mala absorción de proteínas e hidratos de carbono esinfrecuente y, en cualquier caso, no existen métodos estandarizados y aceptados para su demostración.
–La presencia de dispepsia es muy frecuente en pancrea-titis crónica, básicamente por alteración de la motilidad gastrointestinal 19 , sin que pueda objetivarse la insuficiencia pancreática exocrina como causa de ésta.
Fig. 1. Método de la prueba del aliento con mezcla de 13C-triglicéridos. MTG: mezcla de triglicéridos.
Aspectos farmacológicos relevantes de los preparados de enzimas pancreáticas
Con el fin de corregir la mala digestión grasa en pacientes con insuficiencia pancreática exocrina secundaria a pancreatitis crónica, una cantidad óptima de lipasa debe alcanzar la luz duodenal en forma activa junto con la comida: «cantidad suficiente de lipasa activa en el lugar adecuado y en el momento oportuno». Como se ha mencionado, se necesita al menos un 10% de la secreción normal posprandial de lipasa para asegurar una digestión grasa adecuada 1 , lo que equivale a 30.000 U de lipasa que deben alcanzar la luz duodenal en el mismo momento que la comida. Los 3 problemas fundamentales que deben solventar las preparaciones de enzimas pancreáticas para el tratamiento de la insuficiencia pancreática exocrina secundaria a pancreatitis crónica son los siguientes (tabla III):
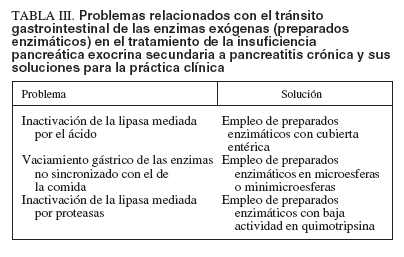
TABLA III. Problemas relacionados con el tránsito gastrointestinal de las enzimas exógenas (preparados enzimáticos) en el tratamiento de la insuficiencia pancreática exocrina secundaria a pancreatitis crónica y sus soluciones para la práctica clínica
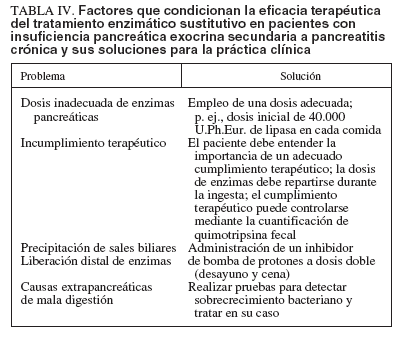
TABLA IV. Factores que condicionan la eficacia terapéutica del tratamiento enzimático sustitutivo en pacientes con insuficiencia pancreática exocrina secundaria a pancreatitis crónica y sus soluciones para la práctica clínica
– Inactivación de la lipasa por el ácido en el interior de lacavidad gástrica.
–Vaciamiento gástrico de las enzimas no sincronizadocon el de la comida.
– Inactivación de la lipasa mediada por proteasas pan-creáticas, básicamente quimotripsina.
Como consecuencia de la inactivación ácida, sólo el 8% de la lipasa administrada por vía oral alcanza el duodeno en forma activa 20 . Esta inactivación puede prevenirse mediante el empleo de preparados enzimáticos con cubierta entérica, que liberan las enzimas activas una vez que el pH intraluminal es de 5,0 o superior (tabla III). El píloro permite sólo el paso de partículas cuyo tamaño sea menor de 2 mm 21 . El vaciamiento gástrico paralelo de enzimas y nutrientes se asegura mediante el empleo de preparados enzimáticos en microesferas (1-2 mm de diámetro) o minimicroesferas (0,7-1,6 mm de diámetro) 22 . En este sentido, debe desaconsejarse el empleo de preparados enzimáticos en tabletas, aunque tengan cubierta entérica, ya que estos preparados no alcanzan el duodeno paralelamente a los nutrientes y su disolución es lenta, e incluso llegan a alcanzar intactas la luz colónica 23 . La superioridad clínica de los preparados en microesferas o minimicroesferas sobre los preparados convencionales se ha demostrado firmemente. Por último, la inactivación de la lipasa mediada por proteasas puede prevenirse mediante el empleo de preparados enzimáticos con baja actividad de quimotripsina (tabla III). Protocolo terapéutico en la práctica clínicaLas medidas dietéticas, salvo la abstinencia alcohólica, tienen un papel secundario en el tratamiento de la insuficiencia pancreática exocrina. Salvo en pacientes con dolor de predominio posprandial, no es necesaria la restricción de la cantidad de grasa en la dieta. De hecho, estudios experimentales han demostrado que la proporción de grasa de la dieta que se absorbe en insuficiencia pancreática exocrina bajo tratamiento enzimático sustitutivo es mayor cuando se administra una dieta rica en grasa que cuando se restringe su ingesta24 . Sólo en los casos excepcionales de esteatorrea intratable mediante las medidas comentadas se recomienda la sustitución de las grasas de la dieta por triglicéridos de cadena media. La base del tratamiento de la insuficiencia pancreática exocrina secundaria a pancreatitis crónica es la administración de enzimas pancreáticas por vía oral. Como se ha comentado en el apartado anterior, se recomienda el empleo de preparados en minimicroesferas con el fin de asegurar el vaciamiento gástrico adecuado de las enzimas, y con cubierta entérica con el fin de evitar la inactivación de la lipasa mediada por el ácido gástrico. A pesar de ello, existe una amplia serie de factores que hay que tener en cuenta para lograr una normalización de la digestión grasa con este tratamiento (tabla IV):
– El primer factor relevante es la administración de unadosis adecuada de enzimas. La cantidad necesaria de lipa-sa activa en la luz duodenal en la fase posprandial debe ser al menos de 30.000 U1 . Una unidad de lipasa equivale a 3 U.Ph.Eur., que es la unidad de actividad enzimática empleada en los distintos preparados comerciales. Esto significa que en un paciente con nula secreción pancreática endógena sería necesario administrar, al menos, 90.000 U.Ph.Eur. de lipasa con cada comida con el fin de asegurar una adecuada digestión grasa, asumiendo que la totalidad de la enzima alcanza la luz duodenal de forma activa en el momento adecuado. Teniendo en cuenta que habitualmente los pacientes con insuficiencia pancreática exocrina suelen mantener cierto grado de secreción pancreática, la dosis inicial de enzimas pancreáticas que se debe administrar puede ser de 20.000 a 40.000 U.Ph.Eur. con cada comida. En nuestra experiencia, una dosis de 40.000 U.Ph.Eur. es capaz de normalizar la digestión grasa de una comida estándar en más de la mitad de los pacientes con insuficiencia pancreática exocrina secundaria a pancreatitis crónica, por lo que es la dosis estándar empleada en nuestra unidad de páncreas. No obstante, casi la mitad de los pacientes no llega a normalizar la digestión grasa con esa dosis, por lo que siempre es recomendable confirmar su eficacia terapéutica mediante cuantificación de grasa fecal o, mejor, mediante la prueba del aliento con 13 C-MTG 15 .
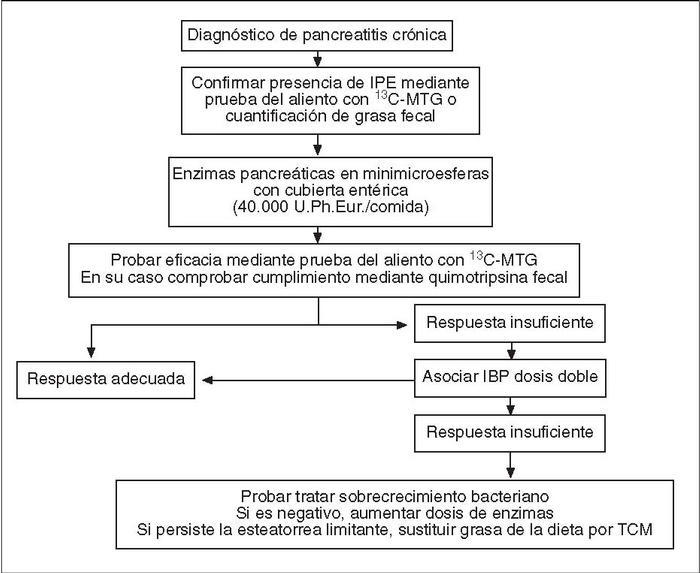
Fig. 2. Algoritmo diagnóstico y terapéutico de la insuficiencia pancreática exocrina secundaria a pancreatitis crónica en la práctica clínica. IPE: insuficiencia pancreática exocrina; MTG: mezcla de triglicéridos; TCM: triglicéridos de cadena media.
– El segundo aspecto clave en la consecución de una digestión grasa normal es un adecuado cumplimiento terapéutico. Los preparados de enzimas pancreáticas adquieren su mayor eficacia terapéutica si se ingieren distribuidos durante la comida25 . Nuestra pauta habitual consiste en la administración de la cuarta parte de la dosis al inicio, la mitad de la dosis a mitad de la ingesta y el cuarto restante de dosis al final (pauta 1-2-1) en cada comida. El paciente debe ser consciente de la importancia de un adecuado cumplimiento terapéutico. En caso de duda sobre el cumplimiento puede ser de utilidad la cuantificación de quimotripsina fecal, que mide tanto la actividad de enzima endógena como exógena.
–A pesar de una dosis adecuada de enzimas y de un ade-cuado cumplimiento, casi la mitad de los pacientes con insuficiencia pancreática exocrina secundaria a pancreatitis crónica no consiguen normalizar la digestión grasa tras una comida estándar. El factor más relevante que debe ser controlado en estos casos es el pH intraluminal. La reducción de la secreción de bicarbonato pancreático en los sujetos con pancreatitis crónica e insuficiencia pancreática exocrina ejerce 2 efectos que impiden una adecuada acción del tratamiento enzimático sustitutivo:- El pH ácido intraduodenal conlleva la precipitación delas sales biliares, impide una adecuada formación micelar de las grasas y evita así la acción de la lipasa.
- En muchos pacientes el pH de 5,0 necesario para la libe-ración de las enzimas de su cubierta entérica no se alcanza hasta tramos distales del intestino, donde la absorción grasa es mucho menor.
El efecto del pH ácido intraluminal puede evitarse mediante la administración de un inhibidor de la bomba de protones (IBP). En nuestra experiencia, la asociación de un IBP a dosis doble (antes del desayuno y la cena), al facilitar la acción de la lipasa en tramos proximales del intestino y evitar la precipitación de las sales biliares, consigue normalizar la digestión grasa en la mayoría de los pacientes en los que el tratamiento enzimático aislado no era suficiente.
– Por último, en caso de respuesta insuficiente al trata-miento combinado de enzimas e IBP, deben descartarse causas extrapancreáticas de mala digestión. En este sentido, la pancreatitis crónica, como consecuencia de una frecuente descoordinación entre la secreción pancreática y la motilidad intestinal interdigestiva19 , se asocia a fenómenos de sobrecrecimiento bacteriano intestinal26 , que pueden ser causantes de una inadecuada digestión grasa.
La figura 2 resume el algoritmo diagnóstico y terapéutico de la insuficiencia pancreática exocrina secundaria a pancreatitis crónica en la práctica clínica diaria. Este algoritmo es el empleado en la unidad de páncreas de nuestro centro y, lógicamente, pretende ser únicamente una recomendación de práctica clínica cuya aplicación a otros centros requiere de una adaptación local.
Correspondencia: Dr. J.E. Domínguez Muñoz. Servicio de Aparato Digestivo. Hospital Clínico Universitario de Santiago. Choupana, s/n. 15706 Santiago de Compostela. La Coruña. España. Correo electrónico: enriquedominguezmunoz@hotmail.com