La enteropatía pierde-proteínas (EPP) se caracteriza por una pérdida excesiva de proteínas séricas a través del tracto gastrointestinal, produciendo hipoproteinemia con hipoalbuminemia y edema, principalmente. Ante la presencia de hipoalbuminemia con edema hay que descartar inicialmente otras causas de proteínas séricas disminuidas, como la malnutrición, la enfermedad renal con proteinuria o alteraciones hepáticas con alteración en la síntesis de proteínas1.
Existen diferentes causas de EPP, como enfermedades metabólicas intestinales, inflamatorias o infecciosas, y también alteraciones en el drenaje linfático, como en la linfangiectasia intestinal1.
Presentamos el caso de una mujer de 57 años que tuvo 2 episodios de pancreatitis aguda idiopática en menos de un año. En ese año, la paciente inicia edema palpebral y de extremidades inferiores con una hipoalbuminemia persistente con cifras de albúmina sérica<2g/dl (niveles normales 3,30-5,20) y disminución de la concentración de las γ-globulinas y proteínas de vida media corta, sin diarrea. En el estudio realizado por este motivo, se objetivaron una elastasa fecal y un test de Van de Kamer normales. La determinación del aclaramiento de alfa-1-antitripisina fue de 797 ml/24h (niveles normales 0,00-12,50) y el test de sobrecrecimiento bacteriano, parásitos en heces y coprocultivos resultaron normales. También se descartó el síndrome nefrótico como causa de hipoalbuminemia.
Tras esto, presentó un nuevo episodio de pancreatitis aguda con trombosis de vena esplénica por la cual se inició anticoagulación; además, se inició tratamiento con corticoides por la sospecha de pancreatitis autoinmune a pesar de presentar IgG4 normal, sin objetivarse mejoría y presentando una nueva reagudización de la pancreatitis. Se realizó un estudio de hipercoagulabilidad con factor v de Leiden, proteínas C y S, antitrombina iii, homocisteinemia y protrombina 20210, que se hallaron dentro de los parámetros de la normalidad. Al mes, se realizó una tomografía por emisión de positrones que objetivó un aumento de la captación en cola pancreática con sospecha de origen neoplásico; finalmente se realizó, vía laparotomía, una pancreatectomía caudal con esplenectomía con anatomía patológica compatible con pancreatitis crónica (inflamación y fibrosis asociadas a áreas de necrosis).
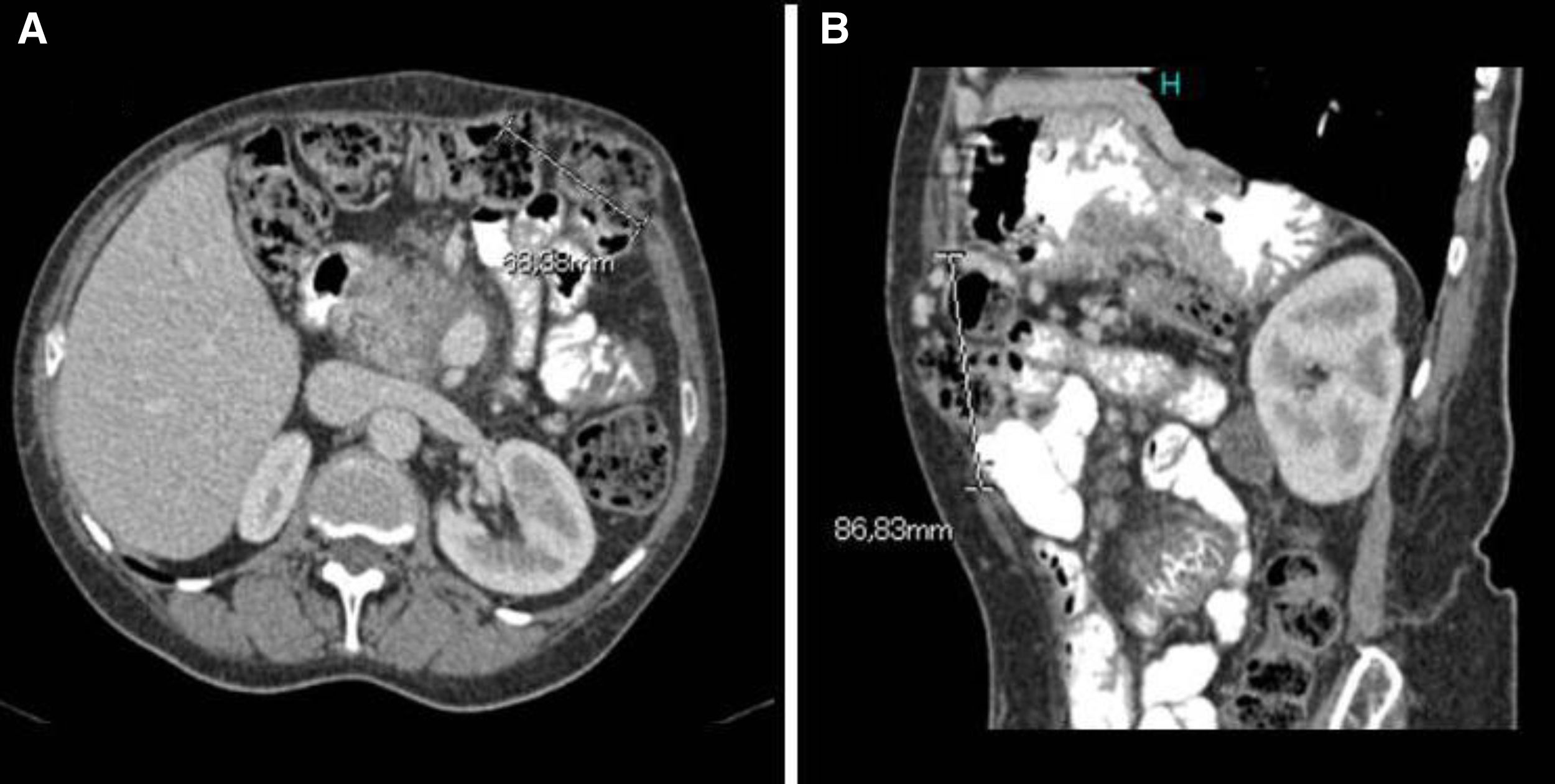
Ante la persistencia de la hipoalbuminemia, se inició la nutrición parenteral con discreta mejoría analítica (albúmina sérica 2,6g/dl) y clínica. Mediante una endoscopia digestiva alta, se objetivaron linfangiectasias duodenales y yeyunales. Se descartaron causas de linfangiectasia secundaria, excepto pancreatitis crónica, entidad que la paciente ya presentaba. Además, se realizó una colonoscopia con mucosa de aspecto normal. Al año de haberse iniciado la nutrición parenteral, la paciente presenta un dolor pancreático resistente a analgésicos de primer y segundo escalón, sin diarrea ni pérdida de peso. Se realiza RM y ecoendoscopia, donde se visualiza pancreatitis crónica calcificante grave en la cabeza de páncreas y quiste de 35mm en la pared duodenal. Se inició octreótido y se realizó PAAF con resultado de contenido inflamatorio. Ante el mal control del dolor, se realizó bloqueo del plexo celíaco con control de dolor durante un año. Pasado dicho período de tiempo, se objetivó en una TC abdominal una eventración subcostal por herida quirúrgica (fig. 1); tras eventroplastia laparoscópica, experimentó una mejoría del dolor con un aumento de la albuminemia y retirada de la nutrición parenteral. Seis meses después de la intervención la albúmina sérica es de 4,21g/dl y el aclaramiento de alfa-1-antitripsina, de 37,96ml/24h.
La resolución de una EPP tras una eventroplastia laparoscópica es un hecho poco común. En nuestro caso, la linfangiectasia intestinal fue causada por la pancreatitis crónica y agravada por la eventración subcostal. Esta eventración, secundaria a la pancreatectomía caudal con esplenectomía, causó congestión en el flujo linfático, lo que produjo un escape de linfa con gran cantidad de proteínas hacia la luz intestinal. Sin embargo, tras la eventroplastia y la consecuente disminución de la presión abdominal y la congestión linfática, el cuadro se resolvió tanto clínica como analíticamente. El hecho de que el diagnóstico de la EPP fuese anterior a la aparición de la eventración nos indica que esta fue un factor añadido a la pancreatitis crónica.
La linfangiectasia intestinal puede ser primaria o secundaria; la primera afecta a niños y se caracteriza por ectasia de los vasos linfáticos intestinales en mucosa o submucosa, con alteraciones linfáticas en otras partes del cuerpo2. En la linfangiectasia intestinal secundaria, la dilatación linfática es causada por obstrucción de los vasos linfáticos o una alta presión linfática, secundaria a una elevada presión venosa. Esta obstrucción puede ser secundaria a enfermedades cardiacas, que es la causa más frecuente, síndrome de Budd-Chiari, cirrosis hepática, fístulas enterolinfáticas, cirugías cardiacas como la intervención de Fontan, enfermedad inflamatoria intestinal, sarcoidosis, linfomas o pancreatitis crónica, entre otras.
La clínica más característica son el edema periférico, la ascitis, el derrame pleural o pericárdico y la diarrea3. Para el diagnóstico de la linfangiectasia intestinal es importante determinar, en primer lugar, la pérdida excesiva de proteínas en el tubo digestivo, donde un marcador útil es el aclaramiento de la alfa-1-antitripsina. Será patológico un aclaramiento>28ml/24h sin diarrea o>57ml/24h con diarrea1. Una vez determinada la pérdida de proteínas, para el diagnóstico definitivo de linfangiectasia es necesaria una valoración endoscópica con biopsias de duodeno y/o yeyuno.
La hernia o eventración abdominal ha sido implicada en la EPP en muy pocos casos de la literatura4–6. En 2005, Tainaka et al. describieron el caso de una niña con EPP causada por una hernia paraduodenal y que tras el tratamiento quirúrgico presentó normalización de las proteínas séricas y la albúmina4. En nuestro caso, se trata de una eventración subcostal tras una cirugía abdominal abierta. La eventración es una complicación frecuente de la cirugía abdominal, con una incidencia que varía entre el 2 y el 20%7,8. Además, la incidencia en desbridamientos pancreáticos es aún más alta, llegando al 42%9. La clínica varía desde la ausencia de sintomatología a dolor abdominal con complicaciones como la incarceración. En relación con el tratamiento, en la mayor parte de los casos se realiza parietoplastia con colocación de prótesis no reabsorbibles10.