INTRODUCCION
Las lesiones focales sólidas pancreáticas detectadas en las técnicas de imagen son causadas habitualmente por procesos inflamatorios crónicos o por tumores pancreáticos primarios malignos. Más raras son las metástasis pancreáticas que representan el 2-4% de los tumores pancreáticos resecados en las series quirúrgicas1-3.
A partir de los resultados de las series autópsicas clásicas se ha considerado que los tumores que con más frecuencia metastatizan en el páncreas son: mama, pulmón, melanoma y tiroides4. Sin embargo, esto contrasta con los resultados de series recientes basadas en los hallazgos de las técnicas de imagen convencionales, en las que se ha descrito el adenocarcinoma renal como el origen más frecuente de las metástasis pancreáticas5.
El correcto diagnóstico de los pacientes con metástasis de localización exclusivamente pancreática tendrá importantes repercusiones clínicas, al ser posible, en casos seleccionados, la resección quirúrgica y conseguir de este modo una supervivencia prolongada. En otros pacientes puede evitar cirugías innecesarias y seleccionar el mejor tratamiento no quirúrgico.
La punción guiada por ecoendoscopia se considera la mejor técnica para el diagnóstico citológico y/o histológico de las lesiones sólidas pancreáticas6. Sin embargo, las características ecoendoscópicas y la utilidad en el diagnóstico de las metástasis pancreáticas del carcinoma renal no se han establecido claramente.
OBSERVACIONES CLINICAS
Caso 1
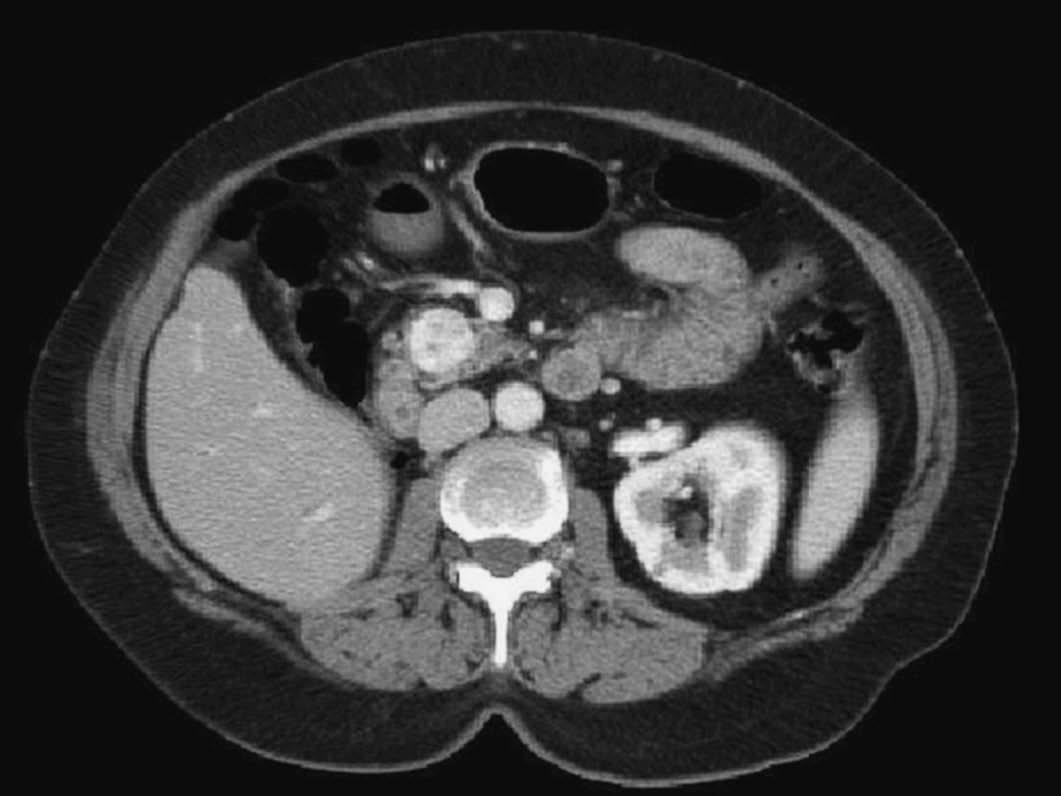
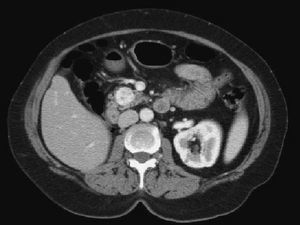
Mujer de 62 años de edad, con antecedente de nefrectomía derecha realizada 8 años antes a causa de un carcinoma renal de células claras sin infiltración vascular, ganglionar ni de la grasa perivisceral (estadio 1 de Robson). Es remitida a consultas de aparato digestivo al detectar en la ecografía abdominal, realizada como parte de un protocolo de seguimiento periódico, la presencia de 2 nódulos de 20 y 10 mm en la cabeza pancreática. En la paciente, asintomática desde el punto de vista digestivo, se decidió completar el estudio analítico sin detectar alteraciones relevantes, y se realizó una tomografía computarizada (TC) toracoabdominal, que identificó las lesiones descritas previamente y permitió determinar su carácter hipervascular con realce intenso en fase arterial (fig. 1), sin identificar ninguna afección de otros órganos.
Fig. 1. Tomografía computarizada abdominal: nefrectomía derecha y lesión focal en la cabeza pancreática que se realza intensamente tras la inyección de un contraste intravenoso.
En el estudio hormonal solicitado con posterioridad se detectaron valores elevados de cromogranina (513 ng/ml; rango, 19-98) con concentraciones de hormonas tiroideas, gastrina, insulina, cortisol, calcitonina, péptido intestinal vasoactivo, serotonina y hormona adrenocorticotropa dentro de los límites normales.
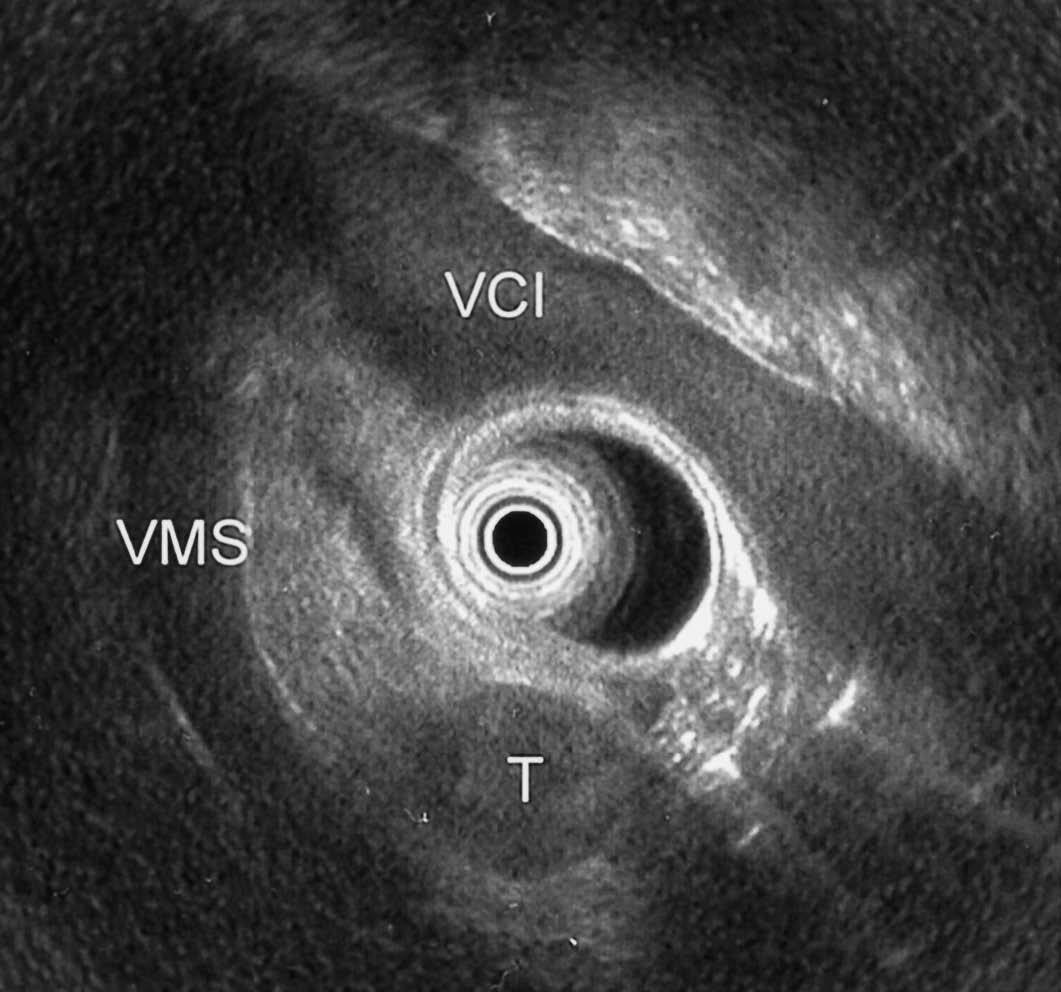
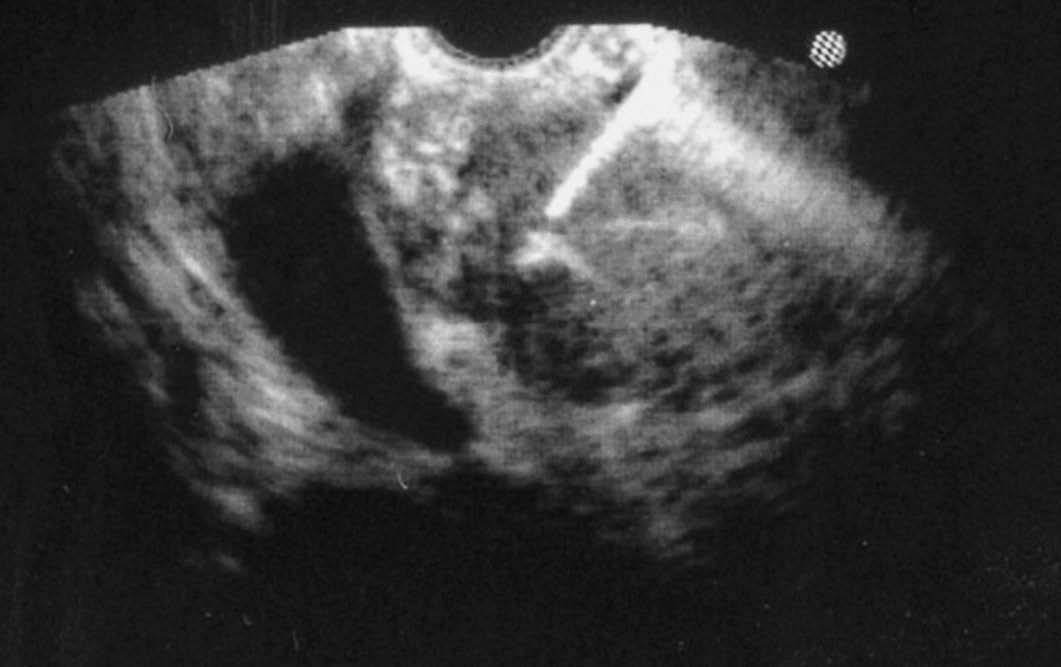
Se procedió a realizar una exploración ecoendoscópica, que permitió visualizar en la cabeza pancreática una lesión focal de 20 mm, homogénea e isoecogénica respecto al parénquima pancreático (fig. 2). Se detectó otra lesión de 10 mm y semejantes características en proceso uncinado. Se llevó a cabo una punción guiada por ecoendoscopia con aguja de 22 G, con el patólogo en la sala de exploración, que requirió dos pases de la aguja. Se obtuvo material hemático, en el que fue posible identificar la presencia de células de citoplasma claro y núcleos prominentes, compatibles con el diagnóstico de metástasis de carcinoma renal.
Fig. 2. Ecoendoscopia radial: lesión focal en la cabeza pancreática redondeada y bien delimitada. T: tumor; VCI: vena cava inferior; VMS: vena mesentérica superior.
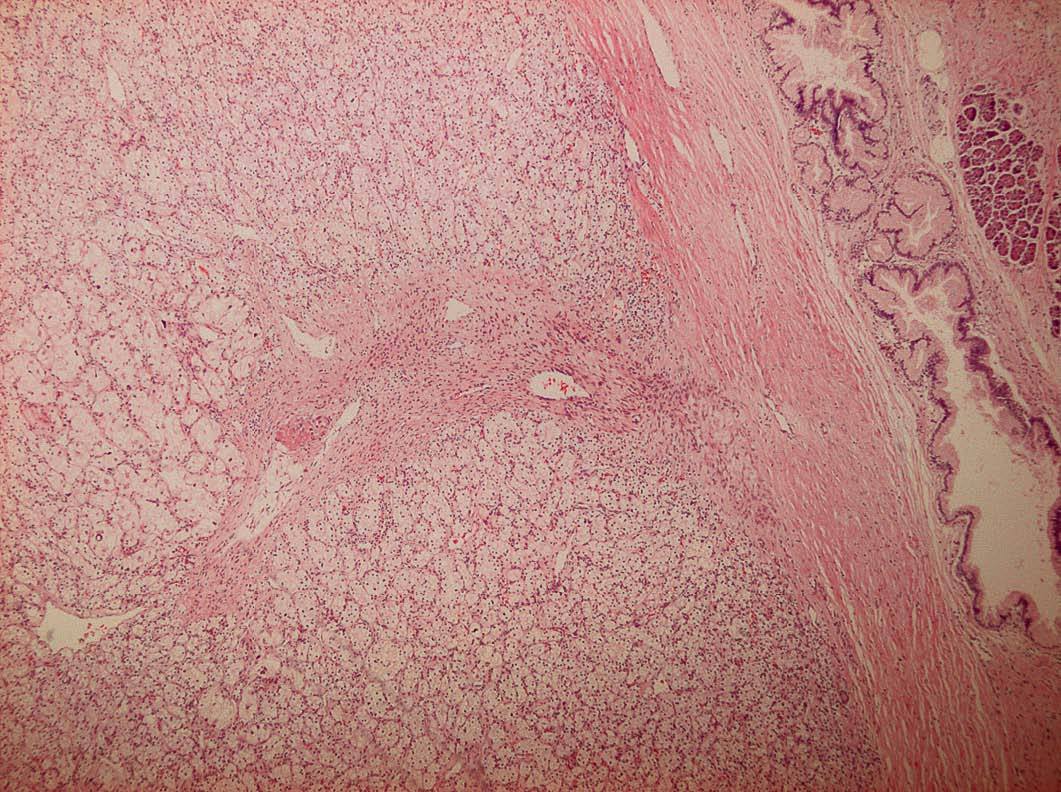
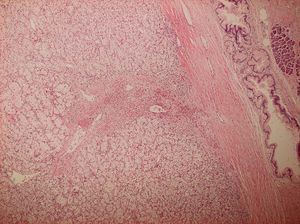
Transcurridas 8 semanas del diagnóstico, la paciente fue intervenida quirúrgicamente con realización de duodenopancreatectomía cefálica y linfadenectomía extendida. El estudio de la pieza operatoria identificó las lesiones pancreáticas descritas en exploraciones previas, que histológicamente eran capsuladas, con arquitectura de semejantes características al tumor primario renal (fig. 3), y presentaban inmunorreacción positiva a la vimentina.
Fig. 3. Imagen histológica correspondiente a un tumor de células claras bien delimitado y encapsulado. Se pone de manifiesto un tejido pancreático normal adyacente (HE,*10).
En el sexto día del postoperatorio la paciente sufrió un deterioro clínico en relación con la dehiscencia de la anastomosis pancreático-yeyunal, por lo que fue reintervenida y se le realizó una pancreatectomía total, a pesar de lo cual presentó una mala evolución clínica con deterioro hemodinámico y de la función renal, falleciendo al octavo día del ingreso.
Caso 2
Varón de 62 años de edad, con antecedente de nefrectomía derecha, realizada 4 años antes, por un carcinoma renal con afección focal de la grasa perirrenal (estadio 2 de Robson). Ingresa por un cuadro de 2 semanas de evolución, consistente en ictericia asociada a dolor abdominal en el hemiabdomen superior, astenia y pérdida de peso. En la ecografía abdominal se observó una dilatación de la vía biliar intrahepática y extrahepática, pero el retroperitoneo no fue valorable por interposición de aire. La TC toracoabdominal puso de manifiesto la presencia de lesiones focales de características hipervasculares en la cabeza pancreática, la suprarrenal izquierda y el pulmón derecho.
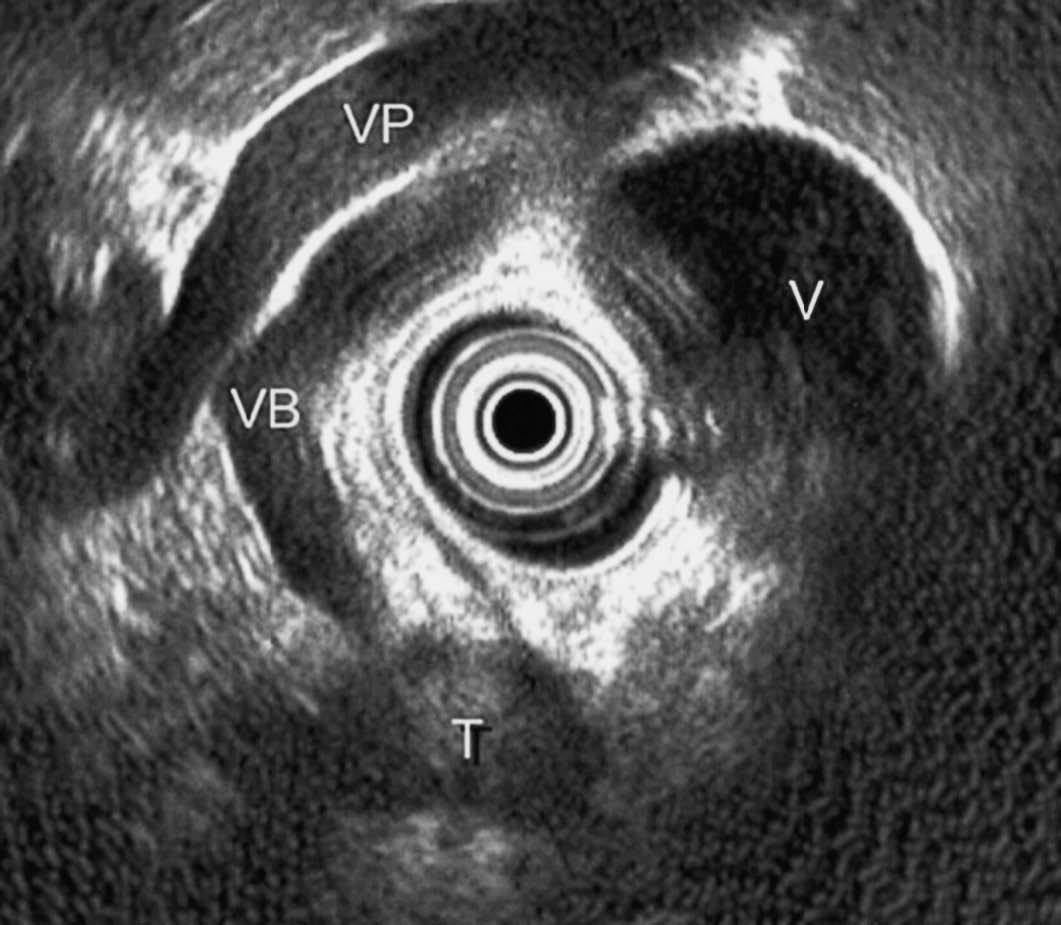
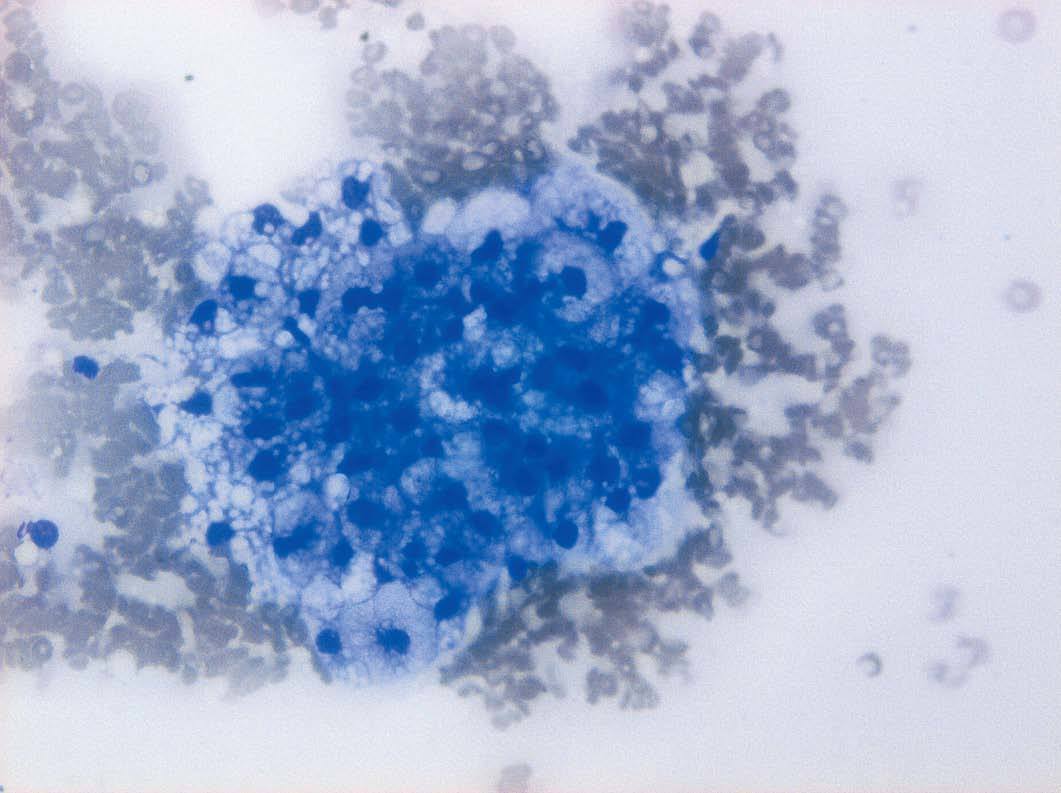
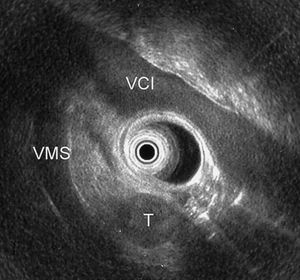
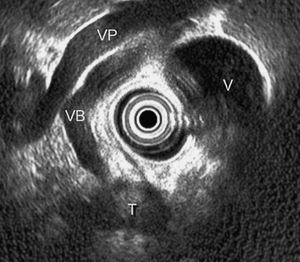
Se realizó una ecoendoscopia que permitió visualizar la lesión descrita previamente en la suprarrenal izquierda, la dilatación de vía biliar extrahepática y una masa hipoecogénica de 20 mm y bordes bien delimitados en la cabeza pancreática (fig. 4), así como otra lesión de semejantes características de 10 mm en proceso uncinado. Se realizó una punción guiada por ecoendoscopia de la lesión en la cabeza pancreática, que requirió 4 pases con aguja de 22 G (fig. 5), y se obtuvo un material citológico constituido por células claras concluyente para el diagnóstico de metástasis de carcinoma renal (fig. 6).
Fig. 4. Ecoendoscopia radial: dilatación de vía biliar extrahepática que finaliza en una lesión redondeada en la cabeza pancreática. T: tumor; V: vesícula; VB: vía biliar; VP: vena porta.
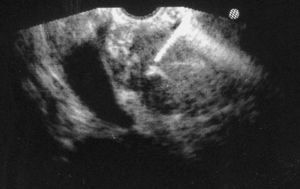
Fig. 5. Punción guiada por ecoendoscopia.
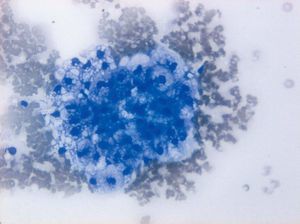
Fig. 6. Citología positiva para células malignas constituida por grupos de células claras (tinción de Giemsa,*40).
La ictericia se resolvió tras la colocación de una prótesis biliar autoexpandible, y 2 semanas después el paciente inició tratamiento con interferón alfa, con mala tolerancia a causa de la fiebre y un deterioro de la función renal. Transcurridas 9 semanas del diagnóstico, el paciente presentó una hemorragia digestiva en relación con la invasión tumoral de la pared duodenal. A pesar del tratamiento endoscópico y las medidas de soporte, presentó una mala evolución clínica y falleció al décimo día del ingreso.
DISCUSION
El adenocarcinoma renal se puede comportar de una forma variable y, en ocasiones, impredecible. El 25% de estos pacientes presenta metástasis a distancia en el momento del diagnóstico, mientras que el 11% de los pacientes a quienes se realiza una nefrectomía presenta en su evolución metástasis a distancia7,8. Su localización más frecuente es el pulmón, el hueso, el hígado, el cerebro y las glándulas suprarrenales. Otras localizaciones mucho más raras son la piel, el tiroides o el páncreas9,10.
Una de las características del carcinoma renal es su recurrencia tras muchos años, con un intervalo de tiempo aproximado de 10 años desde la nefrectomía hasta el diagnóstico de las metástasis, que en algún caso llega a ser de hasta 27 años11, lo que justifica los protocolos de seguimiento a largo plazo en los pacientes intervenidos de este tipo de tumores. Probablemente, este lento crecimiento de los tumores renales explique la mayor frecuencia con la que las metástasis pancreáticas alcanzan un tamaño suficiente como para ser detectadas por las técnicas de imagen disponibles. Mientras que otros tumores que metastatizan en el páncreas dan lugar con frecuencia a pequeños implantes tan sólo evidentes en el estudio microscópico del tejido pancreático obtenido tras la autopsia4.
La vía de extensión del adenocarcima renal al páncreas es desconocida. Si bien se han propuesto como posibles vías de propagación la linfática o, más probable, la vía venosa a través de shunts portorrenales, por los que células malignas con origen en trombos tumorales renales podrían migrar al páncreas1,9.
Los pacientes con metástasis pancreáticas presentan una clínica similar a la de los pacientes con tumores pancreáticos primarios, incluido el dolor abdominal, la ictericia, la alteración del estado general con pérdida de peso, la obstrucción duodenal y/o la hemorragia digestiva como resultado de la invasión de la pared duodenal. Sin embargo, hasta la mitad de estos pacientes se encuentran asintomáticos en el momento del diagnóstico y las lesiones pancreáticas son descubiertas en las exploraciones radiológicas sistemáticas realizadas durante el seguimiento12.
La ecografía y la TC abdominal pueden demostrar la presencia de este tipo de lesiones pancreáticas que, con frecuencia, son redondeadas y bien delimitadas1,13. La inyección de contraste intravenoso permitirá demostrar el carácter hipervascular de estas lesiones con realce intenso y heterogéneo en fase arterial13,14, al igual que los tumores pancreáticos neuroendocrinos, que muestran una apariencia radiológica similar pero que suelen presentar valores hormonales elevados y síntomas endocrinológicos asociados. Por el contrario, los adenocarcinomas de origen pancreático muestran un patrón hipovascular13.
La ecoendoscopia ha demostrado un alto rendimiento diagnóstico en la detección de los tumores pancreáticos, probablemente superior al de otras técnicas de imagen15,16. El aspecto ecoendoscópico de las metástasis pancreáticas es el de una lesión redondeada, de aspecto sólido, bien delimitada, homogénea, con realce periférico o sin atenuación del haz de ultrasonidos, que indican el carácter hipervascular de la lesión y que, respecto al parénquima pancreático subyacente, se suele mostrar hipoecoica, isoecogénica17 o, de modo excepcional, hiperecogénica18,19. Esta técnica permite visualizar algunas lesiones que por su pequeño tamaño pueden no ser visibles con otras técnicas de imagen18, pues en la mitad de las ocasiones son lesiones pancreáticas múltiples.
Las características clínicas y radiológicas, así como los hallazgos ecoendoscópicos, con frecuencia no permiten distinguir con fiabilidad las lesiones benignas, los tumores primarios y las metástasis pancreáticas19. La punción para estudio citológico permitirá diferenciar estas lesiones con importantes implicaciones terapéuticas y pronósticas20. Tradicionalmente, la punción percutánea se ha utilizado en el diagnóstico de las masas pancreáticas. Sin embargo, cuando está disponible, la punción por vía ecoendoscópica ha sustituido a la vía percutánea y ha permitido, de un modo menos invasivo, obtener un diagnóstico citológico con un mayor rendimiento diagnóstico, sobre todo en lesiones de pequeño tamaño6,21,22. Sin embargo, por tratarse las metástasis pancreáticas de tumores friables e hipervasculares, la punción puede complicarse con eventos hemorrágicos17,23, y puede ocurrir que las muestras obtenidas presenten un alto contenido hemático, que por otro lado resulta inusual en la punción de tumores pancreáticos primarios19. Para evitar la aspiración hemática, algunos autores23 han referido un mayor rendimiento y seguridad de la punción utilizando un menor grado de aspiración en este tipo de lesiones.
Todavía no se ha establecido claramente la utilidad real del tratamiento médico en los pacientes con metástasis del carcinoma renal24, por lo que no puede recomendarse su utilización de forma generalizada. En series quirúrgicas, en las que se incluyen pacientes con metástasis de localización exclusivamente pancreática, en quienes se realizó una resección quirúrgica, se ha documentado una baja mortalidad y tasas de supervivencia a los 5 años próximas al 60%1,25,26, superiores a las descritas en los pacientes con metástasis pancreáticas que no recibieron tratamiento quirúrgico, e incluso superiores a las descritas tras el tratamiento quirúrgico del adenocarcinoma primario de páncreas5. Por tanto, la resección quirúrgica de las metástasis pancreáticas, en los pacientes con un aceptable riesgo quirúrgico en los que la resección completa es posible, debe considerarse el mejor tratamiento disponible actualmente12,25.
En conclusión, la ecoendoscopia representa una técnica útil en la detección y la caracterización de estas lesiones y permite completar el estudio con la obtención de material para el estudio citológico, que siempre será recomendable para hacer una aproximación pronóstica lo más fiable posible y decidir la mejor actitud terapéutica en cada caso.