el uso de la enteroscopia con videocápsula fue aprobado por la FDA en 2001. La hemorragia digestiva y la enfermedad inflamatoria intestinal son sus principales indicaciones. En nuestro centro se realiza desde 2004.
Material y métodosHemos recogido de forma retrospectiva los pacientes tratados mediante cápsula de intestino delgado desde octubre de 2004 hasta abril de 2015. Las indicaciones se han dividido en grupos: hemorragia digestiva de origen oscuro, tanto oculta como manifiesta; enfermedad inflamatoria intestinal; otras indicaciones. Los hallazgos se han dividido: lesiones vasculares; lesiones inflamatorias; otras lesiones; estudios normales; estudios no concluyentes.
ResultadosDe un total de 1.291 estudios se ha incluido 1.027 en el análisis. La edad media es 56,45 años, con 471 hombres y 556 mujeres. La enfermedad más frecuentemente observada fueron las lesiones vasculares, asociadas o no a otras lesiones. Cuando la indicación era una hemorragia digestiva, el impacto diagnóstico fue del 80%. En la enfermedad inflamatoria esta cifra solo alcanza el 50%. El rendimiento diagnóstico es mucho menor en el grupo de «otras indicaciones». No se han registrado complicaciones mayores.
DiscusiónLa cápsula de intestino delgado tiene un alto rendimiento diagnóstico en los casos de hemorragia digestiva; el número de estudios con hallazgos positivos es menor en los de enfermedad inflamatoria intestinal.
ConclusionesSe trata de una modalidad diagnóstica segura y de gran utilidad para el diagnóstico de enfermedad del intestino delgado, aunque se precisa mejorar el índice de sospecha en la enfermedad inflamatoria intestinal.
Capsule endoscopy was approved by the FDA in 2001. Gastrointestinal bleeding and inflammatory bowel disease are the main indications. It has been available in our hospital since 2004.
MethodsWe retrospectively analysed data from patients who underwent small bowel capsule endoscopy in our hospital from October 2004 to April 2015. Indications were divided into: Obscure gastrointestinal bleeding (occult and overt), inflammatory bowel disease, and other indications. Findings were divided into: Vascular lesions, inflammatory lesions, other lesions, normal studies, and inconclusive studies.
ResultsA total of 1027 out of 1291 small bowel studies were included. Mean patient age was 56.45 years; 471 were men and 556 women. The most common lesion observed was angiectasia, as an isolated finding or associated with other lesions. Findings were significant in up to 80% of studies when the indication was gastrointestinal bleeding, but in only 50% of studies in inflammatory bowel disease. Diagnostic yield was low in the group «other indications». No major complications were reported.
DiscussionSmall bowel capsule endoscopy has high diagnostic yield in patients with gastrointestinal bleeding, but yield is lower in patients with inflammatory bowel disease.
ConclusionsOur experience shows that capsule endoscopy is a safe and useful tool for the diagnosis of small bowel disease. The diagnostic yield of the technique in inflammatory bowel disease must be improved.
La primera referencia a la cápsula endoscópica (CE) en la literatura científica aparece en mayo del año 2000 en la revista Nature1. En este breve artículo Iddan describía el desarrollo de una cápsula ingerible capaz de capturar imágenes de la mucosa digestiva de forma inalámbrica mientras transitaba impulsada por el peristaltismo, y comunicaba las primeras experiencias de su grupo al administrar el dispositivo a humanos. No tardaron mucho tiempo en aparecer los primeros trabajos que evaluaban la seguridad y eficacia del procedimiento, y lo comparaban con otras técnicas (endoscópicas y radiológicas) para el diagnóstico de la patología del intestino delgado (ID)2–5.
Desde un principio la indicación más importante y por la que más frecuentemente se realizaban estudios de CE fue la hemorragia digestiva de origen oscuro (HDOO); las primeras series se publicaron entre los años 2002 y 20045–10. Aunque de forma marginal, y con un número de procedimientos sensiblemente menor, se establecieron otras indicaciones para la CE, como la enfermedad inflamatoria intestinal (EII), la enfermedad neoplásica o la celiaquía11–14. Estas indicaciones, así como las diferentes recomendaciones al respecto, han sido incluidas en las guías de práctica clínica (y sus actualizaciones) y en los documentos de consenso de sociedades científicas como la European Society of Gastrointestinal Endoscopy (ESGE), la American Society of Gastrointestinal Endoscopy (ASGE) o la European Crohn's and Colitis Organisation (ECCO)15–20.
Hacia 2006 se produjo un hito en el desarrollo tecnológico de la endoscopia con videocápsula: la introducción de la cápsula de colon (CCE). El grupo de Eliakim publicaba una serie de 91 pacientes en la que comunicaba su utilidad para la detección de enfermedad colónica, y su seguridad21. Aunque en un primer momento se propuso la utilización de esta tecnología en pacientes con colonoscopia previa incompleta o con contraindicaciones o dificultades para un estudio endoscópico convencional22, posteriormente se ha extendido el número de posibles indicaciones de la CCE: existen estudios sobre su utilidad en el cribado de cáncer colorrectal, el seguimiento de pacientes con EII e incluso en el paciente pediátrico23–26. En la actualidad, una de las últimas fronteras de los estudios de videocápsula es la posibilidad de realizar exploraciones de todo el tubo digestivo, o al menos panentéricas, con un único dispositivo y en un solo acto27.
El primer estudio de CE de ID en nuestro centro se llevó a cabo en octubre de 2004: fue, por tanto, uno de los primeros en España en incorporar esta tecnología. Durante los primeros años se realizó un número muy limitado de procedimientos, que se incrementó de forma muy importante posteriormente.
En cuanto a las indicaciones, acorde con lo expuesto anteriormente, en los primeros años la gran mayoría de los estudios se realizaban en pacientes con HDOO. Las exploraciones en pacientes con sospecha de enfermedad de Crohn (EC) fueron escasas en esos momentos iniciales, y es solo a partir de 2007 cuando hay un incremento en esta indicación, la cual supone en la actualidad aproximadamente la mitad de los procedimientos que realizamos en nuestro servicio. La CCE ha sido incorporada recientemente en nuestro centro, por tanto, nuestra experiencia es más limitada y queda fuera del presente trabajo.
Presentamos un análisis descriptivo de nuestra experiencia en enteroscopia con videocápsula desde su introducción en nuestro centro en 2004 hasta 2015.
Material y métodosSe han recogido de forma retrospectiva los datos de todos aquellos pacientes diagnosticados mediante estudios de CE de ID en nuestro centro desde octubre de 2004 hasta abril de 2015, incluyendo datos demográficos, indicaciones del estudio, hallazgos y complicaciones. Se ha excluido a todos aquellos con información incompleta o confusa.
IndicacionesLas indicaciones de los estudios de CE se han dividido en 4 grupos:
- -
Hemorragia digestiva de origen oscuro oculta (HDOOoc): definida como aquella anemia de origen digestivo por pérdidas insensibles, en que una endoscopia alta y baja convencionales no han encontrado una lesión que justifique el cuadro.
- -
Hemorragia digestiva de origen oscuro manifiesta (HDOOma): aquel cuadro de sangrado gastrointestinal agudo manifestado como rectorragia, hematoquecia o melenas, en el que tras realizar una endoscopia digestiva alta y baja no se ha obtenido un diagnóstico etiológico.
- -
EEI: incluyendo pacientes con sospecha de EC de ID y estudios de extensión de la enfermedad, si bien esta última circunstancia es en nuestra serie histórica más infrecuente de lo que cabría esperar. En los casos de sospecha de EC, a los pacientes se les había hecho previamente una colonoscopia que había resultado normal. Aunque en un alto porcentaje de casos se informaba en estas de la visualización de íleon terminal y la ausencia de lesiones a este nivel, en otros no fue posible franquear la válvula ileocecal, y en un número menor de pacientes no hay constancia en el informe endoscópico de la exploración ileal o del fracaso al intentarlo.
- -
Otras indicaciones: incluimos en este grupo indicaciones menos frecuentes que la HDOO y la EC, como seguimiento de poliposis intestinal, enfermedad celiaca (tanto en el diagnóstico inicial como en caso de complicaciones), hallazgos radiológicos, dolor abdominal inespecífico, etc.
En lo referente al diagnóstico, los hallazgos de los estudios de CE también se han dividido en varios grupos:
- -
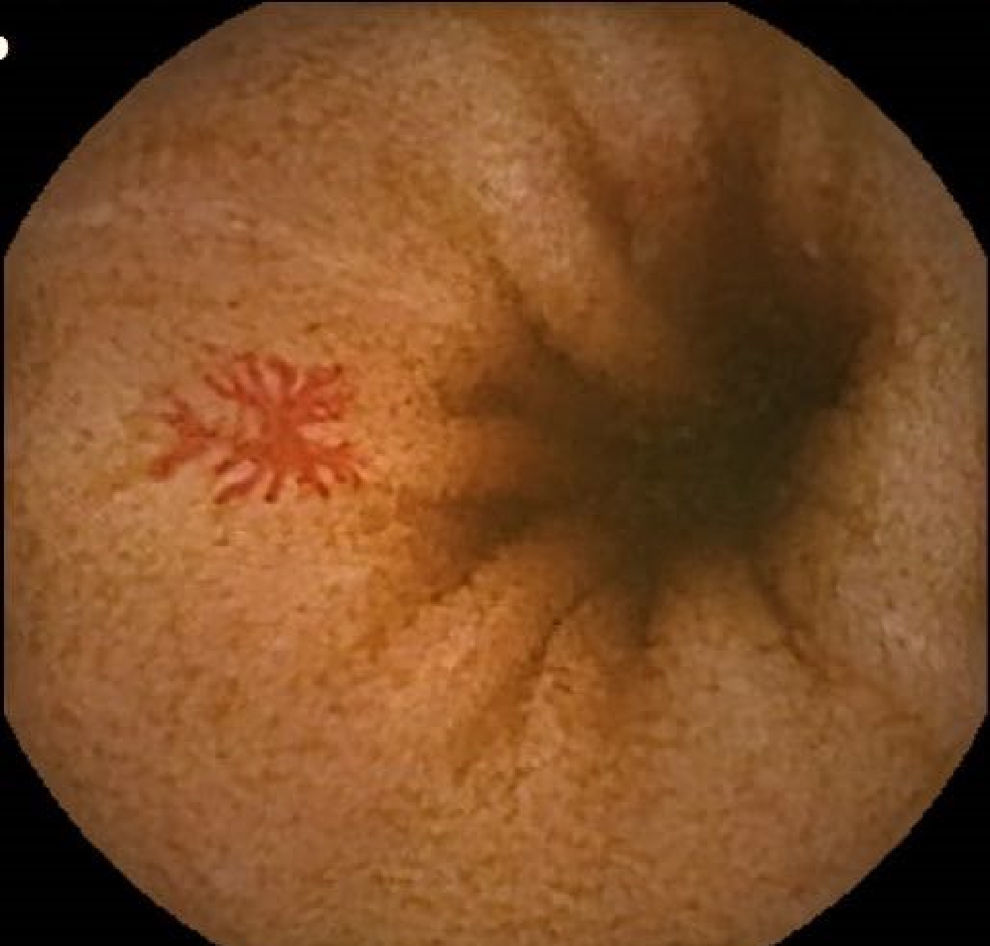
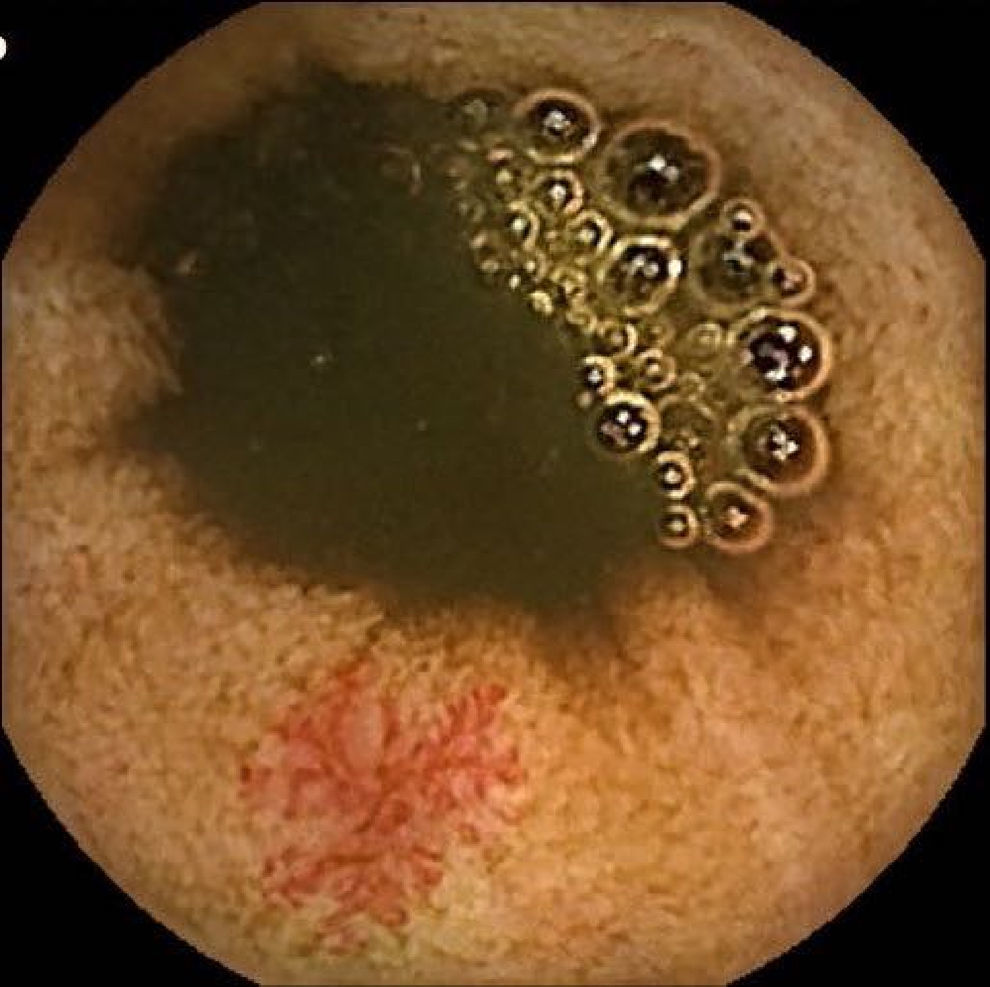
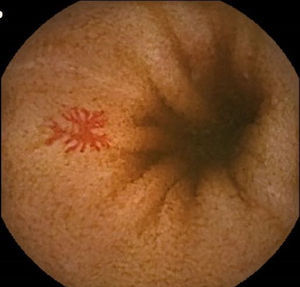
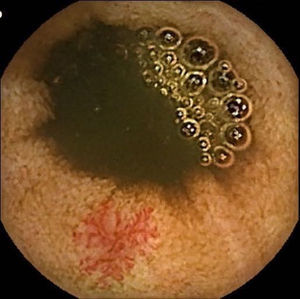
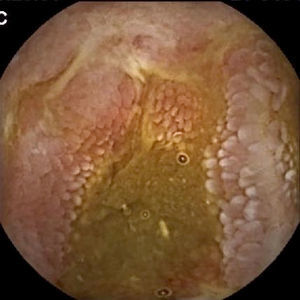
Lesiones vasculares (LV): quedaron recogidas fundamentalmente en este grupo las angioectasias (figs. 1 y 2), aunque también se ha incluido pacientes con otras lesiones menos frecuentes, como las varices intestinales.
- -
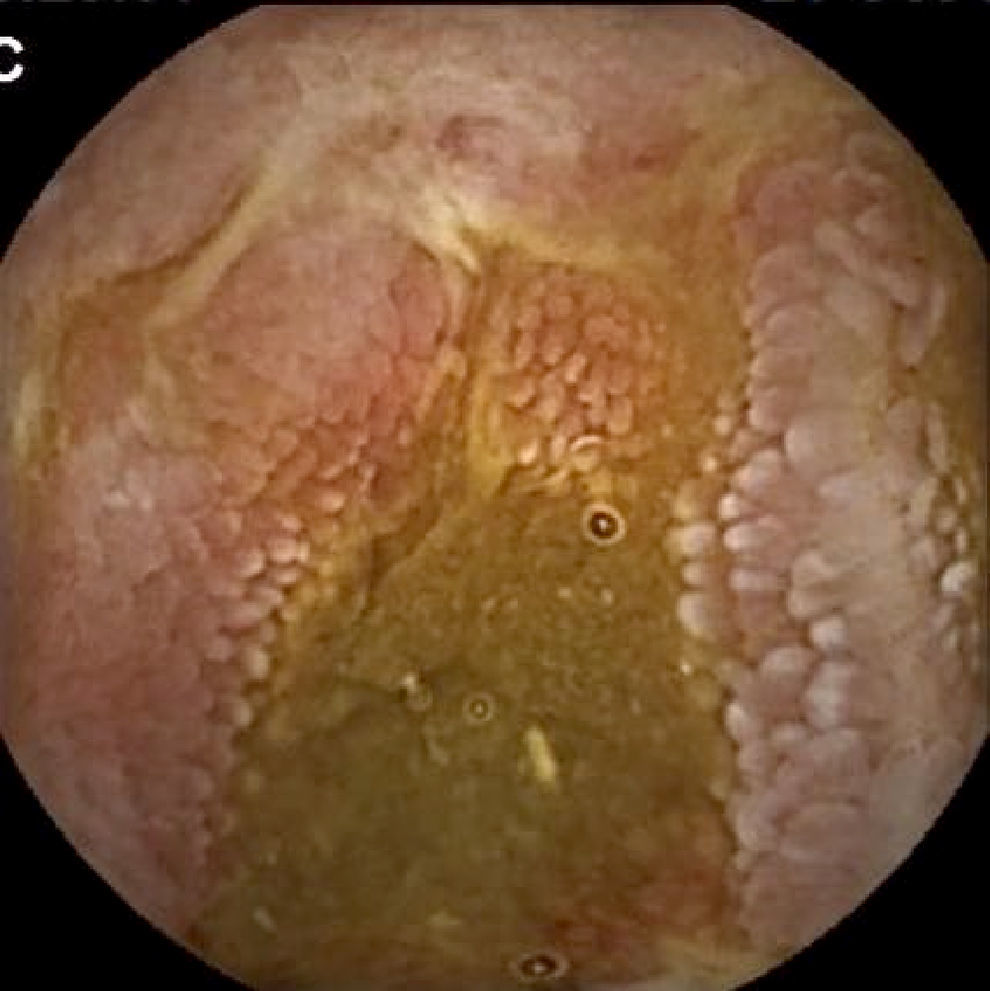
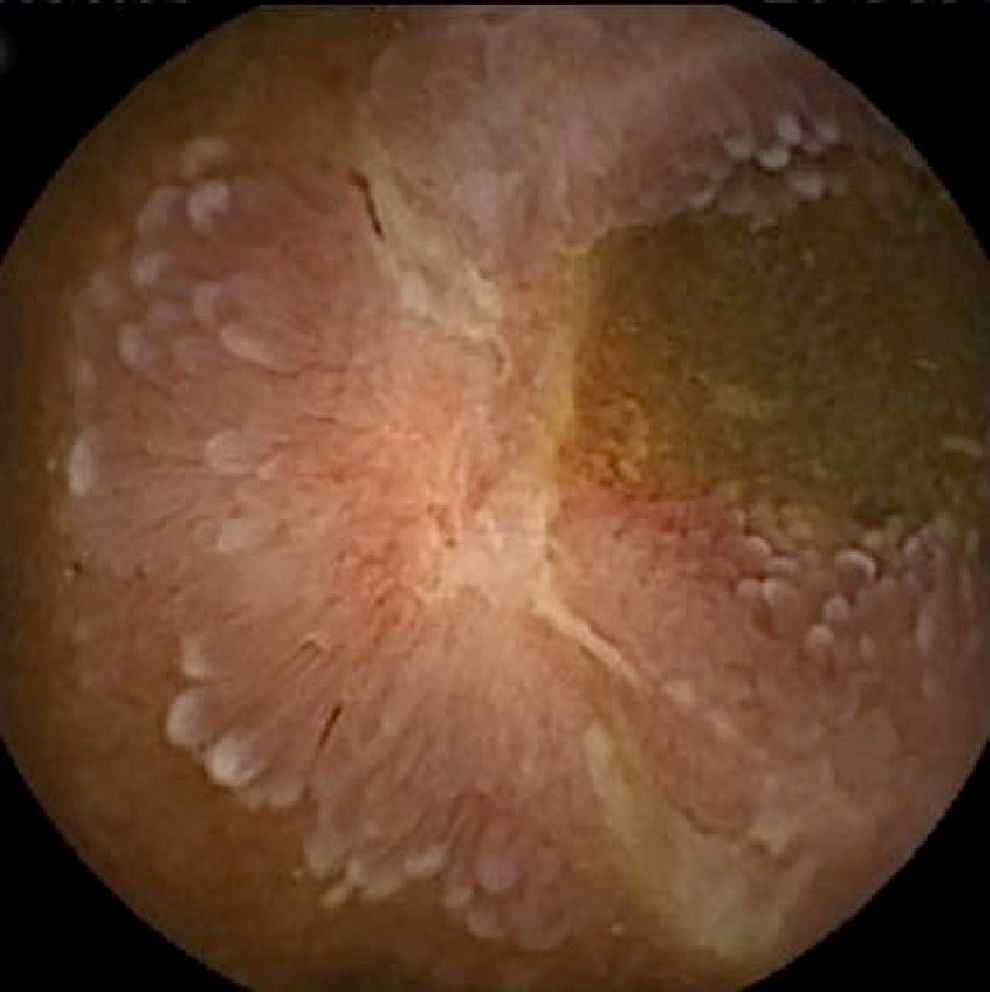
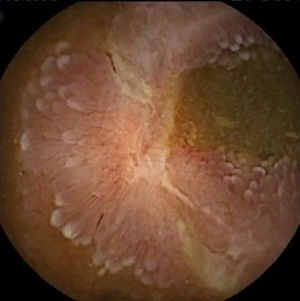
Lesiones inflamatorias (LI): se han incluido todos aquellos hallazgos (edema vellositario y eritema mucoso, erosiones o úlceras, estenosis…) compatibles con una EC de ID (figs. 3 y 4). También se han recogido en este grupo las lesiones erosivas potencialmente relacionadas con la toma de antiinflamatorios no esteroideos (AINE).
- -
Otras lesiones: tal como atrofia vellositaria, pólipos, tumoraciones (mucosas o submucosas), etc.
- -
Estudios sin hallazgos: todas aquellas exploraciones de CE en que no se ha observado ninguna lesión, o en las que había lesiones mínimas que el lector ha considerado no significativas o incidentales en el contexto clínico del paciente.
- -
Estudios no concluyentes: estudios incompletos por retención gástrica o intestinal, en los que ha habido problemas técnicos en la recogida o procesado de las imágenes, o preparación intestinal insuficiente que no permite la valoración de ningún tramo de la mucosa, etc.
Los estudios de CE se han llevado a cabo en todos los casos con los equipos de Given Imaging Ltd. (actualmente Medtronic). A lo largo de los años hemos hecho uso de los diferentes modelos de videocápsula y de software suministrados por esta compañía, desde la M2A® (primera cápsula comercializada) hasta la última generación, la SB3®.
No existe consenso sobre cuál debe ser la preparación intestinal que deben realizar los pacientes antes de un estudio de CE de ID. Se han propuesto preparaciones basadas simplemente en la dieta líquida, y otras a base de diferentes dosis de soluciones evacuantes asociadas o no a procinéticos o antiflatulentos. En algunos trabajos no se han encontrado diferencias al comparar las distintas estrategias28, mientras que en otros se han apuntado ciertas ventajas a favor de las preparaciones a base de polietilenglicol29. En nuestro caso, aunque en algunos momentos hemos utilizado una preparación con polietilenglicol, en la actualidad se indica a los pacientes que acuden a realizarse estudios de CE de ID que sigan una dieta sin fibra los días previos al procedimiento y que permanezcan en ayunas desde la noche anterior. En pacientes encamados o si se sospechan alteraciones de la motilidad, se realiza una preparación con media dosis de solución evacuante.
Con la información recogida se ha realizado, en primer lugar, un análisis descriptivo tomando en cuenta las características demográficas de los pacientes en cada indicación y las diferentes frecuencias con que se ha registrado cada hallazgo. Posteriormente, se ha analizado la frecuencia con que cada hallazgo endoscópico se da en cada indicación, así como el porcentaje de estudios normales, para evaluar el rendimiento diagnóstico de la técnica en cada caso.
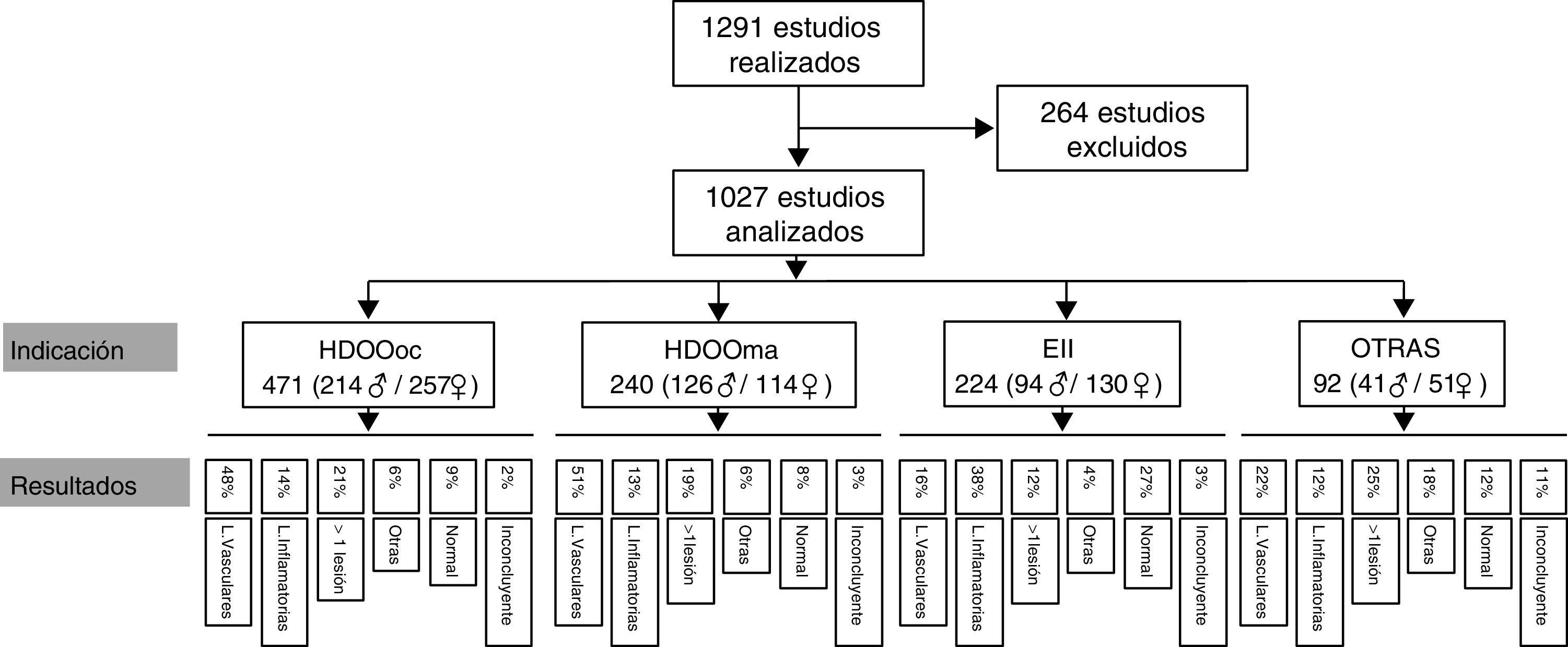
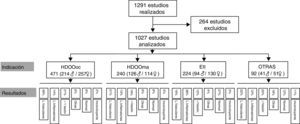
ResultadosSe ha contabilizado un total de 1.291 procedimientos de CE realizados en nuestra unidad desde octubre de 2004 hasta abril de 2015. De todos ellos, en 264 casos no ha sido posible recoger los datos requeridos para este análisis por información incompleta, dudosa o, bien por inaccesible: quedaron, por tanto, un total de 1.027 estudios de CE incluidos en el estudio finalmente.
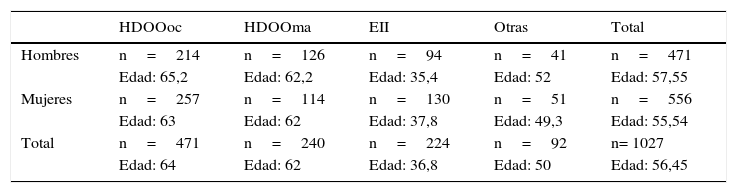
La edad media de los pacientes es de 56,45 años (4–91 años), con un total de 471 hombres (edad media de 57,55 años) y de 556 mujeres (edad media de 55,54 años). La indicación que se ha observado con más frecuencia es HDOOoc (n=471; 214 hombres/257 mujeres), seguida por HDOOma (n=240; 126 hombres/114 mujeres), EII (n=224; 94 hombres/130 mujeres) y «otras indicaciones» (n=92; 41 hombres/51 mujeres). En la tabla 1 se recoge la distribución de las diferentes indicaciones en relación con el sexo y la edad de los pacientes.
Distribución de las diferentes indicaciones de CE en relación con la edad media y el sexo de los pacientes
| HDOOoc | HDOOma | EII | Otras | Total | |
|---|---|---|---|---|---|
| Hombres | n=214 | n=126 | n=94 | n=41 | n=471 |
| Edad: 65,2 | Edad: 62,2 | Edad: 35,4 | Edad: 52 | Edad: 57,55 | |
| Mujeres | n=257 | n=114 | n=130 | n=51 | n=556 |
| Edad: 63 | Edad: 62 | Edad: 37,8 | Edad: 49,3 | Edad: 55,54 | |
| Total | n=471 | n=240 | n=224 | n=92 | n= 1027 |
| Edad: 64 | Edad: 62 | Edad: 36,8 | Edad: 50 | Edad: 56,45 |
EII: enfermedad inflamatoria intestinal; HDOOma: hemorragia digestiva de origen oscuro manifiesta; HDOOoc: hemorragia digestiva de origen oscuro oculta.
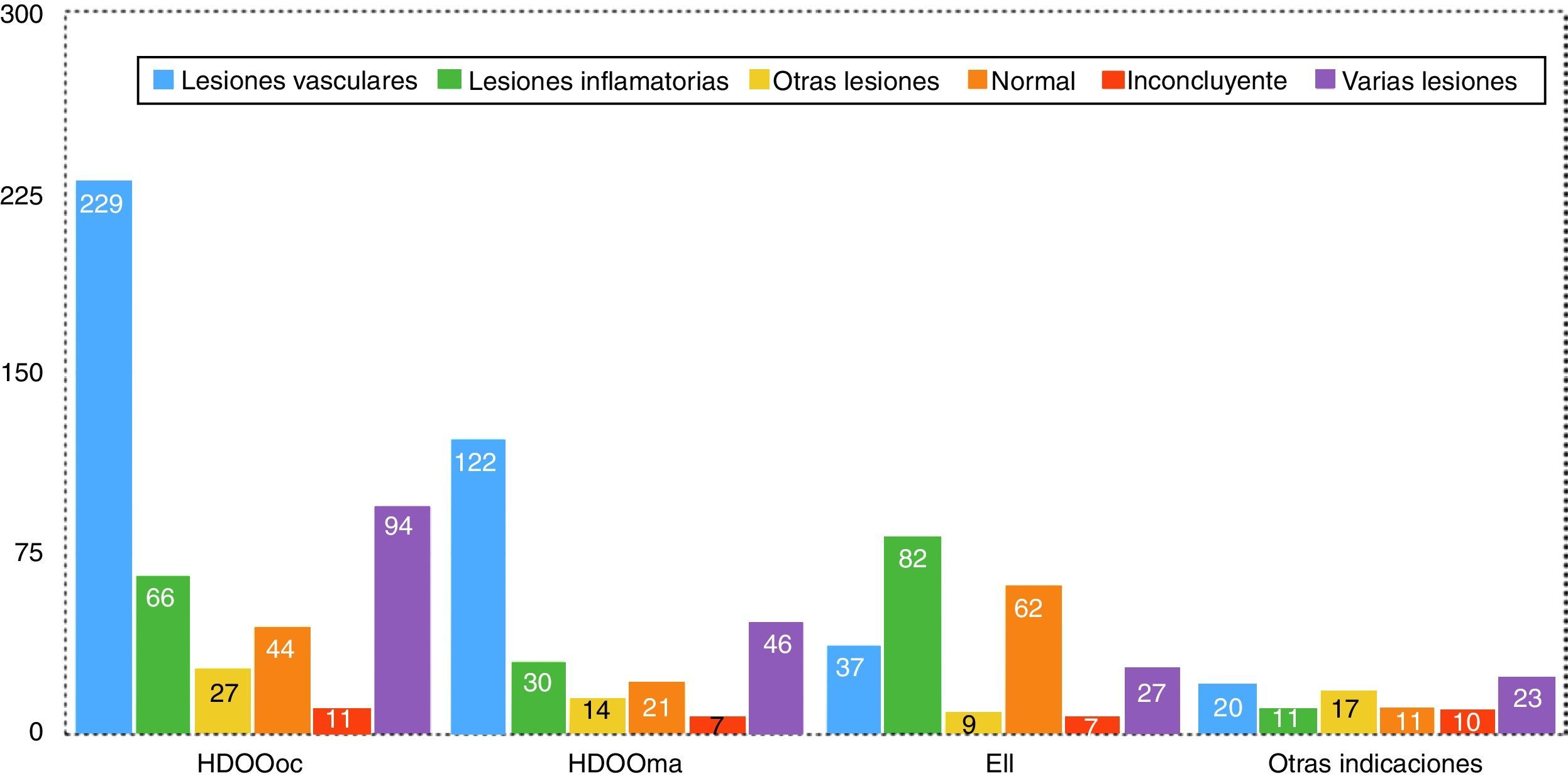
En cuanto al análisis global de los hallazgos en los estudios de CE, el más frecuentemente observado fue LV en 583 casos (57% del total de estudios incluidos), bien como único hallazgo, bien asociado a otros tipos de lesión. Se observó presencia de LI en 329 casos (32% del total de estudios incluidos), como única lesión o en asociación con otras lesiones. Otros tipos de lesión, fundamentalmente pólipos o tumoraciones submucosas, fueron encontrados en 159 casos (15% del total de estudios incluidos), en la mayoría de ellos como hallazgos secundarios o incidentales.
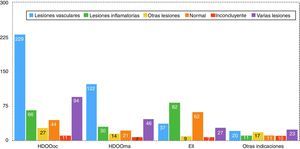
En cuanto a los hallazgos según la indicación, estos se reparten de la siguiente manera (estos datos se resumen también en las figs. 5 y 6): entre los 471 casos de HDOOoc, en 229 se diagnosticó la presencia de LV (48%), 66 pacientes (14%) presentaron LI (en la mayoría de casos se trataba de pacientes en tratamiento con AINE, aunque también se han diagnosticado en este grupo varios pacientes con EC en los que el síntoma cardinal fue la anemia), en 97 (21%) se observó más de un tipo de lesión concomitante (la asociación más frecuente es la de LV y LI en pacientes con tratamiento antitrombótico), en 27 casos (6%) hubo hallazgos incidentales, y en 44 y 11 pacientes (9% y 2%) los estudios fueron normales o no concluyentes respectivamente. Entre los 240 que presentaron HDOOma hubo 122 diagnósticos de LV (51%), 30 pacientes (13%) tenían LI, en 46 casos (19%) hubo varios tipos de lesión (como en el caso de las HDOOoc, en la mayoría de las ocasiones combinación de LV y LI), en 14 enfermos (6%) se observó lesiones incidentales y en 21 y 7 casos (8 y 3%), respectivamente, los estudios fueron normales o no concluyentes. Entre los 224 pacientes cuya indicación fue EII, 82 de ellos presentaron LI (38%), en 37 casos (16%) se observó LV (probablemente hallazgo casual en el contexto de estos pacientes con sospecha de EII), en 9 estudios (4%) hubo hallazgos como pólipos o tumores submucosas, en 27 individuos (12%) hubo más de un tipo de lesión (nuevamente en la mayoría de casos asociación de LV y LI), y en 62 y 7 casos (27 y 3%), respectivamente, los estudios fueron normales o no concluyentes. En el grupo de «otras indicaciones», de los 92 pacientes, encontramos 20 con LV (22%), 11 con LI (12%), 17 con lesiones polipoides o submucosas (18%), 23 con varios tipos de lesión (25%), y 11 y 10 (12 y 11%) con estudios normales o no concluyentes. En este grupo cabe señalar el diagnóstico de un caso de yeyunitis ulcerativa y 3 linfomas intestinales en pacientes celiacos.
Globalmente, en los casos de HDOO se ha observado hasta un 80% de casos en los que los hallazgos (fundamentalmente LV, LI o ambas) podrían justificar la indicación. En el grupo de pacientes con sospecha de EII esta cifra se sitúa en torno al 50%: el resto de los estudios son normales, no concluyentes o con presencia de lesiones incidentales. En el grupo de «otras indicaciones» el rendimiento diagnóstico es mucho menor, con multitud de hallazgos casuales y con solo un 21% de hallazgos relacionados con la indicación.
No se ha registrado en nuestra base de datos ninguna complicación mayor. En cuanto a complicaciones menores, hemos registrado varias retenciones de la CE a diferentes niveles del tubo digestivo. Se han observado 4 casos de retención gástrica transitoria de la CE. En todos ellos la batería de la cápsula se agotó antes de que esta abandonara la cavidad gástrica, pero en ninguno fue preciso retirarla endoscópicamente porque en todos los pacientes se produjo finalmente el paso al intestino delgado. También se han registrado 5 casos de retención de la CE a nivel de ID: una mujer de 65 años cuya indicación era HDOOoc; un varón de 47 años igualmente con indicación de HDOOoc; un varón de 85 años, hospitalizado, cuya indicación era HDOOma; una mujer de 28 años en estudio por sospecha de EII y un varón de 19 años también en estudio por sospecha de EII. Todos estos pacientes presentaban estenosis en relación con EC (no sospechadas previamente a la ingesta de la CE) y fueron manejados de modo conservador, con tratamiento médico inicialmente y sin necesidad de cirugía urgente. Dos de ellos (la mujer de 65 y el varón de 47 años) precisaron tratamiento quirúrgico de su enfermedad inflamatoria estenosante, pero de forma programada y sin que en ningún caso la retención de la cápsula condicionara el momento de la cirugía. En este aspecto es interesante indicar que en nuestra unidad utilizamos la cápsula degradable Agile-Patency® en los casos en que se sospecha una estenosis de ID desde principios del año 2013. Previamente se utilizaban técnicas radiológicas como el tránsito baritado, aunque se abandonó su uso por falta de evidencia en cuanto a su utilidad para prevenir la retención de la CE. Desde ese momento se han administrado un total de 27 cápsulas degradables: en 5 casos se ha contraindicado la ingesta de la CE por no excreción de aquella; en los restantes 22 casos en los que la cápsula degradable fue excretada íntegramente fue administrada la CE posteriormente sin que se observara ninguna complicación. En los casos descritos en los que se produjeron retenciones de la CE no se había sospechado una estenosis del ID y no se había hecho ninguna prueba de permeabilidad previa.
Se ha administrado la CE a pacientes portadores de dispositivos cardiacos sin que hayan mostrado mal funcionamiento en ningún caso. En nuestra experiencia sí hemos constatado fallos en la transmisión de imágenes de la cápsula al registrador en pacientes ubicados en zonas del hospital dotadas de equipos de telemetría (planta de hospitalización de Cardiología o Unidad de Cuidados Intensivos).
DiscusiónDesde su introducción, la CE ha demostrado ser una herramienta muy útil para el diagnóstico de la patología del ID. La indicación por la que se realiza un mayor número de exploraciones y en la que la CE tiene un mayor rendimiento diagnóstico es la HDOO (excepto en la edad pediátrica, cuando la indicación más frecuente es la EII30). Se han publicado múltiples series y revisiones a este respecto, informándose de una eficacia diagnóstica en los casos de HDOO que va desde el 47 hasta el 84%, si bien en muchos casos los estudios son heterogéneos, con variabilidad en especial en lo referente a la precocidad con la que se llevan a cabo los estudios de CE y, por tanto, difíciles de comparar entre sí31–34. La lesión más característica en este grupo de pacientes es la de tipo vascular (equivalente a LV en nuestro análisis), especialmente las angioectasias, seguidas por lesiones de tipo inflamatorio (equivalente a LI en nuestra serie), bien en el contexto de una EC de ID o de la toma de AINE9,10,35,36. En este sentido los resultados de nuestra serie histórica no difieren de lo que se ha informado previamente en la literatura: los casos de HDOO suponen la indicación más habitual y en este grupo se da el mayor rendimiento diagnóstico (observamos, tanto en los casos de HDOOoc como en los de HDOOma, lesiones que podían justificar la indicación en torno al 80% de los casos) y las LV son las más frecuentemente observadas.
Cabe destacar la frecuencia en que hemos observado en nuestra serie la presencia de LV en indicaciones distintas de HDOO, en especial en pacientes de edad avanzada. El hecho de que se observe LV de forma incidental en todos los grupos podría hacernos pensar que en pacientes con HDOO cierto número de estas lesiones pueden aparecer también de forma casual, sin que sean las responsables de los cuadros de anemia. No obstante, no nos es posible confirmar este extremo ni hacer recomendaciones de forma general al respecto. Aunque se han propuesto sistemas para valorar y catalogar el riesgo de sangrado de las diferentes lesiones observadas durante los estudios de CE37, no siempre resulta fácil determinar la relevancia clínica de estas durante la lectura de los estudios.
La principal razón de que los estudios de CE resulten tan rentables desde el punto de vista del diagnóstico en los casos de HDOO es que se han definido en multitud de series y revisiones sistemáticas los factores del paciente que se asocian con un mayor índice de hallazgos. Merced a esto es posible seleccionar a los pacientes que más se pueden beneficiar de la técnica y realizar indicaciones más ajustadas, lo cual cobra especial importancia si tenemos en cuenta los costes asociados a estos procedimientos, tanto en lo referente a material como a consumo de tiempo de trabajo de los profesionales38. Entre estos factores se encuentran el carácter agudo del sangrado, la necesidad de tratamiento con hierro oral o hemoderivados, el sexo masculino y la edad por encima de los 65 años, la toma de AINE o antitrombóticos, enfermedad hepática39–42… No ocurre así en los casos de EII, indicación en la que no se han definido de forma tan prolija cuáles son los factores asociados a un mayor rendimiento diagnóstico de la CE, y en la que observamos una tasa menor de hallazgos positivos. La CE ha demostrado su utilidad en el diagnóstico de la EC43 y su superioridad frente a las técnicas radiológicas11,12, y en 2005, durante una conferencia de consenso (ICCE–International Conference on Capsule Endoscopy), se estableció su utilidad en pacientes con sospecha de EC de ID y estudios previos negativos44. Poco después, y con las conclusiones de esta reunión de expertos, se redactó un documento con diferentes recomendaciones45, entre las que se encuentran un conjunto de criterios en los que debe basarse la sospecha de EC de ID:
- -
Datos clínicos: dolor abdominal, diarrea crónica, pérdida de peso, retraso del crecimiento.
- -
Manifestaciones extraintestinales: artropatía, pioderma, afectación perianal, colangitis esclerosante primaria.
- -
Marcadores analíticos: anemia, elevación de la proteína C reactiva o la velocidad de sedimentación globular, leucocitosis, marcadores serológicos, marcadores fecales.
- -
Anomalías en pruebas de imagen: tránsito baritado de ID, tomografía computarizada.
Posteriormente se ha podido comprobar que los pacientes que presentan estos criterios de sospecha tienen mayores probabilidades de presentar lesiones en los estudios de CE, tanto mayores cuanto mayor número de criterios estén presentes e independientemente de cuáles sean46. Existe un número limitado de trabajos que buscan la relación entre los diferentes síntomas o parámetros analíticos (en su mayoría de forma aislada) y los hallazgos en la CE de ID, se trata, además, de análisis heterogéneos, difíciles en ocasiones de comparar y con resultados dispares47–50. Se han publicado algunas series que analizan la asociación entre diferentes criterios de sospecha, y que concluyen que los pacientes que presentan algún síntoma compatible asociado a alteraciones bioquímicas51 o los que presentan una asociación de anemia y trombocitosis52 son los mejores candidatos para estudios de CE en caso de sospecha de EC de ID, aunque se trata de series cortas. En nuestra serie, en el grupo de pacientes cuya indicación era sospecha de EII se han observado lesiones de tipo inflamatorio en menos de la mitad de los casos. La CE ha mostrado ser una herramienta excelente a la hora de descartar EC de ID, con un alto valor predictivo negativo53, lo cual pone de manifiesto que un estudio negativo puede tener un gran impacto en el manejo del paciente, pero el hecho de que sea una técnica costosa y consumidora de recursos38 nos obliga a realizar una mejor selección de los pacientes.
Aunque las indicaciones más importantes de la CE son la HDOO y la EII, esta modalidad diagnóstica también ha mostrado utilidad en casos de enfermedad celiaca de difícil diagnóstico o refractaria, tumores, seguimiento de poliposis de ID, dolor abdominal, etc.54–57. En la actualización más reciente de la guía europea para el diagnóstico de enfermedad de ID con CE y enteroscopia58 se acepta el uso de la CE para el manejo de pacientes con sospecha de enfermedad celiaca que rechacen o presenten contraindicaciones para los estudios endoscópicos convencionales, o en casos de enfermedad celiaca refractaria, pero no para el diagnóstico de esta enfermedad de forma rutinaria. Esta guía sí recomienda el uso de la CE en el seguimiento de pacientes con síndromes polipósicos y en el de aquellos con sospecha de presentar un tumor de ID. No se emite ninguna recomendación sobre la posible utilidad de la CE en casos de dolor abdominal inespecífico, aunque en algunas series se ha indicado que el rendimiento diagnóstico en este caso es aproximadamente del 21%59. En nuestra serie el número de estudios realizados por estas indicaciones es muy bajo (n=92), y los hallazgos son heterogéneos. La indicación más frecuente, y en la que hemos obtenido un menor número de diagnósticos que la justifiquen, es el dolor abdominal crónico inespecífico. Por el contrario, la situación en la que hemos observado un mayor número de estudios con diagnóstico directamente relacionado con la indicación es la sospecha de enfermedad celiaca refractaria o complicada.
Las tasas de complicaciones comunicadas en la literatura son excepcionalmente bajas. Estas, asociadas a los fallos técnicos y a las exploraciones incompletas, condicionan que en cierto número de estudios no se obtenga un diagnóstico60. La complicación más importante es la retención de la cápsula, bien a nivel gástrico o bien en el ID, generalmente en relación con estenosis por EC. La retención de la CE fue definida en la ICCE como la permanencia en el tracto digestivo durante más de 2 semanas61 y suele ser asintomática, ya que es excepcional que el dispositivo se impacte y provoque un cuadro obstructivo brusco: por lo general, responde a tratamiento médico o conservador, y son pocos los casos que requieren extracción de la cápsula mediante enteroscopia o tratamiento quirúrgico60,61. En nuestra serie hemos observado un número muy limitado de complicaciones: de 9 casos de no progresión de la CE (4 casos en que la batería de la cápsula se agotó antes de abandonar la cavidad gástrica y 5 retenciones en ID) solo 2 pacientes requirieron cirugía y en ambos casos se trató de una intervención electiva para tratamiento de estenosis refractarias a tratamiento médico y la retención de la cápsula no condicionó en ningún caso el momento de la cirugía.
Aunque ha sido objeto de discusión, en la actualidad no se considera que ser portador de un marcapasos o un desfibrilador sea una contraindicación para un estudio de CE62. En nuestra serie se ha administrado la CE a multitud de pacientes portadores de dispositivos cardiacos, sin que se haya observado mal funcionamiento de estos en ningún caso. Sí se ha podido comprobar la interferencia de los sistemas de telemetría de nuestro centro con la transmisión de imágenes de la CE al registrador, con múltiples «gaps» en los vídeos de la práctica totalidad de estos pacientes. Por ello, nuestra norma es evitar administrar la CE a enfermos hospitalizados en el área de Cardiología o en la Unidad de Cuidados Intensivos, y retrasar la exploración hasta que abandonan estas zonas, siempre que no se trate de una urgencia y sea posible.
Hemos recogido pacientes con edades comprendidas entre los 4 y los 91 años. La seguridad y utilidad de la técnica han sido puestas de manifiesto en múltiples estudios en el paciente anciano63,64. La evidencia es menor en la población pediátrica, pero también hay trabajos que confirman la seguridad del procedimiento y su alta capacidad diagnóstica65,66. Hemos incluido un total de 42 pacientes con 16 años o menos, entre los que hay 18 niños con 12 años o menos, sin que se haya registrado ninguna complicación en este grupo de edad.
ConclusionesLa endoscopia con videocápsula ha demostrado ser una técnica de gran utilidad para el diagnóstico de la enfermedad del ID, y se ha convertido en una herramienta muy extendida en el manejo del paciente con anemia crónica de origen digestivo y en la EII.
En los casos de HDOO, tanto oculta como manifiesta, la CE presenta un alto rendimiento diagnóstico, en buena medida gracias a que se han definido en la literatura aquellos factores que más se asocian a la presencia de lesiones en ID. No ocurre así en los casos de EII: se hace necesario en esta indicación una mejor definición de los factores clínicos y analíticos que más pueden aumentar la probabilidad de observar lesiones en los estudios de CE.
Fuera de la HDOO y la EII hay una serie variada de indicaciones en las que la CE puede ser útil, si bien su rendimiento es mucho menor, y es necesaria una cuidadosa selección de los pacientes en estos grupos para que puedan beneficiarse de este estudio.
Se trata, en general, de una técnica segura, con una tasa muy baja de complicaciones las cuales, además, suelen manejarse de forma conservadora: es excepcional la necesidad de tratamientos invasivos. Según nuestra experiencia la endoscopia con videocápsula es también segura en la edad pediátrica y en la senectud.
Nuestro trabajo presenta la limitación de tratarse de un estudio retrospectivo y de un solo centro. Por otra parte, aunque el número final de casos incluidos es grande, ha sido necesario excluir un número también elevado de pacientes del análisis por falta de información, en su mayoría estudios de CE de pacientes muy antiguos o derivados de hospitales periféricos, en los que ha resultado imposible acceder a los datos, situación que supone una limitación añadida.
Conflicto de interesesLos autores declaran que no existen conflictos de interés.