La extracción de muestras sanguíneas a través de un catéter venoso central es una práctica habitual en las unidades de cuidados intensivos. Está indicado desechar un volumen de sangre, denominado volumen de descarte, con la finalidad de evitar que los resultados puedan verse alterados.
ObjetivoDeterminar si un menor volumen de descarte para la obtención de analíticas procedentes de catéter venoso central temporales alojados en la vena yugular interna, femoral o subclavia ofrece resultados válidos.
MétodoEstudio cuasiexperimental, prospectivo, transversal donde se seleccionaron 65 pacientes críticos mayores de 18 años portadores de catéter venoso central temporal de 3 luces durante un período de 8 meses. Para cada paciente se extrajeron 2 analíticas consecutivas de la luz distal con los valores de hemograma, bioquímica y coagulación comúnmente analizados en el paciente crítico. Se obtuvieron 2 muestras consecutivas: la primera, con un descarte de 1,5ml y un volumen extraído total de 10,2ml, similar al desecho habitual en nuestro medio (10 ml). Seguidamente se obtuvo la segunda muestra. Para el análisis de datos se utilizó la prueba t pareada; para medir la concordancia entre métodos, la representación de Bland-Altman y el coeficiente de correlación intraclase. Se estableció el valor de referencia del cambio como límite admisible de variación entre los pares de muestras.
ResultadosSe extrajeron un total de 65 pares de muestras (intervención-control). El contraste de medias encontró diferencias estadísticamente significativas con α=0,05 para cloro (−0,536; 0,012), tiempo de protrombina (−0,092; 0,019) y actividad de protrombina (0,284; 1,375). El coeficiente de correlación intraclase resultó mayor de 0,9 en todas las variables y el valor de referencia del cambio no fue superado por ningún valor.
ConclusionesLos resultados muestran la validez de los análisis de las muestras de sangre extraídas con un volumen de descarte de 1,5ml.
Drawing blood samples through a central venous catheter is a customary practice in intensive care units. It is indicated to discard a volume of waste blood to avoid interference in the results.
AimTo determine whether a lower discard volume for obtaining blood samples from temporary central venous catheters placed into the internal jugular, femoral or subclavian vein offers valid results.
MethodA quasi-experimental prospective cross-sectional study for which 65 patients of over 18 years of age in intensive care units, who had been fitted with a triple lumen central venous catheter, were recruited over a period of 8 months. Two consecutive blood samples were extracted with tubes for biochemistry, coagulation and haemogram from each patient from the distal lumen. The first sample was obtained with a discarded waste of 1.5ml from a total extracted volume of 10.2ml, similar to the usual waste in our ambit (10ml). Subsequently the second sample was obtained. The paired t-test was used to analyse the data. The Bland-Altman plot and intraclass correlation coefficient were used to measure the agreement between methods. The reference change value was established as the admissible limit of variation between the pairs of samples.
ResultsA total of 65 sample pairs were drawn (intervention-control). The paired t-test found statistically significant differences with a significance level of α=0.05 for chlorine (−0.536; 0.012); prothrombin time (−0.092; 0.019) and prothrombin activity (0.284; 1.375). The intraclass correlation coefficient was greater than 0.9 in all the variables and the limit determined for the reference change value was not surpassed by any value.
ConclusionsThe results show the reliability of the blood samples drawn with a discard volume of 1.5ml.
Para la extracción de muestras sanguíneas a través de un catéter venoso central está indicado desechar un volumen de sangre, denominado volumen de descarte, con la finalidad de evitar que los resultados puedan verse alterados. Existe una amplia variabilidad del volumen desechado, que supera en la mayoría de los casos el volumen de purgado del catéter.
¿Qué aporta?Los resultados muestran la fiabilidad de los análisis de las muestras de sangre extraídas con un volumen de descarte de 1,5ml, lo que implica menores pérdidas de sangre.
Se introduce el valor de referencia del cambio como límite admisible de variación entre pares de muestras y el cribado sistemático de las diferencias entre los resultados consecutivos para el mismo paciente y la misma prueba.
Implicaciones del estudioLos resultados obtenidos ofrecen una base para la elaboración de protocolos dirigidos a minimizar la anemia iatrogénica y las complicaciones asociadas, que es uno de los principales problemas en las unidades de cuidados críticos.
Una de las principales complicaciones del paciente crítico es la anemia adquirida intrahospitalaria (AAI)1, que supone un aumento de la estancia en el área de críticos y en el hospital, así como de la mortalidad. La etiología de la AAI es compleja y puede incluir pérdida de sangre y acortamiento de la vida útil, y disminución en la producción de glóbulos rojos2. Entre las estrategias potencialmente modificables en la AAI se incluye minimizar el volumen de descarte en las analíticas2,3.
Los programas Patient Blood Management (PBM) comprenden una serie de recomendaciones para minimizar los riesgos directos e indirectos asociados a la transfusión sanguínea. La revisión de la literatura confirma que no debe ser la opción predeterminada para controlar la anemia o la pérdida de sangre. En cambio, la acumulación de evidencia demuestra que un enfoque proactivo y centrado en el paciente para manejar la propia sangre debería ser el nuevo estándar de atención4. Además de una política de transfusión restrictiva, el programa de PBM en las unidades de cuidados intensivos (UCI) incluye otras medidas, entre las que se encuentra la reducción en la pérdida de sangre5.
Uno de los motivos de estas pérdidas de sangre es la multitud de determinaciones sanguíneas a las que está sometido, ya que se trata de una herramienta básica para el diagnóstico y la optimización de su tratamiento. Comúnmente estas determinaciones son extraídas de un catéter venoso central (CVC).
Los CVC son dispositivos alojados en el espacio intravascular central que aseguran un acceso venoso seguro y que, además de ser útiles para la extracción de muestras, permiten la infusión de medicación, permitiendo varias perfusiones de forma simultánea, monitorización hemodinámica, plasmaféresis o hemodiálisis. En la UCI la presencia de vías centrales de varias luces hace más fácil el procedimiento de extracción de sangre sin necesidad de punciones venosas6, lo que supone un aumento en el bienestar del paciente.
A la hora de extraer una muestra sanguínea, el procedimiento más comúnmente utilizado en las UCI de adultos es el método de descarte7, que consiste en desechar una cantidad de sangre previa a la toma de muestra. El volumen desechado no es despreciable y se estima en un 28,5-33,1% del volumen total extraído7, siendo la cantidad media de sangre desechada en el paciente crítico en las primeras 24h de ingreso de 31,61ml8. El volumen medio de sangre descartado por extracción es de 10,3ml, lo que representaría un total de media de 41,1ml al día9. Específicamente en pacientes críticos portadores de CVC, la cantidad media de volumen de descarte es 5,5ml3.
La bibliografía recoge diferencias en el volumen desechado utilizado para la toma de muestras. Podemos observar que hay trabajos que recomiendan o utilizan volúmenes mayores10–12, si bien es cierto que en la línea del ahorro de sangre han surgido nuevas vías que proponen utilizar volúmenes inferiores, consiguiendo buenos resultados13–18. Por otro lado, también se señala que si hay perfusión de heparina sódica, este volumen de descarte debería ser mayor, sin alcanzar un consenso acerca del mismo19. En cuanto a la técnica, se han encontrado estudios en donde se lavaba previamente la vía con suero salino fisiológico al 0,9%11,15,16 y otros donde no se especifica13,20. En resumen, existe una gran variabilidad en el volumen de sangre desechado en función del centro donde se realiza la extracción y la recomendación de utilizar técnicas de extracción más conservadoras21.
El objetivo general de este trabajo fue determinar si un menor volumen de descarte para la obtención de analíticas procedentes de CVC temporales alojados en la vena yugular interna, femoral o subclavia ofrece resultados válidos.
MetodologíaDiseñoEstudio cuasiexperimental, prospectivo y transversal.
Ámbito y período de estudioUCI de quemados y UCI general del Hospital Universitario La Paz, de abril a noviembre de 2019.
ParticipantesSe seleccionó a los pacientes ingresados en estas unidades portadores de CVC temporal de 3 luces alojados en vena yugular interna, vena subclavia o vena femoral. No formaron parte del estudio los pacientes que cumplieran al menos uno de los criterios de exclusión: menores de 18 años, en tratamiento con perfusión continua de heparina y/o pacientes con hemoglobina<7g/dl.
MuestraSe realizó un muestreo por conveniencia entre los pacientes candidatos ingresados en las unidades donde desarrollan su actividad profesional los responsables de la toma de muestras. Se llevó a cabo en 2 fases: una inicial, donde se realizó un estudio piloto para ajustar el consumo de recursos en caso de no existir concordancia entre métodos, y una fase de continuación, en la cual se aumentó el tamaño muestral para la realización del estudio principal. Para fijar el número de participantes en cada fase se calculó el mínimo tamaño de la muestra para la estimación del coeficiente de correlación intraclase (CCI) de los resultados obtenidos por 2 métodos22 mediante el programa Power Analysis and Simple Size, donde la significación y la mínima potencia requerida quedaron definidas en 0,05 y más alta que 0,8, respectivamente. El objetivo fue determinar un nivel de concordancia alto entre los 2 métodos, por lo que se fijó ρ0=0,75 y ρ1=0,9 para el estudio piloto y ρ0=0,9 y ρ1=0,95 para el estudio principal, con tamaños muestrales mínimos calculados de 25 y 50 pacientes, respectivamente. Fue necesario incrementar el tamaño requerido en un 10 y un 30%, respectivamente, para asegurar se alcanzase el mínimo necesario en todas las variables incorporadas al estudio, ya que no siempre la orden de analítica los incluía.
VariablesSe utilizaron los parámetros sanguíneos comúnmente analizados de forma diaria a los pacientes ingresados en las unidades donde se desarrolló el estudio, dentro de las categorías de hemograma: hematíes, hemoglobina, hematocrito, plaquetas y leucocitos; bioquímica general: glucosa, creatinina, urea, sodio, potasio y cloro; coagulación: tiempo de protrombina, actividad de protrombina, international normalized ratio, tiempo de cefalina y ratio del tiempo de cefalina.
MétodoLas muestras fueron obtenidas por 5 enfermeras: 2 pertenecientes a la UCI de quemados y 3 a la UCI general. Se realizaron 2 analíticas consecutivas con tubos de bioquímica, coagulación y hemograma, de 3; 2,7 y 3ml, respectivamente, que fueron llenados en ese orden siguiendo los protocolos internos del hospital. La obtención de la primera muestra (intervención) se obtuvo mediante el método explicado por Moureau15 para la obtención de muestras utilizando un CVC. El volumen de cebado de la luz distal del CVC de 3 luces utilizado fue 0,44ml y el triple del espacio muerto correspondió a 1,32ml, que fue definido como 1,5ml para simplificar el método. El manejo fue aséptico, siguiendo todas las recomendaciones del Proyecto Bacteriemia Zero23.
Primero se pararon las perfusiones en curso de la luz distal del catéter sin interrumpir las perfusiones de la luz medial y proximal. A continuación, se administraron 10ml de suero salino al 0,9% con una jeringa de 10ml a través de la conexión de la luz distal para eliminar posibles restos de medicación que pudiese alterar las mediciones. Posteriormente se obtuvieron las 2 muestras de forma consecutiva. El volumen para la muestra intervención fue de 1,5ml de descarte más 8,7ml de la muestra sanguínea a analizar, con un total de volumen desechado de 10,2ml. Este volumen fue similar al que generalmente se descarta (10ml), asegurando no extraer un volumen mayor para la realización del estudio. Una vez obtenida una única muestra intervención y una única muestra control, la participación del sujeto se dio por terminada. Las muestras fueron enviadas al laboratorio de urgencias del hospital mediante los medios habituales y procesadas inmediatamente para evitar sesgos en los resultados por variables de tiempo y temperatura.
Análisis de datosSe efectuó mediante la prueba t pareada, a excepción de las variables tiempo de protrombina, actividad de protrombina e international normalized ratio, donde se aplicó el test de los rangos de Wilcoxon, ya que las muestras obtenidas no seguían una distribución normal. Para el contraste de medias fue necesario definir la variable diferencias (d=intervención-control), así como su media (ׯd) y desviación estándar. El nivel de significación estadística empleado fue α=0,05. La representación de Bland-Altman24 y el CCI25 se utilizaron como medidas del acuerdo o reproducibilidad entre los 2 métodos. Si el CCI es inferior a 0,4, se hablará de un pobre acuerdo; si está por encima de 0,75, será excelente. En caso de estar entre ambos, se considerará bueno (moderado). Para la representación gráfica los límites de concordancia al 95% fueron definidos como ׯd±1,96 desviaciones estándar. El valor de referencia del cambio (VRC) marcó el límite admisible de variación entre los pares de muestras. Se trata de una herramienta estadística que combina el error analítico (coeficiente de variación analítico [CVA]) y la variación biológica intraindividuo (coeficiente de variación biológica individual [CVI])26. Si las diferencias de la muestra control con la muestra intervención exceden el cambio explicable por el CVI y el CVA, se puede atribuir a un cambio en el estado de salud del paciente27 y las 2 muestras no podrían ser consideradas iguales. Para su cálculo se tomaron los valores de 1,96 o 2,58 (z) para un nivel de significación del 95% (VRC95%) o del 99% (VRC99%), respectivamente; el CVI26 y el CVA suministrados por el laboratorio para cada parámetro. La formulación para su cálculo fue la siguiente: VRC=2z(CVI2+CVA2)1/228,29.
El programa estadístico utilizado fue R versión 3.6.1 (última actualización 5-07-2017).
Aspectos éticosEl estudio fue aprobado por el Comité de Ética e Investigación con medicamentos del Instituto de Investigación Hospital Universitario La Paz. No fue necesario recoger consentimiento informado dadas las características y el objetivo pragmático del estudio de acuerdo con el informe de evaluación emitido por el citado comité (PI-3596). Los datos fueron tratados de forma confidencial según la Ley Orgánica 15/1999 de Protección de Datos.
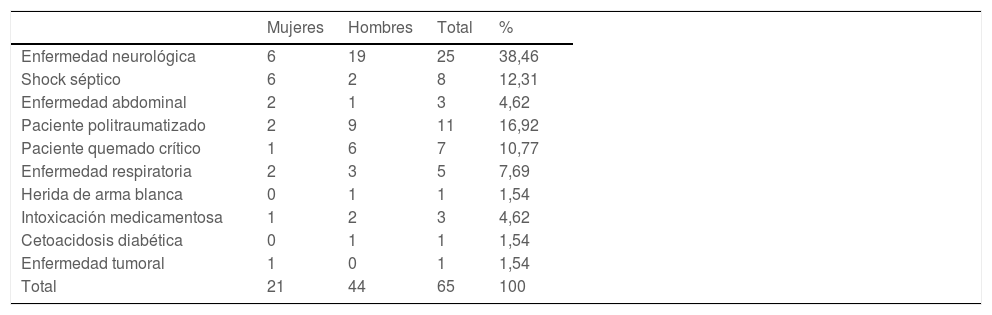
ResultadosLa muestra final estuvo formada por 65 pacientes. El 66,15% fueron hombres y el 33,85% mujeres, con un promedio de edad de 56,92 años en el rango de 18 a 82 años, con múltiples cuadros clínicos que precisaron atención en una unidad de pacientes críticos y con predominio de enfermedad neurológica (tabla 1).
Características sociodemográficas de la muestra
| Mujeres | Hombres | Total | % | |
|---|---|---|---|---|
| Enfermedad neurológica | 6 | 19 | 25 | 38,46 |
| Shock séptico | 6 | 2 | 8 | 12,31 |
| Enfermedad abdominal | 2 | 1 | 3 | 4,62 |
| Paciente politraumatizado | 2 | 9 | 11 | 16,92 |
| Paciente quemado crítico | 1 | 6 | 7 | 10,77 |
| Enfermedad respiratoria | 2 | 3 | 5 | 7,69 |
| Herida de arma blanca | 0 | 1 | 1 | 1,54 |
| Intoxicación medicamentosa | 1 | 2 | 3 | 4,62 |
| Cetoacidosis diabética | 0 | 1 | 1 | 1,54 |
| Enfermedad tumoral | 1 | 0 | 1 | 1,54 |
| Total | 21 | 44 | 65 | 100 |
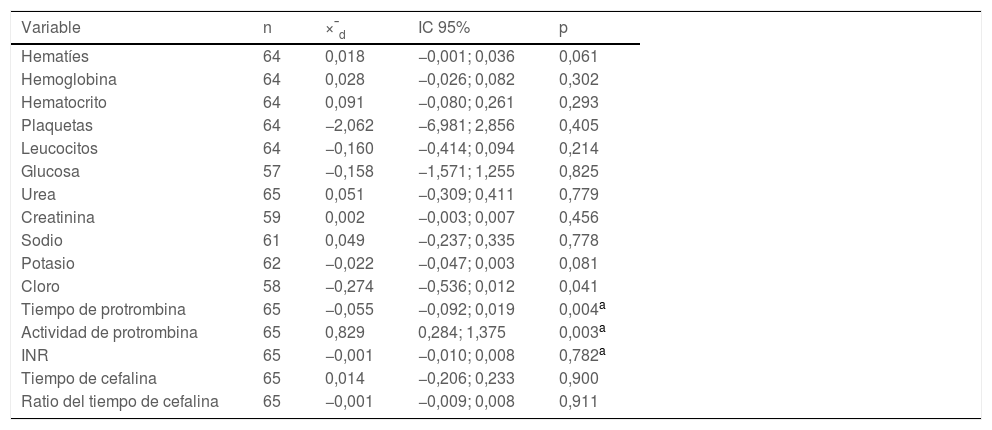
El contraste de medias (tabla 2) no encontró diferencias entre ambos métodos a excepción de las variables cloro (p=0,041), tiempo de protrombina (p=0,004) y actividad de protrombina (p=0,003). La media de las diferencias para estos parámetros fue pequeña y cercana a cero, con intervalos de confianza de poca amplitud: cloro (−0,536; 0,012); tiempo de protrombina (−0,092; 0,019) y actividad de protrombina (0,284; 1,375) (tabla 2), por lo que las diferencias encontradas no representaron ninguna implicación clínica.
Resultados de la comparación de medias de ambas muestras
| Variable | n | ׯd | IC 95% | p |
|---|---|---|---|---|
| Hematíes | 64 | 0,018 | −0,001; 0,036 | 0,061 |
| Hemoglobina | 64 | 0,028 | −0,026; 0,082 | 0,302 |
| Hematocrito | 64 | 0,091 | −0,080; 0,261 | 0,293 |
| Plaquetas | 64 | −2,062 | −6,981; 2,856 | 0,405 |
| Leucocitos | 64 | −0,160 | −0,414; 0,094 | 0,214 |
| Glucosa | 57 | −0,158 | −1,571; 1,255 | 0,825 |
| Urea | 65 | 0,051 | −0,309; 0,411 | 0,779 |
| Creatinina | 59 | 0,002 | −0,003; 0,007 | 0,456 |
| Sodio | 61 | 0,049 | −0,237; 0,335 | 0,778 |
| Potasio | 62 | −0,022 | −0,047; 0,003 | 0,081 |
| Cloro | 58 | −0,274 | −0,536; 0,012 | 0,041 |
| Tiempo de protrombina | 65 | −0,055 | −0,092; 0,019 | 0,004a |
| Actividad de protrombina | 65 | 0,829 | 0,284; 1,375 | 0,003a |
| INR | 65 | −0,001 | −0,010; 0,008 | 0,782a |
| Tiempo de cefalina | 65 | 0,014 | −0,206; 0,233 | 0,900 |
| Ratio del tiempo de cefalina | 65 | −0,001 | −0,009; 0,008 | 0,911 |
IC 95%: intervalo de confianza al 95% para la media de las diferencias; INR: international normalized ratio; ׯd: media de las diferencias de los valores obtenidos por cada método.
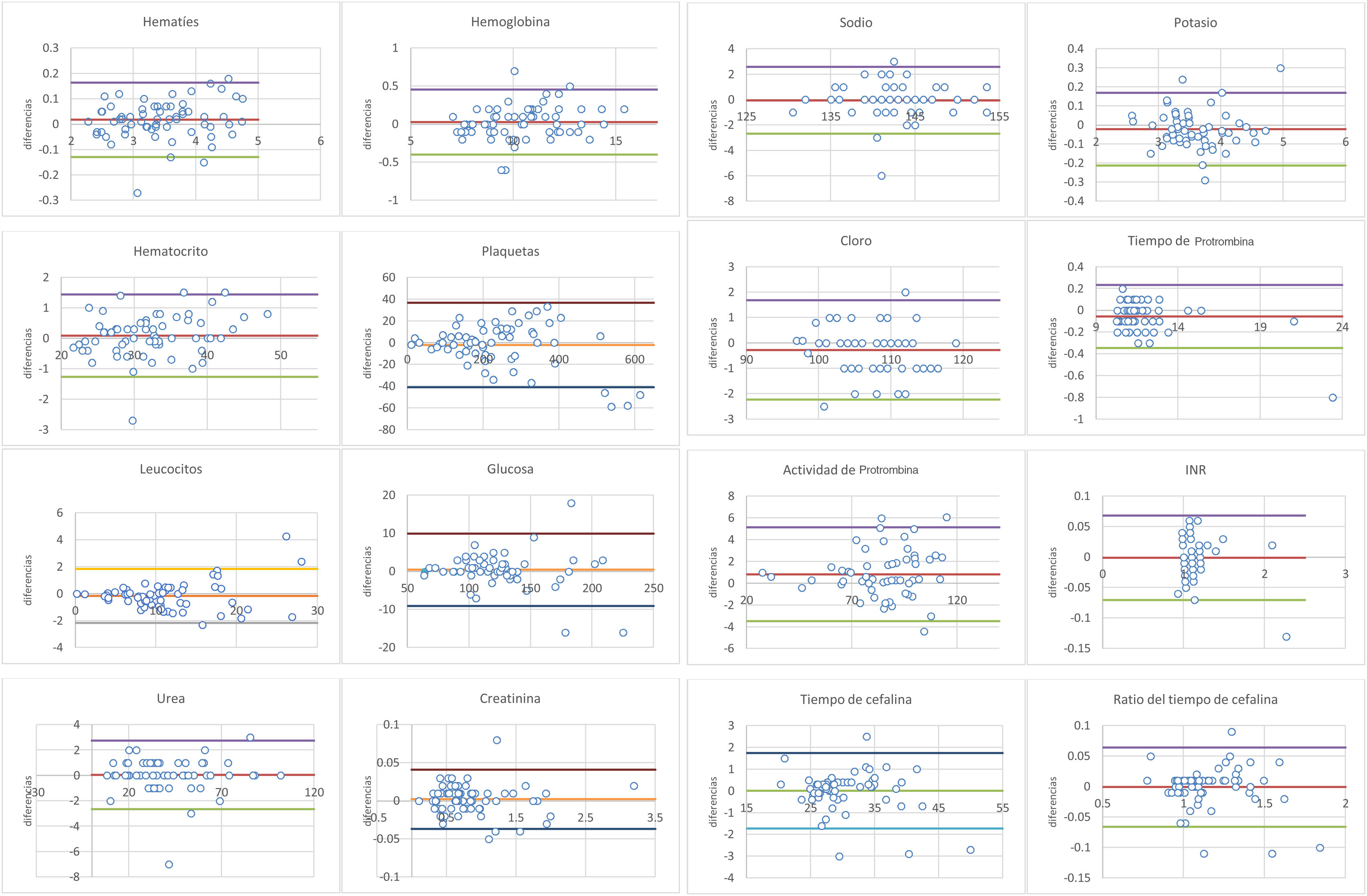
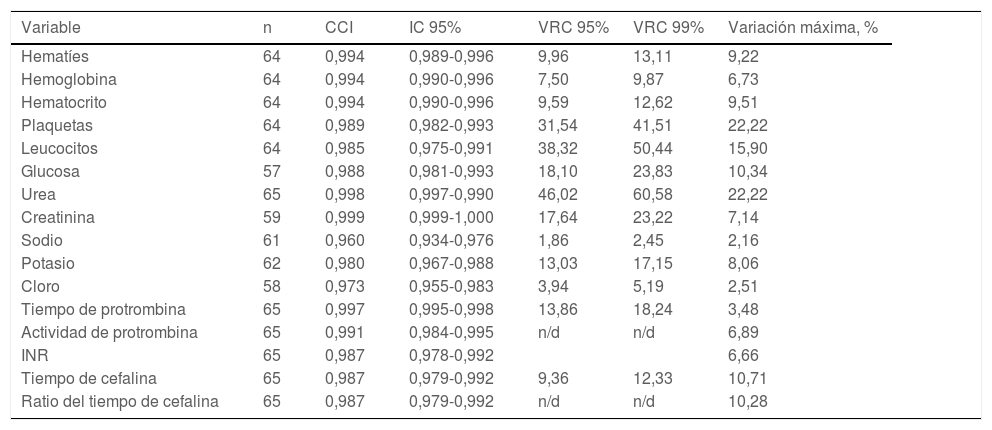
En las medidas de concordancia, el CCI calculado (tabla 3) fue siempre mayor de 0,9, lo cual indicó una fiabilidad excelente entre los 2 métodos. Los márgenes definidos por los límites superior e inferior en los gráficos de Bland-Altman y las diferencias de valores obtenidos por el método de descarte de 1,5ml frente al estándar no representaron significación clínica (fig. 1).
Coeficiente de correlación intraclase y valor de referencia del cambio
| Variable | n | CCI | IC 95% | VRC 95% | VRC 99% | Variación máxima, % |
|---|---|---|---|---|---|---|
| Hematíes | 64 | 0,994 | 0,989-0,996 | 9,96 | 13,11 | 9,22 |
| Hemoglobina | 64 | 0,994 | 0,990-0,996 | 7,50 | 9,87 | 6,73 |
| Hematocrito | 64 | 0,994 | 0,990-0,996 | 9,59 | 12,62 | 9,51 |
| Plaquetas | 64 | 0,989 | 0,982-0,993 | 31,54 | 41,51 | 22,22 |
| Leucocitos | 64 | 0,985 | 0,975-0,991 | 38,32 | 50,44 | 15,90 |
| Glucosa | 57 | 0,988 | 0,981-0,993 | 18,10 | 23,83 | 10,34 |
| Urea | 65 | 0,998 | 0,997-0,990 | 46,02 | 60,58 | 22,22 |
| Creatinina | 59 | 0,999 | 0,999-1,000 | 17,64 | 23,22 | 7,14 |
| Sodio | 61 | 0,960 | 0,934-0,976 | 1,86 | 2,45 | 2,16 |
| Potasio | 62 | 0,980 | 0,967-0,988 | 13,03 | 17,15 | 8,06 |
| Cloro | 58 | 0,973 | 0,955-0,983 | 3,94 | 5,19 | 2,51 |
| Tiempo de protrombina | 65 | 0,997 | 0,995-0,998 | 13,86 | 18,24 | 3,48 |
| Actividad de protrombina | 65 | 0,991 | 0,984-0,995 | n/d | n/d | 6,89 |
| INR | 65 | 0,987 | 0,978-0,992 | 6,66 | ||
| Tiempo de cefalina | 65 | 0,987 | 0,979-0,992 | 9,36 | 12,33 | 10,71 |
| Ratio del tiempo de cefalina | 65 | 0,987 | 0,979-0,992 | n/d | n/d | 10,28 |
CCI: coeficiente de correlación intraclase; IC 95%: intervalo de confianza al 95%; INR: international normalized ratio; VRC 95%: valor de referencia del cambio con significación del 95%; VRC 99%: valor de referencia del cambio con significación del 99%; n/d: valores de la variación biológica intraindividuo para el cálculo del VRC no disponibles en European Federation of Clinical Chemistry and Laboratory Medicine26.
Gráficos de Bland-Altman: el gráfico permite evaluar la magnitud del desacuerdo entre ambos métodos o identificar valores atípicos o periféricos. Las líneas superior e inferior representan la concordancia estadística para las diferencias entre las muestras control e intervención con un intervalo de confianza del 95% (ׯd±1,96 desviaciones estándar).
No hubo ningún resultado con una variación mayor al límite fijado por el VRC95% excepto el sodio (VRC95%=1,86% frente al valor con mayor variación de la muestra de 2,16%) y el tiempo de cefalina (VRC95%=9,36 frente a 10,71%). Ambos parámetros se encontraron dentro de rango de aceptación con VRC 99% (2,45 y 12,33%, respectivamente) (tabla 3).
DiscusiónEl principal hallazgo de este trabajo ha sido la posibilidad de obtener analíticas de los CVC temporales usados en nuestras unidades válidas para su uso habitual con un volumen de desecho de 1,5ml. Este resultado representa, en términos absolutos, una mejora respecto al ahorro de sangre por extracción si lo comparamos con el volumen propuesto por otros autores (5ml20, 3ml11,30, 2ml16); aunque, si bien se constata la reducción en el volumen de descarte, sería más útil establecer esta comparación en términos relativos definiendo para ello la relación entre el volumen de descarte y el volumen de purgado de la luz utilizada para la extracción, y de este modo averiguar si el volumen desechado es mayor o menor debido a las diferencias en el tamaño del CVC usado. En concreto, para el presente trabajo se utiliza la relación 3:1 (triple del volumen del espacio muerto) que Moureau15 define como la mínima cantidad que debería ser utilizada para la obtención de la muestra, y al igual que ocurre con la comparación en términos absolutos, se encontraron divergencias de cuántas veces el espacio muerto se debería desechar: 6:111 o 5:116, este último con desecho total de 2ml para un volumen de cebado de 0,39ml. No obstante, no siempre se menciona el volumen de purgado18,20,30, por lo que esta relación no se puede usar sistemáticamente para comprobar si hay disparidad entre distintos estudios. En cuanto al descarte de 10ml10, utilizado como control, hay que señalar que se trata de una práctica extendida entre los profesionales, con escaso respaldo bibliográfico y que aproximadamente representa una relación 23:1 para nuestro catéter (0,44ml de volumen de cebado frente a 10ml de desecho), muy superior a cualquier valor señalado anteriormente, por lo que está justificado trabajar en la línea de disminuir el volumen desechado de acuerdo con los objetivos propuestos en los programas PBM4.
Por otra parte, la comparación entre métodos de extracción atendiendo al volumen de descarte trata de responder a la pregunta de si los resultados cambian al aplicar una u otra técnica de extracción. Para revelar la respuesta, las herramientas de análisis estadístico deberían de acompañarse de alguna medida de la significación clínica. Dalton et al.19 señalan que la dicotomía entre significación estadística y significación clínica ya fue introducida por Mayo et al.31 en 1996 al encontrar diferencias estadísticamente significativas para distintas muestras de coagulación que se hallaban dentro de un rango normal. Para el contraste de medias los resultados varían en ambos sentidos, ya sea encontrando diferencias significativas (p<0,05) en todas las variables estudiadas16, o, por el contrario, no existiendo diferencias estadísticamente relevantes en ningún parámetro30 (p>0,05). En este trabajo coexisten los 2 escenarios descritos, con diferencias estadísticamente significativas para los parámetros de tiempo de protrombina, actividad de protrombina y cloro. Una de las razones para esta dualidad podría apoyarse en los reducidos tamaños muestrales19,20. La medida de la concordancia o reproducibilidad de ambos métodos brinda una realidad más homogénea con valores que indican fiabilidad excelente (CCI>0,75)16,30, lo que apoya los resultados de este trabajo con cifras para el CCI superiores a 0,9 en todas las variables (tabla 3).
Por último, si atendemos a la representación de Bland-Altman (fig. 1), los resultados periféricos o atípicos, es decir, los mayores o menores a los límites de concordancia al 95%, carecieron de relevancia médica16,30. Sin embargo, se hizo fundamental definir este concepto a priori para fijar los intervalos de aceptación clínica (IAC) y así poder utilizar el volumen de desecho propuesto de forma inequívoca. La manera de abordar este problema ha sido bastante empírica y generalmente se ha realizado de acuerdo con el consenso del personal experto16,30,32 implicado en el cuidado del paciente. Otra solución propuesta, utilizada por Wyant y Crickman12, es evaluar si el tratamiento a aplicar hubiese sido diferente en caso de usar los valores de la analítica control o los correspondientes a la muestra intervención, al estimar la cantidad de unidades de insulina administradas según el valor de glucosa obtenido por uno u otro método. Con todo lo anterior, ambas soluciones se enfrentan al inconveniente de la complejidad de generalizar los IAC, ya que los consensos sobre los valores a establecer pueden variar entre los distintos expertos; véanse como ejemplo los IAC establecidos por Villalta García et al.16 para el potasio (−1,01-1,03) y el sodio (−4,12-6,5), frente a los fijados por Lalthanthuami et al.30: ±0,4 y ±4, respectivamente. De igual forma, los protocolos establecidos para la administración de distintos fármacos pueden ser distintos entre diferentes centros.
Como un intento de dotar de objetividad a los límites que definan la relevancia médica de las diferencias se introduce el VRC, que al tratarse de una herramienta estadística carece de implicaciones subjetivas en la interpretación de los cambios32. Otra ventaja añadida del VRC, al estar expresado en porcentaje, es que los rangos de aceptación quedan individualizados para cada valor y, por consiguiente, es capaz de detectar alteraciones en valores pequeños de la muestra intervención que estarían en rango de aceptación si fuesen definidos de forma estática16,30. En particular y para establecer comparaciones con los estudios de Villalta García et al.16 y Lalthanthuami et al.30, en el presente trabajo se aceptaron diferencias para el mayor valor de sodio de la muestra (150mEq/l) de±2,85 y±3,75 según se aplique VRC95% o VRC99%. De igual forma, para el menor valor de sodio (131mEq/l) los IAC quedaron definidos en±2,49 (VRC95%) y±3,28 (VRC99%). En el caso del potasio, los límites fluctuaron entre±0,62 y±0,33 para el VRC95%, y entre±0,82 y±0,44 para el VRC 99%. La importancia de los IAC se apoya en la necesidad de cuantificar y acotar la afirmación de si existe o no significación clínica de los resultados obtenidos; no obstante, no siempre se mencionan de forma explícita11,13 o únicamente para alguna de las variables a estudio16,30, razón por la cual, aunque quede señalado que los resultados no tienen relevancia clínica, se complica establecer relaciones entre los límites de variación aceptados entre los diferentes estudios.
Dada la relevancia de la AAI y su mayor repercusión en el paciente crítico, la aplicación práctica de la disminución del volumen desechado en la toma de muestras podría contribuir a minimizar la anemia iatrogénica del paciente promoviendo el ahorro de sangre y así disminuir la necesidad de transfusiones, reduciendo las complicaciones posteriores.
Las limitaciones encontradas subyacen en el carácter monocéntrico del estudio, el cual se limita a un solo tipo de catéter cuyas características (marca, material, tamaño, volumen de purgado, etc.) pueden variar de una institución a otra, al igual que el procesamiento de las muestras y las máquinas necesarias para su análisis. Además, se trabaja sobre unas variables concretas de hemograma, bioquímica y coagulación que, aunque básicas en todo estudio de rutina, excluyen el amplio abanico de determinaciones de laboratorio. Tampoco se conoce en qué grado afectaría la infusión de heparina a través del catéter en el volumen de desecho, al tratarse de un criterio de exclusión. El uso de técnicas de muestreo no probabilístico (muestreo de conveniencia) podría introducir sesgos que no permitan la generalización de resultados, debido a que podría darse el caso de que la muestra no sea representativa de la población a estudio.
A partir de los resultados obtenidos surgen nuevos interrogantes para su investigación en un futuro, como la aplicabilidad del método a otros tipos de catéteres (arteriales, PICC, tunelizados y/o centrales de reservorio subcutáneo implantado) y la extensión a otros parámetros analíticos.
ConclusiónLos resultados muestran que es factible conseguir valores válidos de las muestras de sangre extraídas con un volumen de descarte de 1,5ml para su uso clínico y constituye una práctica a incluir en los programas PBM, ya que permite reducir las pérdidas sanguíneas en nuestros pacientes.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesNinguno.
A todos los pacientes que han participado en el estudio.
A Esther Presa Vázquez, Elena Fernández Saiz y Manuel Prieto Zurera, enfermeros de la Unidad de Cuidados Intensivos, por su implicación y colaboración en la recolección de muestras.
Al personal del Laboratorio de Urgencias del Hospital Universitario La Paz.