Los catéteres centrales de inserción periférica se han convertido en una prioridad en los neonatos que necesitan terapia intravenosa de larga duración, pero su uso no está exento de riesgos.
ObjetivoDescribir la aparición de eventos adversos en neonatos portadores de catéteres venosos centrales de inserción periférica y determinar factores de riesgo asociados a ellos.
MétodosSe llevó a cabo un estudio descriptivo transversal en el que se incluyeron la totalidad de neonatos portadores de catéteres venosos centrales de inserción periférica desde el 1 de octubre de 2014 hasta el 30 de septiembre de 2015. Se registraron los eventos adversos y variables sociodemográficas y clínicas relacionadas con los neonatos y los catéteres analizados.
ResultadosSe incluyeron en el estudio un total de 116 neonatos y 140 catéteres. Se registraron eventos adversos en el 16,4% de ellos: bacteriemia asociada al catéter (5,7%), obstrucción (5,7%), extravasación (2,1%) y flebitis (2,1%). Los factores asociados a bacteriemia con el odds de prevalencia corresponde a neonatos: <27semanas de gestación (OR=1,2; p=0,02), con peso <1.000g (OR=6,7; p=0,02), portadores de catéter >1semana (OR=9,8; p=0,02) y con perfusión de antibióticos por catéter (OR=1,3; p<0,01). La flebitis se asocia con la inserción del catéter en miembros inferiores y cabeza (OR=1,1; p=0,03). Los factores asociados a bacteriemia con odds de prevalencia ajustada corresponde a neonatos de peso extremo (OR=6,38; p=0,03) y portadores del catéter >7días (OR=9,41; p=0,04).
ConclusionesLa evaluación periódica de eventos adversos relacionados con catéteres es de gran utilidad para elaborar planes de mejora. Esto permitirá extremar la seguridad en los RN más vulnerables, en especial los neonatos con extremo bajo peso que precisan tratamientos muy prolongados.
Peripherally inserted central catheters have become a priority in infants who require long-term intravenous therapy, but their use involves certain risks.
ObjectiveThe aim of the study was to describe the occurrence of adverse events in newborns with peripherally inserted central catheters and to determine the risk factors associated with them.
MethodsA descriptive cross-sectional study was designed and performed. All neonates with peripherally inserted central catheters from October 1st, 2014 to September 30th, 2015 were included. The adverse events and sociodemographic and clinical variables related to neonates and analyzed catheters were recorded.
ResultsA total of 140 catheters were placed in 116 infants. All of them were analyzed. Adverse events occurred in 16.4%: catheter-associated bacteraemia (5.7%), obstruction (5.7%), extravasation (2.1%) and phlebitis (2.1%), <27weeks of pregnancy (OR=1.2, P=.02), birth weight <1000g (OR=6.7, P=.02), with catheters in situ for longer than one week (OR=9.8, P=.02) and with perfusion of antibiotics per catheter (OR=1.3, P<.01). Phlebitis is associated with the insertion of the catheter in LL and head (OR=1.1, P=.03). Factors associated with bacteraemia risk with adjusted prevalence odds ratio are extremely low birth weight neonates (OR=6.38; P=.03) and with a catheter in situ for longer than one week (OR=9.41; P=.04).
ConclusionsThe periodic evaluation of catheter-related adverse events is very useful to prepare improvement plans. This will maximize safety for the most vulnerable newborns, especially those of extremely low birth weight that require very long treatments.
El catéter central de inserción periférica (CCIP), denominado en inglés peripherally inserted central catheter (PICC), es el acceso vascular de primera elección en el recién nacido (RN) que necesita terapia intravenosa de larga duración. Se trata de una técnica segura y eficaz para la administración prolongada de soluciones intravenosas en vasos de mayor calibre y causa menos fenómenos inflamatorios irritativos en el endotelio vascular. Aun así, esta técnica no está exenta de riesgos, y el principal problema son las infecciones o bacteriemias asociadas al mismo, además de otras complicaciones de tipo mecánico, como obstrucción, extravasación, rotura del catéter y extracción no electiva.
La enfermera juega un papel fundamental al ser el responsable de la inserción, mantenimiento y prevención de eventos adversos asociados a estos catéteres. La seguridad de los neonatos hospitalizados es un reto para los profesionales que los cuidan. La cultura de seguridad permite conocer, a través de evaluaciones periódicas, el estado y la evolución de eventos adversos relacionados con la práctica clínica y las percepciones de los profesionales frente a estos.
Qué aportaLos resultados de este estudio, llevado a cabo en una unidad de cuidados intensivos neonatales en un hospital general de tercer nivel, aportan datos para la prevención de eventos adversos relacionados con los CCIP en neonatos con extremo bajo peso y con permanencia del catéter superior a una semana.
Implicaciones para la práctica enfermeraLos datos obtenidos aportan información relevante para todas las enfermeras que desarrollan su práctica clínica en unidades de cuidados intensivos neonatales. Además, dichos hallazgos son comparables y coinciden en líneas generales con otros estudios. Los resultados resaltan la vulnerabilidad ante los eventos adversos asociados a catéteres, concretamente la bacteriemia, en los neonatos de muy bajo peso para la edad gestacional y con permanencia de catéteres mayor a una semana. Esta información es fundamental para que las enfermeras establezcan e incidan en medidas extremas de asepsia en el manejo clínico-asistencial de estos niños. El uso de protocolos específicos, como el de «Bacteriemia Cero», aumenta la seguridad clínica y disminuye la morbilidad de los neonatos.
Desde el punto de vista sanitario, el término «pediatría» se aplica a niños con edades inferiores a los 18años. Según la Organización Mundial de la Salud (OMS), este amplio periodo se divide en: recién nacidos (RN) o neonatos (de 0 a 28días), lactantes y niños de corta edad (de 1mes a 2años), niños pre-escolares (de 2 a 5años), escolares (de 6 a 11años) y adolescentes (de 12 a 18años)1. La Sociedad Española de Neonatología (SEN) clasifica a los niños RN según la edad gestacional con la que nacen. Según esta clasificación se denomina: RN a término cuando nacen con 37 o más semanas de gestación y RN prematuro al niño que nace antes de completar la semana 37 de gestación, siendo la gestación una variable fisiológica fijada en 280±15días. A su vez, los RN prematuros se dividen en prematuros moderados-tardíos (nacen con 32-36semanas), muy prematuros (entre 28-31semanas) y prematuros extremos (nacen con 27 o menos semanas de gestación)2,3.
Las patologías más prevalentes del prematuro derivan de su inmadurez, principalmente por el acortamiento gestacional y por la hipoxia (por ineficaz adaptación respiratoria posnatal tras la supresión de la oxigenación transplacentaria). Por ello, la mayor parte de la morbimortalidad afecta a los RN muy prematuros y prematuros extremos, siendo necesario su ingreso en unidades neonatales para su manejo clínico-asistencial3.
En los últimos años la supervivencia de los niños más prematuros ha aumentado gracias a la especialización de la asistencia, a nuevas tecnologías y a tratamientos más prolongados. Dichos tratamientos requieren un incremento de técnicas o procedimientos invasivos (intervenciones quirúrgicas, intubación, inserción de catéteres, etc.), aumentando las estancias hospitalarias, concretamente en las unidades de cuidados intensivos neonatales (UCIN)2.
Durante su hospitalización, estos niños, suelen requerir la administración de líquidos y fármacos intravenosos durante largos períodos de tiempo. En estos casos, los accesos venosos centrales se han convertido en la vía de elección5. Existen distintas formas de acceso venoso central: a través de la vía umbilical; mediante acceso directo en las venas femoral, yugular o subclavia, y el acceso a la vena cava a través de venas periféricas empleando para ello catéteres centrales de inserción periférica (CCIP), denominados también por las siglas de su nombre inglés peripherally inserted central catheters (PICC)4,5. La elección del tipo de acceso depende de la inmadurez y de la patología del prematuro, eligiendo siempre la vía de menor riesgo y la de mayor rendimiento, preservando lo mejor posible el estado vascular del niño4,5. La vía principal de elección es la umbilical, la cual tiene como principales complicaciones sepsis graves y trombosis. Por ello se aconseja retirarla lo antes posible (entre el 5.° y el 7.° día). Los accesos venosos en las venas femoral, yugular o subclavia tampoco están exentos de complicaciones. Además de producir las mismas complicaciones que la vía umbilical, pueden tener otras más específicas dependiendo del acceso venoso, como neumotórax o hemorragias4,5. Por ello, el PICC se ha convertido en el acceso vascular de primera elección en el RN que necesita terapia intravenosa de larga duración. Se trata de una técnica de acceso venoso segura y eficaz para la administración intermedia (más de 7días y menos de 3meses) o prolongada (más de 3meses) de soluciones intravenosas (fluidos, nutrición parenteral, fármacos vasoactivos y antibióticos)3-6. Sin embargo, esta vía no está exenta de riesgos. El principal problema derivado de su uso son las infecciones o bacteriemias, además de otras complicaciones de tipo mecánico, como obstrucción, extravasación, rotura del catéter y extracción no electiva2,4-10. Tampoco es aconsejable su uso para la perfusión de sangre ni para determinados fármacos como las prostaglandinas (en neonatos se usa la prostaglandinaE1 o alprostadilo para la apertura y/o mantenimiento de la permeabilidad del ductus arterioso persistente en determinadas cardiopatías). En estos casos se utilizan los catéteres venosos periféricos, aunque el uso de estas vías es reservado por sus riesgos (extravasación y flebitis, principalmente). Estos riesgos determinan una duración escasa de estas, de 2 a 3días, siendo necesario reemplazarlas frecuentemente4,5.
El responsable de la inserción, del mantenimiento y de la prevención de eventos adversos (EA) asociados al PICC es la enfermera9,11. La canalización de esta vía de forma más sencilla y satisfactoria sucede cuando el paciente tiene los accesos vasculares intactos, aunque requiere la presencia de profesionales entrenados y con gran experiencia para su inserción y manejo12. En los últimos años algunos estudios han demostrado que el uso de la ecografía facilita el procedimiento de colocación del PICC, aumentando con esta técnica la seguridad y el éxito tanto en su inserción como en su correcta localización12,13.
La seguridad de los pacientes hospitalizados es un reto de todos los profesionales sanitarios. La cultura de seguridad permite conocer, a través de evaluaciones periódicas, el estado y la evolución de EA relacionados con la práctica clínica y las percepciones de los profesionales frente a estos14. Este reto se hace imprescindible en la UCIN, donde los RN prematuros son muy vulnerables, con un alto riesgo de morbimortalidad asociado a sus características anatómico-fisiológicas y clínicas.
En nuestro centro, desde el 1 de junio del año 2014 se aplica el protocolo «Bacteriemia Cero». Este protocolo, impulsado por la OMS y avalado por el Ministerio de Sanidad, Servicios Sociales e Igualdad (MSSSI)2, contempla una serie de medidas a implementar por parte de las enfermeras para disminuir los EA relacionados con los catéteres vasculares. Estas medidas consisten en la higiene y la desinfección de manos, el manejo estéril de los catéteres tanto en la inserción como en el mantenimiento, la desinfección de la piel con clorhexidina acuosa al 2% y el uso de clorhexidina alcohólica al 0,5% para las llaves de tres vías y conectores2,15. Con motivo de esta nueva metodología de trabajo, basada en la cultura de seguridad, el objetivo del estudio ha sido describir los factores de riesgo asociados a EA en RN portadores de PICC en una UCIN tras la aplicación del protocolo «Bacteriemia Cero».
MétodoDiseño, población y muestraPara alcanzar los objetivos de este trabajo se llevó a cabo un estudio descriptivo transversal. La población de estudio fueron todos los RN ingresados en la UCIN de un hospital general de tercer nivel portadores de un PICC. La muestra la formaron la totalidad de niños portadores de este tipo de catéteres durante el periodo de estudio, desde el 1 de octubre de 2014 hasta el 30 de septiembre de 2015. El tamaño de la muestra de 140PICC, analizados en 116 niños, garantizó la estimación de la proporción de riesgo de EA asociados a catéteres con una precisión del 5%, un nivel de confianza del 95% y una proporción del 10%16.
VariablesLas variables que se incluyeron fueron las siguientes:
Como variable dependiente y principal del estudio: la aparición de EA (sí o no).
Como variables independientes:
- -
Las relacionadas con el RN: edad gestacional, peso y sexo. Las categorías de edad gestacional y peso se determinaron en función de las establecidas por la Sociedad Española de Pediatría3. En este sentido, se consideró a los RN de ≤27semanas como prematuros extremos, RN entre 28 y 31semanas como muy prematuros, RN entre 32 y 36semanas como prematuros moderados a tardíos y RN a término a los nacidos con ≥37semanas. En cuanto al peso, se dividió en RN de extremo bajo peso con ≤999g, RN de muy bajo peso entre 1.000 y 1.499g, RN de bajo peso entre 1.500 y 2.499g y RN de peso normal ≥2.500g.
- -
Las relacionadas con el catéter: calibre medido en French (Fr) (1 o 2Fr), zona anatómica de inserción del catéter: miembros superiores (MMSS), miembros inferiores (MMII) o cabeza (con localización correcta de la punta del catéter según comprobación radiológica en vena cava superior o inferior), número de días que el catéter estuvo insertado, tipo de infusión por el catéter (diferenciando perfusiones con y sin antibióticos) y número de catéteres que se insertaron en el mismo paciente (uno, dos o más de dos). Se especificó el tipo de EA cuando apareció.
Para recoger la información se utilizó un documento ad hoc. Los datos fueron extraídos de las historias clínicas informatizadas de cada uno de los neonatos incluidos en la muestra. El registro se realizó durante el mes de enero de 2016, periodo donde se dispuso de todos los datos necesarios para esta investigación (específicamente los relacionados con los EA asociados a los catéteres a través del registro de determinaciones analíticas y cultivo de la punta del catéter). La cumplimentación de las variables del estudio la llevaron a cabo durante el turno de mañana en la UCIN tres enfermeras de la unidad, de tal forma que el análisis y la recogida de información siempre se realizaron por pares para eliminar el sesgo de registro y codificación.
Análisis estadísticoTodos los datos recogidos fueron introducidos en una base de datos y analizados con el paquete estadístico SPSS® (IBM SPSS Statistics) en su versión 20.0. En el análisis descriptivo de las características generales de la muestra las variables numéricas fueron escritas como media aritmética y desviación típica y los resultados de las variables categóricas en frecuencias y porcentajes. La hipótesis de normalidad de las distribuciones en las variables continuas se ha evaluado mediante el test de Kolmogorov-Smirnov. Para alcanzar el objetivo general se identificaron los EA aparecidos y relacionados con la inserción del PICC en todos los neonatos estudiados, presentando los datos en frecuencias y porcentajes. Se realizó un análisis bivariado para identificar qué factores influyen en la aparición de EA. En él se relacionó la variable dependiente (la aparición o no de EA) con el resto de variables independientes estudiadas (edad gestacional, sexo, peso, calibre del catéter, tiempo de permanencia del catéter en días, punto de punción, medicación con/sin antibióticos y número de catéter). Se calculó el test chi cuadrado o el estadístico exacto de Fisher para muestras pequeñas, considerando en estas pruebas un nivel de significación de p<0,05.
Acompañando a las medidas de prevalencia se indicó la razón de prevalencia determinando la odds ratio (OR) no ajustada y el intervalo de confianza (IC) del 95%. Finalmente, se ajustó el modelo para las variables que obtuvieron significación en el análisis bivariado, resultando el modelo final de la regresión logística por el método hacia delante, con criterio de entrada de 0,05 y de salida de 0,10.
Aspectos ético-legalesPrevio a la recogida de datos se realizó la solicitud formal de permiso a los responsables de la UCIN (supervisora y jefe de servicio médico de la unidad). Todos los padres de los RN integrantes de la muestra habían dado el consentimiento para la utilización de los datos con fines clínicos y de investigación. La autorización de este consentimiento forma parte de la documentación proporcionada en la acogida a la unidad. Durante la recogida de datos, a cada niño se le asignó un código para mantener la confidencialidad de los mismos. Los datos obtenidos se trataron según el Reglamento General de Protección de Datos de la Unión Europea 2016/679 del Parlamento Europeo, aplicable en España el 25 de mayo de 2018, y la ley 41/2002, de 14 de noviembre, básica reguladora de la autonomía del paciente, de derechos y obligaciones en materia de información y documentación clínica.
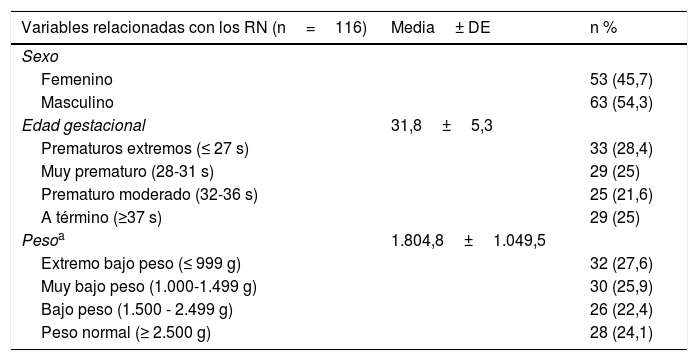
ResultadosCaracterísticas sociodemográficas y clínicas de la muestraUn total de 116 RN ingresados en la UCIN fueron analizados en el periodo de estudio. De ellos, un 54,3% eran niños y un 45,7% niñas, con una edad gestacional media de 31,8±5,3semanas. El peso se encuentra con una mediana de 1.415g (980-2.450) (tabla 1).
Descripción de las variables sociodemográficas y clínicas de la muestra
| Variables relacionadas con los RN (n=116) | Media± DE | n % |
|---|---|---|
| Sexo | ||
| Femenino | 53 (45,7) | |
| Masculino | 63 (54,3) | |
| Edad gestacional | 31,8±5,3 | |
| Prematuros extremos (≤ 27 s) | 33 (28,4) | |
| Muy prematuro (28-31 s) | 29 (25) | |
| Prematuro moderado (32-36 s) | 25 (21,6) | |
| A término (≥37 s) | 29 (25) | |
| Pesoa | 1.804,8±1.049,5 | |
| Extremo bajo peso (≤ 999 g) | 32 (27,6) | |
| Muy bajo peso (1.000-1.499 g) | 30 (25,9) | |
| Bajo peso (1.500 - 2.499 g) | 26 (22,4) | |
| Peso normal (≥ 2.500 g) | 28 (24,1) | |
| Variables relacionadas con los PICC (n=140) | Media±DE | n % |
|---|---|---|
| Punto de punción del catéter | ||
| Miembro superior | 94 (67,1) | |
| Miembro inferior | 28 (20) | |
| Cabeza | 18 (12,9) | |
| Localización anatómica del catéter | ||
| Vena cava | 95 (67,9) | |
| Vena subclavia | 35 (25) | |
| Otras | 10 (7,1) | |
| Calibre del catéter | ||
| 1 French | 89 (63,6) | |
| 2 French | 51 (36,4) | |
| Permanencia del catéter (1-49 días)b | 9,5±8,1 | |
| 1-7 días | 78 (55,8) | |
| 8-14 días | 38 (27,1) | |
| ≥ 15 días | 24 (17,1) | |
| Terapia infundida por catéter | ||
| Sin antibióticos (nutrición parenteral, lípidos, otros) | 71 (50,7) | |
| Con antibióticos | 69 (49,3) | |
| Número de catéter insertado en el mismo niño (1-4 catéteres) | ||
| Primero | 1,2±0,5 | 116 (82,9) |
| Segundo o más | 24 (17,1) | |
DE: desviación estándar.
En los 116 neonatos estudiados, se han analizado un total de 140PICC, en la mayoría de los casos (63,6%) de 1Fr. En este sentido, hay que resaltar que 24 de ellos precisaron durante su ingreso más de dos catéteres (de 2 a 4) para su tratamiento. La mayor parte de catéteres estuvieron insertados en prematuros extremos (35,7%), muy prematuros (22,9%) y, en un 57,9%, en niños con peso inferior a 1.500g. El 67,1% de los catéteres fueron canalizados en MMSS. Los catéteres estuvieron insertados una mediana de 7días (5-10,75). En cuanto a la terapia que se infundió por los catéteres, prácticamente la mitad fueron antibióticos (49,3%) (tabla 1).
Aparición de eventos adversosEn la mayoría de los catéteres estudiados no aparecieron EA (83,6%). Ordenados por orden de frecuencia decreciente, los eventos aparecidos fueron: bacteriemia asociada al catéter (5,7%), obstrucción (5,7%), extravasación (2,1%) y flebitis (2,1%). En un solo caso fue necesaria la retirada del catéter por mal estado del mismo (0,8%).
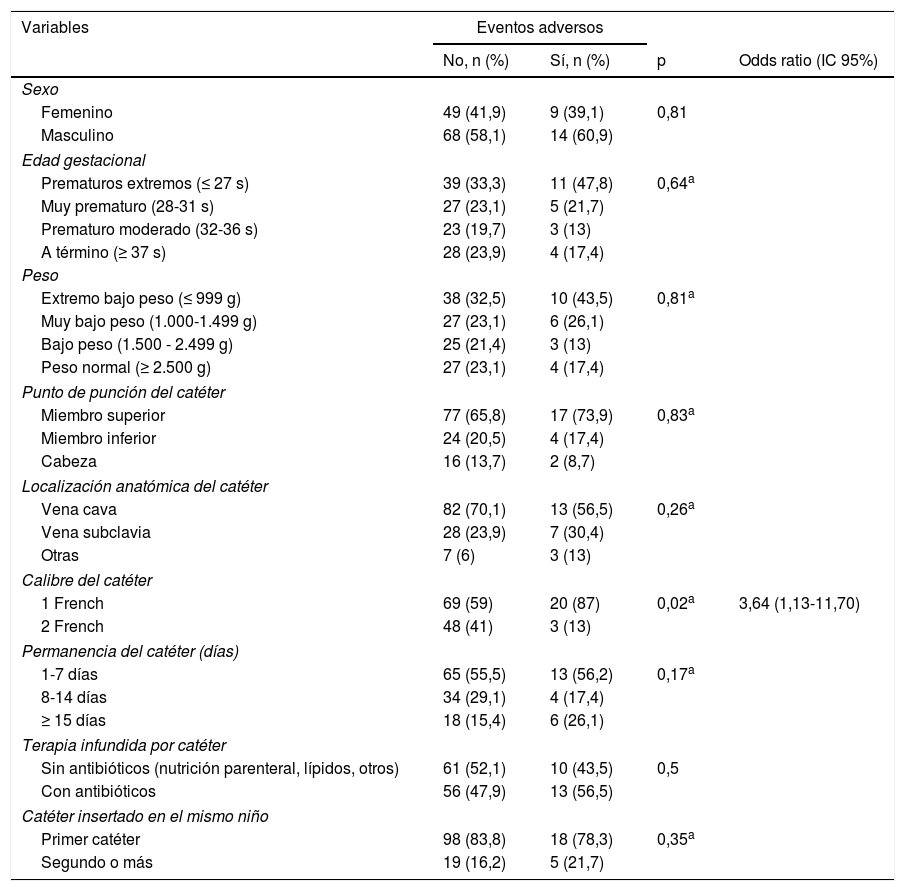
Factores que influyen en la aparición de eventos adversosEl calibre del catéter fue la única variable que se asoció de forma significativa (OR=3,6; p=0,02) con la aparición o no de cualquier EA en general. Los RN portadores de un PICC de calibre pequeño (1Fr) tenían más probabilidad de que apareciera un EA que los portadores de un catéter de calibre superior (2Fr) (tabla 2).
Variables asociadas a la aparición de eventos adversos
| Variables | Eventos adversos | |||
|---|---|---|---|---|
| No, n (%) | Sí, n (%) | p | Odds ratio (IC 95%) | |
| Sexo | ||||
| Femenino | 49 (41,9) | 9 (39,1) | 0,81 | |
| Masculino | 68 (58,1) | 14 (60,9) | ||
| Edad gestacional | ||||
| Prematuros extremos (≤ 27 s) | 39 (33,3) | 11 (47,8) | 0,64a | |
| Muy prematuro (28-31 s) | 27 (23,1) | 5 (21,7) | ||
| Prematuro moderado (32-36 s) | 23 (19,7) | 3 (13) | ||
| A término (≥ 37 s) | 28 (23,9) | 4 (17,4) | ||
| Peso | ||||
| Extremo bajo peso (≤ 999 g) | 38 (32,5) | 10 (43,5) | 0,81a | |
| Muy bajo peso (1.000-1.499 g) | 27 (23,1) | 6 (26,1) | ||
| Bajo peso (1.500 - 2.499 g) | 25 (21,4) | 3 (13) | ||
| Peso normal (≥ 2.500 g) | 27 (23,1) | 4 (17,4) | ||
| Punto de punción del catéter | ||||
| Miembro superior | 77 (65,8) | 17 (73,9) | 0,83a | |
| Miembro inferior | 24 (20,5) | 4 (17,4) | ||
| Cabeza | 16 (13,7) | 2 (8,7) | ||
| Localización anatómica del catéter | ||||
| Vena cava | 82 (70,1) | 13 (56,5) | 0,26a | |
| Vena subclavia | 28 (23,9) | 7 (30,4) | ||
| Otras | 7 (6) | 3 (13) | ||
| Calibre del catéter | ||||
| 1 French | 69 (59) | 20 (87) | 0,02a | 3,64 (1,13-11,70) |
| 2 French | 48 (41) | 3 (13) | ||
| Permanencia del catéter (días) | ||||
| 1-7 días | 65 (55,5) | 13 (56,2) | 0,17a | |
| 8-14 días | 34 (29,1) | 4 (17,4) | ||
| ≥ 15 días | 18 (15,4) | 6 (26,1) | ||
| Terapia infundida por catéter | ||||
| Sin antibióticos (nutrición parenteral, lípidos, otros) | 61 (52,1) | 10 (43,5) | 0,5 | |
| Con antibióticos | 56 (47,9) | 13 (56,5) | ||
| Catéter insertado en el mismo niño | ||||
| Primer catéter | 98 (83,8) | 18 (78,3) | 0,35a | |
| Segundo o más | 19 (16,2) | 5 (21,7) | ||
IC: intervalo de confianza.
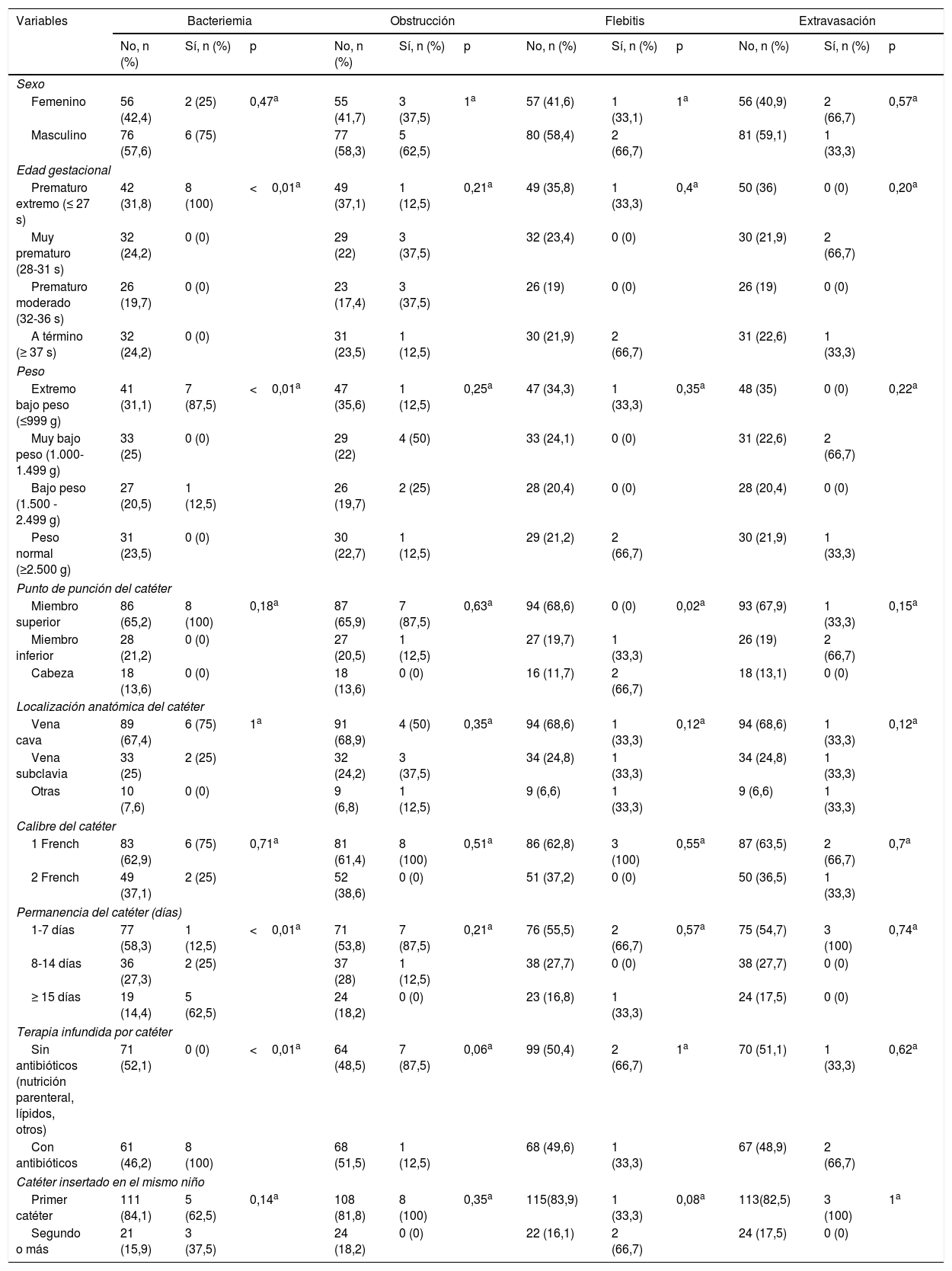
Al analizar los motivos de retirada del catéter observamos que la bacteriemia se asoció de forma estadísticamente significativa con los RN <27semanas (OR=1,2; p=0,02), con un peso <1.000g (OR=6,7; p=0,02), permanencia superior a 7días (OR=9,8; p=0,02) y con la infusión de terapia con antibióticos (OR=1,3; p<0,01). La flebitis se asoció solamente con la zona anatómica donde estaba colocado el catéter, de tal forma que el 66,7% de los casos aparecieron en catéteres insertados en la cabeza (p=0,02). Además, los RN con PICC insertados en MMII y en la cabeza tenían más flebitis respecto a los que portaban los catéteres en MMSS (OR=1,07; p=0,03). No se halló asociación significativa entre las variables estudiadas y el riesgo de obstrucción y extravasación (tablas 3 y 4).
Relación entre los motivos de retirada del catéter y los factores de riesgo
| Variables | Bacteriemia | Obstrucción | Flebitis | Extravasación | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| No, n (%) | Sí, n (%) | p | No, n (%) | Sí, n (%) | p | No, n (%) | Sí, n (%) | p | No, n (%) | Sí, n (%) | p | |
| Sexo | ||||||||||||
| Femenino | 56 (42,4) | 2 (25) | 0,47a | 55 (41,7) | 3 (37,5) | 1a | 57 (41,6) | 1 (33,1) | 1a | 56 (40,9) | 2 (66,7) | 0,57a |
| Masculino | 76 (57,6) | 6 (75) | 77 (58,3) | 5 (62,5) | 80 (58,4) | 2 (66,7) | 81 (59,1) | 1 (33,3) | ||||
| Edad gestacional | ||||||||||||
| Prematuro extremo (≤ 27 s) | 42 (31,8) | 8 (100) | <0,01a | 49 (37,1) | 1 (12,5) | 0,21a | 49 (35,8) | 1 (33,3) | 0,4a | 50 (36) | 0 (0) | 0,20a |
| Muy prematuro (28-31 s) | 32 (24,2) | 0 (0) | 29 (22) | 3 (37,5) | 32 (23,4) | 0 (0) | 30 (21,9) | 2 (66,7) | ||||
| Prematuro moderado (32-36 s) | 26 (19,7) | 0 (0) | 23 (17,4) | 3 (37,5) | 26 (19) | 0 (0) | 26 (19) | 0 (0) | ||||
| A término (≥ 37 s) | 32 (24,2) | 0 (0) | 31 (23,5) | 1 (12,5) | 30 (21,9) | 2 (66,7) | 31 (22,6) | 1 (33,3) | ||||
| Peso | ||||||||||||
| Extremo bajo peso (≤999 g) | 41 (31,1) | 7 (87,5) | <0,01a | 47 (35,6) | 1 (12,5) | 0,25a | 47 (34,3) | 1 (33,3) | 0,35a | 48 (35) | 0 (0) | 0,22a |
| Muy bajo peso (1.000-1.499 g) | 33 (25) | 0 (0) | 29 (22) | 4 (50) | 33 (24,1) | 0 (0) | 31 (22,6) | 2 (66,7) | ||||
| Bajo peso (1.500 - 2.499 g) | 27 (20,5) | 1 (12,5) | 26 (19,7) | 2 (25) | 28 (20,4) | 0 (0) | 28 (20,4) | 0 (0) | ||||
| Peso normal (≥2.500 g) | 31 (23,5) | 0 (0) | 30 (22,7) | 1 (12,5) | 29 (21,2) | 2 (66,7) | 30 (21,9) | 1 (33,3) | ||||
| Punto de punción del catéter | ||||||||||||
| Miembro superior | 86 (65,2) | 8 (100) | 0,18a | 87 (65,9) | 7 (87,5) | 0,63a | 94 (68,6) | 0 (0) | 0,02a | 93 (67,9) | 1 (33,3) | 0,15a |
| Miembro inferior | 28 (21,2) | 0 (0) | 27 (20,5) | 1 (12,5) | 27 (19,7) | 1 (33,3) | 26 (19) | 2 (66,7) | ||||
| Cabeza | 18 (13,6) | 0 (0) | 18 (13,6) | 0 (0) | 16 (11,7) | 2 (66,7) | 18 (13,1) | 0 (0) | ||||
| Localización anatómica del catéter | ||||||||||||
| Vena cava | 89 (67,4) | 6 (75) | 1a | 91 (68,9) | 4 (50) | 0,35a | 94 (68,6) | 1 (33,3) | 0,12a | 94 (68,6) | 1 (33,3) | 0,12a |
| Vena subclavia | 33 (25) | 2 (25) | 32 (24,2) | 3 (37,5) | 34 (24,8) | 1 (33,3) | 34 (24,8) | 1 (33,3) | ||||
| Otras | 10 (7,6) | 0 (0) | 9 (6,8) | 1 (12,5) | 9 (6,6) | 1 (33,3) | 9 (6,6) | 1 (33,3) | ||||
| Calibre del catéter | ||||||||||||
| 1 French | 83 (62,9) | 6 (75) | 0,71a | 81 (61,4) | 8 (100) | 0,51a | 86 (62,8) | 3 (100) | 0,55a | 87 (63,5) | 2 (66,7) | 0,7a |
| 2 French | 49 (37,1) | 2 (25) | 52 (38,6) | 0 (0) | 51 (37,2) | 0 (0) | 50 (36,5) | 1 (33,3) | ||||
| Permanencia del catéter (días) | ||||||||||||
| 1-7 días | 77 (58,3) | 1 (12,5) | <0,01a | 71 (53,8) | 7 (87,5) | 0,21a | 76 (55,5) | 2 (66,7) | 0,57a | 75 (54,7) | 3 (100) | 0,74a |
| 8-14 días | 36 (27,3) | 2 (25) | 37 (28) | 1 (12,5) | 38 (27,7) | 0 (0) | 38 (27,7) | 0 (0) | ||||
| ≥ 15 días | 19 (14,4) | 5 (62,5) | 24 (18,2) | 0 (0) | 23 (16,8) | 1 (33,3) | 24 (17,5) | 0 (0) | ||||
| Terapia infundida por catéter | ||||||||||||
| Sin antibióticos (nutrición parenteral, lípidos, otros) | 71 (52,1) | 0 (0) | <0,01a | 64 (48,5) | 7 (87,5) | 0,06a | 99 (50,4) | 2 (66,7) | 1a | 70 (51,1) | 1 (33,3) | 0,62a |
| Con antibióticos | 61 (46,2) | 8 (100) | 68 (51,5) | 1 (12,5) | 68 (49,6) | 1 (33,3) | 67 (48,9) | 2 (66,7) | ||||
| Catéter insertado en el mismo niño | ||||||||||||
| Primer catéter | 111 (84,1) | 5 (62,5) | 0,14a | 108 (81,8) | 8 (100) | 0,35a | 115(83,9) | 1 (33,3) | 0,08a | 113(82,5) | 3 (100) | 1a |
| Segundo o más | 21 (15,9) | 3 (37,5) | 24 (18,2) | 0 (0) | 22 (16,1) | 2 (66,7) | 24 (17,5) | 0 (0) | ||||
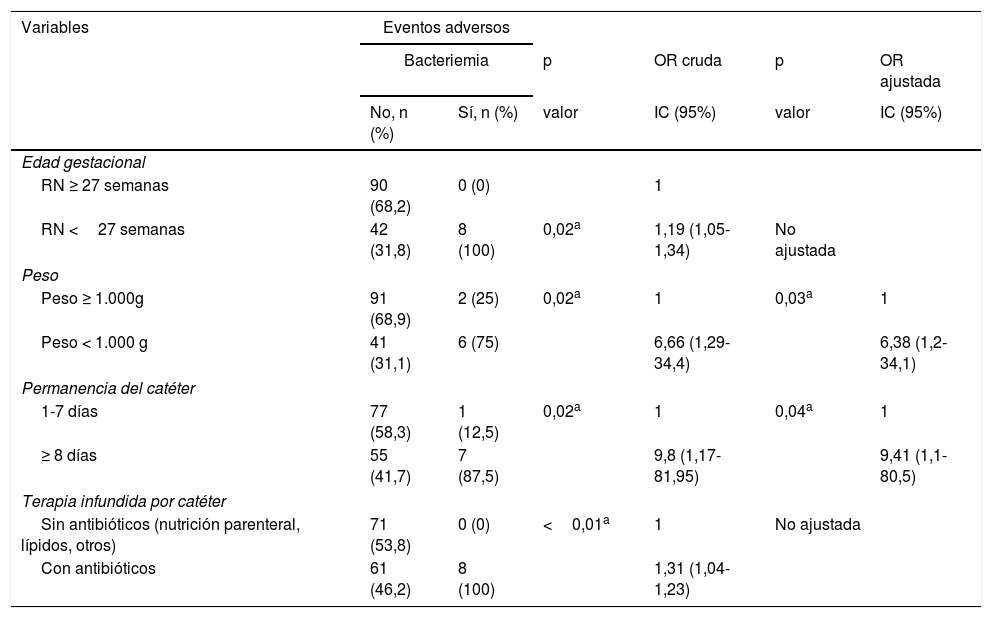
Eventos adversos asociados a características de los RN estudiados
| Variables | Eventos adversos | |||||
|---|---|---|---|---|---|---|
| Bacteriemia | p | OR cruda | p | OR ajustada | ||
| No, n (%) | Sí, n (%) | valor | IC (95%) | valor | IC (95%) | |
| Edad gestacional | ||||||
| RN ≥ 27 semanas | 90 (68,2) | 0 (0) | 1 | |||
| RN <27 semanas | 42 (31,8) | 8 (100) | 0,02a | 1,19 (1,05-1,34) | No ajustada | |
| Peso | ||||||
| Peso ≥ 1.000g | 91 (68,9) | 2 (25) | 0,02a | 1 | 0,03a | 1 |
| Peso < 1.000 g | 41 (31,1) | 6 (75) | 6,66 (1,29-34,4) | 6,38 (1,2-34,1) | ||
| Permanencia del catéter | ||||||
| 1-7 días | 77 (58,3) | 1 (12,5) | 0,02a | 1 | 0,04a | 1 |
| ≥ 8 días | 55 (41,7) | 7 (87,5) | 9,8 (1,17-81,95) | 9,41 (1,1-80,5) | ||
| Terapia infundida por catéter | ||||||
| Sin antibióticos (nutrición parenteral, lípidos, otros) | 71 (53,8) | 0 (0) | <0,01a | 1 | No ajustada | |
| Con antibióticos | 61 (46,2) | 8 (100) | 1,31 (1,04-1,23) | |||
| Flebitis | p | OR cruda | p | OR ajustada | ||
|---|---|---|---|---|---|---|
| No, n % | Sí, n % | valor | IC (95%) | valor | IC (95%) | |
| Punto de punción del catéter | ||||||
| Miembro superior | 94 (68,6) | 0 (0) | 0,03a | 1 | No ajustada | |
| Miembro inferior/cabeza | 43 (31,4) | 3 (100) | 1,07 (0,99-1,15) | |||
IC: intervalo de confianza; OR: odds ratio.
En la tabla 4 se pueden observar los resultados obtenidos tras ajustar el modelo de regresión logística según las variables que han aparecido significativas en el análisis bivariado (bacteriemia y flebitis). Los resultados han indicado un mayor riesgo de bacteriemia asociada al catéter en RN con peso extremo (<1.000g) (OR=6,38; p=0,03) y en aquellos que portan el catéter más de 7días en relación con los que lo mantienen 7 o menos días (OR=9,41; p=0,04).
DiscusiónEn el presente estudio el calibre del PICC más empleado en los RN analizados fue de 1Fr. Este hecho es debido a que más de la mitad de la muestra son prematuros extremos y de muy bajo peso, con edad gestacional <31semanas. Los neonatos portadores de catéter pequeño (1Fr) muestran un mayor riesgo de aparición de EA que los niños portadores de catéteres de mayor calibre (2Fr). Estos resultados coinciden con algunos estudios donde los PICC de menor calibre tienen una duración menor y una mayor probabilidad de aparición de EA17,18.
En los neonatos estudiados la zona anatómica de elección más habitual para la inserción del PICC han sido los MMSS (67,1%), siendo la vena cava superior la de elección. Este dato coincide con los de otros estudios11,19,20. En este sentido, se ha comprobado que la localización de los catéteres se asocia a complicaciones. En un estudio realizado por Lloreda-Garcia et al.10 los PICC medioclaviculares presentaron más riesgo de complicaciones que los localizados en vena cava o braquiocefálica. Otros autores han descrito graves complicaciones (aparición de neumotórax, taponamiento cardíaco, trombosis e incluso parada cardiorrespiratoria) ocasionadas por un mal posicionamiento del catéter, debido a una inadecuada localización de la punta del mismo3,8,9. En la muestra analizada, ningún evento de estas características ha ocurrido como consecuencia del mal posicionamiento del catéter. Este hecho puede ser debido a la rápida comprobación radiológica de la localización de la punta del catéter, actuación que ha permitido la rectificación y evitar una inadecuada posición del mismo. El motivo más habitual de retirada en los PICC examinados ha sido electivo, principalmente debido a la finalización del tratamiento intravenoso, hallándose en línea con otras investigaciones publicadas11,17,19.
El porcentaje de EA aparecidos en los RN estudiados portadores de catéteres epicutáneos es del 16,4%. En la bibliografía revisada se han obtenido cifras que oscilan entre el 10 y el 57,2%2,3,9,10,13,16-26. Si comparamos el porcentaje obtenido en esta investigación con los estudios revisados, observamos porcentajes más bajos. Aunque no se disponen de datos anteriores al presente estudio, se cree que este resultado puede ser debido a la implantación del protocolo de «Bacteriemia Cero» que, aunque solo llevaba implantado 3meses antes del inicio de la recogida de datos, ha podido influir positivamente. Aun así, para comprobarlo con mayor certeza habrá que realizar un seguimiento longitudinal más exhaustivo.
En diversos estudios se obtienen resultados donde las complicaciones de tipo no infeccioso asociadas a los PICC son más frecuentes que las complicaciones de tipo infeccioso11,18,19. En el presente estudio también se encontraron más complicaciones mecánicas (10,7%) que de tipo infeccioso (5,7%). Aun así, los resultados obtenidos son inferiores a los hallados por otros autores. Concretamente, en el estudio de Gomes et al.11 se obtuvo un 21,4% de complicaciones mecánicas frente a un 14,3% de eventos de tipo infeccioso. Van den Berg et al.19 también encuentran más complicaciones de tipo mecánico (71%) que infeccioso (13%). Igualmente, en un estudio realizado en la India, Singh et al.18 obtienen cifras de un 12,2% de complicaciones no infecciosas frente a un 10,7% de complicaciones infecciosas.
Respecto a las complicaciones mecánicas se han encontrado un 5,7% de obstrucciones como las más frecuentes en los catéteres analizados. Este resultado es inferior al que reflejan otros estudios, que obtienen desde el 13,1% hasta el 30,9% de obstrucción9,11,17,21,23,24. La extravasación, con el 2,1%, ha sido la segunda complicación más prevalente hallada en nuestro estudio, cifra que supera a la obtenida por Costa et al.24 (1,2%) y se halla por debajo de las obtenidas en otros estudios (del 5% hasta el 11,9%)9,21,27. Sin embargo, no se halló asociación significativa entre las variables estudiadas y estas dos complicaciones mecánicas, y tampoco se ha encontrado en la bibliografía revisada. La rotura del catéter ocurrió en un solo caso (el 0,8% de todos los RN estudiados), siendo este porcentaje mayor en la literatura consultada (oscila entre el 8,8% y el 16,4%)9,11,21,23,24.
En relación con el tratamiento administrado a través del catéter, el 49,3% de los PICC analizados fueron empleados para administrar terapias con antibióticos. En el análisis bivariado se observa un mayor riesgo de bacteriemia asociada al catéter en los neonatos con infusión de antibióticos respecto a los que no llevaban estos tratamientos. No se han encontrado estudios que coincidan con este hallazgo. Tras realizar un análisis de regresión logística, se ha comprobado que los tratamientos con antibióticos no influyen de forma independiente en la aparición de bacteriemia.
La aparición de flebitis asociada al catéter puede ser de causa infecciosa o mecánica. En este estudio hemos obtenido una incidencia muy baja (2,1%) si lo comparamos con otras investigaciones. Así, Donovan et al.21 obtienen cifras del 3,6% y Ma et al.27 del 11,5%, siendo este EA mayor en niños de menor peso y de menor edad gestacional. Nuestros resultados muestran una asociación entre la aparición de flebitis con la zona anatómica de punción, de tal forma que si el catéter está insertado en MMII y cabeza hay mayor probabilidad de que aparezca este EA que si está insertado en MMSS. Estos datos coinciden con algunos autores que afirman que hay más complicaciones en PICC insertados en MMII que en los situados en MMSS27,28. Sin embargo, hay estudios que difieren, como el realizado por Njere et al.29, que encuentra una menor incidencia de EA en PICC insertados en MMII en comparación con los de MMSS, y en el estudio de Callejas et al.30, que muestra una mayor incidencia de infección en catéteres insertados en venas del cuero cabelludo y de MMSS que en los insertados en MMII.
En el presente estudio se observan complicaciones infecciosas (bacteriemia) en el 5,7% de los neonatos. En el análisis bivariado se halla una asociación con la edad gestacional y con un extremo bajo peso de los RN con la administración de antibióticos por el catéter y con los días de permanencia del mismo. Tras realizar un análisis de regresión logística y calcular los factores que independientemente influyen en la aparición de EA asociados al catéter, se halla asociación entre bacteriemia y neonatos de peso igual o menor a 1.000g (siendo 6,4 veces mayor la probabilidad de tener este EA que en los neonatos que pesan más de 1kg) y en aquellos con una permanencia superior a 7días de catéter (con un riesgo 9,4 veces mayor respecto a los que mantienen el catéter menos de una semana).
La duración de la canalización depende fundamentalmente de las características del paciente (peso, gravedad, dificultad para la canalización, etc.). El tiempo de permanencia de los catéteres es variable según diferentes publicaciones revisadas y se sitúa entre los 3 y los 18días de media7,11,17,18,22-25,29-31. En nuestro estudio se verifica un periodo de permanencia con una mediana de 7días (5-10,75), estando este dato en la misma línea de los estudios revisados.
En una investigación realizada en dos hospitales de Turquía17 se observó un incremento significativo de la contaminación del catéter a partir de la tercera semana de permanencia. A la vez, Njere et al.29 detectaron que la probabilidad de bacteriemia asociada al catéter se incrementaba en 3,1 veces si su permanencia era de 9días o más, resultado similar al obtenido en esta investigación, donde aumenta la probabilidad de bacteriemia a partir de 7días de permanencia del catéter.
Según un informe del MSSSI2, la incidencia de sepsis nosocomial es inversamente proporcional al peso y a la edad gestacional y afecta a más del 20% de los RN de muy bajo peso, alcanzando hasta el 50% en RN con peso inferior a 1.000g. Varios estudios describen la edad gestacional y el peso como factores de riesgo de bacteriemia relacionada con el PICC. Wen et al.16, Zhao et al.26 y García González et al.32 encuentran asociación entre bacteriemia y RN con peso <1.500g. Nercelles et al.7 y Van den Berg et al.19 hallan una asociación significativa entre la bacteriemia relacionada con el CCIP en neonatos de peso inferior a 1.000g, coincidiendo los hallazgos de estos dos estudios con los resultados de esta investigación.
Limitaciones y fortalezas del estudioUna de las limitaciones de este estudio ha sido la muestra reducida de RN junto a la baja incidencia de EA hallados. Esto ha ocasionado no poder estudiar los factores independientes asociados a EA detectados, como obstrucción, flebitis y extravasación. Otra limitación ha sido no incluir en este trabajo el análisis de los catéteres umbilicales como se hace en otros estudios, lo que nos ha impedido obtener información sobre estos catéteres y comparar resultados.
La fortaleza principal de esta investigación ha sido contener la totalidad de neonatos con PICC a lo largo de un año natural, no existiendo sesgo de temporalidad. La baja prevalencia de EA hallados también ha sido una de las fortalezas del estudio y de la unidad. Este hecho nos hace plantearnos el éxito en la implantación del protocolo «Bacteriemia Cero», aunque hay que realizar más estudios para comparar resultados.
ConclusionesLa atención del RN en la UCIN se asocia a un alto riesgo de EA. Su inmadurez fisiológica, la gravedad de su patología, así como la complejidad y la duración de los tratamientos hacen que estos niños sean muy vulnerables. Una asepsia estricta y una mínima manipulación de los sistemas de perfusión son medidas preventivas eficaces. Cualquier medida adoptada para disminuir la incidencia de complicaciones está siempre justificada, puesto que el RN con infección relacionada con el PICC incrementa su morbimortalidad y el coste sanitario.
En el presente estudio hemos auditado nuestra práctica clínica y obtenido más información sobre los EA relacionados con los PICC. Los resultados aportan información relevante para todas las enfermeras que desarrollan su práctica clínica en la UCIN. Estos hallazgos permitirán extremar la seguridad en los RN más vulnerables, en especial los neonatos con extremo bajo peso que precisan tratamientos muy prolongados. Extremar las medidas de asepsia con protocolos específicos como el de «Bacteriemia Cero» contribuye a aumentar la seguridad clínica y disminuir la morbimortalidad en estos niños. La evaluación periódica de EA relacionados con catéteres es de gran utilidad para elaborar planes de mejora. Esto nos permitirá actualizar los protocolos relacionados con la inserción y el mantenimiento de catéteres, teniendo en cuenta los factores de riesgo asociados a sus complicaciones, mejorando la calidad de los cuidados.
FinanciaciónEste trabajo no ha recibido ninguna beca ni subvención.
Conflicto de interesesNo existe conflicto de intereses por parte de los autores de este estudio.
A todas las enfermeras que han participado en el estudio, y al hospital por haber dado los permisos para su realización.