Evaluar la efectividad de la implantación de un protocolo de control glucémico del paciente crítico liderado por enfermeras, en términos de mantenimiento de un rango preestablecido de glucemias, reducción de hiperglucemia y prevención de hipoglucemia severa.
MétodoEstudio cuasiexperimental prospectivo «pre-pos» realizado en una unidad de cuidados intensivos polivalente. Se incluyeron pacientes adultos en tratamiento con insulina endovenosa. Se registraron todas las determinaciones de glucemia desde noviembre de 2014 a agosto de 2015 (preintervención) y desde noviembre de 2015 a agosto de 2016 (pos). La intervención consistió en la implementación de un protocolo basado en la evidencia, para conseguir rangos de glucemia entre 140-180mg/dl. Las variables principales incluyeron proporciones de glucemias dentro de rango, tasas de hipoglucemia severa (menos de 40mg/dl) y tasas de hiperglucemia superior a 200mg/dl.
ResultadosSe evaluaron 7864 determinaciones de glucemia pertenecientes a 125 pacientes, 66 preintervención y 59 postintervención. La edad media fue de 66,24±13,99 años, el 64% eran hombres. La proporción de determinaciones dentro del rango fue superior en el grupo postintervención (38,82 vs. 44,34 p<0,001). Se identificó un caso de hipoglucemia severa, que sucedió en el grupo preintervención. La tasa de hiperglucemia severa resultó menor en el grupo postintervención (19,19 vs. 16,28 p=0,001).
ConclusionesNuestra experiencia muestra que una implantación basada en la evidencia puede mejorar el control glucémico en pacientes críticos. Se observaron mayores tasas de glucemia dentro de rango. El protocolo resultó útil en la prevención de la hipoglucemia severa. El liderazgo del equipo de enfermería y la toma de decisiones autónomas basadas en datos clínicos permitió mejorar los resultados en salud de los pacientes.
To assess the effectiveness of the implementation of a protocol for glycaemic control in critical care, in terms of maintenance of a pre-established target of blood glucose level, reduction of hyperglycaemia and prevention of severe hypoglycaemia.
MethodProspective “pre-post” quasi-experimental study carried out in a general critical care unit. Adult patients treated with intravenous insulin were included. We recorded all glycaemic tests performed from November 2014 to August 2015 (pre-intervention) and from November 2015 to August 2016 (post-intervention). The intervention consisted of the implementation of an evidence-based glycaemic control protocol to achieve glycaemic levels in a range of 140-180mg/dl. Main variables analysed were: proportion of glycaemic tests in the target range, proportions of severe hypoglycaemia (under 40mg/dl) and hyperglycaemia over 200mg/dl.
ResultsWe analysed 7864 glycaemic tests from 125 patients, 66 pre-intervention and 59 post-intervention. Average age was 66.24±13.99 years, 64% of patients were male. The proportion of tests within the target range was higher in the intervention group (38.82 vs. 44.34 p<.001). Only one case of severe hypoglycaemia was identified, which happened in the pre-intervention period. The rate of severe hyperglycaemia was lower in the post-intervention group (19.19 vs. 16.28 p=.001).
ConclusionsOur experience shows that implementation of evidence-based interventions can improve glycaemic control during critical illness. We found higher glycaemia levels in the target range. The protocol proved useful in the prevention of severe hypoglycaemia. Nurse-led interventions based on clinical data improved health results in our patients.
La hiperglucemia del paciente crítico ha sido asociada a diversos efectos adversos y a un aumento de la morbilidad durante la atención en cuidados intensivos. Su control supone un reto asistencial para los profesionales de cuidados intensivos. La infusión de insulina endovenosa requiere un control estricto que puede resultar complejo, debido al riesgo de hipoglucemia grave y su relación directa con la mortalidad del paciente crítico.
La implantación de protocolos guiados por enfermeras supone una mejora en la práctica asistencial y en la seguridad clínica de los pacientes críticos que reciben insulina endovenosa. Nuestro estudio aporta información sobre las mejoras en el control glucémico introducidas por una estrategia de implantación de evidencias y de normalización de la práctica asistencial liderada por el equipo de enfermería. El papel de la enfermera en la monitorización continua de la glucemia y en la correcta dosificación de la insulinoterapia, es esencial para la seguridad de la administración de insulina, consiguiendo una mejor adaptación de la terapia a la situación clínica cambiante.
¿Implicaciones del estudio?Nuestra experiencia puede ayudar a mejorar los protocolos de actuación o promover la implantación de acciones similares, que reduzcan la variabilidad clínica y mejoren el control glucémico del paciente. Se muestra que el liderazgo de las enfermeras en una intervención multidisciplinar y la autonomía en la toma de decisiones por parte de estos profesionales pueden derivar en mejoras en la eficacia del control glucémico. En este sentido, debe resultar útil para profesionales asistenciales y gestores del ámbito del paciente crítico comprometidos con la mejora continua. También puede resultar de utilidad a investigadores interesados en la implantación de evidencias en el ámbito clínico.
La hiperglucemia por estrés, también conocida como hiperglucemia del paciente crítico o diabetes por estrés, es un evento común en los pacientes atendidos en unidades de cuidados intensivos (UCI), con una incidencia de entre el 30 y el 50%1,2. En general, se entiende por hiperglucemia por estrés a la aparición de hiperglucemia mantenida superior a 200mg/dl durante el padecimiento de enfermedad grave, independientemente de que la persona haya presentado o no diabetes mellitus previamente. Aunque los mecanismos causales por los que se produce no han sido totalmente aclarados, las posibles causas que se han propuesto tienen que ver con el incremento de niveles de cortisol y otras hormonas contrarreguladoras de la glucemia1,3. La resistencia a la insulina es otro posible factor relacionado, cuya incidencia en pacientes con enfermedad crítica puede llegar hasta el 80%4.
Diferentes estudios han asociado la hiperglucemia mantenida con un aumento de la mortalidad y otros resultados indeseados5–7, incluyendo aumento en el tiempo de estancia hospitalaria, aumento del tiempo en UCI y mayor incidencia de infecciones nosocomiales. Dado que la mayor parte de la evidencia disponible procede de estudios observacionales, es difícil establecer si la hiperglucemia es causante del aumento de la mortalidad o un marcador asociado a la gravedad de un determinado proceso patológico. Incluso algunos investigadores sugieren que una cierta tendencia a la hiperglucemia podría ser un factor protector en determinadas patologías o perfiles de pacientes8. En cualquier caso, la mayoría de las guías de práctica clínica usadas en nuestro entorno coinciden en que la hiperglucemia incontrolada presenta efectos potencialmente nocivos y debe ser evitada9–11. Las acciones para reducir la hiperglucemia han resultado en reducción de la mortalidad en algunos estudios, aunque no en todos12.
Esta situación propició el desarrollo de protocolos de control estricto de la glucemia en el paciente crítico, referenciados en algunas publicaciones como protocolos de insulinoterapia intensiva13–17, cuyo objetivo es mantener de forma continuada niveles de glucemia fisiológicos, entre 80 y 110mg/dl, usando para ello perfusiones de insulina rápida por vía endovenosa (EV). Diversos ensayos clínicos han mostrado, sin embargo, que el manejo de estos rangos de glucemia puede resultar complejo18–20, principalmente debido a la mayor incidencia de hipoglucemia severa (glucemia menor de 40mg/dl) que llega hasta el 19%, e hipoglucemia moderada (glucemia menor de 80mg/dl) con incidencias de hasta el 32%. Además, estos protocolos requieren una mayor frecuencia de determinaciones de glucemia y un seguimiento extremadamente riguroso. Los mencionados ensayos coinciden en relacionar la aparición de hipoglucemia grave con el aumento de la mortalidad, suponiendo por sí sola un factor de riesgo de muerte independiente de la diabetes, gravedad de la enfermedad primaria, edad, sepsis o uso de ventilación mecánica21–23.
Por esta razón, el rango objetivo de niveles de glucemia en el paciente crítico es, a día de hoy, objeto de controversia científica. La mayor parte de la comunidad científica entiende que la hiperglucemia mantenida es un efecto indeseado, pero los protocolos de insulinoterapia intensiva reportan riesgos que no han sido controlados por completo en la actualidad. Así, cada vez es más extendido el uso de protocolos con rangos más seguros en la prevención de la hipoglucemia, siendo los valores de referencia más frecuentemente utilizados: 110-150mg/dl, o bien 140-180mg/dl24. El desarrollo y la implantación de protocolos de control glucémico fiables y acordados por el equipo de salud ha cobrado un creciente interés entre los profesionales dedicados al paciente crítico. La unificación de criterios y la protocolización del control glucémico enfocados hacia la reducción de la incidencia de hipoglucemia grave pueden reducir el riesgo de muerte en el paciente que requiere cuidados intensivos25.
En los últimos años se han testado diferentes herramientas y protocolos con eficacia variable. En general, las herramientas informáticas han mostrado mayor capacidad y agilidad en el mantenimiento de rangos adecuados de glucemia y en la reducción de eventos adversos26. Sin embargo, el control riguroso de los niveles de glucosa requiere considerar gran diversidad de variables, incluyendo el control del aporte nutricional; el posible aporte de glúcidos en sueros, diluciones o fármacos; el efecto de algunos fármacos en la glucemia o en la insulina; la interferencia de pruebas diagnósticas y procedimientos terapéuticos en la administración de dieta, insulina u otros fármacos; el uso de contrastes que pueden requerir interrupciones del aporte nutricional y otras situaciones clínicas27. Además, deben tenerse en cuenta algunos aspectos técnicos relacionados con la actividad de la insulina EV, como la necesidad de uniformidad de las diluciones y concentraciones o la compatibilidad de los fármacos infundidos en una misma luz. Por último, es imprescindible asegurar la validez de las medidas de obtención de muestras de sangre para análisis de la glucemia asegurando que todas las determinaciones sean equivalentes entre sí. Todos estos factores pueden influir en el mantenimiento de los niveles diana de glucemia, resultando todas ellas variables de difícil gestión en una herramienta única27,28.
Como respuesta a esta multitud de factores, los protocolos guiados por enfermeras se han centrado en la formación, sensibilización y fortalecimiento del equipo de enfermería en la toma de decisiones y manejo de situaciones clínicas complejas para el mantenimiento de unos niveles diana de glucemia, generalmente apoyados por herramientas informáticas o calculadoras de dosis de insulina12,29.
En el presente estudio se pretende evaluar la efectividad de la implantación de un protocolo de control glucémico en UCI, en cuanto al mantenimiento de niveles diana de glucemia preestablecidos (140-180mg/dl) y la prevención de la hipoglucemia severa. También se pretende valorar el impacto en la prevención de la hiperglucemia superior a 200mg/dl (hiperglucemia severa).
MétodoEstudio cuasiexperimental prospectivo «pre-pos» realizado en una UCI polivalente de un hospital comarcal de las Islas Baleares. La unidad dispone de 6 boxes y atiende más de 200 enfermos críticos anualmente con una ocupación media superior al 80%. Se dispone de forma permanente de 3 enfermeras y 3 auxiliares de enfermería, manteniendo un ratio de 2 pacientes por enfermera durante las 24 h. La totalidad de la plantilla médica está compuesta por médicos intensivistas, disponiendo de 3 médicos en horario de mañana (8 a 15 h) y un médico el resto de la jornada.
La intervención consistió en el diseño e implementación de un protocolo basado en la evidencia, para conseguir rangos de glucemia diana entre 140-180mg/dl, apoyado en una herramienta informática de acceso público disponible en http://rccc.eu/protocolos/HG/index.html. Esta herramienta se basa en el algoritmo publicado por el grupo NICE-SUGAR en 2004, que sirve de referencia para el cálculo de dosis de insulinoterapia. Este protocolo se enmarca en un conjunto de acciones para la mejora de la seguridad clínica en cuidados intensivos de nuestro centro. La intervención se desarrolló entre septiembre y noviembre de 2015.
Para el diseño del protocolo se realizaron búsquedas bibliográficas estructuradas en bases de datos y metabuscadores de ciencias de la salud: EBSCO-HOST (Medline, CINHAL y Cochrane), PubMed, Embase, CuidenPlus y Guiasalud, usando los términos «insulina», «terapia con insulina», «cuidados críticos», «guía» y «protocolo» y los equivalentes en inglés del lenguaje Medical Subject Headings (MeSH). Se seleccionaron investigaciones de cualquier metodología cuyos objetivos trataran sobre la administración de insulina EV (comparación de alternativas terapéuticas, protocolos y guías, compatibilidad e interacciones farmacológicas, entre otros). Se elaboraron tablas descriptivas con los principales resultados de cada estudio.
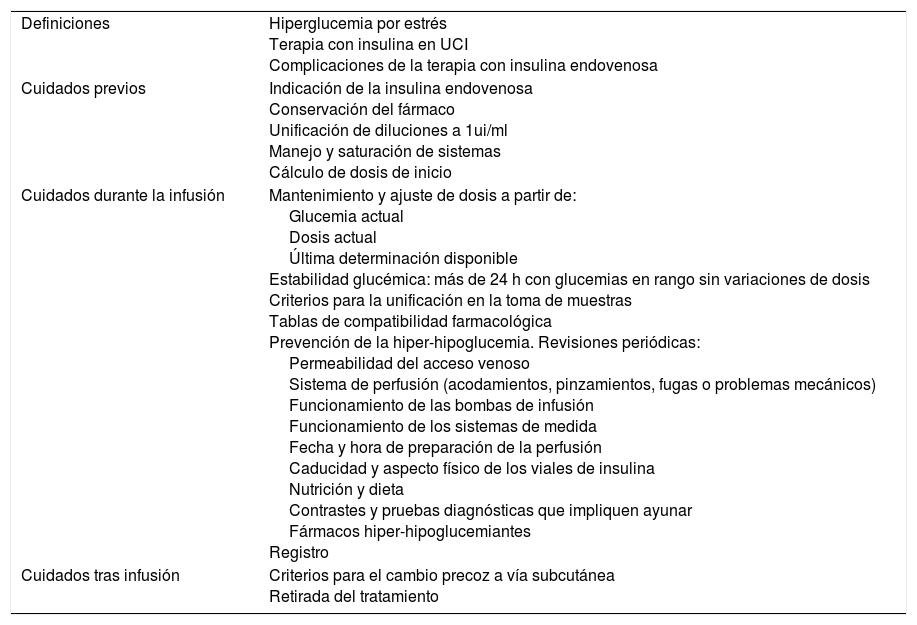
Se consensuaron de forma interdisciplinaria más de 50 actividades y recomendaciones que incluyen la preparación de la infusión, conservación, sustitución periódica de sistemas, algoritmos de cálculo de dosis, tablas de compatibilidad farmacológica, criterios de uniformidad en la toma de muestras, criterios para la toma de decisiones por las enfermeras, interrelaciones con protocolos de dietoterapia y acciones de prevención de complicaciones, estableciendo como criterio de resultado el mantenimiento de glucemias entre 140 y 180mg/dl. En este proceso participaron 4 enfermeras, 2 médicos intensivistas y una farmacéutica. Posteriormente las acciones consensuadas en el protocolo fueron revisadas por el equipo de seguridad del paciente en UCI. La versión final fue validada por la comisión hospitalaria de cuidados asistenciales. La tabla 1 resume el contenido más relevante incluido en esta versión definitiva.
Resumen de contenidos del protocolo asistencial
| Definiciones | Hiperglucemia por estrés Terapia con insulina en UCI Complicaciones de la terapia con insulina endovenosa |
| Cuidados previos | Indicación de la insulina endovenosa Conservación del fármaco Unificación de diluciones a 1ui/ml Manejo y saturación de sistemas Cálculo de dosis de inicio |
| Cuidados durante la infusión | Mantenimiento y ajuste de dosis a partir de: Glucemia actual Dosis actual Última determinación disponible Estabilidad glucémica: más de 24 h con glucemias en rango sin variaciones de dosis Criterios para la unificación en la toma de muestras Tablas de compatibilidad farmacológica Prevención de la hiper-hipoglucemia. Revisiones periódicas: Permeabilidad del acceso venoso Sistema de perfusión (acodamientos, pinzamientos, fugas o problemas mecánicos) Funcionamiento de las bombas de infusión Funcionamiento de los sistemas de medida Fecha y hora de preparación de la perfusión Caducidad y aspecto físico de los viales de insulina Nutrición y dieta Contrastes y pruebas diagnósticas que impliquen ayunar Fármacos hiper-hipoglucemiantes Registro |
| Cuidados tras infusión | Criterios para el cambio precoz a vía subcutánea Retirada del tratamiento |
El proceso de implementación siguió el modelo descrito en la guía de implementación de la Registered Nurses's Association of Ontario30, que ha sido utilizado en diferentes entornos a nivel internacional. Se realizaron sesiones formativas multidisciplinarias, acompañamiento de profesionales en la práctica y seguimiento de casos complejos o dudosos. También se puso a disposición de los profesionales una dirección de correo grupal y se colocó un buzón para la recogida anónima de opiniones de los integrantes del equipo de salud. Las opiniones relevantes se utilizaron para incorporar cambios o correcciones en el protocolo. Las acciones de implementación fueron lideradas por enfermeras y desarrolladas en un equipo multidisciplinar.
La puesta en funcionamiento del protocolo supuso que todas las intervenciones y decisiones derivadas del manejo de la infusión de insulina EV, a excepción de la prescripción del inicio de perfusión, fueran realizadas por la enfermera responsable del paciente. En caso de necesidad, la enfermera podía consultar al médico intensivista o al servicio de farmacia.
Para la evaluación, se incluyeron de forma consecutiva todos los pacientes adultos que precisaban tratamiento con insulina EV por hiperglucemia en el contexto de enfermedad crítica de cualquier origen, para lo cual era necesaria la aparición de hiperglucemia superior a 180mg/dl en al menos 2 determinaciones independientes. Se excluyeron pacientes con dieta oral o con alimentación enteral a dosis estables, puesto que son candidatos a recibir insulinización subcutánea de forma precoz.
Para el cálculo del tamaño de la muestra se ha usado como referencia el ensayo clínico publicado por Praiser en 200920, que utilizaba en una de sus ramas el mismo rango diana de glucemia que proponemos para nuestro protocolo, resultando una incidencia de hipoglucemia grave del 2,7%. Así, aceptando un riesgo alfa de 0,05 y un riesgo beta de 0,2 en un contraste bilateral, se precisaba un mínimo de 43 sujetos en cada fase para detectar como estadísticamente significativa la diferencia entre dos proporciones, que para el grupo 1 se esperaba que fuera de 0,27 y el grupo 2 de 0,05. Se estimó una tasa de pérdidas de seguimiento del 10%. Se utilizó la aproximación del Arcoseno. Para estimar el tiempo necesario de observación se realizó una revisión retrospectiva de los registros enfermeros entre los meses de marzo y junio de 2014.
Se evaluaron variables demográficas (edad y sexo) así como diversas condiciones del proceso de salud:
Motivo de ingreso agrupado por categorías diagnósticas de la Clasificación Internacional de Enfermedades (CIE-10).
Motivo de alta.
Duración de la estancia.
Escalas de gravedad del proceso crítico: Acute Physiology and Chronic Health Evaluation II (APACHE II) y Simplified Acute Physiology Score (SAPS III).
Variables del proceso patológico potencialmente asociadas con la hiperglucemia: shock de cualquier origen, cirugía reciente (tiempo posquirúrgico inmediato), sepsis o infección grave y enfermedad metabólica.
Se registró el valor de glucemia de todos los test glucémicos realizados a cada paciente incluido en la muestra desde noviembre de 2014 a agosto de 2015 (preintervención) y desde noviembre de 2015 a agosto de 2016 (postintervención). Las muestras fueron extraídas de catéter venoso o arterial tras desechar entre 4 y 5ml de sangre. También se incluyeron muestras de origen capilar en aquellos pacientes en que se comprobaba que la diferencia con respecto a las muestras venosas era inferior a ±10mg/dl. El diseño del protocolo se inició en la fase preintervención y las acciones de difusión e implementación se realizaron progresivamente entre mayo y noviembre de 2015. La herramienta informática de apoyo al cálculo de dosis se utilizó desde el inicio de la observación, antes de la fase preintervención.
Los datos fueron extraídos de la historia clínica informatizada del paciente, donde las enfermeras registran su actividad en cada turno de trabajo. La información se volcó progresivamente en una hoja de Microsoft Excel para su posterior análisis.
Las variables principales de análisis incluyeron las proporciones de determinaciones glucémicas dentro de rango, tasas de hipoglucemia grave (inferior a 40mg/dl) y tasas de hiperglucemia superior a 200mg/dl, siguiendo criterios de las guías de referencia31.
La explotación de datos se realizó con el programa Epidat 4.1. Se realizó un análisis descriptivo de todas las variables de estudio, utilizando media y desviación estándar para las variables continuas, y frecuencias y porcentajes para las variables categóricas. En variables continuas, se realizó la prueba de Kolmogorov-Smirnov para comprobar la normalidad en la distribución. La comparación entre los periodos de estudio se realizó mediante la t de Student para variables continuas y χ2 para nominales. La significación estadística se estableció con valores de p inferiores a 0,05.
El proyecto fue aprobado por el comité de investigación del hospital. Los autores declaran la ausencia de conflictos de intereses.
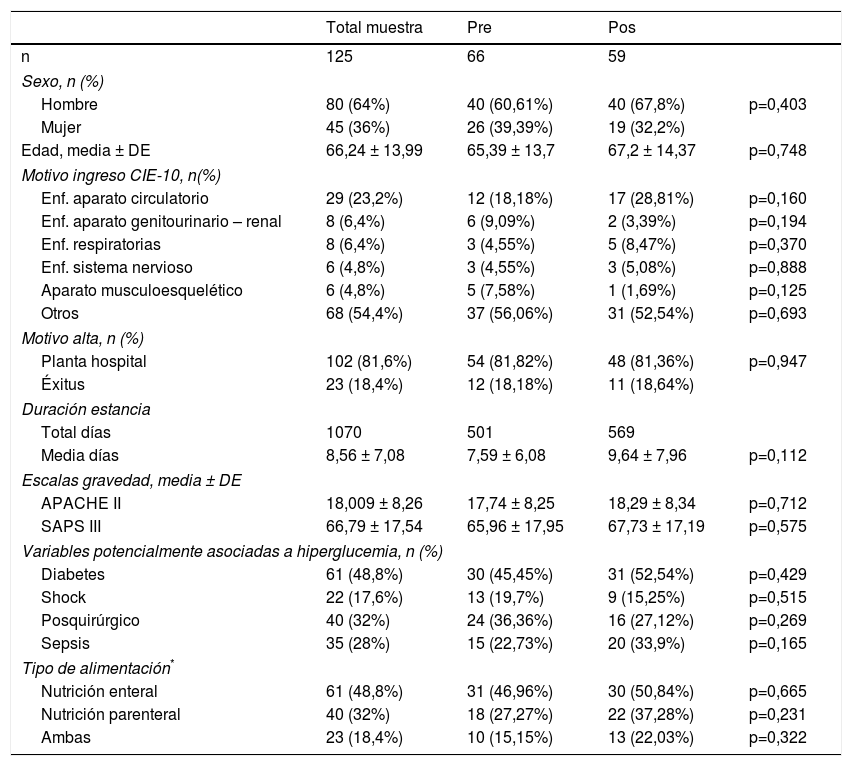
ResultadosSe evaluaron 7864 determinaciones de glucemia pertenecientes a 125 pacientes, 66 preintervención y 59 postintervención. Los grupos pre- y postintervención resultaron homogéneos. No se identificaron diferencias significativas en cuanto a la gravedad del proceso crítico o la incidencia de circunstancias potencialmente relacionadas con la aparición de hiperglucemia por estrés. La distribución de edad, sexo, diabetes, shock y otras variables de ajuste resultó similar en ambos grupos (tabla 2).
Características de los pacientes
| Total muestra | Pre | Pos | ||
|---|---|---|---|---|
| n | 125 | 66 | 59 | |
| Sexo, n (%) | ||||
| Hombre | 80 (64%) | 40 (60,61%) | 40 (67,8%) | p=0,403 |
| Mujer | 45 (36%) | 26 (39,39%) | 19 (32,2%) | |
| Edad, media ± DE | 66,24 ± 13,99 | 65,39 ± 13,7 | 67,2 ± 14,37 | p=0,748 |
| Motivo ingreso CIE-10, n(%) | ||||
| Enf. aparato circulatorio | 29 (23,2%) | 12 (18,18%) | 17 (28,81%) | p=0,160 |
| Enf. aparato genitourinario – renal | 8 (6,4%) | 6 (9,09%) | 2 (3,39%) | p=0,194 |
| Enf. respiratorias | 8 (6,4%) | 3 (4,55%) | 5 (8,47%) | p=0,370 |
| Enf. sistema nervioso | 6 (4,8%) | 3 (4,55%) | 3 (5,08%) | p=0,888 |
| Aparato musculoesquelético | 6 (4,8%) | 5 (7,58%) | 1 (1,69%) | p=0,125 |
| Otros | 68 (54,4%) | 37 (56,06%) | 31 (52,54%) | p=0,693 |
| Motivo alta, n (%) | ||||
| Planta hospital | 102 (81,6%) | 54 (81,82%) | 48 (81,36%) | p=0,947 |
| Éxitus | 23 (18,4%) | 12 (18,18%) | 11 (18,64%) | |
| Duración estancia | ||||
| Total días | 1070 | 501 | 569 | |
| Media días | 8,56 ± 7,08 | 7,59 ± 6,08 | 9,64 ± 7,96 | p=0,112 |
| Escalas gravedad, media ± DE | ||||
| APACHE II | 18,009 ± 8,26 | 17,74 ± 8,25 | 18,29 ± 8,34 | p=0,712 |
| SAPS III | 66,79 ± 17,54 | 65,96 ± 17,95 | 67,73 ± 17,19 | p=0,575 |
| Variables potencialmente asociadas a hiperglucemia, n (%) | ||||
| Diabetes | 61 (48,8%) | 30 (45,45%) | 31 (52,54%) | p=0,429 |
| Shock | 22 (17,6%) | 13 (19,7%) | 9 (15,25%) | p=0,515 |
| Posquirúrgico | 40 (32%) | 24 (36,36%) | 16 (27,12%) | p=0,269 |
| Sepsis | 35 (28%) | 15 (22,73%) | 20 (33,9%) | p=0,165 |
| Tipo de alimentación* | ||||
| Nutrición enteral | 61 (48,8%) | 31 (46,96%) | 30 (50,84%) | p=0,665 |
| Nutrición parenteral | 40 (32%) | 18 (27,27%) | 22 (37,28%) | p=0,231 |
| Ambas | 23 (18,4%) | 10 (15,15%) | 13 (22,03%) | p=0,322 |
APACHE II: Acute Physiology and Chronic Health Evaluation II; DE: desviación estándar; SAPS III: Simplified Acute Physiology Score.
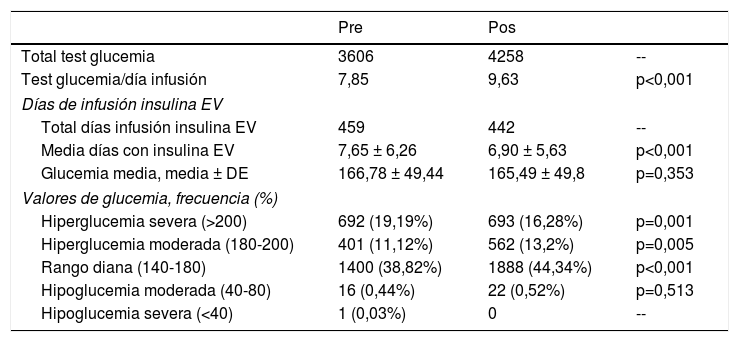
Se identificó un solo caso de hipoglucemia severa, que sucedió en el grupo preintervención y no produjo efectos observables en el paciente. La proporción de determinaciones dentro del rango diana fue superior en el grupo postintervención (38,82 vs. 44,34 p<0,001). La tasa de hiperglucemia severa también resultó menor en el grupo postintervención (19,19 vs. 16,28 p=0,001). También se observó una reducción no significativa en la glucemia media tras la intervención (166,78±49,44 vs. 165,49 ±49,8). El número de determinaciones diarias realizadas para el control glucémico resultó superior en el grupo postintervención. La tabla 3 muestra los resultados agrupados de los test de glucemia en ambos periodos.
Resultados del control glucémico
| Pre | Pos | ||
|---|---|---|---|
| Total test glucemia | 3606 | 4258 | -- |
| Test glucemia/día infusión | 7,85 | 9,63 | p<0,001 |
| Días de infusión insulina EV | |||
| Total días infusión insulina EV | 459 | 442 | -- |
| Media días con insulina EV | 7,65 ± 6,26 | 6,90 ± 5,63 | p<0,001 |
| Glucemia media, media ± DE | 166,78 ± 49,44 | 165,49 ± 49,8 | p=0,353 |
| Valores de glucemia, frecuencia (%) | |||
| Hiperglucemia severa (>200) | 692 (19,19%) | 693 (16,28%) | p=0,001 |
| Hiperglucemia moderada (180-200) | 401 (11,12%) | 562 (13,2%) | p=0,005 |
| Rango diana (140-180) | 1400 (38,82%) | 1888 (44,34%) | p<0,001 |
| Hipoglucemia moderada (40-80) | 16 (0,44%) | 22 (0,52%) | p=0,513 |
| Hipoglucemia severa (<40) | 1 (0,03%) | 0 | -- |
DE: desviación estándar; EV: endovenosa.
Nuestra experiencia muestra que una intervención de implementación de recomendaciones basadas en la evidencia puede resultar efectiva para mejorar el control glucémico en pacientes críticos que precisan insulina EV.
La tasa de hipoglucemia observada resultó muy inferior a estudios previos en ambos periodos de observación ya que el único caso observado ocurrió en la fase preintervención y supuso un 0,03% de incidencia en este grupo, muy por debajo de la mayoría de las series publicadas18,20,32. La herramienta informática resultó útil para la prevención de la principal complicación en estos pacientes y causa independiente de mortalidad. Entendemos que la eficacia de esta herramienta en la prevención de la hipoglucemia severa no dependió solamente del proceso de implementación, sino también del uso de un rango objetivo de 140-180mg/dl que resulta alejado de los valores de riesgo, concediendo mayor margen para la prevención de hipoglucemias y resultando, por tanto, más seguro. Los riesgos atribuibles a la hipoglucemia secundaria al tratamiento con insulina EV pueden reducirse implementando algoritmos terapéuticos adecuados, minimizando errores de monitorización y evitando la sobrecorrección de la hipoglucemia.
La mejora obtenida en las tasas de glucemia dentro de rango resultó muy similar a un estudio previo publicado en 2011 por Khalaila et al.33, que mostró una mejora en la glucemia diana del 10,2% usando un rango de glucemia objetivo de 110-149mg/dl. Otros estudios previos consiguieron mayores tasas de glucemias dentro de rango diana aunque también presentaron mayor aparición de hipoglucemia severa29,34,35. Esto orienta a la necesidad de realizar controles glucémicos muy frecuentes que permitan constantes adaptaciones en la dosificación. Así, los protocolos de control glucémico deben ser lo suficientemente flexibles para resultar realmente seguros en la prevención de la hipoglucemia severa. En nuestro caso, hemos optado por la implantación de medidas que aumenten la seguridad del paciente para, en un futuro, plantear acciones de mejora de su eficacia y mantenimiento en el tiempo.
Nuestro protocolo supuso un aumento significativo de los controles realizados, lo que podría entenderse como un marcador de la adherencia de las enfermeras clínicas al procedimiento. No obstante, el número de controles resulta inferior a los realizados en la mayoría de los estudios previos20,27,36. Esta situación puede deberse a las medidas incluidas en nuestro protocolo para evitar controles innecesarios que conllevan a su vez manipulación y riesgos añadidos. Así, en caso de estabilidad glucémica mantenida durante más de 24 h, el tiempo entre controles podía ser aumentado hasta 6 h si no existían cambios en los aportes glucémicos a través de nutrición o sueroterapia, administración de contrastes, cambios de dosis de fármacos que interaccionan con la insulina o cambios en el estado general del paciente y el tratamiento en curso. De esta forma, nuestro protocolo supone una mejora en la seguridad del paciente y aporta mayor seguridad legal en la toma de decisiones clínicas por parte de las enfermeras asistenciales.
El consenso multidisciplinario resultó clave para impulsar algunas de las medidas incluidas en el protocolo. Fomentar el trabajo en equipo es fundamental para favorecer una cultura de seguridad clínica37,38 y sus beneficios pueden ir mucho más allá de los observados en esta experiencia. Este campo no está, sin embargo, exento de complejidad, siendo conveniente establecer acciones mantenidas en el tiempo para fomentar la colaboración interdisciplinar y la toma de decisiones compartidas39, en que se incluya al paciente y su familia como parte integrante del equipo de salud.
Al igual que en otras intervenciones multidisciplinares lideradas por enfermeras40, el liderazgo y autonomía en la toma de decisiones resultó clave en la intervención, puesto que además de una monitorización estricta del paciente, perimió realizar adaptaciones frecuentes de la insulinoterapia en función de situaciones clínicas o del tratamiento.
En cuanto a las limitaciones, cabe señalar que el diseño, los métodos de implantación de evidencias y la eficacia de las intervenciones están muy condicionados por el contexto en que se pretenden implantar, lo que limita su generalización. En este sentido, algunos aspectos concretos del protocolo dependen de las preferencias y acuerdos del equipo de salud a la hora de cuidar o tratar al paciente, por lo que su formato puede requerir cambios o matizaciones para adaptarse a otros centros o unidades.
El tamaño muestral obtenido puede resultar limitado para la generalización de resultados. Por ello, el tiempo de observación se prolongó 9 meses tras la intervención, aunque no se puede conocer el impacto a más largo plazo de las recomendaciones incluidas en el protocolo o el mantenimiento de las mismas tras la rotación de personal asistencial y posibles cambios en la estructura de liderazgo de la unidad.
Por otro lado, al no existir información previa sobre la incidencia de hiperglucemia e hipoglucemia en nuestro centro, no es posible el abordaje con metodologías que permitan la comparación de la eficacia del protocolo con un estado basal. Así mismo, algunas variables potencialmente confusoras como el uso de fármacos hiperglucemiantes no han podido ser incluidas en el análisis de homogeneidad de la muestra.
Nuestra intervención ha producido un impacto positivo en la eficacia del control glucémico en UCI, lo que potencialmente redunda en la seguridad del paciente. Por ello, nuestro estudio puede ayudar al diseño y mejora de protocolos de actuación en el control de la hiperglucemia del paciente crítico liderados por enfermeras, así como a la reducción de la variabilidad clínica.
ConclusionesCon la implementación del protocolo guiado por enfermeras se obtuvieron mejores tasas de glucemia dentro de rango en el grupo postintervención. Por otro lado, en este grupo hubo un menor número de hiperglucemias severas sin que se observara ningún caso de hipoglucemia inferior a 40mg/dl.
Nuestro estudio muestra que una intervención multidisciplinar liderada por enfermeras puede resultar segura y eficaz para el control de la hiperglucemia del paciente crítico.
FinanciaciónEste estudio recibió una beca de investigación del Colegio Oficial de Enfermería de las Islas Baleares (556/14). La entidad financiadora no intervino en ninguna fase de la investigación.
Estudio financiado por el Colegio Oficial de Enfermería de las Islas Baleares (556/2014).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos la colaboración de los profesionales de la Unidad de Cuidados Intensivos del Hospital Manacor y del Colegio Oficial de Enfermería de las Islas Baleares (COIBA).