Haemophilus influenzae (Hi) representaba la segunda causa de neumonía, sepsis y meningitis bacteriana en menores de 5 años en la era prevacunal1. Su incidencia disminuyó drásticamente en España tras la introducción de la vacuna conjugada frente a Hi en el año 2001. Las vacunas disponibles en nuestro medio utilizan el polisacárido polirribosil ribitol fosfato conjugado en su mayoría a toxoide tetánico2.
Presentamos el caso de una lactante sana de 9 meses de edad, con calendario vacunal completo, incluyendo 2 dosis de vacuna conjugada frente a Hi (2 y 4 meses). Consulta en Urgencias por fiebre de 48h de duración, asociada a vómitos, decaimiento y rechazo de tomas. Presenta mal estado general, con tono y fuerza disminuidos, sin exantema ni petequias. Analíticamente se observan 25.890 leucocitos/mm3 con 83% de neutrófilos y elevación de proteína C reactiva (161,9mg/l) y procalcitonina (49,03ng/ml). El líquido cefalorraquídeo fue turbio, con 2.460 células/mm3 (95% polimorfonucleares) e hipoglucorraquia (19mg/dl). Se inicia tratamiento con cefotaxima, vancomicina y dexametasona. En hemocultivo y cultivo de líquido cefalorraquídeo se aísla Hi serotipo b (Hib). Presenta fiebre persistente, realizándose resonancia magnética, donde se visualizan empiemas subdurales milimétricos bifrontales. Se descarta asplenia con una ecografía abdominal. Es valorada por Otorrinolaringología y Neurología, descartando problemas auditivos y neurológicos. La paciente queda afebril el día 12 de ingreso. Se completan 4 semanas de antibioterapia intravenosa.
Se realiza estudio inmunológico, encontrándose títulos de IgG bajos frente a neumococo. El resto de las pruebas, incluyendo subpoblaciones linfocitarias, expresión de moléculas HLA de clase i y ii, proliferación con mitógenos, inmunoglobulinas, respuesta vacunal a tétanos y CH50, fueron normales. Tras el alta la paciente evoluciona favorablemente, con desarrollo psicomotor y potenciales evocados auditivos normales. A las 7 semanas se realiza resonancia magnética, con resolución de los empiemas.
La paciente presentó enfermedad invasiva por Hib de acuerdo con la definición del Centro Europeo para la Prevención y el Control de las Enfermedades, que incluye los casos de infección sistémica con aislamiento de Hi o sus ácidos nucleicos en una localización habitualmente estéril3.
En el caso presentado, la paciente desarrolló sepsis y meningitis a pesar de estar correctamente vacunada para su edad, por lo que se trata de un verdadero fallo vacunal (TVF, por true vaccine failure). Este se define como la presencia de enfermedad invasiva por Hib al menos 2 semanas después de haber administrado una dosis de vacuna en mayores de un año o al menos una semana después de haberse administrado≥2 dosis de la vacuna antes de los 12 meses de vida4,5, como ocurre en esta paciente.
La incidencia de TVF en Hib es muy baja y se ha relacionado con distintos factores: prematuridad, alteración inmunológica (incluyendo inmunodeficiencias humorales, retraso en la maduración del sistema inmune con inmunoglobulinas bajas para la edad y escasa avidez de anticuerpos antipolirribosil ribitol fosfato), razones técnicas (alteraciones en la administración y/o conservación de la vacuna, empleo de distintas proteínas transportadoras), circulación persistente del microorganismo en la comunidad, movilidad de poblaciones con casos importados, o influencia de factores genéticos o raciales5–9. En nuestro caso, el estudio inmunológico fue normal y no identificamos ningún otro factor causal de TVF, aunque no se pudo estudiar la avidez de los anticuerpos antipolirribosil ribitol fosfato al no estar el test disponible actualmente en nuestro medio.
Realizamos una revisión de los casos de enfermedad invasiva por Hi registrados en la Comunidad de Madrid entre los años 2001-201910. Se identificaron 202, 156 en adultos y 46 en niños (tabla 1). El 78% de los casos pediátricos (36/46) afectó a menores de 5 años, 8 fueron causados por Hib (17,4%) y 6 cumplían criterios de TVF, apareciendo 5 de ellos en los últimos 8 años. Esto corresponde a una incidencia anual de enfermedad invasiva por Hi y por Hib de 0,254 y 0,044 casos por 100.000 habitantes, respectivamente, en niños menores de 14 años.
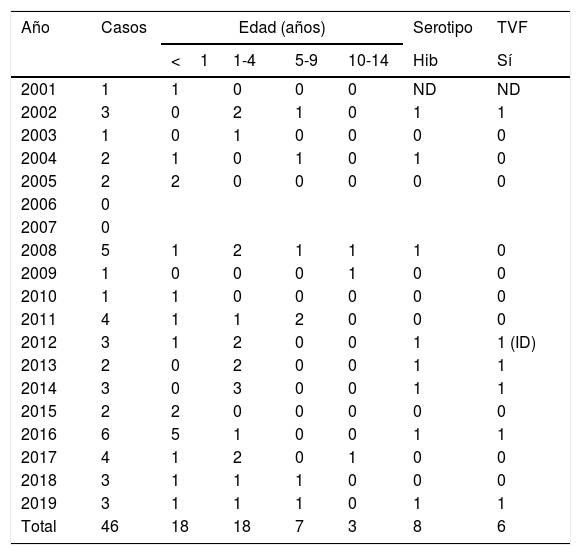
Resumen de casos de enfermedad invasiva por Haemophilus influenzae en menores de 14 años en la Comunidad de Madrid en el periodo 2001-2019
| Año | Casos | Edad (años) | Serotipo | TVF | |||
|---|---|---|---|---|---|---|---|
| <1 | 1-4 | 5-9 | 10-14 | Hib | Sí | ||
| 2001 | 1 | 1 | 0 | 0 | 0 | ND | ND |
| 2002 | 3 | 0 | 2 | 1 | 0 | 1 | 1 |
| 2003 | 1 | 0 | 1 | 0 | 0 | 0 | 0 |
| 2004 | 2 | 1 | 0 | 1 | 0 | 1 | 0 |
| 2005 | 2 | 2 | 0 | 0 | 0 | 0 | 0 |
| 2006 | 0 | ||||||
| 2007 | 0 | ||||||
| 2008 | 5 | 1 | 2 | 1 | 1 | 1 | 0 |
| 2009 | 1 | 0 | 0 | 0 | 1 | 0 | 0 |
| 2010 | 1 | 1 | 0 | 0 | 0 | 0 | 0 |
| 2011 | 4 | 1 | 1 | 2 | 0 | 0 | 0 |
| 2012 | 3 | 1 | 2 | 0 | 0 | 1 | 1 (ID) |
| 2013 | 2 | 0 | 2 | 0 | 0 | 1 | 1 |
| 2014 | 3 | 0 | 3 | 0 | 0 | 1 | 1 |
| 2015 | 2 | 2 | 0 | 0 | 0 | 0 | 0 |
| 2016 | 6 | 5 | 1 | 0 | 0 | 1 | 1 |
| 2017 | 4 | 1 | 2 | 0 | 1 | 0 | 0 |
| 2018 | 3 | 1 | 1 | 1 | 0 | 0 | 0 |
| 2019 | 3 | 1 | 1 | 1 | 0 | 1 | 1 |
| Total | 46 | 18 | 18 | 7 | 3 | 8 | 6 |
ID: inmunodeficiencia; Hib: Haemophilus influenzae tipo b; ND: no disponible; TVF: fallo vacunal verdadero.
En conclusión, aunque la vacuna conjugada frente a Hib es muy efectiva, se producen algunos casos de TVF5. En estos pacientes se recomienda una evaluación completa, incluyendo estudio inmunológico2. Sin embargo, en la mayoría no se identifica una inmunodeficiencia humoral subyacente6 y, como ocurre en el caso presentado y en los registrados en las últimas 2 décadas en la Comunidad de Madrid, no se puede establecer la causa del fallo vacunal.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.