En estas casi tres décadas de epidemia de infección por VIH, se han ido desarrollando estrategias para disminuir el riesgo de transmisión cuando una persona no infectada se pone en contacto con el VIH. Uno de los hitos clave fue la demostración de que la utilización de zidovudina desde el segundo trimestre de embarazo, durante el parto y durante unas semanas en el recién nacido disminuyó el riesgo de trasmisión vertical de la infección por VIH de 25 a 8%. Posteriormente, estas estrategias se han ido perfeccionando hasta conseguir tasas de transmisión vertical por debajo del 1%. Casi de una forma simultánea se han ido desarrollando estrategias para intentar disminuir el riesgo de transmisión de la infección tras accidentes ocupacionales laborales, y en los últimos años la profilaxis postexposición no ocupacional ha sido un campo de especial preocupación. Incluso en este último año se han publicando distintas experiencias de profilaxis preexposición que están generando un intenso debate sobre su aplicabilidad. En este artículo sintetizamos el estado del arte en la prevención de transmisión vertical y la profilaxis postexposición ocupacional y no ocupacional, desde una perspectiva de aplicación en el mundo desarrollado. Revisamos asimismo, los datos publicados respecto a profilaxis preexposición.
In these almost thirty years since the epidemic of HIV infection strategies have been developed to decrease the transmission risk when a non-infected person comes into contact with HIV. One of the key landmarks was the use zidovudine was shown to reduce the risk of HIV infection by vertical transmission from 25% to 8% when given from the second trimester of pregnancy, during partum and for several weeks in the newborn. These strategies have been subsequently perfected until achieving vertical transmission rates less than 1%. Almost at the same time, strategies have been developed in an attempt to reduce the risk of transmission of infection after occupational accidents and, in the last few years prophylaxis after non-occupational exposure has been a field of particular concern. Even in this past year several experiments on pre-exposure prophylaxis have been published, which are generating an intense debate on is applicability. In this article, we analyse the state of the art in the prevention of vertical transmission and occupational and non-occupational prophylaxis, from a perspective of applying this in the developed world. We also review the published data on pre-exposure prophylaxis.
A pesar de que lo más importante en prevención de la infección por VIH es, precisamente implementar todas las medidas necesarias para impedir su adquisición: aplicación de precauciones universales en la atención a pacientes; evitar el embarazo en las mujeres infectadas por VIH; métodos de barrera en las relaciones sexuales, entre otros, la realidad indica que: a) los accidentes ocupacionales, a pesar de todas las precauciones son, de alguna forma, inherentes a la práctica clínica; b) muchas mujeres infectadas por VIH tienen descendencia, especialmente en países en vías de desarrollo, y c) que a pesar de las campañas preventivas respecto a sexo seguro, las relaciones sexuales no protegidas en parejas serodiscordantes (esto es, parejas en las que un miembro de la pareja está infectado y otro no) son un hecho demasiado frecuente, especialmente en algunos colectivos como en hombres que practican sexo con hombres (HSH). Por otro lado, las agresiones sexuales son una desagradable realidad que precisan, entre otras respuestas, de políticas preventivas.
En estas casi tres décadas de epidemia de infección por VIH, se han ido desarrollando estrategias en un intento de disminuir el riesgo de transmisión cuando, en algunas de las circunstancias antedichas, una persona no infectada se pone en contacto con el VIH. El aldabonazo de salida de estas estrategias fue la demostración de que la utilización de zidovudina desde el segundo trimestre de embarazo, durante el parto y durante unas semanas en el recién nacido disminuyó el riesgo de trasmisión vertical de la infección por VIH de 25 a 8%1. Posteriormente estas estrategias se han ido perfeccionando hasta conseguir tasas de transmisión vertical por debajo del 1%. Casi de una forma simultánea se han ido desarrollando estrategias para intentar disminuir el riesgo de transmisión de la infección tras accidentes ocupacionales y, en los últimos años, la profilaxis postexposición no ocupacional ha sido un campo de especial preocupación.
En este artículo, sintetizamos el estado del arte en la prevención de transmisión vertical y la profilaxis postexposición ocupacional y no ocupacional. Toda la información (incluida la de prevención de transmisión vertical), se recoge desde una perspectiva de aplicación en el mundo desarrollado. Por razones de espacio no hemos abordado la prevención de transmisión vertical en países en vías de desarrollo por lo que la información aportada debe utilizarse en el contexto de países desarrollados como el nuestro.
Prevención de la transmisión vertical del VIHSe estima que a finales de 2009 vivían en el mundo 33,3 millones de personas infectadas por el VIH, de las cuales aproximadamente la mitad son mujeres en edad fértil2. Diferentes estudios perinatales han calculado, que dejando el VIH a su evolución natural las tasas de transmisión vertical (TV) oscilarían entre un 13 y un 48% según si las madres amamantaban o no a los recién nacidos y según el lugar del estudio3. La TV disminuyó drásticamente en el mundo desarrollado con el uso de zidovudina (ZDV) en el embarazo, parto y en el recién nacido, y posteriormente con el tratamiento antirretroviral de gran actividad (TAR)4. A pesar de ello, se estima que en 2009, alrededor de 370.000 niños (220.000-520.000) contrajeron el VIH en el período perinatal y durante la lactancia2, la inmensa mayoría en países subdesarrollados. En Europa sin embargo, la tasa de TV ha disminuido, desde un 15,5% antes de 1994 a cifras menores al 1% con las medidas actuales5.
El principal factor de riesgo para la TV del VIH es la carga viral plasmática (CVP) en la madre > 1.000 copias/ml (OR=12,1). Otros factores que aumentan el riesgo son la ausencia de TAR, el parto pretérmino, los CD4 < 200 células/μL, la no realización de cesárea electiva y la ausencia de tratamiento con ZDV en el parto y en el recién nacido5.
Deseo reproductivoLa mejoría en la supervivencia y la calidad de vida de los pacientes infectados por el VIH ha motivado un interés creciente de éstos por la posibilidad de tener hijos. Si bien ningún método actual garantiza un riesgo nulo de transmisión, éste disminuye de forma importante cuando el miembro de la pareja infectado recibe TAR y presenta CVP indetectable (definida como < 50 copias/ml). Sin embargo, es importante insistir en que «ninguna técnica o tratamiento garantiza la ausencia de transmisión», ya que, aunque la CVP sea indetectable, ello no indica necesariamente que ocurra lo mismo en el tracto genital6.
Si finalmente la opción de la pareja es tener descendencia, se deben descartar en ambos miembros de la pareja otras infecciones de transmisión sexual (ITS). En el caso del miembro infectado es aconsejable que se encuentre en condiciones óptimas, es decir, tomando TAR con buen nivel de CD4 y con CVP indetectable. Por último, siempre que vayan a utilizarse técnicas de reproducción asistida se recomienda la realización de estudios de fertilidad previos.
Hombre VIH+ y mujer VIH−En estos casos se recomienda el lavado seminal, que consiste en separar los espermatozoides (que carecen de receptores para el virus) del resto de componentes del semen. En la muestra resultante se descarta la presencia de partículas virales mediante reacción en cadena de la polimerasa (PCR) y se utiliza posteriormente para realizar alguna de las dos técnicas de reproducción asistida recomendadas: la inseminación intrauterina (IIU) o la fecundación in vitro con microinyección espermática (FIV-ICSI). No hay consenso acerca de cuál de ellas es más adecuada y no se han documentado casos de TV con ninguna de las dos7,8. Algunos autores9 han señalado que el riesgo de transmisión horizontal es muy bajo si se dan las siguientes circunstancias («todas»): miembro de la pareja infectada con TAR y CVP indetectable mantenidamente en el tiempo, ausencia de infecciones de transmisión sexual en ambos miembros y pareja monógama. Se ha sugerido, que en estas circunstancias se podría informar a la pareja de la posibilidad de previo estudio de fertilidad en ambos miembros intentar una concepción natural mediante relaciones no protegidas durante los días fértiles10. Sin embargo, existe controversia respecto al riesgo de una recomendación generalizada en este sentido11 ante el riesgo de banalización de un riesgo pequeño, pero real.
Mujer VIH+ y hombre VIH−La mujer en este caso puede inyectarse el semen de su pareja obtenido tras relación sexual con preservativo. Si no se consigue la gestación, estarían indicadas técnicas de reproducción asistida como la IIU o FIV.
Hombre y mujer VIH+Si ambos tienen un virus con patrón de resistencias similar, puede aconsejarse el método reproductivo natural. Si no es así, habrá que aplicar las recomendaciones previas según cuál de los dos miembros tenga riesgo de reinfección.
Diagnóstico de la infección VIH en mujeres gestantesDebe indicarse la serología de VIH en la primera visita al ginecólogo de toda mujer gestante y debe ofrecerse a toda mujer con deseo reproductivo.
En las mujeres seronegativas con prácticas de riesgo o con pareja VIH+, debería repetirse en cada trimestre de la gestación, pero sobre todo en el tercer trimestre, antes de la semana 3612,13. Si la mujer llega al parto sin que haya constancia de haberse realizado la serología frente a VIH, está indicada una prueba rápida de detección.
Recomendaciones en la mujer gestante VIH+ (tablas 1 y 2)Recomendaciones acerca del tratamiento antirretroviralSe recomienda TAR a todas las gestantes VIH+, independientemente de su situación inmunovirológica. Si la mujer no llevaba tratamiento previamente al embarazo, está indicado iniciarlo entre las semanas 10 y 14 porque la mayoría de los casos de TV se dan en las últimas semanas de gestación. Disminuye así el riesgo teratogénico y se evitan las primeras semanas en que son más frecuentes las náuseas. Está indicada la realización de un test de resistencias en toda paciente naïve o con CVP detectable (> 500-1.000 copias/mL) a pesar de tratamiento, previo al inicio de un tratamiento antirretroviral nuevo.
Se recomienda el tratamiento con dos análogos de nucleósidos (AN) junto con un inhibidor de la proteasa (IP) o un no análogo de nucleósidos (NN) teniendo en cuenta las siguientes consideraciones (tablas 1 y 2): a) zidovudina (ZDV) debe ser siempre un componente de la triple terapia salvo efecto secundario grave o resistencia documentada; b) en caso de que la mujer llevara tratamiento sin ZDV previamente a la gestación y se encontrara con CVP indetectable se podría valorar el mantenimiento de su tratamiento original; c) la combinación de AN con la que existe más experiencia es zidovudina/lamivudina (ZDV + 3TC), y d) la asociación de didanosina (ddI) y estavudina (d4T) está contraindicada por el riesgo de acidosis láctica potencialmente mortal en la madre.
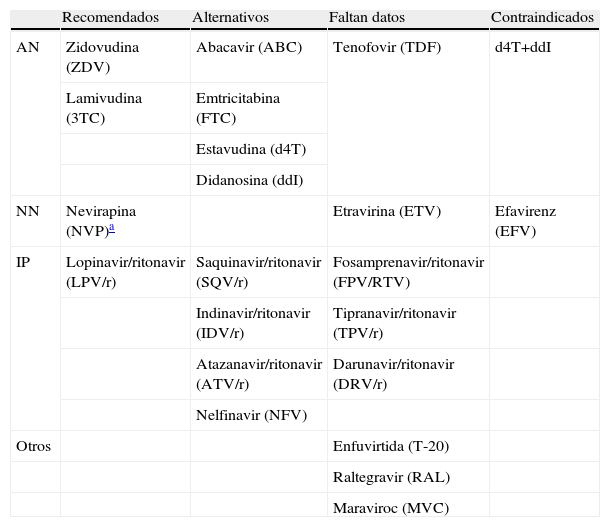
Fármacos antirretrovirales recomendados durante la gestación
| Recomendados | Alternativos | Faltan datos | Contraindicados | |
| AN | Zidovudina (ZDV) | Abacavir (ABC) | Tenofovir (TDF) | d4T+ddI |
| Lamivudina (3TC) | Emtricitabina (FTC) | |||
| Estavudina (d4T) | ||||
| Didanosina (ddI) | ||||
| NN | Nevirapina (NVP)a | Etravirina (ETV) | Efavirenz (EFV) | |
| IP | Lopinavir/ritonavir (LPV/r) | Saquinavir/ritonavir (SQV/r) | Fosamprenavir/ritonavir (FPV/RTV) | |
| Indinavir/ritonavir (IDV/r) | Tipranavir/ritonavir (TPV/r) | |||
| Atazanavir/ritonavir (ATV/r) | Darunavir/ritonavir (DRV/r) | |||
| Nelfinavir (NFV) | ||||
| Otros | Enfuvirtida (T-20) | |||
| Raltegravir (RAL) | ||||
| Maraviroc (MVC) |
Tratamiento antirretroviral recomendado para evitar la transmisión vertical en las principales situaciones
| Gestación | Parto | Recién nacido | |
| Gestante VIH+ conocida con tratamiento antirretroviral previo | - Si CVP indetectable, mantener TAR, intentando incluir ZDV y únicamente fármacos recomendados en la gestación | - ZDV 2 mg/kg la primera hora (empezando 1 h antes del parto vaginal o 2-3 h antes de la cesárea) y posteriormente 1 mg/kg/h hasta pinzamiento del cordón | - ZDV desde las primeras 8 horas hasta 4-6 semanas de vidaa |
| - Si CVP detectable cambiar TAR previo estudio de resistencias | - Dosis ZDV: 2 mg/kg/12 h vo o 1,5 mg/kg iv cada 6 horas | ||
| Gestante VIH+ conocida sin criterios previos de iniciar tratamiento | - Iniciar TAR a partir de la semana 12 preferiblemente con ZDV + 3TC y un tercer fármaco (IP/r o NVP si CD4 < 250 cel/μL) | - Cesárea programada en la semana 38 si CVP más cercana a la fecha del parto es > 1.000 copias/mL o desconocida | |
| Gestante VIH+ diagnosticada durante el embarazo | - Si la gestante cumple criterios de inicio de tratamiento per se, iniciar TAR cuanto antes previo estudio de resistencias | ||
| - Si la gestante no cumple criterios de inicio de tratamiento per se, iniciar tratamiento a partir de la semana 12 previo estudio de resistencias | |||
| - Usar preferiblemente ZDV + 3TC y un tercer fármaco (IP/r o NVP si CD4 < 250 cel/μL) | |||
| Gestante VIH+ diagnosticada muy cerca del parto | - Si hay tiempo iniciar TAR, con ZDV + 3TC y un tercer fármaco (IP/r o NVP) | - Si el diagnóstico se hace en el momento del parto, administrar a la madre 3TC + NVP si da tiempo a administrarlo vía oral, además de la perfusión de ZDV- ZDV 2 mg/kg la primera hora (empezando 1 h antes del parto vaginal o 2-3 h antes de la cesárea) y posteriormente 1 mg/kg/h hasta pinzamiento del cordón- Cesárea siempre | - ZDV desde las primeras 8 horas hasta 4 semanas de vidaa a dosis de 2mg/kg/12 h vo o 1,5mg/kg iv cada 6horas- En casos de alto riesgo de TVb, se recomienda triple terapia: ZDV (misma dosis) y 3TC (2 mg/kg/12 h) durante 4 semanas y NVP (una primera dosis de 2 mg/kg las primeras 12 horas –si la madre no ha recibido NVP durante el embarazo o el parto–, una segunda a las 72 horas y a partir del 5.° día una dosis de 4 mg/kg/día durante 2 semanas |
Aunque la pauta clásica es de 6 semanas, hay trabajos que muestran eficacia similar con 4 semanas de tratamiento.
Se considera alto riesgo de TV: embarazo mal controlado, no tratamiento antirretroviral o tratamiento incorrecto, CVP previa al parto > 1.000 copias/mL o desconocida, CD4 < 200/μL, sida, diagnóstico VIH muy cercano al parto, no administración correcta de ZDV intraparto, gran prematuridad (< 32-34 semanas), sangrado grave durante el expulsivo o rotura de membranas > 4h.
Debe considerarse además, que en cuanto a los NN, efavirenz (EFV) está contraindicado por ser teratógeno y nevirapina (NVP) sólo debe usarse en mujeres con cifras de linfocitos CD4 inferiores a 250 células/μL en el momento de iniciar tratamiento por riesgo de rash y hepatotoxicidad graves. El IP de primera elección en gestantes es lopinavir potenciado con ritonavir, aunque atazanavir, saquinavir e indinavir, todos potenciados, son alternativas válidas. No hay datos suficientes para recomendar el uso de inhibidores de la integrasa, de la fusión o del correceptor CCR513.
Controles recomendadosSe recomienda un recuento de linfocitos CD4 en la primera visita y cada tres meses durante el embarazo. La determinación de CVP debe realizarse en la primera visita a las 2-4 semanas de haber iniciado un tratamiento antirretroviral nuevo, de forma mensual hasta que la CVP sea indetectable y posteriormente cada tres meses hasta que finalice el embarazo. Debe hacerse un último control de CVP entre las semanas 34 y 36 para decidir sobre el modo del parto12,13.
Actitud que seguir en los diferentes escenariosGestante VIH+ conocida con tratamiento antirretroviral previoSi la paciente se encuentra en una situación estable con CVP indetectable, se intentará mantener el mismo tratamiento, sustituyendo los fármacos contraindicados en la gestación e intentado cambiar aquellos con los que no hay experiencia suficiente. Salvo intolerancia o resistencia demostrada, es aconsejable incluir ZDV en la pauta.
Si la CVP es detectable, habrá que realizar un test de resistencias y modificar el tratamiento a una nueva pauta supresiva que incluya, a ser posible, ZDV.
Gestante VIH+ conocida sin criterios previos de iniciar tratamientoPrevia realización de test de resistencias, se recomienda iniciar TAR a partir de la semana 10-14 con una pauta que incluya ZDV y otro AN y un tercer fármaco que podría ser un IP potenciado o NVP (únicamente si los CD4 fueran inferiores a 250 células/μL). Mantener el tratamiento hasta el parto, y posteriormente se puede retirar si la mujer no cumple criterios de TAR (si la pauta incluye NVP, suspender ésta una semana antes que el resto de fármacos para evitar el desarrollo de resistencia a la misma).
Gestante VIH+ diagnosticada durante el embarazoSi la mujer cumple criterios de iniciar tratamiento, éste deberá iniciarse lo antes posible, incluso en el primer trimestre de gestación, evitando los fármacos teratógenos y tóxicos para las gestantes y aquellos con menor experiencia de uso, y procurando incluir ZDV en la pauta. Si la mujer no cumple criterios de inicio de tratamiento per se, se deberán aplicar las recomendaciones del párrafo anterior.
Gestante VIH+ diagnosticada muy cerca del partoSi quedan días antes del parto, se debe iniciar tratamiento con ZDV + 3TC junto con un tercer fármaco que puede ser un IP potenciado o NVP. Si el diagnóstico se hace en el momento del parto, se deberá administrar a la madre ZDV + 3TC + NVP, que se seguirá o no después del parto dependiendo de la necesidad de la madre de TAR.
Tratamiento antirretroviral durante el parto y postpartoTodas las gestantes VIH+ salvo aquellas con hipersensibilidad demostrada, deberán recibir ZDV intravenosa durante el parto, empezando una hora antes en caso de parto vaginal, y entre dos y tres horas antes en caso de cesárea. Las dosis recomendadas son 2mg/kg la primera hora y posteriormente perfusión continúa a un ritmo de 1mg/kg/hora hasta el final del parto.
Además, todos los recién nacidos deberán recibir tratamiento con ZDV iniciado en las primeras 8 horas de vida y mantenido durante 4-6 semanas14. Las dosis serían de 2mg/kg vía oral o 1,5mg/kg intravenoso cada 6 horas.
Se debe recomendar tratamiento combinado en el recién nacido en aquellas situaciones que se asocian a un mayor riesgo de transmisión: diagnóstico tardío de VIH en el momento del parto o postparto en que no haya dado tiempo a realizar cesárea; embarazo mal controlado, no tratamiento antirretroviral o tratamiento incorrecto; CVP previa al parto > 1.000 copias/ml o desconocida, CD4 < 200 células/μl, sida, no administración correcta de ZDV intraparto, prematuridad, sangrado grave durante el expulsivo, o rotura de membranas > 4 horas. En estos casos se recomendará tratamiento del recién nacido durante 4-6 semanas con ZDV (dosis previamente descrita) asociada a 3TC (2mg/kg cada 12 horas) y nevirapina (esta última durante dos semanas, con una primera dosis de 2mg/kg las primeras 12 horas, una segunda a las 72 horas y a partir del 5.° día una dosis de 4mg/kg/día)12.
Modo de partoSe deberá indicar cesárea programada en la semana 38 a toda gestante VIH+ cuya CVP más cercana a la fecha del parto sea superior a 1.000 copias/mL o desconocida15,16. En caso de CVP < 1.000 copias/mL o indetectable no está demostrado que la cesárea electiva disminuya el riesgo de TV por lo que la decisión se deberá tomar en conjunto con la madre.
Rotura prematura de membranasLa rotura prematura de membranas (RPM) está asociada a un mayor riesgo de TV. De hecho, por cada hora que la bolsa permanezca rota, aumenta el riesgo de TV un 2%17. El manejo de la gestante con infección VIH que sufre una RPM viene determinado fundamentalmente por la edad gestacional12: a) menos de 26 semanas: tratamiento conservador (antibióticos, corticoides y continuar TAR); b) entre 26 y 30 semanas: individualizar la decisión teniendo en cuenta la CVP materna, si lleva o no TAR y desde cuándo, la situación fetal y los resultados de cada centro; c) entre 30 y 36 semanas: se aconseja finalizar la gestación mediante cesárea electiva, por el mayor riesgo de TV, y d) más de 36 semanas: si el índice de Bishop es favorable (≥ 6) y no existen contraindicaciones para el parto vaginal, se puede inducir el parto con oxitocina. De lo contrario habrá que realizar cesárea.
Otras recomendaciones para disminuir la TVSe deben limitar al máximo los procedimientos invasivos que pudieran incrementar el riesgo de TV. En caso de que fuera necesario, podría realizarse una amniocentesis evitando atravesar la placenta durante el procedimiento, intentando que la paciente esté con TAR e idealmente con CVP indetectable18. No deben realizarse biopsias de corion por mayor riesgo de TV.
Deberán evitarse durante el parto, en la medida de lo posible, todos los procedimientos que puedan aumentar el riesgo de TV como episiotomía, colocación de electrodos en el cuero cabelludo, uso de fórceps, etc.
La lactancia materna está contraindicada sea cuál sea la situación inmunovirológica de la madre12,13.
Diagnóstico en el recién nacidoLa determinación de serología de VIH no es útil en el recién nacido puesto que hasta los 12-18 meses pueden detectarse anticuerpos anti-VIH transferidos por la madre. Para establecer el diagnóstico es precisa la identificación del ADN o ARN del virus en suero del recién nacido mediante técnicas de PCR. Se realizará una u otra prueba en el momento del nacimiento (en sangre del recién nacido, no de cordón), a las 2-3 semanas de vida, a los 2-3 meses y a los 6 meses. Esta última determinación es especialmente importante en niños con mayor riesgo de transmisión en el parto12,13.
Para confirmar la infección por VIH en el recién nacido será necesaria la detección de ADN o ARN del virus en 2 muestras diferentes. Para descartarla, sin embargo tendrán que cumplirse alguna de las siguientes condiciones: 1) tres test virológicos (PCR-ADN o PCR-ARN) negativos en los primeros meses de vida siendo el último negativo a los 6 meses de vida, y 2) en niños mayores de 18 meses: una prueba de detección de ADN o ARN negativa y una serología negativa; o 2 serologías negativas separadas al menos 1 mes entre ellas12,13.
Profilaxis post-exposición ocupacionalLa exposición ocupacional se define como el contacto con sangre y/u otros fluidos biológicos a través de inoculación percutánea o contacto con mucosas o piel no íntegra, durante el desarrollo de actividades laborales19. Según datos de la OMS, se estima que hay más de 3 millones de exposiciones percutáneas accidentales anuales entre el personal sanitario, atribuyéndose a esta vía la transmisión de hasta 1.000 casos de VIH anuales, 66.000 casos de virus hepatitis B (VHB) y 16.000 casos de virus hepatitis C (VHC)20. El personal de enfermería es el grupo más expuesto21 y con relativa frecuencia se omite su comunicación22.
Cualquier exposición ocupacional con riesgo para el trabajador requiere una evaluación clínica urgente y en algunos casos debe iniciarse una profilaxis antirretroviral sin demora19,21. Todos los servicios sanitarios deben de disponer de un manual escrito sobre las actuaciones a seguir en el caso de exposición al VIH, ocupacional o no, con disponibilidad de diagnóstico serológico rápido y con accesibilidad de 24 horas a los fármacos utilizados en la profilaxis postexposición ocupacional (PPEO)19,23–25.
Riesgo de transmisión de VIH en exposición ocupacionalA pesar de las cifras anteriormente mencionadas, el riesgo de transmisión tras exposición ocupacional es en general bajo y dependerá de las «características de la exposición» y de las de la fuente. En cuanto a las características de la exposición es preciso valorar:
- a)
Tipo de fluido al que ha sido expuesto que podemos clasificar en: 1) fluidos implicados en la transmisión de VIH (sangre o fluidos que contengan sangre, semen, secreciones vaginales y leche materna); 2) fluidos potencialmente infecciosos (líquido cefalorraquídeo, pleural, sinovial, peritoneal, pericárdico y amniótico), y 3) no infecciosos (saliva, orina, heces, lágrimas, sudor, vómitos, secreción nasal y esputo).
- b)
Vía de exposición, que puede ser: 1) percutánea, con un riesgo estimado tras exposición a sangre infectada por VIH, del 0,3%26, variable en cualquier caso en función de si la exposición ha sido superficial (erosión), de profundidad intermedia (aparición de sangre) o profunda; 2) mucosa, con un riesgo estimado de transmisión del 0,09%27, o 3) con piel no intacta (riesgo no bien cuantificado, pero estimado como inferior).
- c)
Tipo de material al que se ha expuesto: aguja hueca (mayor riesgo), aguja maciza o bisturí (menos riesgo).
- d)
Utilización de factores de barrera (guantes, etc.) que ayudan a disminuir el riesgo de transmisión.
En cuanto a las «características de la fuente»19,23,28 podemos diferenciar tres grandes grupos: a) paciente VIH+ conocido, en cuyo caso es importante conocer si presenta una CVP detectable o no (mayor riesgo si la fuente tiene una CVP elevada), además de CD4, si está en TAR, historia de TAR y de potencial resistencia previa a algún fármaco); b) paciente VIH− conocido, y c) situación serológica no conocida frente al VIH, en cuyo caso, siempre que sea posible, hay que intentar realizar un estudio serológico completo de la fuente y tener los resultados de dichos estudios en un periodo mínimo (< 2 horas) para actuar como proceda (preferiblemente test rápido de ELISA o CVP de RNA-VIH si no se puede descartar período ventana). Si no fuera posible, se considerará a efectos de PPEO que la fuente es potencialmente VIH+ cuando el paciente fuente pertenezca a grupos sociales en los que la prevalencia de VIH+ se considera suficientemente elevada: hombres que tienen sexo con hombres (HSH), hombres bisexuales, trabajadores del sexo, UDVP, antecedentes de encarcelamiento, originarios de países con prevalencia de infección de VIH ≥ 1%, y personas cuya pareja corresponda a alguno de estos grupos.
El peso de cada característica en el riesgo final es dispar siendo las más importantes29, la exposición a aguja utilizada directamente en vena/arteria de la fuente (OR 4,3), pinchazo profundo (OR 15), existencia de sangre visible en material expuesto (OR 6,2) y fuente con enfermedad VIH evolucionada (sida) o infección reciente (OR 5,6).
Basándonos en estas características y con la finalidad de facilitar la valoración de la PPEO, podemos agrupar las distintas exposiciones en19,28:
Exposiciones ocupacionales de bajo riesgoExposición a agujas macizas (no huecas) o lesión superficial (no sangrado) con fuente de bajo riesgo (p.ej. VIH con CVP indetectable), así como exposiciones mucocutáneas en general.
Exposiciones ocupacionales de alto riesgoExposición a agujas huecas con sangre visible en dispositivo, exposición a agujas utilizadas directamente en arteria o vena de fuente y exposiciones mucocutáneas a gran volumen de sangre de fuente VIH+ con CVP > 50 copias/ml.
Indicaciones para PPEO con fármacos antirretroviralesAspectos generalesAdemás del riesgo final de la exposición, hay una serie de condiciones generales imprescindibles para la indicación de PPEO con fármacos antirretrovirales: a) «exposición esporádica y excepcional» (no se recomienda profilaxis postexposición –PPE– en personas con exposiciones de riesgo repetidas), b) «ausencia de contraindicaciones para la toma de TAR», c) «instauración precoz» (la PPE debe iniciarse idealmente dentro de las primeras 4 horas y siempre antes de las 72 horas desde la exposición), y d) «disposición a seguimiento» (la persona expuesta tiene que estar dispuesta al seguimiento posterior necesario tras inicio de PPE). Además, a los candidatos a inicio de PPE deberemos de informar sobre los riesgos, eficacia e indicaciones de PPE con TAR, consensuar su uso, recoger en el consentimiento informado su conformidad para el inicio del mismo y cerciorarnos de su condición de VIH negativo. Es conveniente recalcar que la efectividad de la PPE, no es del 100%. Todos los casos en los que se indique PPE, deben ser controlados y revalorados por un experto dentro de las primeras 72 horas23. A toda persona expuesta hay que ofrecerle la posibilidad de seguimiento clínico e informarle sobre las medidas preventivas a seguir, así como explicarle cuáles son las características del cuadro clínico de primoinfección para que en caso de presentarlo consulte con su médico.
Indicaciones de profilaxis postexposición ocupacionalEn la tabla 3 se resumen las recomendaciones19,23,25,28 dependiendo de las características de la fuente aunque cabe reseñar que, en la mayoría de los casos, el factor determinante para inicio o no de la PPE es el deseo de la persona expuesta.
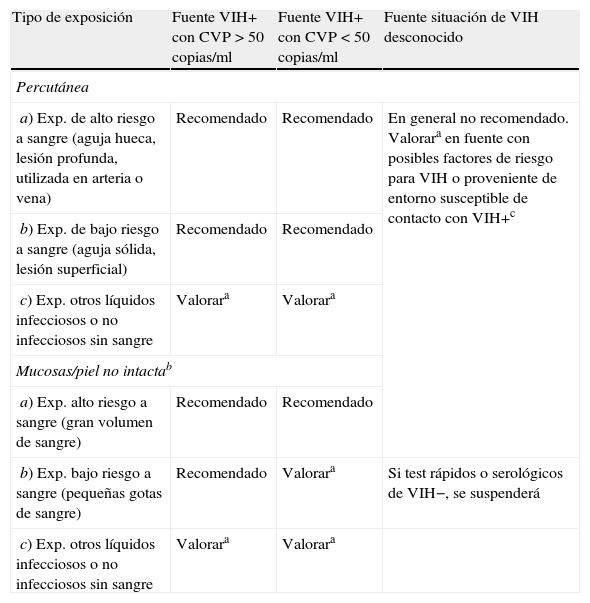
Indicaciones de profilaxis postexposición ocupacional (PPEO)
| Tipo de exposición | Fuente VIH+ con CVP > 50 copias/ml | Fuente VIH+ con CVP < 50 copias/ml | Fuente situación de VIH desconocido |
| Percutánea | |||
| a) Exp. de alto riesgo a sangre (aguja hueca, lesión profunda, utilizada en arteria o vena) | Recomendado | Recomendado | En general no recomendado. Valorara en fuente con posibles factores de riesgo para VIH o proveniente de entorno susceptible de contacto con VIH+c |
| b) Exp. de bajo riesgo a sangre (aguja sólida, lesión superficial) | Recomendado | Recomendado | |
| c) Exp. otros líquidos infecciosos o no infecciosos sin sangre | Valorara | Valorara | |
| Mucosas/piel no intactab | |||
| a) Exp. alto riesgo a sangre (gran volumen de sangre) | Recomendado | Recomendado | |
| b) Exp. bajo riesgo a sangre (pequeñas gotas de sangre) | Recomendado | Valorara | Si test rápidos o serológicos de VIH−, se suspenderá |
| c) Exp. otros líquidos infecciosos o no infecciosos sin sangre | Valorara | Valorara | |
a La PPE es opcional y depende de la valoración individualizada del caso, realizada entre la persona expuesta y el clínico.
b Se considera piel no intacta: zonas de piel con dermatitis, erosiones o heridas.
c HSH, hombres bisexuales, trabajadores del sexo, UDVP, antecedentes de encarcelamiento, originarios de países con prevalencia de infección de VIH ≥ 1% y personas cuya pareja corresponda a algunos de estos grupos.
Si la fuente tiene una CVP detectable, primoinfección o enfermedad avanzada, se recomienda PPE en todos los casos. En caso de CVP indetectable, aunque el riesgo sea considerablemente menor se recomienda también en la mayoría de los casos (tabla 3).
Fuente con estado serológico no conocidoNo se recomienda PPE de forma sistemática. Deberá valorarse PPE en caso de fuente con factores de riesgo para VIH o proveniente de entorno susceptible de contacto con VIH+ (ver apartado «Riesgo de transmisión de VIH en exposición ocupacional. Características de la fuente»).
Fuente VIH−Ante test de ELISA rápida de fuente (−), a no ser que se sospeche posibilidad de período ventana, no es necesaria la PPE.
TAR en profilaxis postexposiciónEfectividadLas recomendaciones de uso de TAR en la PPE se basan en estudios observacionales de profesionales sanitarios expuestos y en evidencias indirectas procedentes de modelos experimentales y de ensayos clínicos que han demostrado su eficacia en la prevención de la transmisión vertical. En este sentido, varios estudios de modelos animales, apoyan la eficacia de ZDV en la prevención de la transmisión del VIH30,31. En cuanto a estudios en humanos, en un estudio retrospectivo de casos control, el uso profiláctico de ZDV tras exposición ocupacional al VIH se asoció con una reducción del riesgo de transmisión del 81%29. En otro estudio ya mencionado previamente, la administración de ZDV a mujeres VIH+ durante el embarazo y parto, así como a los recién nacidos, redujo la transmisión vertical en un 67%1. Estudios más recientes han demostrado que el TAR es significativamente mejor que la ZDV en la reducción de la tasa de transmisión perinatal32.
Es conveniente recalcar que la efectividad de la PPE tanto ocupacional como no ocupacional no es absoluta, habiéndose descrito casos de seroconversión incluso tras inicio de PPE con ZDV en las primeras 2 horas19.
Selección del régimen (tabla 4)No existen estudios comparativos que permitan establecer recomendaciones firmes sobre los fármacos o combinaciones a emplear tras una exposición accidental23. Aunque no existen estudios que demuestren que la PPE con tres fármacos sea mejor que con dos, prevalece la opción de indicar triple terapia de modo similar a TAR de inicio, sobre todo en aquellas exposiciones de mayor riesgo19,23–25,28. Sólo en las exposiciones de bajo riesgo se puede plantear una PPE basada solo en dos AN.
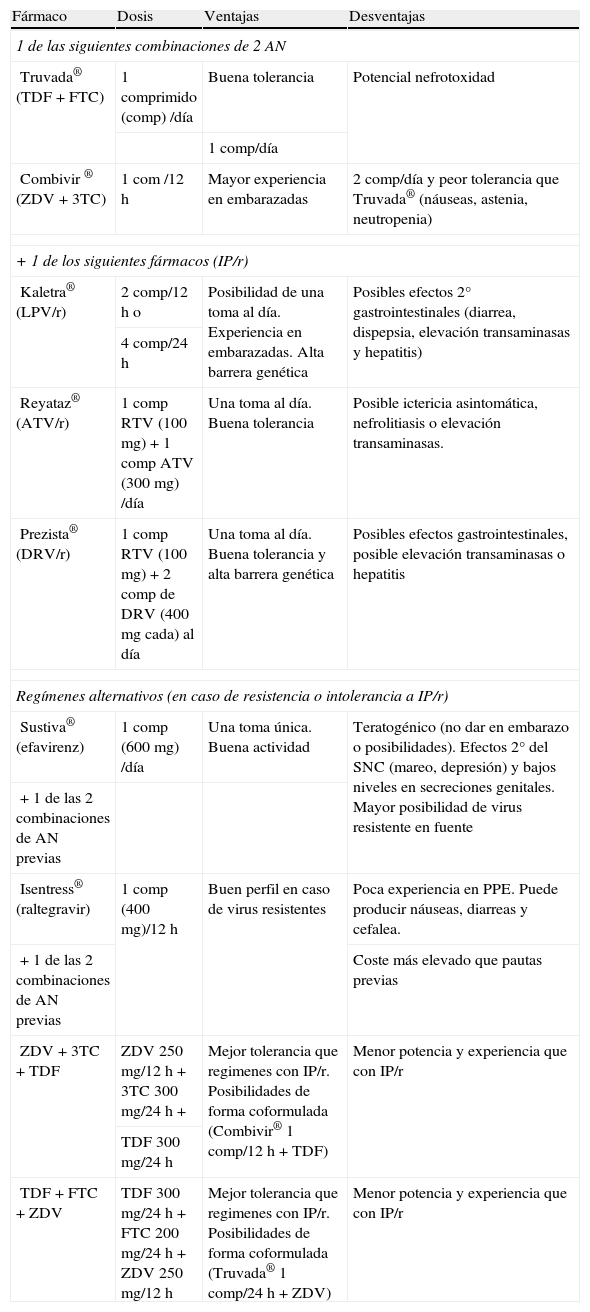
Fármacos preferidos en profilaxis postexposición (adultos): principio activo, nombre comercial, dosis, ventajas y desventajas
| Fármaco | Dosis | Ventajas | Desventajas |
| 1 de las siguientes combinaciones de 2 AN | |||
| Truvada® (TDF + FTC) | 1 comprimido (comp) /día | Buena tolerancia | Potencial nefrotoxidad |
| 1 comp/día | |||
| Combivir ® (ZDV + 3TC) | 1 com /12 h | Mayor experiencia en embarazadas | 2 comp/día y peor tolerancia que Truvada® (náuseas, astenia, neutropenia) |
| + 1 de los siguientes fármacos (IP/r) | |||
| Kaletra® (LPV/r) | 2 comp/12 h o | Posibilidad de una toma al día. Experiencia en embarazadas. Alta barrera genética | Posibles efectos 2° gastrointestinales (diarrea, dispepsia, elevación transaminasas y hepatitis) |
| 4 comp/24 h | |||
| Reyataz® (ATV/r) | 1 comp RTV (100 mg) + 1 comp ATV (300 mg) /día | Una toma al día. Buena tolerancia | Posible ictericia asintomática, nefrolitiasis o elevación transaminasas. |
| Prezista® (DRV/r) | 1 comp RTV (100 mg) + 2 comp de DRV (400mg cada) al día | Una toma al día. Buena tolerancia y alta barrera genética | Posibles efectos gastrointestinales, posible elevación transaminasas o hepatitis |
| Regímenes alternativos (en caso de resistencia o intolerancia a IP/r) | |||
| Sustiva® (efavirenz) | 1 comp (600 mg) /día | Una toma única. Buena actividad | Teratogénico (no dar en embarazo o posibilidades). Efectos 2° del SNC (mareo, depresión) y bajos niveles en secreciones genitales. Mayor posibilidad de virus resistente en fuente |
| + 1 de las 2 combinaciones de AN previas | |||
| Isentress® (raltegravir) | 1 comp (400 mg)/12 h | Buen perfil en caso de virus resistentes | Poca experiencia en PPE. Puede producir náuseas, diarreas y cefalea. |
| + 1 de las 2 combinaciones de AN previas | Coste más elevado que pautas previas | ||
| ZDV + 3TC + TDF | ZDV 250 mg/12 h + 3TC 300 mg/24 h + | Mejor tolerancia que regimenes con IP/r. Posibilidades de forma coformulada (Combivir® 1 comp/12 h + TDF) | Menor potencia y experiencia que con IP/r |
| TDF 300 mg/24 h | |||
| TDF + FTC + ZDV | TDF 300 mg/24 h + FTC 200 mg/24 h + ZDV 250 mg/12 h | Mejor tolerancia que regimenes con IP/r. Posibilidades de forma coformulada (Truvada® 1 comp/24 h + ZDV) | Menor potencia y experiencia que con IP/r |
Fármacos a evitar en PPE: Abacavir (ABC): posibilidades de reacción de hipersensibilidad importante; Nevirapina (NVP): posibilidades de hepatitis fulminante; Efavirenz (EFV): evitar en embarazo o posibilidades de embarazo y en pacientes con antecedentes psiquiátricos; Indinavir (IDV): posibilidades de nefrolitiasis.
Las combinaciones de AN preferidas para la PPE son lamivudina (3TC) o emtricitabina (FTC) + tenofovir (TDF) o ZDV. Las presentaciones coformuladas (Combivir® –ZDV+3TC– y Truvada® –TDF + FTC–), pueden facilitar la adherencia al tratamiento, prevaleciendo en la mayoría la opción de Truvada®19,25. No se recomienda el uso de abacavir (ABC) ni la combinación de ddI + d4T debido al mayor riesgo de acontecimientos adversos graves.
En cuanto a los IP potenciados (IP/r), el más utilizado e indicado es lopinavir+ritonavir (LPV/r). Otros como atazanavir+RTV (ATV/r), darunavir+RTV (DRV/r) y fosamprenavir + RTV (FPV/r) tienen cada vez mayor presencia en las diferentes guías de práctica clínica25,28.
El uso de NN está limitado por los efectos secundarios precoces e importantes que pueden presentar. En este sentido, EFV es una alternativa a considerar en situaciones de resistencia o intolerancia a IP/r, siempre y cuando el paciente no presente antecedentes psiquiátricos ni esté embarazada debido a los frecuentes efectos secundarios sobre el sistema nervioso central y riesgo de teratogenicidad asociados a su uso19,25,28. Por otra parte, NVP es otro de los fármacos a evitar en la PPE debido al potencial (aunque raro) riesgo de hepatitis fulminante y síndrome de Steven-Johnson que presenta33,34.
Maraviroc (MVC), raltegravir (RAL) y enfuvirtida (T20) no se recomiendan para uso inicial de la PPE, siendo opciones a considerar en pautas alternativas y sobre todo en caso de exposición de alto riesgo a virus multirresistente25. Otra pauta alternativa sería la basada en tres AN24,25,28 (ZDV /3TC + TDF o TDF/FTC + ZDV).
Los efectos secundarios del TAR en la PPE ocupacional son frecuentes, y aunque en la mayoría de casos son de intensidad moderada, son la causa fundamental de abandono del tratamiento23,25. Estas tasas de abandono tan altas de la PPE (17-47%)23, contrastan con las observadas durante el primer mes entre los pacientes infectados por VIH que inician TAR (< 5%), lo que se podría explicar por el hecho del inicio frecuente de PPE bajo situaciones de estrés y/o la insuficiente interacción médico-paciente. Otro aspecto importante a tener en cuenta a la hora de elegir la pauta de PPE son las interacciones medicamentosas: todos los fármacos antirretrovirales tienen interacciones (sobre todo los IP/r y los NN), por lo que hay que considerar todos los medicamentos e incluso suplementos concomitantes que toma el paciente para evitar interacciones potencialmente importantes.
La creciente complejidad de la elección del régimen de PPE, hace recomendable la valoración del caso por un experto19,23,25. El consejo del experto es uno de los factores más importantes para el adecuado cumplimiento de la PPE siendo éste obligatorio en casos de exposiciones de riesgo moderado o alto19, así como en exposiciones a fuente portadora de VIH potencialmente resistente. En este último caso, las pautas habituales pueden ser inapropiadas y el experto tendrá que analizar la historia clínica y farmacológica del paciente fuente, evaluando de forma especial los test de resistencia y pautas de fracaso virológico. El uso de MVC, RAL y T20, así como de IP/r con mejor perfil para virus resistentes (DRV y TPV), son opciones a considerar en estos casos19,25,28 con el objetivo de seleccionar una pauta de TAR con la que el paciente fuente no haya fracasado.
Momento de inicio y duración del TARExiste consenso, basándose en estudios con macacos35 en que debe iniciarse tan rápido como sea posible, preferiblemente antes de las primeras 4 horas y en todo caso antes de las 72 horas. Nada debe retrasar el inicio de la PPE, siendo siempre mejor, iniciar PPE con una pauta básica y decidir posteriormente si está indicado continuar19,23,25,28,36. Una vez pasadas las 72 horas desde la exposición, en general, se desaconseja la PPE. Algunos expertos limitan aún más este período no recomendando iniciar la PPE más allá de las 36 horas24.
Aunque la duración óptima de la PPE no es conocida, basándose en estudios en animales y en resultados de estudios de exposición ocupacional, se recomienda un régimen de 28 días. Obviamente, si tras inicio de la PPE se confirma que la fuente es VIH− (sin riesgo de que esté en período ventana), se debe suspender la PPE sin esperar finalizar pauta de 28 días19,23–25,28,36.
Profilaxis postexposición no ocupacionalLa exposición no ocupacional se define como el contacto por vía sexual o parenteral, de manera accidental, con sangre y/u otros fluidos biológicos potencialmente infectados de VIH fuera del ámbito ocupacional o perinatal. En este contexto se consideran fluidos potencialmente infecciosos: la sangre, el semen, las secreciones vaginales y rectales, así como la leche materna19,36,37. No obstante, en la práctica clínica diaria, la mayoría de potenciales exposiciones no ocupacionales al VIH, se limitan a exposiciones sexuales y parenterales19.
El éxito de las estrategias de prevención de exposición ocupacional y transmisión perinatal han impulsado el interés en aplicar estrategias similares en exposición no ocupacional37–39. El aumento de la demanda de la profilaxis postexposición no ocupacional (PPENO) es un fenómeno generalizado y cada vez son más las situaciones no claramente indicadas en las guías, en las que se aplica25. A diferencia de la PPEO, en la PPENO, el inicio de la profilaxis suele ser más tardía, los abandonos son más frecuentes y la situación serológica de la fuente es más veces desconocida e imposible de conocer19,39.
La actuación médica debe ser integral, abordando además de la indicación de la PPENO otros aspectos como la educación en medidas preventivas, la valoración de la potencial transmisión concomitante de otras infecciones y el seguimiento clínico que realizar19,28,36,37.
Riesgo de transmisión del VIH en exposición no ocupacionalEl riesgo de transmisión va a depender de la probabilidad de que la fuente sea VIH+ y del tipo de exposición. En este sentido, la exposición que mayor riesgo tiene, por exposición puntual, es la transfusión sanguínea, seguida de compartir jeringas entre UDVP, relación anal receptiva y exposición percutánea con aguja. Los riesgos estimados por acto en caso de exposición insertiva anal, exposición pene-vaginal y sexo oral son substancialmente inferiores19,25,28,36. Además, este riesgo aumentará en caso de existencia de lesiones genitales y otras ITS, sangrado durante la relación, displasia cervical o anal, ausencia de circuncisión, exposición a virus con alta virulencia, existencia de carga viral de VIH elevada en sangre y secreciones de la fuente, eyaculación y agresión sexual19,28,36,40,41.
En las tablas 5–7, se detalla el riesgo estimado de las diferentes exposiciones, dependiendo del estado serológico de la fuente. La exposición transfusional (a sangre o hemoderivados de paciente infectado por VIH) no es clasificable en ninguno de estos grupos.
Riesgo estimado de infección tras exposición sexual con fuente VIH+, sin uso de preservativo, rotura o mal uso
| Riesgo apreciable (0,8-3%) | Bajo riesgo (0,05-0,8%) | Riesgo mínimo (0,01-0,05%) |
| - Recepción anal con eyaculación | - Recepción vaginal con o sin eyaculación | - Sexo oral sin eyaculación |
| - Recepción anal sin eyaculación | - Sexo orogenital femenino | |
| - Penetración anal | ||
| - Penetración vaginal | ||
| - Sexo orogenital con eyaculación |
Fuente: Tomado de Polo R et al.19.
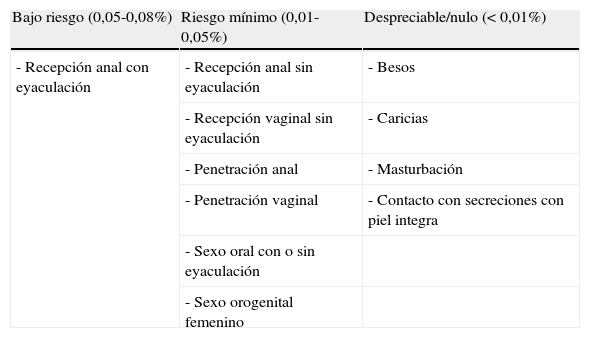
Riesgo estimado de infección tras exposición sexual con fuente VIH desconocido, sin uso de preservativo, rotura o mal uso
| Bajo riesgo (0,05-0,08%) | Riesgo mínimo (0,01-0,05%) | Despreciable/nulo (< 0,01%) |
| - Recepción anal con eyaculación | - Recepción anal sin eyaculación | - Besos |
| - Recepción vaginal sin eyaculación | - Caricias | |
| - Penetración anal | - Masturbación | |
| - Penetración vaginal | - Contacto con secreciones con piel integra | |
| - Sexo oral con o sin eyaculación | ||
| - Sexo orogenital femenino |
Fuente: Tomado de Polo R et al.19.
Riesgo estimado de infección por VIH tras diferentes tipos de exposición
| Riesgo apreciable (0,8-3%) | Bajo riesgo (0,05-0,8%) | Riesgo mínimo (0,01-0,05%) |
| - Compartir jeringuillas o agujas usadas- Pinchazo profundo o con abundante sangrado con jeringa, de forma inmediata tras uso por fuente desconocida | - Uso de jeringuilla de origen desconocido- Pinchazo superficial tras uso por caso fuente- Contacto abundante con sangre del caso fuente con mucosas del sujeto afecto | - Compartir resto de material de inyección (recipiente, cuchara, algodón, filtro, etc.)- Pinchazo accidental con poco sangrado con aguja de jeringa de procedencia desconocida |
Fuente: Tomado de Polo R et al.19.
a) «El riesgo es apreciable» (tablas 5-7); b) «La situación serológica de VIH de la fuente es desconocida pero pertenece a grupos sociales en los que la prevalencia de infección por VIH se considera suficientemente elevada» como para justificar la toxicidad y coste del tratamiento (ver apartado «Riesgo de transmisión VIH en exposición ocupacional. Características de la fuente») y c) «En caso de agresión sexual».
Valorar PPENO cuandoel riesgo es bajo (tablas 5–7) o seroestado de fuente imposible de conocer. Valorar el caso de forma individualizada entre médico y persona expuesta.
No se recomienda PPENOa) en exposiciones con riesgo mínimo o nulo (tablas 5–7), y b) ante test de ELISA rápida de fuente, a no ser que se sospeche posibilidad de período ventana.
Indicaciones de profilaxis postexposición no ocupacional (PPENO)
| Riesgo según tipo de exposición | Indicación de profilaxis |
| Riesgo apreciable (0,8-3%) | Recomendado |
| Ver tablas 5, 6 y 7 | |
| Riesgo bajo (0,05-0,8%) | Valorar PPE. Analizar de forma individualizada cada caso (tipo exposición, características fuente) |
| Ver tablas 5, 6 y 7 | |
| Riesgo mínimo (< 0,05%) | Se desaconseja PPE |
| Ver tablas 5, 6 y 7 |
Los resultados de varios estudios observacionales42,43 y comunicaciones de casos individuales44,45, sugieren la posible utilidad de la PPE con TAR en la prevención secundaria en exposición no ocupacional. Por otro lado, en estudios de costo efectividad, la PPENO ha demostrado ser costo-efectiva en exposiciones de alto riesgo con fuentes VIH+39,43,46. Estos datos han hecho que la PPENO sea comúnmente aceptada como estrategia útil, eficaz y segura, a pesar de que el nivel de evidencia no sea el óptimo. No obstante, es importante recalcar que la efectividad de la PPE no es del 100%19, siendo necesario informar de este hecho a la persona subsidiaria de PPENO e incidir en la importancia de extremar las medidas preventivas y cumplimiento de seguimiento serológico (tabla 9).
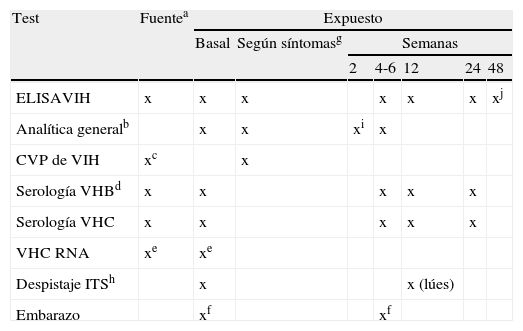
Cronograma del seguimiento que realizar
| Test | Fuentea | Expuesto | ||||||
| Basal | Según síntomasg | Semanas | ||||||
| 2 | 4-6 | 12 | 24 | 48 | ||||
| ELISAVIH | x | x | x | x | x | x | xj | |
| Analítica generalb | x | x | xi | x | ||||
| CVP de VIH | xc | x | ||||||
| Serología VHBd | x | x | x | x | x | |||
| Serología VHC | x | x | x | x | x | |||
| VHC RNA | xe | xe | ||||||
| Despistaje ITSh | x | x (lúes) | ||||||
| Embarazo | xf | xf | ||||||
aSi fuente desconocida, imposibilidad de realización serologías o no da consentimiento, considerar (+).
bCreatinina, función hepática y hemograma.
cEn caso de exposición reciente (2-4 semanas) o posible periodo ventana.
dHBsAg, HBsAc y HBcAc. En caso de expuesto con HBsAg, HBsAc y HBcAc (−), se debe iniciar vacunación de VHB. Sí expuesto HBsAg (+) y PPE con TDF, FTC o 3TC, se recomienda control mensual de transaminasas tras final de PPE ± derivación a digestivo.
eEn caso de exposición reciente o serología de VHC (+).
fEn caso de exposición sexual y/o posible uso de fármacos teratogénicos.
gTest a realizar en caso de signos o síntomas de efectos tóxicos (rash, náuseas, vómitos, dolor abdominal) o seroconversión VIH (fiebre, fatiga, linfadenopatía, rash).
hEn caso de exposición sexual. Test serológicos de Lues, frotis uretral, faríngeo y rectal según tipo de exposición sexual. En casos de urgencia o difícil seguimiento considerar profilaxis empírica: ceftriaxona 125mg im + metronidazol 2g vo + azitromicina 1g vo en dosis única.
iSolo en caso de PPE, para monitorizar posibles efectos adversos de TAR.
jSe recomienda serología de VIH en pacientes que se infecten de VHC tras exposición a fuente coinfectada por VHC y VIH.
Además, en todos los casos: ofrecer información y apoyo psicológico, así como recomendarles medidas para evitar transmisiones secundarias durante el período de seguimiento.
Tanto las condiciones básicas para la indicación de PPENO con TAR como las pautas de TAR a utilizar (elección de TAR, numero y duración) son similares a las ya mencionadas para la PPEO, con la salvedad del uso de EFV, fármaco no aconsejado en este contexto, dada la baja concentración que alcanza en secreciones genitales (< 10% de la plasmática) y su potencial efecto teratogénico19.
Profilaxis preexposición no ocupacionalEl considerable número de personas con exposiciones de riesgo repetidas en los que la PPENO no es aplicable (trabajadoras del sexo, HSH, parejas serodiscordantes, UDVP), la creciente incidencia de nuevas infecciones de VIH, especialmente en HSH, a pesar de todos los programas de prevención llevadas a cabo (53% de las nuevas infecciones de VIH en EE. UU. se dan entre HSH47) y el éxito de programas de profilaxis preexposición aplicados en otras patologías infecciosas, ha motivado que la comunidad científica busque nuevas estrategias de prevención primaria frente al VIH que se ajusten a esta población. En este sentido, la profilaxis preexposición no ocupacional (PrEP) frente al VIH puede ser una opción potencialmente válida tal como sugieren recientes estudios48–50. Así, en el estudio CAPRISA 004, la aplicación previa y postcoital de TDF al 1% en gel vaginal, se ha relacionado con una disminución de la transmisión de VIH del 39% (estudio realizado en mujeres sudafricanas con exposiciones de riesgo)49. En otro ensayo clínico (multicéntrico, aleatorizado y doble ciego, fase III), que compara la eficacia de la toma diaria de TDF/FTC oral frente a placebo en HSH se observa una reducción de transmisión del VIH del 44% (IC 15-63%) en aquellos que recibieron TDF/FTC oral diario frente a placebo tras una mediana de seguimiento de 1,2 años. A ambos grupos se les educó en la utilización de métodos de barrera para disminuir la transmisión. La eficacia se correlacionó en gran medida con la adherencia50.
A pesar de estos resultados alentadores, aún no hay datos suficientes sobre la eficacia de dicha estrategia en otros grupos de riesgo, su coste-efectividad y seguridad clínica del uso de forma crónica de TDF/FTC en VIH negativos. Actualmente hay varios estudios en marcha que analizan estos aspectos y la comunidad científica espera a su finalización y posterior valoración para emitir recomendaciones generales sobre las indicaciones de la PrEP25. No obstante, basándose en los datos disponibles y mientras se aclaren las dudas existentes, los CDC han elaborado unas recomendaciones provisionales47 sobre la PrEP, donde se recalca que de momento esta estrategia es aplicable únicamente en HSH con exposiciones repetidas de alto riesgo, siempre y cuando: 1) no haya contraindicaciones para la toma diaria de TDF/FTC; 2) se acompañe del adecuado asesoramiento sobre reducción de prácticas de riesgo, importancia de uso de otras medidas de prevención y de adherencia a medicación; 3) se garantice accesibilidad a despistaje y tratamiento de otras ITS, y 4) se monitorice de forma periódica el estado serológico de VIH, adherencia a medicación, efectos secundarios y existencia de prácticas de riesgo. Por ello, estas recomendaciones deben ser entendidas, en el momento actual, como aplicables exclusivamente a colectivos muy concretos en Estados Unidos. Son necesarios más datos antes de evaluar su potencial generalización a otros colectivos de alto riesgo en otras zonas geográficas.
Valoración inicial y seguimiento en consultas para PPEO y PPENOA toda persona que se haya evaluado para PPE debe ofrecérsele un plan de seguimiento, aspecto esencial de cualquier programa de profilaxis postexposición que incluirá controles clínicos y analíticos (durante 6-12 meses), información, apoyo psicológico y control de los posibles síntomas de primoinfección. Además, y teniendo en cuenta que la exposición al VIH (tanto ocupacional como no ocupacional) se puede acompañar de exposición a otras enfermedades que comparten mismas vías de transmisión (VHB, VHC, otras ITS, tétanos), éstas también tienen que ser valoradas, tratadas (si es que procede) y serológicamente monitorizadas. Ello incluye también, valorar las necesidades de vacunación frente a VHB y tétanos, así como en el caso de exposición sexual la posibilidad de embarazo19,23,28,36. Las pruebas, serologías, controles y otras actuaciones que realizar tanto en la persona fuente como en la expuesta, se detallan en el cronograma (tabla 9). En la tabla 10 se recoge una guía rápida de actuación.
Guía rápida de actuación
| 1) La PPE está claramente recomendada en exposición excepcional ocupacional con líquidos biológicos de fuente VIH+ con CVP detectable y en exposición excepcional no ocupacional, cuando ha existido recepción anal con eyaculación sin preservativo o en caso de pinchazo profundo o con abundante sangrado con una jeringuilla de forma inmediata a su uso. En situaciones de bajo riesgo (ver tablas 5, 6 y 7) valorar de forma consensuada con el paciente posible PPE. Ante la duda de indicación de PPE, dar la primera dosis de TAR |
| 2) Si consideramos subsidiario de PPE, ésta debe comenzarse lo antes posible, idealmente en las 2-6 h siguientes de la exposición y en todo caso antes de la 72 h. Nada debe retrasarla |
| 3) La pauta de TAR para PPE, si no existe posibilidad de consejo especializado inmediato, será un régimen de 3 fármacos compuesto por: |
| - 2 AN (ZDV o TDF + 3TC o FTC), preferible para facilitar adherencia dar combinaciones fijas ya existentes de Truvada® o Combivir® |
| - + 1 IP potenciado (LPV/r, ATV/r, FPV/r o DRV/r) |
| 4) Valoración inicial y seguimiento según cronograma (tabla 9) |
| 5) El paciente debe ser remitido en la mayor brevedad posible a una consulta hospitalaria con capacidad para su estudio y seguimiento |
| 6) La duración de la PPE deberá ser de 28 días y se hará un seguimiento clínico y serológico de la persona expuesta durante al menos 6 meses, recomendando en ese período extremar medidas para evitar transmisiones secundarias |
Los autores declaran no tener ningún conflicto de intereses.
A la Dra. Juncal Lecuona del Servicio de Pediatría de la Universidad del País Vasco, por la revisión del manuscrito.