El uso de los dispositivos semicríticos reutilizables se ha extendido en la práctica médica actual tanto con fines diagnósticos como terapéuticos. Sin embargo, la reutilización de estos instrumentos conlleva el riesgo de una transmisión cruzada de microorganismos de un paciente a otro. El proceso de limpieza y desinfección de estos dispositivos es complejo, largo, caro y muy sensible a que se produzcan fallos. En el presente documento se analizan los aspectos epidemiológicos de las infecciones asociadas a la reutilización de los dispositivos semicríticos, y el papel del laboratorio de Microbiología en la monitorización del proceso de limpieza y desinfección de los mismos a través de los controles microbiológicos. Se revisan las recomendaciones de diferentes sociedades científicas sobre la pertinencia de dichos controles y se establecen recomendaciones específicas para la toma y el procesamiento de las muestras, la interpretación de los resultados y las medidas a tomar en función de los resultados obtenidos.
The use of reusable semi-critical devices has been extended in current medical practice for both diagnostic and therapeutic purposes. However, reuse of these instruments carries the risk of cross-transmission of microorganisms from one patient to another. The process of cleaning and disinfecting these devices is complex, long, expensive and very error-prone. This paper analyses the epidemiological aspects of infections associated with the reuse of semi-critical devices and the role of the Microbiology laboratory in monitoring the cleaning and disinfecting process through microbiological controls. The recommendations of different scientific societies on the relevance of such controls are reviewed and specific recommendations are proposed for the taking and processing of the samples, interpretation of the results and measures to be taken depending on the results obtained.
En la práctica médica actual se utilizan una enorme variedad de dispositivos médicos tanto con fines diagnósticos como terapéuticos. En algunos casos, estos dispositivos pueden comportarse como vehículos de transmisión de agentes infecciosos a un huésped susceptible originando la aparición de una infección nosocomial o asociada a la asistencia sanitaria1–4. No todos los dispositivos médicos se comportan igual en lo que al riesgo de infección se refiere, ya que esto depende del uso para el que estén diseñados.
Son los dispositivos reutilizables clasificados por Spaulding5 como semicríticos los que con mayor frecuencia se han asociado a la aparición de infecciones asociadas a la asistencia sanitaria. Dentro de esta categoría entrarían los endoscopios flexibles en general, entendidos como aparatos que acceden al interior del organismo a través de orificios naturales (gastroscopio, colonoscopio, fibrobroncoscopio, cistoscopio), los tubos endotraqueales, los laringoscopios y los termómetros rectales.
La reutilización de estos dispositivos exige que sean sometidos, entre paciente y paciente, a un proceso de desinfección de alto nivel que en muchos casos resulta complicado no solo por la complejidad estructural de los dispositivos (lúmenes largos y estrechos, válvulas, etc.), sino también porque, en sí mismo, es un proceso laborioso con diferentes etapas (limpieza mecánica, control de fugas, limpieza con detergentes enzimáticos, enjuagues, desinfección, secado, almacenaje) que son muy dependientes de la adecuada formación del personal sanitario encargado del reprocesamiento de los mismos, lo cual lo hace susceptible de no realizarse siempre correctamente2,6–8. Es en este contexto donde los controles microbiológicos periódicos pueden servir como un indicador de calidad que garantice que todas las etapas del proceso de limpieza y desinfección se han realizado de forma adecuada8–11.
El material no crítico habitualmente no supone directamente un riesgo de infección para los pacientes y no requiere de controles microbiológicos. Sin embargo, ocasionalmente y en el contexto de brotes epidémicos puede ser necesario el muestreo de estos dispositivos para localizar el foco y/o la presencia de fómites contaminados que puedan suponer un eslabón en la cadena de transmisión de un determinado microorganismo. Un ejemplo de esta situación es el brote internacional, descrito recientemente, de infección por Mycobacterium chimaera asociado al uso de los dispositivos frío-calor utilizados para regular la temperatura de la sangre y de la solución de cardioplejía durante la circulación extracorpórea en intervenciones de cirugía cardiaca. En este sentido, el European Centre for Disease Prevention and Control ha publicado un documento técnico para la detección de laboratorio de M. chimaera en estos dispositivos y en el ambiente12.
Consideraciones clínicasLa infección asociada a un procedimiento diagnóstico o terapéutico en el que se ha utilizado algún instrumento semicrítico es aquella que se detecta tras haber realizado este tipo de procedimiento y está relacionado con el mismo. En algunos casos la infección es una complicación asociada al propio procedimiento como consecuencia del arrastre o la transferencia de microorganismos del propio paciente de un lugar a otro (fuente de infección endógena), pero en otros casos es el instrumento contaminado el que se comporta como un vehículo en la transmisión de microorganismos (fuente de infección exógena).
Existen pocos estudios prospectivos bien diseñados sobre la incidencia de la transmisión de patógenos asociados al uso de este tipo de dispositivos. En la mayoría de los casos documentados en la bibliografía, esta transmisión se ha producido en relación con deficiencias en alguno de los pasos del proceso de limpieza y desinfección, poniendo de manifiesto no solo la elevada frecuencia con la que estos procedimientos no se realizan correctamente, sino también la escasa vigilancia a la que están sometidos1,4,6 y, lo que es más preocupante, la colonización persistente de algunos de estos instrumentos a pesar de haberlos procesado siguiendo estrictamente las recomendaciones13.
La mayoría de los casos publicados están en el contexto de brotes o pseudobrotes producidos por microorganismos poco habituales o multirresistentes que son fácilmente detectados por tratarse de microorganismos que en muchos centros están sometidos a vigilancia6,13,14. Parece probable que el problema se esté infraestimando y que la contaminación cruzada por otro tipo de microorganismos, más habituales, pueda pasar desapercibida2–4,7,8. En general, los microorganismos que en la literatura médica se han asociado con más frecuencia a transmisiones a través de estos dispositivos son bacilos gramnegativos multirresistentes (Escherichia coli, Klebsiella pneumoniae, Pseudomonas aeruginosa, Serratia marcescens, entre otros), micobacterias y los virus de la hepatitis B y C2,4,6.
Síndromes clínicosEn muchas ocasiones la transmisión cruzada de microorganismos de un paciente a otro no se asocia al desarrollo de una infección clínica, sino que lo que produce es una colonización asintomática del huésped. En los casos en los que tiene lugar una infección sintomática los cuadros clínicos son muy variados. Cuando se trata de cistoscopias suelen producirse infecciones urinarias asociadas o no a bacteriemia; en el caso de endoscopias digestivas pueden producirse bacteriemias, colangitis, colecistitis o hepatitis, y en el caso de fibrobroncoscopias o material para ventilación pueden aparecer neumonías o bacteriemias.
Mecanismos patogénicosEl mecanismo por el cual se produce la transmisión cruzada de algún microorganismo pasa por la contaminación del instrumento. Esta contaminación puede producirse, bien a partir de la microbiota de un paciente al que se le ha realizado previamente algún procedimiento, bien a partir del ambiente inanimado (soluciones de irrigación, dispositivos de lavado automático, etc.). La contaminación puede persistir en este tipo de instrumentos por diferentes motivos: errores en el proceso de limpieza/desinfección del aparato, formación de biopelículas o presencia de alteraciones estructurales en el mismo (fugas) que hacen que sea imposible la erradicación de las bacterias a pesar de la correcta aplicación de los protocolos de limpieza2,6.
Papel de los controles microbiológicosEl control microbiológico de los dispositivos semicríticos reutilizables es una herramienta para detectar fallos en el proceso de limpieza y desinfección o la presencia de disrupciones de la superficie del dispositivo que favorezcan la persistencia de los microorganismos11. No existe un consenso unánime ni sobre la necesidad de los controles ni sobre la metodología que debe emplearse, pero hay diferentes sociedades científicas que recomiendan la realización de cultivos periódicos como parte del control de calidad del proceso de desinfección y dan indicaciones sobre el proceso de toma de muestras, el procesamiento de las mismas y la interpretación de los resultados9,13,15-20. En lo que se refiere a la periodicidad para la realización de los cultivos, tampoco existe un consenso unánime y en las diferentes guías se ha recomendado su realización con una periodicidad mensual, trimestral y hasta anual9,16,19,20.
Recogida de muestras para cultivo microbiológicoPara la toma de muestras es necesario disponer de material estéril (guantes, jeringas, cepillos y recipientes). La recogida de las diferentes muestras se realizará siempre con las máximas condiciones de asepsia. El momento ideal para la recogida es tras el proceso de desinfección y almacenado para valorar si hay contaminación durante el mismo.
Canales del endoscopio: utilizando jeringas estériles se instilan 10 o 20ml de suero salino al 0,9% estéril o agua destilada estéril a través de cada uno de los canales por separado y se recogen por la parte distal del endoscopio en un recipiente estéril. La recogida de muestra se puede completar introduciendo un cepillo estéril en el interior del canal, realizando un cepillado de la parte interna y mezclándolo posteriormente con 10ml de suero salino al 0,9% estéril o agua destilada estéril en un recipiente estéril9.
Superficies externas del endoscopio: se utiliza una torunda estéril humedecida en suero salino al 0,9% estéril que se frota por las diferentes superficies externas del endoscopio (extremo distal, puntos de apertura de los canales, puente elevador). Cada torunda se recoge en un recipiente estéril con tryptic soy broth (TSB).
Botella de agua conectada al endoscopio: se recogen 2 muestras de 100ml de agua utilizando una jeringa estéril a través del conector habitual entre la botella y el endoscopio y se transfieren a un recipiente estéril.
Lavadoras desinfectadoras automáticas: se deben recoger 2 muestras de 100ml del agua de aclarado final en un recipiente estéril (normas UNE EN-ISO 15883).
Agua de aclarado final: en caso de no utilizar lavadoras desinfectadoras automáticas se deben tomar con una jeringa estéril 2 muestras de 100ml de agua.
Transporte y conservación de las muestrasLas muestras se enviarán en recipientes estériles cerrados y etiquetados indicando el punto de toma de la muestra y la identificación del endoscopio o de la lavadora desinfectadora.
El procesamiento debe realizarse de forma inmediata para evitar un posible sobrecrecimiento bacteriano que altere el recuento en el cultivo cuantitativo. Si se va a retrasar el procesamiento es necesario conservar las muestras refrigeradas entre 2-5°C durante un máximo de 24h. En algunos casos y según el producto desinfectante utilizado podría añadirse un agente neutralizante para eliminar posibles trazas de agentes químicos que puedan limitar la detección de microorganismos.
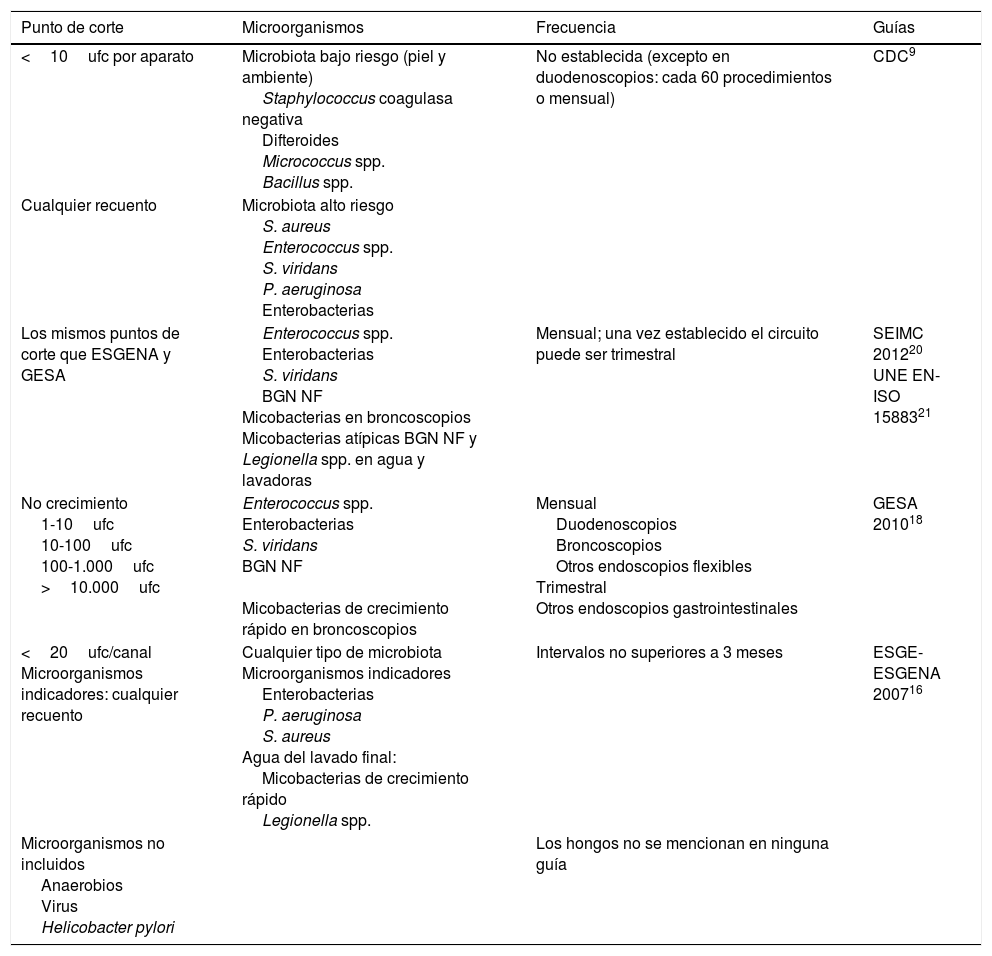
Manejo y procesamiento de las muestrasDiferentes sociedades nacionales e internacionales9,16–21 han establecido que el cultivo microbiológico de los endoscopios en general (gastrointestinales, cistoscopios, fibrobroncoscopios) debe estar orientado a la búsqueda de microorganismos presentes en la microbiota oral y entérica. En la tabla 1 se describen en detalle los microorganismos que se comportan como indicadores de un inadecuado proceso de limpieza y desinfección. No se recomienda la búsqueda de virus, ya que la detección de virus intactos y con capacidad infectiva es un proceso complejo y de alto coste.
Recomendaciones para el estudio microbiológico de los endoscopios
| Punto de corte | Microorganismos | Frecuencia | Guías |
|---|---|---|---|
| <10ufc por aparato | Microbiota bajo riesgo (piel y ambiente) Staphylococcus coagulasa negativa Difteroides Micrococcus spp. Bacillus spp. | No establecida (excepto en duodenoscopios: cada 60 procedimientos o mensual) | CDC9 |
| Cualquier recuento | Microbiota alto riesgo S. aureus Enterococcus spp. S. viridans P. aeruginosa Enterobacterias | ||
| Los mismos puntos de corte que ESGENA y GESA | Enterococcus spp. Enterobacterias S. viridans BGN NF Micobacterias en broncoscopios Micobacterias atípicas BGN NF y Legionella spp. en agua y lavadoras | Mensual; una vez establecido el circuito puede ser trimestral | SEIMC 201220 UNE EN-ISO 1588321 |
| No crecimiento 1-10ufc 10-100ufc 100-1.000ufc >10.000ufc | Enterococcus spp. Enterobacterias S. viridans BGN NF Micobacterias de crecimiento rápido en broncoscopios | Mensual Duodenoscopios Broncoscopios Otros endoscopios flexibles Trimestral Otros endoscopios gastrointestinales | GESA 201018 |
| <20ufc/canal Microorganismos indicadores: cualquier recuento | Cualquier tipo de microbiota Microorganismos indicadores Enterobacterias P. aeruginosa S. aureus Agua del lavado final: Micobacterias de crecimiento rápido Legionella spp. | Intervalos no superiores a 3 meses | ESGE-ESGENA 200716 |
| Microorganismos no incluidos Anaerobios Virus Helicobacter pylori | Los hongos no se mencionan en ninguna guía |
BGN NF: bacilos gramnegativos no fermentadores; CDC: Centers for Disease Control and Prevention; ESGE-ESGENA: European Society of Gastrointestinal Endoscopy-European Society of Gastroenterology and Endoscopy Nurses and Associates; GESA: Gastroenterological Society of Australia; SEIMC: Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica; ufc: unidades formadoras de colonias.
Habitualmente no es necesario realizar antibiogramas a todos los microorganismos aislados; no obstante, en determinadas situaciones (posibles brotes, aislamientos repetidos de enterobacterias o P. aeruginosa) puede ser útil su realización para detectar la presencia de bacterias multirresistentes.
Selección de medios de cultivo y condiciones de incubación de las muestrasMuestras obtenidas de los canales del endoscopio: habitualmente se realiza una mezcla o pool de todas las muestras recogidas mediante lavado y cepillado de los diferentes canales del endoscopio y se procesan de forma conjunta. Sin embargo, si los cultivos microbiológicos son repetidamente positivos en un determinado endoscopio puede ser necesario procesar las muestras de los diferentes canales de forma individual.
Los medios de cultivo recomendados9,16–20 son:
- -
Microorganismos aerobios: agar sangre, tryptic soy agar (TSA), Reasoner's 2-agar y caldo TSB.
- -
Micobacterias: agar Middlebrook 7H10.
Las muestras pueden procesarse mediante 2 técnicas9,16–20:
- -
Inoculación directa: se siembra 1ml de la muestra en una placa de agar sangre o TSA.
- -
Concentración mediante centrifugación o mediante filtración. La centrifugación se realiza durante 15min a 3.000rpm, se decanta el sobrenadante, se resuspende el sedimento y se siembra 0,1ml en agar sangre. Para la filtración se recogen 10ml de muestra y se hace pasar por un filtro con diámetro de poro no superior a 0,45μm. El filtro se incuba en agar TSA.
En ambas técnicas las placas pueden incubarse a 30 o 37°C durante 48h o 7 días (revisión a las 48h). Para cultivo de micobacterias se incuba a 37°C durante 21 días.
Muestras obtenidas de las superficies externas del endoscopio: se agita la torunda en 10ml de caldo TSB, se agita nuevamente utilizando un vórtex y se incuba 48h a 37°C. A las 48h se realizan subcultivos a medios selectivos.
Agua de aclarado de la lavadora automática y agua de la botella conectada al endoscopio: se filtran entre 100-200ml de muestra utilizando filtros con diámetro de poro no superior a 0,45μm y el filtro se incuba en agar sangre o Reasoner's 2-agar a 30°C durante 3-5 días o a 37°C durante 2 días9,10,16,18. En caso de no disponer de filtros se podrían añadir 100ml de agua de aclarado a 100ml de caldo TSB e incubar a 37°C durante 48h, y después hacer un subcultivo en medios selectivos, aunque esta metodología no está validada. Para el cultivo de micobacterias debe utilizarse un medio específico como el agar Middlebrook 7H10 y se incuba a 37°C durante 21 días.
Criterios para la interpretación de los resultadosEn la tabla 1 se detalla el tipo de microorganismos que se deben buscar y los recuentos de unidades formadoras de colonias a partir de los cuales se deben considerar significativos. En la tabla 2 se describe la interpretación orientativa de los resultados de los cultivos y las acciones recomendadas en función de los mismos.
Interpretación orientativa de los resultados microbiológicos
| Microorganismos aislados | Interpretación/acción a tomar |
|---|---|
| Crecimiento de S. epidermidis en recuentos bajos | Sospecha de contaminación, bien en la toma o procesamiento de la muestra, bien en el almacenamiento |
| Se recomienda repetir la toma de muestras | |
| Recuentos significativos de microorganismos en varios aparatos Aislamiento de enteropatógenos como Salmonella spp. Aislamiento de P. aeruginosa | Sospecha de fallos en el proceso de limpieza/desinfección de los dispositivos Se recomienda revisar el procedimiento de limpieza y desinfección y tomar nuevamente muestras |
| Aislamiento de P. aeruginosa y otros BGN no fermentadores | Sospecha de fallos en el secado y almacenamiento de los dispositivos o contaminación del agua de lavado. Valorar la pertinencia de la colocación de filtros |
| Crecimiento repetido en recuentos significativos de un microorganismo en un solo aparato | Sospecha de problemas estructurales en los dispositivos |
| Se recomienda la revisión del aparato por el fabricante, control de fugas |
Se debe contactar e informar al departamento correspondiente y además entregar un informe al equipo responsable de la prevención y control de infecciones del centro sanitario. Además, según el/los microorganismo/s detectado/s y el inóculo, hay que recomendar que se lleven a cabo las medidas adecuadas (nueva toma de muestra, revisión del aparato, revisión de los procedimientos de limpieza y desinfección).
Cualquier material contaminado debe ser retirado de su uso hasta que los controles microbiológicos sean correctos. En caso de aislamiento de determinados microorganismos, tales como P. aeruginosa, otros bacilos gramnegativos no fermentadores, Salmonella spp. y Shigella spp., se hará un seguimiento dirigido de los pacientes expuestos. Este seguimiento también es necesario en el caso de aislamiento de Mycobacterium tuberculosis o Mycobacterium chelonae a partir de muestras de broncoscopios. En los últimos años se han notificado casos de infección cardiovascular invasiva por M. chimaera asociados al uso de los sistemas frío-calor que se utilizan durante la circulación extracorpórea22.
El laboratorio de Microbiología debe realizar un dictamen escrito con los resultados de los cultivos y también un informe a la Comisión de Infecciones/Seguridad del Paciente de la incidencia, las medidas adoptadas y la resolución del problema.
Otros procedimientos para la detección de residuos orgánicosUno de los principales inconvenientes de los cultivos microbiológicos como herramienta de control del proceso de desinfección de los dispositivos semicríticos radica en la demora en la obtención de resultados. Por ello, se han desarrollado otras técnicas que permiten detectar de forma rápida la presencia de restos orgánicos. Entre las técnicas actualmente disponibles se encuentra la medición del ATP y de residuos de proteínas, hemoglobina e hidratos de carbono.
El ATP es una molécula presente en todas las células vivas, lo que la convierte en un buen marcador para evaluar la presencia de residuos orgánicos. La presencia de ATP se mide por bioluminiscencia. Para ello, se emplea la enzima luciferasa, que utiliza el ATP y la proteína luciferina para generar una señal luminosa que se mide en unidades relativas de luz mediante un luminómetro. Como la relación entre la cantidad de ATP y la cantidad de luz producida es lineal, a mayor presencia de residuos orgánicos, más ATP está presente y más luz se produce. Esta técnica puede emplearse para medir la contaminación en tiempo real tanto de las superficies como de los canales de los endoscopios. La mayor parte de los trabajos publicados han evaluado esta técnica para medir la eficacia del proceso de limpieza manual previo al proceso de desinfección11,17. De esta forma, valores de bioluminiscencia elevados tras la limpieza manual indican que la cantidad de residuos orgánicos es demasiado alta para lograr que el proceso de desinfección sea eficaz23. Se ha establecido un valor de referencia de<200 unidades relativas de luz para considerar apto el canal y la superficie del endoscopio tras el proceso de limpieza manual23.
Para la detección de proteínas, hemoglobina e hidratos de carbono hay disponibles diferentes kits comerciales basados en reacciones colorimétricas de fácil manejo y que proporcionan resultados de forma rápida. Los puntos de corte de aceptación después de un adecuado proceso de limpieza y antes de la desinfección son de<6,4,<1,2 y<2,2mg/cm para las proteínas, los hidratos de carbono y la hemoglobina, respectivamente11,17.
Actualmente, ninguna guía recomienda la sustitución de los cultivos microbiológicos por el empleo de estos biomarcadores, ya que son necesarios más estudios para su validación9.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.