Hay escasa información sobre los recursos disponibles tanto en las consultas como en el laboratorio para hacer frente a las infecciones de transmisión sexual (ITS). El objetivo es describir y conocer la realidad de las consultas y laboratorios que atienden las ITS en España.
MétodosEstudio observacional transversal con obtención de datos mediante una encuesta dirigida a los miembros del Grupo de ITS de la SEIMC (GEITS).
ResultadosSe obtuvieron respuestas de 24 centros (tasa de respuesta, 38,1%) pertenecientes a 10comunidades autónomas. Respecto a las consultas de ITS, el 38% precisan que el paciente presente tarjeta sanitaria para proporcionar asistencia, y un 31,8% solo la prestan mediante derivación de otro médico. El 52,4% realizan métodos diagnósticos en la propia consulta. El 18,2% de los laboratorios no ofrecen pruebas diagnósticas de respuesta inmediata, aunque el 100% disponen de PCR frente a Neisseria gonorrhoeae y Chlamydia trachomatis, el 47,8% frente a Mycoplasma genitalium y el 65% detectan genotipos del linfogranuloma venéreo. El 20% realizan técnicas de detección molecular de resistencias antimicrobianas. Todos los laboratorios realizan cultivo y técnicas de sensibilidad a gonococo.
ConclusionesExiste una gran variabilidad en las dotaciones de medios humanos y materiales en las consultas y en los laboratorios que atienden ITS. En un número importante de centros existen limitaciones para el acceso de los pacientes. Todos los laboratorios disponen de técnicas de biología molecular y detectan la infección de N.gonorrhoeae mediante PCR y cultivo, lo que permite la realización de pruebas de sensibilidad en todos los centros.
Scarce information is available on the resources to deal with the Sexually Transmitted Infections (STIs), both in the clinic and in the laboratory. The objective is to describe and know the reality of the clinics and laboratories that treat these infections in Spain.
MethodsCross-sectional observational study with data collection through a survey aimed at the members of the GEITS Group.
ResultsResponses were obtained from 24 centers (response rate 38.1%) belonging to 10Autonomous Communities. Regarding STI consultations, 38% require that the patient present a health card to provide assistance, and 31.8% only provide it by referral from another doctor. The 52.4% perform diagnostic methods in the care center. Regarding laboratories, 18.2% do not offer immediate response diagnostic tests, although 100% have PCR against Neisseria gonorrhoeae and Chlamydia trachomatis, 47.8% against Mycoplasma genitalium and 65% detect lymphogranuloma venereum genotypes. All laboratories continue to perform culture and gonococcal sensitivity techniques, and 20% perform molecular methods for detection of MG antimicrobial resistance.
ConclusionThere is great variability in the provision of human and material resources both in the clinics and in the laboratories that attend STIs. In a significant number of centers there are limitations for patient access. Although laboratories have molecular biology technologies, not all of them offer immediate response tests. All laboratories detect N.gonorrhoeae infection by PCR and also by culture, which allows sensitivity testing in all centers.
Las infecciones de transmisión sexual (ITS) han experimentado un importante incremento en su incidencia desde inicios del siglo. Además, si no son diagnosticadas y tratadas de forma precoz, pueden tener consecuencias clínicas importantes, como la enfermedad pélvica inflamatoria, infertilidad, y también se ha demostrado que algunas de ellas favorecen la transmisión del VIH. Por ello las ITS constituyen un problema de salud pública importante a nivel mundial, y para dar respuesta a dicho problema la OMS ha establecido una estrategia global para su reducción1.
El Grupo de Estudio de ITS (GEITS) de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) tiene entre sus fines la cooperación y la coordinación de los socios implicados e interesados en el diagnóstico y el manejo clínico y epidemiológico de las ITS. Para poder llevar a cabo estas funciones resulta de vital importancia conocer la realidad de nuestros centros asistenciales, tanto en lo que se refiere a las consultas como a los laboratorios de microbiología. Por ello, desde la junta directiva del GEITS se impulsó la realización de una encuesta de recursos diagnósticos entre sus miembros.
Los objetivos de este trabajo son conocer los recursos de que disponen tanto las consultas como los laboratorios que trabajan en el manejo de las ITS en España, así como obtener información sobre sus necesidades. Posteriormente, y derivado de la información obtenida mediante esta encuesta, desde GEITS se pretende establecer algoritmos diagnósticos unificados y favorecer la coordinación con centros de referencia en este ámbito, con el objetivo final de diseñar estrategias coordinadas en la lucha contra las ITS.
MétodosSe diseñó un estudio descriptivo observacional y transversal. La recogida de datos se realizó mediante un cuestionario dirigido a los socios de la SEIMC miembros del GEITS sobre recursos diagnósticos tanto en las consultas de ITS como en los laboratorios. Los miembros fueron invitados a participar mediante un correo electrónico en el que se explicaba el proyecto, los objetivos, la metodología y las instrucciones para la realización. Un enlace permitía acceder a un cuestionario online con las preguntas. El soporte informático fue aportado por la secretaría técnica de la SEIMC.
El cuestionario fue diseñado y consensuado por la Junta del GEITS, y constaba de 104 preguntas: 4 de carácter identificativo, 23 referidas a recursos en la consulta y 77 referidas a recursos en el laboratorio; de estas últimas, 7 eran preguntas generales, 14 sobre técnicas de PCR, 25 de cultivos, 10 de sífilis, 7 de hepatitis, 5 de VIH, 6 de herpes y 3 referidas a temas de control de calidad.
Cada centro de trabajo respondió una sola encuesta. El periodo para responder se estableció entre el 16 de abril y el 11 de mayo de 2018 (25días).
ResultadosRespuestas recibidasSe enviaron invitaciones de participación a los 124 miembros de GEITS pertenecientes a 63 centros diferentes. Respondieron la encuesta 24 centros (tasa de respuesta del 38,1%) de 10 comunidades autónomas diferentes. La distribución de centros respondedores por cada una de las comunidades autónomas fue la siguiente: del País Vasco se obtuvo respuesta de 5 centros; 4 centros de Andalucía; de la Comunidad Valenciana y de Madrid respondieron 3 centros de cada una; 2 centros de Asturias, Canarias y Cataluña, y respondió un único centro de las comunidades de Castilla y León, Galicia y Navarra.
Las respuestas se organizaron en dos grandes bloques (consulta y laboratorio), y dependiendo del perfil de cada respondedor se completaban las preguntas de uno de los bloques o de ambos, tal como se expresa en la tabla 1. Al ser las preguntas de cada bloque muy específicas, en algunos casos los participantes contestaron las preguntas de un bloque, pero contestaron de forma parcial o directamente no contestaron las preguntas dirigidas al otro bloque, por lo que no todos los centros respondieron a la totalidad de las preguntas (tabla 1). Por esta razón los porcentajes obtenidos de cada una de las preguntas efectuadas van calculados respecto al total de respuestas obtenidas para dicha pregunta y no al total de centros participantes.
Respuestas por cada bloque (consulta/laboratorio) y grado de cumplimentación
| Bloques respondidos y grado de cumplimentación | Respuestas, n (%) |
|---|---|
| Consulta y laboratorio ambos completos | 15 (62,5%) |
| Consulta completo. No responde a laboratorio | 1 (4,2%) |
| Laboratorio completo. No responde a consulta | 1 (4,2%) |
| Consulta completa y laboratorio incompleto | 3 (12,5%) |
| Consulta incompleta y laboratorio completo | 2 (8,3%) |
| Consulta y laboratorio ambos incompletos | 2 (8,3%) |
Las principales características de las consultas se exponen en la tabla 2.
Características de las consultas de ITS
| Característica | Respuesta, n (%) |
|---|---|
| Tipo de centro | |
| Hospital de referencia | 15 (65,2%) |
| Hospital comarcal | 5 (21,7%) |
| Centro de ITS | 3 (13,1%) |
| Localización | |
| Hospital | 13 (68,4%) |
| Extrahospitalaria | 6 (31,6%) |
| Dependencia funcional | |
| Enfermedades infecciosas | 6 (31,6%) |
| Microbiología | 5 (26,3%) |
| Dermatología | 3 (15,8%) |
| Salud pública | 2 (10,5%) |
| Otros (centro monográfico, multidisciplinar) | 3 (15,8%) |
| Especialidad de los facultativos | |
| Microbiología y parasitología | 7 (33,3%) |
| Medicina interna | 4 (19%) |
| Dermatología | 3 (14,3%) |
| Medicina de familia | 2 (9,5%) |
| Ginecología | 1 (4,8%) |
| Varias especialidades | 4 (19%) |
| Facultativos que trabajan en exclusiva en la consulta | |
| 1 facultativo | 5 (26,3%) |
| 2 facultativos | 8 (42,1%) |
| Entre 3 y 5 | 5 (26,3%) |
| 8 o más | 1 (5,2%) |
| Personal de enfermería que trabaja en exclusiva | |
| 1 enfermero/a | 9 (60%) |
| 2 enfermeros/as | 4 (26,7%) |
| 4 o más | 2 (13,3%) |
| Días de la semana en los que funciona la consulta | |
| 1 día | 3 (15%) |
| 2 días | 2 (10%) |
| 4 días | 2 (10%) |
| 5 días | 13 (65%) |
| Número de pacientes/año | |
| <1.000 | 8 (47,1%) |
| Entre 1.000 y 2.000 | 4 (23,5%) |
| Entre 2.000 y 3.000 | 2 (11,8%) |
| Más de 4.000 | 3 (17,6%) |
| Número de consultas/año | |
| <1.000 | 8 (47,1%) |
| Entre 1.000 y 5.000 | 5 (29,4%) |
| Entre 5.000 y 10.000 | 2 (11,8%) |
| Más de 10.000 | 2 (11,8%) |
Las consultas de ITS dependen mayoritariamente de un hospital de referencia (15 consultas, 65,2%) frente a 5 (21,7%) que dependen de un hospital comarcal y 3 (13,1%) de un centro de ITS. El 31,6% dependen del Servicio de Enfermedades Infecciosas y el 68,4% de las consultas de ITS están dentro del propio hospital. La disponibilidad temporal de la consulta para los usuarios es la siguiente: en 13 centros (65%) la consulta funciona de lunes a viernes, mientras que en 2centros la consulta abre 4días de la semana, en otros dos centros abre 2días y en 3 centros abre solamente un día a la semana. La actividad se cuantificó mediante el número de consultas realizadas al año y el número de pacientes que acudieron.
En la tabla 3 se resumen la facilidad de acceso y los recursos diagnósticos disponibles en la propia consulta. En el 62% de los centros no se exige tarjeta sanitaria, y en el 68,2% el paciente puede acudir de forma espontánea. En 7 consultas (33%) disponen de microscopio y en 11 (52,4%) realizan pruebas diagnósticas «cerca del paciente» (POCT).
Acceso y recursos diagnósticos de las consultas
| Recurso | Sí (%) | No (%) |
|---|---|---|
| Acceso sin necesidad de tarjeta sanitaria | 13 (62%) | 8 (38%) |
| Acceso espontáneo de los pacientes, sin derivación médica | 15 (68,2%) | 7 (31,8%) |
| Realiza métodos diagnósticos «cerca del paciente» (POCT) | 11 (52,4%) | 10 (47,6%) |
| Se realiza en la consulta tinción de Gram o examen en fresco | 7 (33%) | 14 (66%) |
| Se realizan otros POCT diferentes del Gram o fresco | 8 (38%) | 13 (62%) |
| Se realiza PCR a muestras extragenitales de varones | 22 (96%) | 1 (4%) |
| Se realiza PCR a muestras extragenitales de mujeres | 19 (83%) | 4 (17%) |
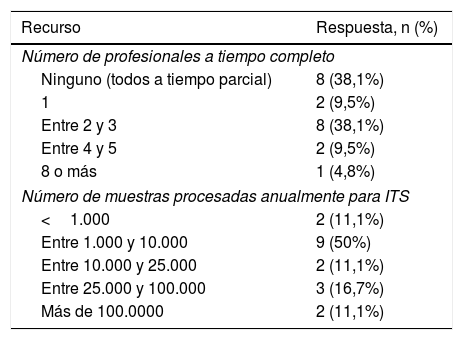
Todos los laboratorios que contestaron la encuesta son laboratorios que no se dedican exclusivamente al diagnóstico de las ITS. Esto se refleja en el número de trabajadores que se dedican a tiempo completo al diagnóstico de las ITS: en 8 centros solo tienen personal con dedicación parcial a ITS, mientras que en 13 de ellos sí disponen de personal exclusivo, en diferente número según se expone en la tabla 4. En ella también se refleja el número de muestras que anualmente se procesan para ITS, lo que es indicador de las cargas de trabajo de los diferentes laboratorios.
Laboratorios: recursos humanos y muestras procesadas
| Recurso | Respuesta, n (%) |
|---|---|
| Número de profesionales a tiempo completo | |
| Ninguno (todos a tiempo parcial) | 8 (38,1%) |
| 1 | 2 (9,5%) |
| Entre 2 y 3 | 8 (38,1%) |
| Entre 4 y 5 | 2 (9,5%) |
| 8 o más | 1 (4,8%) |
| Número de muestras procesadas anualmente para ITS | |
| <1.000 | 2 (11,1%) |
| Entre 1.000 y 10.000 | 9 (50%) |
| Entre 10.000 y 25.000 | 2 (11,1%) |
| Entre 25.000 y 100.000 | 3 (16,7%) |
| Más de 100.0000 | 2 (11,1%) |
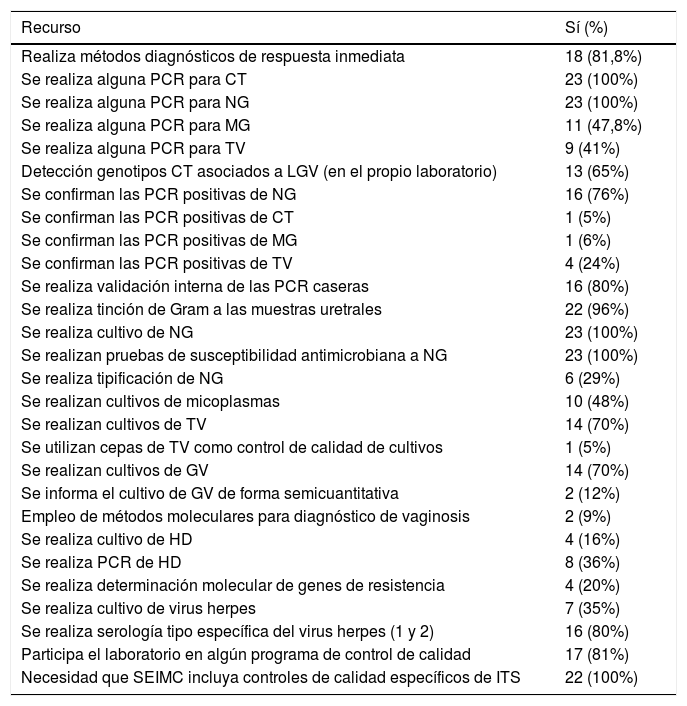
En la tabla 5 se expresan los resultados de los recursos diagnósticos de los laboratorios. En primer lugar se preguntó sobre la capacidad de realizar e informar pruebas diagnósticas de respuesta inmediata, estando disponibles en 18 centros (81,8%); son mayoritariamente la tinción de Gram (7 centros), el campo oscuro para sífilis (7 centros) y diferentes PCR (11 centros).
Recursos diagnósticos de los laboratorios
| Recurso | Sí (%) |
|---|---|
| Realiza métodos diagnósticos de respuesta inmediata | 18 (81,8%) |
| Se realiza alguna PCR para CT | 23 (100%) |
| Se realiza alguna PCR para NG | 23 (100%) |
| Se realiza alguna PCR para MG | 11 (47,8%) |
| Se realiza alguna PCR para TV | 9 (41%) |
| Detección genotipos CT asociados a LGV (en el propio laboratorio) | 13 (65%) |
| Se confirman las PCR positivas de NG | 16 (76%) |
| Se confirman las PCR positivas de CT | 1 (5%) |
| Se confirman las PCR positivas de MG | 1 (6%) |
| Se confirman las PCR positivas de TV | 4 (24%) |
| Se realiza validación interna de las PCR caseras | 16 (80%) |
| Se realiza tinción de Gram a las muestras uretrales | 22 (96%) |
| Se realiza cultivo de NG | 23 (100%) |
| Se realizan pruebas de susceptibilidad antimicrobiana a NG | 23 (100%) |
| Se realiza tipificación de NG | 6 (29%) |
| Se realizan cultivos de micoplasmas | 10 (48%) |
| Se realizan cultivos de TV | 14 (70%) |
| Se utilizan cepas de TV como control de calidad de cultivos | 1 (5%) |
| Se realizan cultivos de GV | 14 (70%) |
| Se informa el cultivo de GV de forma semicuantitativa | 2 (12%) |
| Empleo de métodos moleculares para diagnóstico de vaginosis | 2 (9%) |
| Se realiza cultivo de HD | 4 (16%) |
| Se realiza PCR de HD | 8 (36%) |
| Se realiza determinación molecular de genes de resistencia | 4 (20%) |
| Se realiza cultivo de virus herpes | 7 (35%) |
| Se realiza serología tipo específica del virus herpes (1 y 2) | 16 (80%) |
| Participa el laboratorio en algún programa de control de calidad | 17 (81%) |
| Necesidad que SEIMC incluya controles de calidad específicos de ITS | 22 (100%) |
CT: Chlamydia trachomatis; GV: Gardnerella vaginalis; HD: Haemophilus ducreyi; LGV: linfogranuloma venéreo; MG: Mycoplasma genitalium; NG: Neisseria gonorrhoeae; TV: Trichomonas vaginalis.
Para valorar el acceso a tecnología molecular se preguntó si el laboratorio disponía de alguna técnica de PCR, y la respuesta fue afirmativa en 23 (100%). Los patógenos que con mayor frecuencia se determinan mediante técnicas de PCR son Chlamydia trachomatis (CT) y Neisseria gonorrhoeae (NG) en 23 centros (100%), seguido de Mycoplasma genitalium (MG) en 11 (47,8%). La detección específica de genotipos L1-L3 asociados a linfogranuloma venéreo (LGV) se realiza en 13 de los laboratorios participantes (65%), mientras que en otros 7 (35%) se envía a un centro externo.
El cultivo de NG se realiza en la totalidad de los laboratorios, y en todos ellos también se llevan a cabo pruebas de susceptibilidad antimicrobiana, utilizando la técnica de E-test en el 73,9% de los casos. Para la interpretación de la sensibilidad, 11 laboratorios (50%) utilizan los puntos de corte definidos por EUCAST, mientras que 9 centros (41%) emplean los establecidos por el CLSI, y en dos casos emplean ambos criterios dependiendo del antimicrobiano a valorar.
La detección de marcadores moleculares de resistencia antimicrobiana en MG mediante técnicas de biología molecular se realiza en 4centros (en 2 de ellos mediante técnica casera y en otros 2 comercial), detectando mutaciones en el gen 23S rRNA (macrólidos, en 3 centros), parC y gyrA (fluoroquinolonas, en 2 centros).
Se realiza detección de Treponema pallidum (TP) mediante PCR en 7 centros, frente a microscopia de campo oscuro en 5. Para la serología de lúes, en 16 (80%) realizan algoritmo inverso, mientras que en 4 centros siguen el esquema clásico de iniciar el cribado serológico mediante una prueba no treponémica que se confirma con una treponémica.
De los 20 laboratorios que contestan a las preguntas referidas a los recursos diagnósticos empleados para el diagnóstico del virus del herpes simple (HS), 7 (35%) hacen cultivo, 16 (80%) PCR y otros 16 (80%) serología tipo específica.
De las respuestas sobre diagnóstico de los virus de las hepatitisB yC, destaca la capacidad de los laboratorios para realizar pruebas de quimioluminiscencia, si bien en un centro el diagnóstico de las hepatitis se realiza en el Laboratorio de Análisis Clínicos. En el caso de la hepatitisC, confirman la serología positiva 16 (80%) de los laboratorios que contestaron a la pregunta, y de estos 13 (81,3%) mediante una prueba de inmunoblot. El diagnóstico en un único paso (anticuerpos y carga viral en la misma muestra) no fue objeto de este estudio. Con respecto al diagnóstico del VIH, en 10 laboratorios ofertan prueba rápida. La confirmación de los resultados positivos se realiza en el propio laboratorio en el 89,5% de los casos, enviándose a un centro de referencia en el resto.
Respecto a los controles de calidad, 17 de los 21 laboratorios que contestaron (81%) realizan algún control de calidad externo, mayoritariamente el de la SEIMC (88%). Todos los que respondieron reconocen la necesidad de que el programa de control de calidad de la SEIMC incluya controles de calidad para patógenos de ITS diferentes de los habituales para VIH, hepatitis y lúes.
DiscusiónEl presente estudio es una iniciativa del GEITS que pretende conocer los recursos de que disponen las consultas y laboratorios especializados en ITS en España, partiendo de la premisa de que los diferentes profesionales que dedican gran parte de su esfuerzo profesional a estas infecciones pertenecen al grupo, si bien es cierto que ello constituye una limitación del estudio, pues nos ha impedido hacer llegar el cuestionario a otros profesionales que, dedicando su actividad a las ITS, no forman parte del GEITS.
Las respuestas obtenidas proporcionan al estudio un adecuado grado de representación, pues han participado tanto consultas como laboratorios de centros repartidos por gran parte de la geografía nacional, y ha involucrado no solamente a grandes centros especializados, sino también a consultas y laboratorios más pequeños y con menos recursos pero que también están implicados en la lucha contra las ITS. Este trabajo refleja una realidad diversa y heterogénea representativa de las distintas situaciones que se dan en nuestro país.
Según nuestros conocimientos, existen pocos estudios de este tipo realizados en otros países. El European Center for Disease Prevention and Control (ECDC) realizó una encuesta en 2010, pero solamente iba dirigida a centros de referencia de los diferentes países europeos2. Más parecido es el estudio publicado en Irlanda3 en 2018, dirigido solamente a laboratorios, en el que respondieron 36 centros con una tasa de respuesta del 92%, probablemente tan elevada debido a que se trataba de un cuestionario oficial enviado por el Servicio de Salud Irlandés, lo que presupone cierto grado de obligación a responder.
En nuestro entorno, las consultas de ITS se localizan mayoritariamente en centros hospitalarios, habitualmente de gran tamaño, con dependencia funcional muy variable y con facultativos de formación muy diversa. Los recursos de personal son muy variables dependiendo del tamaño del centro. Cabe destacar el dato de que en el 38% de las consultas el paciente precisa presentar la tarjeta sanitaria, lo que excluye de la atención a grupos de población en situación de vulnerabilidad que son diana de estas infecciones4-6.
Las ITS precisan un diagnóstico y, sobre todo, un tratamiento rápido que evite la diseminación de la infección a otros individuos. Es por ello que el acceso rápido y abierto a la consulta es muy importante7, y en las consultas estudiadas el acceso inmediato se produce en el 68,2% de ellas, pero deja otro 31,8% de consultas en las que el paciente debe acudir a su médico de atención primaria para que le derive a la consulta de ITS si lo considera oportuno. En la misma línea es importante conocer la disponibilidad de pruebas rápidas POCT en la consulta, ya que aunque su sensibilidad y especificidad varían según cada caso, contribuyen a dispensar tratamientos dirigidos en la primera consulta sin necesidad de prescribir tratamientos empíricos o a programar una segunda consulta demorada en el tiempo8. Nuestro estudio revela que en el 52,4% de las consultas se realiza algún tipo de diagnóstico rápido, destacando que el 33% tienen microscopio y capacidad para realizar tinción de Gram o examen en fresco de los exudados. Esto indica un alto nivel de preparación y compromiso por parte de los clínicos que asumen pruebas de examen microscópico, ya que son técnicas con cierto grado de subjetividad y que requieren una gran experiencia del microscopista.
Respecto a los laboratorios, ninguno de los que respondieron se dedica exclusivamente al diagnóstico de las ITS, existiendo una gran variabilidad en el tamaño, y en general, con una elevada carga asistencial. La mayoría de ellos realizan pruebas diagnósticas de respuesta inmediata, aunque la capacidad real de ofrecer un diagnostico inmediato, idealmente antes de que el paciente abandone la consulta, viene mediada por la localización, la distancia y la facilidad para el envío de muestras desde la consulta al laboratorio, aspectos no contemplados en la encuesta.
Con respecto a las técnicas de PCR, existe una implantación completa en todos los laboratorios de la determinación de CT y NG, pero en cambio solamente el 47,8% realizan la PCR para detectar MG, lo cual es muy preocupante si tenemos en cuenta que es la única tecnología capaz de detectar dicho microorganismo. Así pues, en el momento de realizar la encuesta el 52,2% de los laboratorios no pueden determinar la presencia de uno de los principales patógenos productores de uretritis no gonocócicas persistentes.
Otro hecho relevante es que el 24% de los laboratorios no realizan confirmación de las PCR de NG positivas de origen extragenital, lo que puede dar lugar a falsos positivos9.
A pesar de que el 100% de los laboratorios son capaces de realizar detección genómica de NG mediante PCR, todos ellos continúan manteniendo la capacidad realizar cultivo de gonococo, fundamentales para monitorizar la sensibilidad antimicrobiana de este microorganismo y detectar de forma precoz la aparición de cepas multirresistentes, tan necesario en el contexto de gonococos multirresistentes en el que nos encontramos10. Mientras no existan técnicas moleculares fiables de detección de resistencias, el cultivo es nuestra única herramienta que nos permite realizar técnicas de susceptibilidad contrastadas y, adicionalmente, poder hacer estudios de tipificación que nos ayuden a comprender la epidemiología de esta infección.
La detección de resistencias en MG solo puede hacerse mediante técnicas moleculares, y esta capacidad solo la tienen 4 laboratorios en el momento del estudio, lo que resulta preocupante, puesto que las tasas de resistencia de MG a azitromicina se sitúan, según series11,12, entre el 16 y el 36%.
Este trabajo presenta varias limitaciones. No se evaluaron los recursos diagnósticos disponibles frente a todas las ITS existentes, debido a que incrementaría de forma muy importante la extensión de una encuesta ya de por sí prolija (104 preguntas), por lo que no se preguntó específicamente por el virus del papiloma humano ni por el virus de la hepatitisA (entre otros), y en el caso de los virusB yC de las hepatitis se hizo de forma somera, pues consideramos que son entidades que por sí mismas merecen estudios específicos, tal como recientemente ha sido publicado en esta revista sobre el diagnóstico en un solo paso del virus de la hepatitisC13. Otras limitaciones derivan del carácter descriptivo del estudio, que nos muestra una realidad muy heterogénea en el tipo de centro, en la población de estudio y en los recursos disponibles. Ello dificulta la estratificación de los centros en función de distintas variables e impide la realización de estudios comparativos.
En conclusión, este trabajo refleja la realidad en cuanto a la capacidad de diagnóstico y manejo de las ITS en nuestro país. En él se objetiva una importante variabilidad de recursos entre los diferentes centros, pero también permite identificar la excelente dotación diagnóstica de un número nada despreciable de ellos. Desde GEITS se pretende que el conocimiento aquí generado incentive el trabajo colaborativo y la unificación de criterios que permitan abordar de forma coordinada y eficaz el diagnóstico de las ITS.
Conflicto de interesesNinguno.
Agradecemos a los hospitales e investigadores de cada centro que han respondido a la encuesta su participación en el estudio.
También agradecemos a Javier Ávila, de la Secretaría de la SEIMC, por la elaboración del formulario online de preguntas y su distribución entre los miembros de GEITS.
José Ángel Alava Menica (Hospital Universitario de Basurto), Alicia Barreales Fonseca (Hospital Universitario de Burgos), Josefina Belda Ibáñez (Centro de Información y Prevención del VIH/SIDA e ITS, Alicante), Xabier Beristain Rementería (Complejo Universitario de Navarra), Amaia Cuñado Eizaguirre (Hospital Mendaro, Guipúzcoa), Billie Caceda (Hospital Alto Deba, Guipúzcoa), Cori Gázquez Gómez (Hospital San Juan, Alicante), Araceli Hernández Betancor (Hospital Universitario Insular de Gran Canaria, Las Palmas), Melisa Hernández Febles (Hospital Universitario de Gran Canaria Dr. Negrín, Las Palmas), Leonora Hernández Ragpa (Hospital Universitario de Basurto), Marta Herrero Romero (Hospital Virgen del Rocío, Sevilla), Joaquín López-Contreras González (Hospital de la Santa Creu i San Pau, Barcelona), David Navarro Ortega (Hospital Clínico Universitario de Valencia), María Palomo Lastra (Hospital General Universitario Gregorio Marañón, Madrid), Begoña Palop-Borras (Hospital Regional Universitario de Málaga), Luis Piñeiro (Hospital Universitario Donostia), Carmen Potel Alvarellos (Complejo Hospitalario Universitario de Vigo), Carmen Rodríguez (Centro Sanitario Sandoval, Madrid), Manuel Rodríguez-Iglesias (Hospital Universitario Puerta del Mar/Hospital San Carlos, Cádiz), Juan Romanyk Cabrera (Hospital Príncipe de Asturias, Alcalá de Henares), Jesús Santos (Hospital Virgen de la Victoria, Málaga), Laura Villa Bajo (Hospital Universitario Central de Asturias, Oviedo).