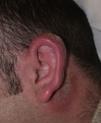
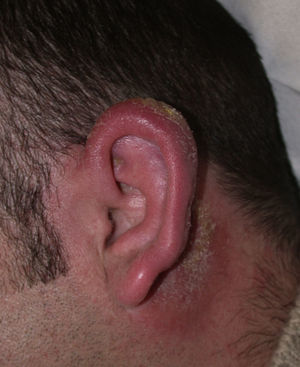
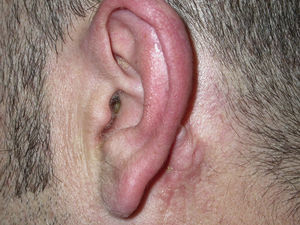
Varón de 33años, residente en Mallorca, sin antecedentes patológicos ni familiares de interés ni viajes recientes; remitido al servicio de dermatología de nuestro hospital por una llamativa inflamación del pabellón auricular derecho de 2meses de evolución, mostrándose edematizado, con zonas costrosas y descamativas (fig. 1).
Había recibido varios tratamientos tópicos (pomada de gentamicina, betametasona y clotrimazol) y sistémicos (amoxicilina-clavulánico y ciprofloxacino) sin ninguna mejoría.
EvoluciónSe realizó un frotis con escobillón y una biopsia de la lesión, dividiéndose en 2porciones, para estudio anatomopatológico y microbiológico.
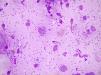
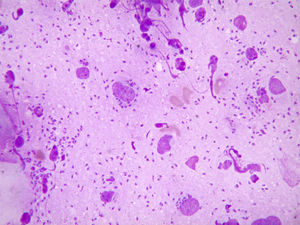
Los cultivos en medios habituales resultaron negativos. Los cortes histológicos con tinción de hematoxilina-eosina y el frotis con tinción de Giemsa mostraron numerosos amastigotes (fig. 2). Se cultivó en medio bifásico de agar sangre (NNN) y se identificó la especie Leishmania infantum mediante técnicas de reacción en cadena de la polimerasa.
El tratamiento consistió en antimoniato de meglumina intramuscular (10mg/kg/día) durante 20días, obteniendo la resolución completa del cuadro (fig. 3).
DiscusiónLas leishmaniasis son producidas por la infección de protozoos del género Leishmania, inoculados por hembras de dípteros Phlebotomus y Lutzomyia. La leishmaniasis cutánea por L.infantum es frecuente en España, especialmente en determinadas áreas geográficas, como las Islas Baleares1,2. El diagnóstico de leishmaniasis cutánea es difícil por la diversidad de presentaciones clínicas y la necesidad de medios de cultivo específicos.
Las manifestaciones clínicas son muy variadas, dependiendo del tropismo de la especie y de su capacidad infectiva, así como factores propios del vector y de la situación de inmunocompetencia del huésped1. Existen formas viscerales (kala-azar), mucocutáneas y cutáneas. Dentro de las lesiones cutáneas encontramos desde el más frecuente botón de oriente hasta las formas en placa, hiperqueratósicas, verrugosas y papilomatosas, zosteriformes, esporotricoides y las formas erisipeloides y eccematiformes3-5, como la mostrada.
Aunque usualmente autolimitada, el tratamiento de la leishmaniasis cutánea está indicado para acelerar la curación, disminuir las cicatrices y evitar la diseminación del parásito en determinadas lesiones6,7. Los tratamientos físicos, como la crioterapia, pueden ser utilizados solos o de forma coadyuvante. En lesiones bien delimitadas, como el botón de oriente, el tratamiento intralesional es el de elección, salvo que su localización o extensión lo desaconsejen.
El tratamiento sistémico con antimoniales pentavalentes es la medicación de primera línea cuando está indicado el tratamiento sistémico. Se utilizan el antimoniato de meglumina y el estibogluconato de sodio. Las pautas habituales son de 10-20mg/kg/día, por vía intramuscular o intravenosa, durante 10-20días8-10, vigilando efectos secundarios típicos, como síntomas gastrointestinales, y otros graves, como alteraciones electrocardiográficas, elevación de las transaminasas, pancreatitis y neuropatía periférica. Existen otras alternativas, como anfotericinaB liposomal11, con eficacia similar y menos efectos secundarios aunque con un mayor coste inicial12,13, y pentamidina14, con los que tenemos menos experiencia.
Con este caso pretendemos demostrar que la leishmaniasis cutánea puede adoptar una gran variedad de formas clínicas; muy diferentes al clásico botón de oriente o pápula ulcerada. Aun tratándose de pacientes inmunocompetentes, debemos tener en cuenta esta entidad en el diagnóstico diferencial de lesiones dérmicas de evolución atípica y comunicar esta sospecha al servicio de microbiología para detectar el parásito con la mayor celeridad.