La criptococosis meníngea es una de las patologías con mayor mortalidad en pacientes con sida. La diabetes mellitus (DM) comprende un grupo de enfermedades metabólicas que afecta a gran parte de la población mundial. La evolución de las infecciones en pacientes diabéticos ha demostrado ser siempre más grave.
El objetivo de este trabajo fue analizar la evolución de pacientes con criptococosis meníngea, DM e infección por VIH, comparándola con la de enfermos VIH-positivos con criptococosis meníngea de similar gravedad, pero no diabéticos.
Materiales y métodosSe analizaron las historias clínicas de 182 pacientes con diagnóstico de criptococosis meníngea. Fueron seleccionados 28 pacientes con características clinicoepidemiológicas similares, se los dividió en 2 grupos, 14 pacientes con DM (grupo A) y los restantes sin alteraciones en el metabolismo de los glúcidos (grupo B).
ResultadosSolo 3/14 pacientes del grupo A (21,4%) lograron la negativización del cultivo de LCR, antes de las 10 semanas de tratamiento. Con respecto al grupo B, esto sucedió en 11/14 enfermos (78,5%).
La mortalidad global para el grupo A fue del 85,7% (12/14 pacientes), para el grupo B del 21,4% (3/14 pacientes).
En todos los casos los aislamientos de Cryptococcus neoformans resultaron sensibles in vitro a la anfotericina B y al fluconazol.
ConclusionesLa vinculación de DM y meningitis por Cryptococcus spp. se asoció a la evolución desfavorable en la gran mayoría de los casos; esto plantea la posibilidad de extender el tratamiento de inducción.
Cryptococcal meningitis is a severe AIDS-related infectious disease, with a high mortality rate. Diabetes mellitus (DM) is a metabolic disorder very common worldwide. Infectious diseases in diabetic patients are always more severe than in non-diabetic ones.
The aim of this study was to compare the outcome of a group of HIV-positive patients with DM and cryptococcal meningitis with a similar group HIV-positive patients with cryptococcal meningitis, but without DM.
Material and methodsA total of 182 clinical records of HIV-positive patients suffering cryptococcal meningitis were reviewed, and 28 of them with similar clinical and epidemiological characteristics, were chosen. They included 14 patients with DM (group A) and the remaining 14 who did not suffer this metabolic disorder (group B).
ResultsOnly 21.4% (3/14 cases) of group A patients had negative CSF cultures after 10 weeks of treatment. In group B patients, 78.5% (11/14 cases) achieved negative CSF cultures before 10 weeks.
A higher overall mortality rate was observed in the diabetic patients (85.7%, 12/14 cases) than in the non-diabetic group (21.4%, 3/14 cases).
All CSF isolates were identified as Cryptococcus neoformans, and all strains were susceptible in vitro to amphotericin B and fluconazole.
ConclusionsCryptococcal meningitis in diabetic patients was associated with a poor clinical outcome and a high mortality rate. A longer treatment induction period is suggested in order to improve the outcome of cryptococcal meningitis in diabetic patients.
Dentro de los complejos mecanismos que desarrolla el hígado para mantener la homeostasis se encuentra la conservación de la concentración plasmática de glucosa, la cual se altera entre otras causas en las hepatopatías virales crónicas1. Numerosas comunicaciones demuestran una fuerte asociación entre diabetes mellitus (DM) e infecciones por el virus de la hepatitis B y fundamentalmente por el virus de la hepatitis C2,3. Asimismo se han publicado varios casos de DM posteriores a los tratamientos con interferón pegilado4.
La DM comprende un grupo de enfermedades metabólicas caracterizadas por hiperglucemias asociadas a defectos en la secreción de insulina, en la acción de esta hormona o en ambas5. Actualmente se clasifica la DM en tipo 1 (insulina-deficiente de causa inmunológica o idiopática), tipo 2 (con resistencia a la insulina y alteraciones en la secreción de insulina en menor medida), la diabetes mellitus gestacional, y otros tipos específicos de DM, entre los que se incluyen defectos genéticos en la función de la célula beta, defectos genéticos en la acción de la insulina, enfermedades del páncreas exocrino, endocrinopatías en general, DM inducida por fármacos, las formas inmunológicas denominadas raras o poco habituales de DM, síndromes genéticos asociados a DM, y por último las de causas infecciosas5.
La criptococosis es una micosis sistémica, común al hombre y a otras especies de animales, producida por el complejo Cryptococcus neoformans (C. neoformans)/Cryptococcus gattii, hongos levaduriformes capsulados de distribución universal6. En la actualidad ha pasado de ser un patógeno infrecuente para el hombre a ser un agente oportunista habitual, debido al espectacular incremento de pacientes inmunocomprometidos en la población general.
La asociación de la criptococosis meníngea (pacientes con cultivo positivo de LCR) y la DM en pacientes VIH-positivos es un serio desafío para el tratamiento de la infección fúngica.
ObjetivoAnalizar la evolución de pacientes con infección por VIH y criptococosis meníngea asociada a DM en un período comprendido desde octubre del 2008 hasta septiembre del 2011 y compararla con los enfermos VIH-positivos con criptococosis meníngea de similar gravedad, pero no diabéticos.
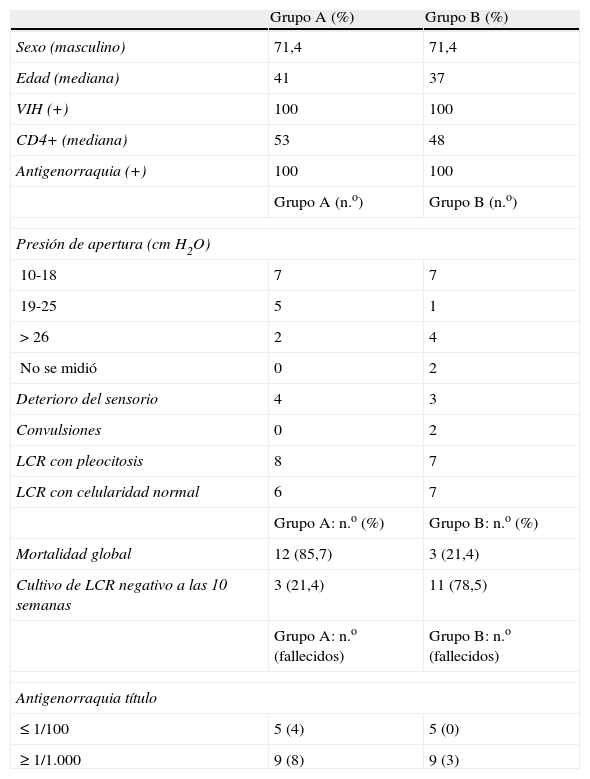
Materiales y métodosEstudio observacional, descriptivo y retrospectivo. Se analizaron las historias clínicas de 182 pacientes con diagnóstico de criptococosis meníngea en nuestro hospital. La prevalencia de DM en pacientes con criptococosis fue del 7,7%. Fueron seleccionados 28 pacientes con características clinicoepidemiológicas similares, que a su vez fueron divididos en 2 grupos comparables, 14 pacientes con DM (grupo A) y los restantes sin alteraciones en el metabolismo de los glúcidos (grupo B). Las principales características de los pacientes incluidos en ambos grupos se exponen en la tabla 1.
Características de los pacientes con criptococosis con y sin diabetes
| Grupo A (%) | Grupo B (%) | |
| Sexo (masculino) | 71,4 | 71,4 |
| Edad (mediana) | 41 | 37 |
| VIH (+) | 100 | 100 |
| CD4+ (mediana) | 53 | 48 |
| Antigenorraquia (+) | 100 | 100 |
| Grupo A (n.o) | Grupo B (n.o) | |
| Presión de apertura (cm H2O) | ||
| 10-18 | 7 | 7 |
| 19-25 | 5 | 1 |
| >26 | 2 | 4 |
| No se midió | 0 | 2 |
| Deterioro del sensorio | 4 | 3 |
| Convulsiones | 0 | 2 |
| LCR con pleocitosis | 8 | 7 |
| LCR con celularidad normal | 6 | 7 |
| Grupo A: n.o (%) | Grupo B: n.o (%) | |
| Mortalidad global | 12 (85,7) | 3 (21,4) |
| Cultivo de LCR negativo a las 10 semanas | 3 (21,4) | 11 (78,5) |
| Grupo A: n.o (fallecidos) | Grupo B: n.o (fallecidos) | |
| Antigenorraquia título | ||
| ≤1/100 | 5 (4) | 5 (0) |
| ≥1/1.000 | 9 (8) | 9 (3) |
Todos los pacientes del grupo A presentaron por lo menos 2 valores de glucemia en ayunas mayores de 200mg/dl durante la internación; asimismo se realizaron controles de glucemia predesayuno, prealmuerzo y precena, siendo los valores mayores de 160mg/dl corregidos con insulina corriente subcutánea.
En todos los casos la especie aislada en LCR fue C. neoformans identificada por los procedimientos habituales del laboratorio7.
Los títulos de antigenorraquia se determinaron por aglutinación de partículas de látex (Crypto Latex antigen detection system IMMY®, Immunomycologics, EE. UU.).
Se realizaron las pruebas de sensibilidad a los antifúngicos utilizados mediante la concentración inhibitoria mínima por microdilución, según documento M27-A3 (normas del CLSI)8.
Para comparar la mortalidad entre ambos grupos se utilizó como medida de asociación el odds ratio (OR), para lo que se empleó el programa estadístico Epi Info 3.5.4.
ResultadosSeis enfermos del grupo A eran diabéticos tipo 2, uno de los cuales era insulinorrequiriente. Solo un enfermo era diabético tipo 1 y los 7 restantes se clasificaron como otros tipos específicos de DM relacionados con hepatopatías virales, 6 eran positivos para el virus de la hepatitis C y uno portaba virus de la hepatitis B.
Se logró la negativización del cultivo de LCR en 3/14 pacientes del grupo A (21,4%) antes de las 10 semanas de tratamiento. Con respecto al grupo B esto sucedió en 11/14 enfermos (78,5%), 6 necesitaron entre 4 y 6 semanas, los 5 restantes lo hicieron entre 8 y 10 semanas.
La mortalidad global para ambos grupos se expone en la tabla 1. Hubo asociación estadísticamente significativa entre la mortalidad y el pertenecer al grupo A de pacientes (OR 22; IC95% 3,08-157,3; p=0,0009).
Los títulos de antigenorraquia para Cryptococcus de los pacientes diabéticos no fue un dato útil para predecir la evolución a diferencia de lo que ocurre en los pacientes que no presentan esta patología9. Estos datos se observan en la tabla 1.
Diez de los 14 pacientes del grupo A fueron tratados con anfotericina B desoxicolato 0,7mg/kg/día por vía intravenosa y fluconazol 800mg/día en forma simultánea, hasta una dosis acumulativa de anfotericina B igual a 1.200mg, para continuar después con fluconazol 800mg hasta las 12 semanas. Tres pacientes realizaron tratamiento de inducción solo con anfotericina B desoxicolato 0,7mg/kg/día por vía intravenosa. Un solo enfermo del grupo A pudo ser tratado con anfotericina B desoxicolato más 5-fluorocitosina 100mg/kg/día, con mala respuesta clínica.
Diez pacientes del grupo B recibieron tratamiento de inducción con anfotericina B desoxicolato y fluconazol en forma simultánea con igual dosis y tiempo que el grupo A; 4 pacientes de este grupo recibieron tratamiento de inducción únicamente con anfotericina B.
Las formulaciones lipídicas de anfotericina B incluyen anfotericina B liposomal (3-4mg/kg/día) y anfotericina B complejos lipídicos (5mg/kg/día); estas deben sustituir a la anfotericina B desoxicolato en pacientes que presenten predisposición a la insuficiencia renal. Debido a su alto costo, en nuestra institución solo se utilizan estas formulaciones en los enfermos que presenten como efecto adverso el deterioro de la función renal durante el tratamiento.
Es importante destacar que, además del tratamiento antifúngico y del control de la DM, los pacientes que presentaron hipertensión endocraneal requirieron reiteradas punciones lumbares hasta normalizar la presión de apertura.
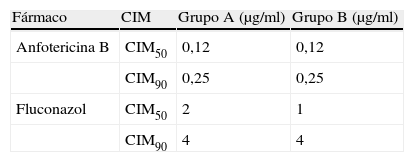
En todos los casos los aislamientos de C. neoformans resultaron sensibles a los 2 fármacos utilizados mediante la determinación de concentración inhibitoria mínima por microdilución (tabla 2), según documento M27-A3 (normas del CLSI)8.
Cinco pacientes del grupo A fallecieron durante el período de inducción y 6 durante el período de consolidación, solo uno falleció después de las 12 semanas. Respecto al grupo B, los 3 fallecidos presentaron el deceso durante el período de inducción. En todos los casos la causa fue la criptococosis meníngea.
La carga viral del VIH no es un examen que se realice rutinariamente a los pacientes internados en nuestro hospital. Solamente se realizó esta determinación a 3 pacientes el mes previo a la internación, 2 pertenecían al grupo B y uno al grupo A; en todos los casos fue menor de 50 copias/ml. Solo 2 enfermos del grupo A y 3 del grupo B se encontraban con tratamiento antirretroviral al momento del ingreso hospitalario, todos con igual esquema terapéutico (lamivudina 300mg/día, zidovudina 600mg/día, efavirenz 600mg/día). Durante la internación ningún paciente recibió antirretrovirales.
Discusión y conclusionesEl tratamiento de primera línea para la criptococosis meníngea consiste en administrar concomitantemente anfotericina B desoxicolato 0,7 a 1mg/kg diario por vía intravenosa, más 5-fluorocitosina 100mg/kg/día por vía oral dividido en 4 tomas. Ese esquema sigue siendo el más efectivo para tratar estos casos10, pero este último fármaco no se produce ni se importa en nuestro país, por ese motivo se utilizó durante muchos años anfotericina B como monoterapia de inducción y luego fluconazol como tratamiento de consolidación. En los últimos 24 meses se implementó de manera sistemática en nuestro hospital la utilización de terapia combinada, anfotericina B más fluconazol en el período de inducción según las recomendaciones internacionales11.
Luego del tratamiento de inducción y consolidación el paciente continúa con controles clínicos y de antigenemia y recibe profilaxis secundaria con fluconazol 200mg/día, hasta alcanzar 2 recuentos de CD4+ superiores a 200 células/μl, con carga viral para el VIH indetectable, durante un mínimo de 3 meses. Además la duración de la terapia antifúngica no debe ser nunca menor de un año6–12
En la respuesta inmunológica del huésped frente al género Cryptococcus merece destacarse la participación de los componentes celulares de la inmunidad innata, neutrófilos, macrófagos y células natural killer13. Los linfocitos T CD4+ sensibilizados estimulan la producción de citocinas proinflamatorias como γ-INF, IL2, IL12, IL18, que dan origen de esta forma a una respuesta con predominio de citocinas de tipo Th1, la que genera la estimulación de los macrófagos y la producción de granulomas epitelioides compactos que controlan la infección14.
Las alteraciones del sistema inmunológico producidas en pacientes diabéticos son consecuencia de desarreglos metabólicos asociados con la enfermedad y tornan a estos huéspedes más susceptibles a padecer procesos infecciosos15,16.
Estudios experimentales llevados a cabo in vitro han demostrado que la DM reduce la actividad de los polimorfonucleares neutrófilos17, inhibe la respuesta de los linfocitos T y disminuye la capacidad fagocítica del sistema monocítico-histiocitario18,19
Habitualmente se duda acerca de la relación que presentan los fenómenos observados in vitro, cuando se los vincula a la evolución clínica de estos enfermos. De acuerdo a lo demostrado en nuestro estudio, parecería existir cierta concordancia en la relación in vitro-in vivo con respecto a los fenómenos inmunológicos que se observan en enfermos que padecen DM y criptococosis asociada a sida.
Las infecciones que más frecuentemente presentan los pacientes con DM son de etiología bacteriana, producidas especialmente por Streptococcus pneumoniae, Staphylococcus aureus y Escherichia coli entre los más involucrados. Estos microorganismos generan infecciones de los tractos respiratorio y urinario así como de la piel y las mucosas17–19. Las micosis se observan en menor medida y se asocian al género Candida y al orden Mucorales20. Cryptococcus spp. ha sido hallado en escasas ocasiones como causa de enfermedad pulmonar exclusivamente y afección del SNC en pacientes con DM, pero no hay publicaciones, hasta la fecha, de enfermos que presenten DM y criptococosis meníngea asociada a sida.
La meningitis por Cryptococcus spp. en pacientes diabéticos presentó una evolución desfavorable en la gran mayoría de los casos; esto plantea la posibilidad de extender el período de inducción.
Es muy importante que estos enfermos permanezcan internados hasta tener por lo menos un cultivo negativo de LCR. Además es vital mantener al paciente en normoglucemia mientras se encuentre en tratamiento específico antimicótico, debido a que algunos microorganismos se vuelven más virulentos cuando los niveles de glucosa en sangre son superiores a los normales17.
Es posible que la comorbilidad que presentan estos pacientes con el virus C y B modifique la evolución de la criptococosis meníngea. Hasta la fecha no hay publicaciones y creemos que nuestro trabajo puede ser el comienzo para posteriores investigaciones al respecto; en nuestro hospital siempre se priorizó el tratamiento de la criptococosis meníngea sobre las otras comorbilidades que pueda presentar el enfermo, con lo cual en ninguno de los casos se les realizó carga viral para virus C o B
Los fracasos terapéuticos en ambos grupos de pacientes no se relacionaron con resistencia a los antifúngicos empleados, ya que todos los aislamientos fueron sensibles in vitro a fluconazol y anfotericina B21,22. Sin embargo, como se ha expuesto hubo fracasos terapéuticos. Esto destaca, una vez más, las dificultades que existen en la interpretación de las pruebas de sensibilidad in vitro frente a fármacos antifúngicos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.