La pandemia de gripe A (H1N1) 2009 repercutió inicialmente de forma leve en los hospitales de Cataluña, pero en el otoño se produjo una destacada onda pandémica. Se describen las principales características de los pacientes atendidos en el Hospital Universitaro Vall d’Hebron de Barcelona (HUVH) en el transcurso de la pandemia, la factores asociados a riesgo de hospitalización y la carga asistencial generada.
Pacientes y métodosSe incluyen todos los casos de gripe A (H1N1) 2009 con confirmación microbiológica, atendidos desde el 2 de julio de 2009 al 22 de enero de 2010. Se ha realizado un análisis descriptivo de los casos y un análisis multivariado para conocer las variables asociadas al riesgo de hospitalización.
ResultadosEl diagnóstico se confirmó en 741 pacientes, de los que el 56,8% tenían menos de 16 años, mientras que los de 65 y más años representaron únicamente el 2,8%. Un 33% de los niños no presentaron ningún factor de riesgo de complicaciones, en cambio en los adultos fueron el 45%. Fueron hospitalizados 190 casos, de ellos 26 en UCI con 5 defunciones. La edad inferior a un año, la inmunodeficiencia y la patología neuromuscular fueron los factores asociados de forma significativa al riesgo de hospitalización en niños, y la patología crónica pulmonar en los adultos. El diagnóstico de neumonía en urgencias fue un factor determinante de hospitalización, tanto en niños como adultos. La máxima carga asistencial se registró el 19 de noviembre con 43 pacientes hospitalizados, 6 de ellos en UCI.
ConclusiónEntre julio y septiembre la pandemia tuvo una repercusión asistencial reducida, pero en el otoño ocasionó un marcado aumento de las urgencias y las hospitalizaciones. La mayor frecuencia de casos confirmados se registró en los niños, mientras que la de hospitalizados se produjo entre los adultos. El riesgo de ingreso fue más elevado en los pacientes con determinados factores de riesgo y en especial en aquellos con neumonía. La onda pandémica supuso una carga de intensidad moderada para el HUVH, pues no implicó la modificación de sus programas asistenciales habituales.
The influenza A (H1N1) 2009 pandemic initially had a mild impact in Catalonian hospitals, but in the autumn there was an important pandemic wave. We describe the main characteristics of patients seen in the Vall d’Hebron University Hospital in Barcelona (HUVH) during this pandemic, the risk factors associated with hospitalization and the health-care burden generated.
Material and methodWe included all cases of influenza A (H1N1) 2009 with laboratory confirmation seen in the HUVH from July 2, 2009 to January 22, 2010. We performed a descriptive analysis of the cases and a multivariate analysis to identify variables associated with the risk of hospitalization.
ResultsThe diagnosis was confirmed in 741 patients; 56.8% were under 16 years, while only 2.8% were 65 and over. Thirty three per cent of children had no risk factor for complications, whereas in adults it was 45%. One hundred and ninety cases were hospitalized, 26 of them in the intensive care unit (ICU) with 5 deaths. The factors associated with risk of hospitalization were, age less than one year, immunodeficiency, and neuromuscular disease in children; and chronic lung disease in adults. The diagnosis of pneumonia in the emergency department was an important predictor of hospitalization in both children and adults. The maximum caseload was recorded on November 19, with 43 hospital admissions, 6 of them in the ICU.
ConclusionsBetween July and September 2009 the pandemic had a low impact on hospital resources, but in autumn there was a marked increase in emergency department visits and hospitalizations. Children had higher rates of confirmed cases, while adults had higher rates of hospitalizations. The risk of hospitalization was higher in patients with certain conditions especially in those with pneumonia. The pandemic wave was a moderate work load for HUVH, since it did not involve any modification of the usual health care programs.
El 17 de abril de 2009 fueron notificados en California los dos primeros casos de gripe A (H1N1) 20091, y el día 27 del mismo mes fue declarado el primer caso confirmado por el laboratorio en España2. La fase inicial de la pandemia, desde finales de abril hasta mediados de agosto de 2009 afectó con cierta intensidad a México, Estados Unidos y Reino Unido, pero en España y otros países de Europa continental las visitas y hospitalizaciones fueron limitadas. Posteriormente, en los meses de octubre y noviembre, en España y en la mayoría de los países del hemisferio norte se produjo una destacada onda pandémica3–6.
El 11 de junio, al declarar establecida la situación de pandemia, la Directora General de la Organización Mundial de la Salud (OMS) informó que la nueva gripe tenía unas características clínicas similares a las de la gripe estacional, afectaba principalmente a los jóvenes y su gravedad era reducida7. Por otro lado, al iniciarse la diseminación pandémica enseguida se detectó que las personas que tenían alguno de los conocidos factores de riesgo de complicaciones por la gripe estacional, como patología pulmonar, inmunodeficiencia, cardiopatía y embarazo, mostraban también riesgo de complicaciones por la nueva gripe. Como novedad, la obesidad mórbida fue añadida a la lista de factores8.
Tras la eclosión de la pandemia, en España, los hospitales y centros asistenciales de acuerdo con las autoridades sanitarias9–11 pusieron en marcha protocolos de diagnóstico, tratamiento y prevención, así como planes de contingencia para hacer frente a la carga asistencial que pudiera producirse.
En el presente artículo se exponen las características de los pacientes atendidos, las variables asociadas al riesgo de hospitalización y la carga asistencial registrada durante la pandemia en el Hospital Universitario Vall d’Hebron de Barcelona (HUVH).
Material y métodosDiseñoEstudio de cohorte retrospectiva.
ÁmbitoEl HUVH es un centro terciario de 1.186 camas, en el que en el año 2008 ingresaron 66.536 pacientes. Atiende a pacientes de todas las especialidades médicas y quirúrgicas, tanto de adultos como pediátricas, e incluye programas de trasplante tanto de órgano sólido como hemopoyético. Está situado en el noreste de la urbe de Barcelona y su población de referencia es de 453.196 habitantes12.
Con objeto de coordinar las actuaciones asistenciales del hospital ante la pandemia, en el mes de mayo de 2009 se constituyó un grupo multidisciplinar con representantes de los servicios y áreas más implicadas. Se elaboró un plan de contingencia que preveía la sucesiva afectación de camas de hospitalización general y de UCI en función de las necesidades que se presentaran. Durante la onda pandémica este grupo se reunió como mínimo una vez al día, en los días laborables.
Población estudiada y períodoSe han incluido en el estudio todos los casos de gripe A (H1N1) 2009 confirmados por el laboratorio, y atendidos en los servicios de urgencias de las Áreas General y Materno-Infantil del HUVH, o en los servicios de hospitalización y de consultas externas, desde julio de 2009 a enero de 2010.
Variables estudiadasSe recogió información sobre: datos demográficos (edad en años y sexo), presencia de factores de riesgo de complicaciones (cardiopatía, diabetes, inmunodeficiencia, insuficiencia renal, neoplasia, obesidad mórbida, patología neuromuscular, patología pulmonar crónica y embarazo), presencia de neumonía, ingreso hospitalario, estancia hospitalaria en días, ingreso en UCI y estancia en UCI, ventilación mecánica, período desde el inicio de los síntomas hasta la realización de la prueba de confirmación en días, y desde el inicio de los síntomas hasta el inicio del tratamiento en días y evolución, administración de tratamiento antiviral y fármaco recibido. La definición usada de las anteriores variables ha sido la señalada en los protocolos internacionales vigentes en aquel momento sobre la gripe A13,14. La información se recogió a partir de las historias clínicas informatizadas. No se dispuso de información sobre la situación vacunal de los pacientes ante la gripe estacional en la temporada previa o ante la pandémica. Los casos de gripe de tipo comunitario o nosocomial sucedidos en el personal del hospital, no se incluyen en este trabajo. En la categoría de edades que denominamos «niños» se incluyen todos los pacientes menores de 16 años, y en la de «adultos» todos los de 16 y más años.
Selección de los casosEl Servicio de Microbiología del HUVH proporcionó los resultados de las pruebas de confirmación realizadas diariamente en muestras respiratorias de los que se seleccionaron los casos positivos. No se incluyen 4 casos hospitalizados procedentes de otros hospitales cuya confirmación diagnóstica se realizó en el centro de origen. No se trasladaron pacientes a otros centros.
Metodología de la confirmación mediante el laboratorioPara la confirmación microbiológica de la infección por influenza A (H1N1) 2009 se recogieron dos muestras por paciente, un frotis nasal y un frotis faríngeo, o bien un aspirado nasofaríngeo. Para determinar el tipo y el subtipo del virus influenza, inicialmente se aplicaron dos técnicas no comerciales, multiplex one-step y en tiempo real, de la reacción en cadena de la polimerasa (PCR-TR). Se usaron cebadores (primers) y sondas (probes) específicas. La primera PCR-TR permitió detectar los virus influenza A y B, y la segunda los subtipos H1, H3 y H5 del virus influenza A. Además, se realizó una tercera PCR-RT con Seeplex®Flu A ACE subtyping (Seegene, Inc Rockville, MD. EE.UU.) para detectar la nueva variante del subtipo H1 del virus influenza A. A partir del 13 de octubre de 2009, se emplearon dos ensayos comerciales multiplex one-step PCR-RT para determinar el tipo y el subtipo del virus A, usando ProFlu plus (ProFlu +, Prodesse, Inc. Gen-Probe. Waukesha, WI. EE.UU.) y ProFlu influenza A subtyping (ProFlu-ST, Prodesse, Inc. Gen-Probe. Waukesha, WI. EE.UU.). El ensayo Proflu+ detecta los virus influenza A y B y el virus respiratorio sincitial y el ProFlu-ST los virus estacionales H1 y H3 y la nueva variante del subtipo H1 del virus influenza A.
Análisis estadístico generalSe ha realizado un análisis descriptivo de las variables recogidas. Para las de tipo cualitativo se determinó el número de casos (N) y la proporción sobre el total expresada en porcentaje (%). Para las variables cuantitativas se determinó si seguían una distribución normal mediante la prueba de Kolmogorov-Smirnov y la inspección de gráficos específicos. Las variables cuya distribución se ajustaba a la normalidad se han descrito mediante la media aritmética y su desviación estándar (DE), y las que no, mediante la mediana y el rango o recorrido. Se ha realizado un análisis bivariado de las variables demográficas, factores de riesgo de complicaciones incluido el embarazo, presencia de neumonía, período desde el inicio de los síntomas hasta la realización de la prueba, tratamiento y período desde el inicio de los síntomas hasta el inicio del tratamiento, según ingreso hospitalario. Se ha estimado el riesgo de hospitalización asociado a las principales variables, para niños y para adultos, mediante modelos específicos de regresión logística en los que se han introducido las variables: sexo, edad de forma categorizada, factores de riesgo de complicaciones, tratamiento antiviral administrado a partir de las 48 horas del inicio de los síntomas y presencia de neumonía. La variable embarazo no ha sido incluida en el modelo de adultos porque su probabilidad de ingreso resultó ser baja en relación a la de los otros factores. El análisis se ha desarrollado mediante el programa Stata v10.
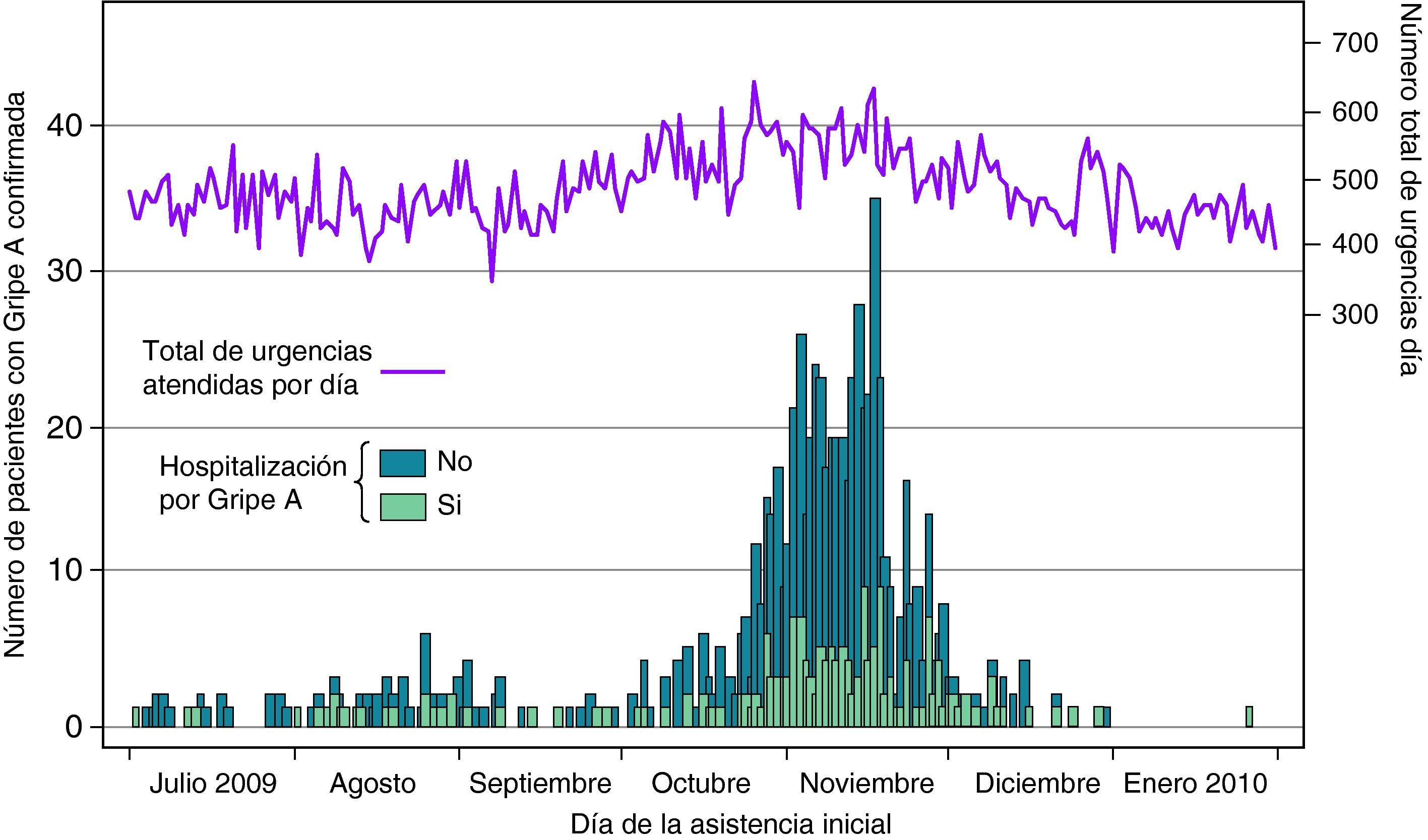
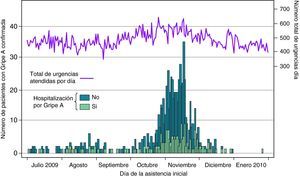
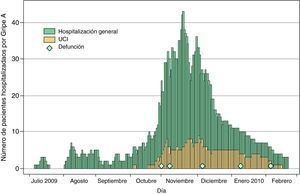
ResultadosEvolución de la pandemia en el HUVHEl primer paciente con gripe confirmada fue atendido el 2 de julio de 2009 y el último el 22 de enero de 2010. En la figura 1 se muestra la curva epidémica del conjunto de casos confirmados en la que destaca la onda pandémica de los meses de octubre-noviembre. En los meses de julio a septiembre la casuística diaria fue reducida. A partir de la primera semana de octubre se produjo un aumento de los casos con una acentuada subida a finales de mes e inicio de noviembre. El porcentaje de ingresos en los citados primeros meses fue del 27,7% y en octubre-noviembre del 23,6% (p=0,38). En el otoño la pandemia tuvo un impacto notable en el número total de visitas por día de los servicios de urgencias, pues la cifra basal de julio-agosto se incrementó hasta un 15% en noviembre (véase la línea evolutiva representada en la parte superior de la figura 1).
Distribución de los casos de gripe A(H1N1) 2009 confirmados por el laboratorio, según la fecha de la asistencia en el hospital. Se muestra también la evolución del número total de urgencias diarias atendidas en el HUVH, del 2 de julio de 2009 al 22 de enero de 2010. Número de casos confirmados: 741; hospitalizados: 190.
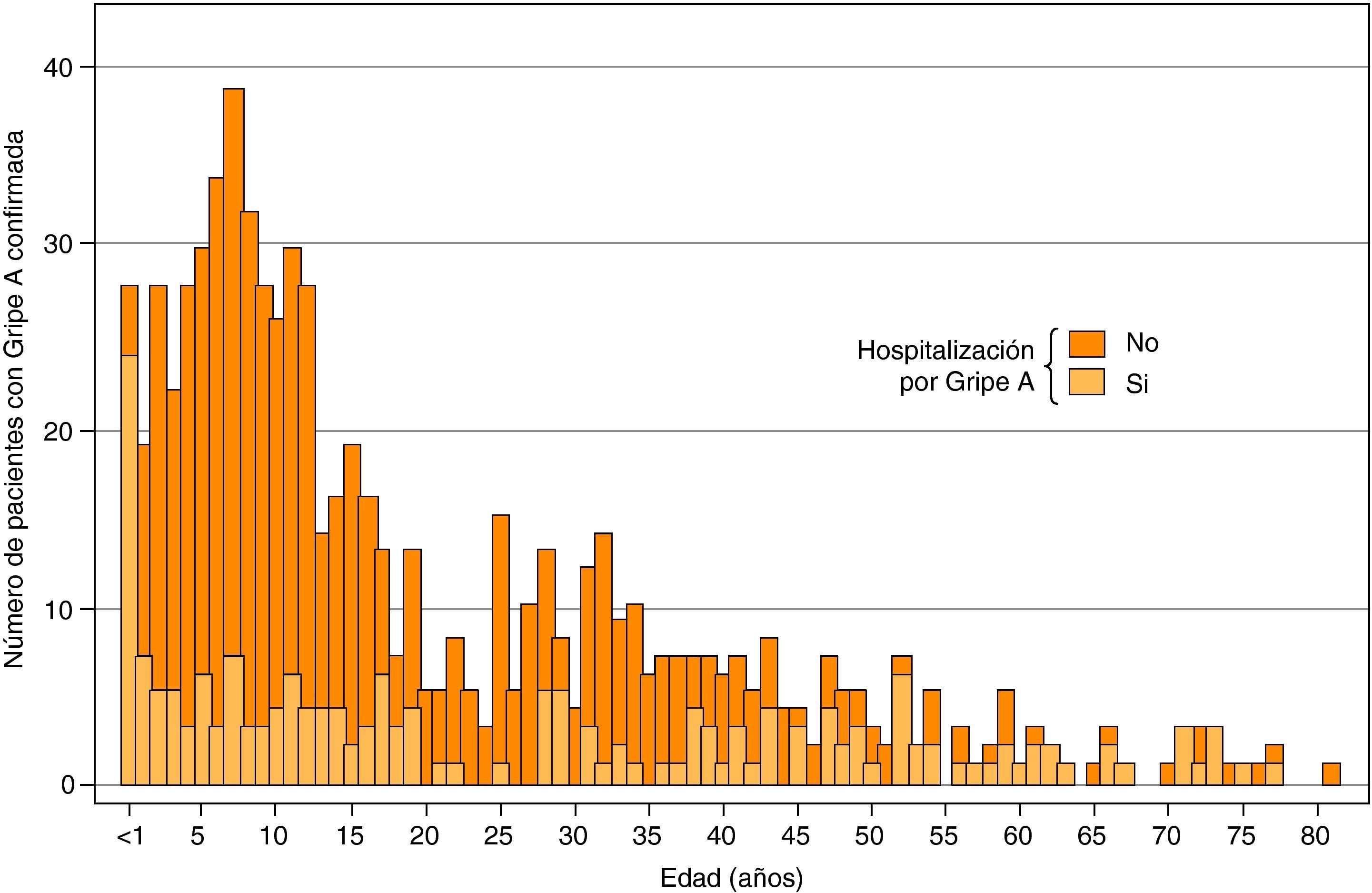
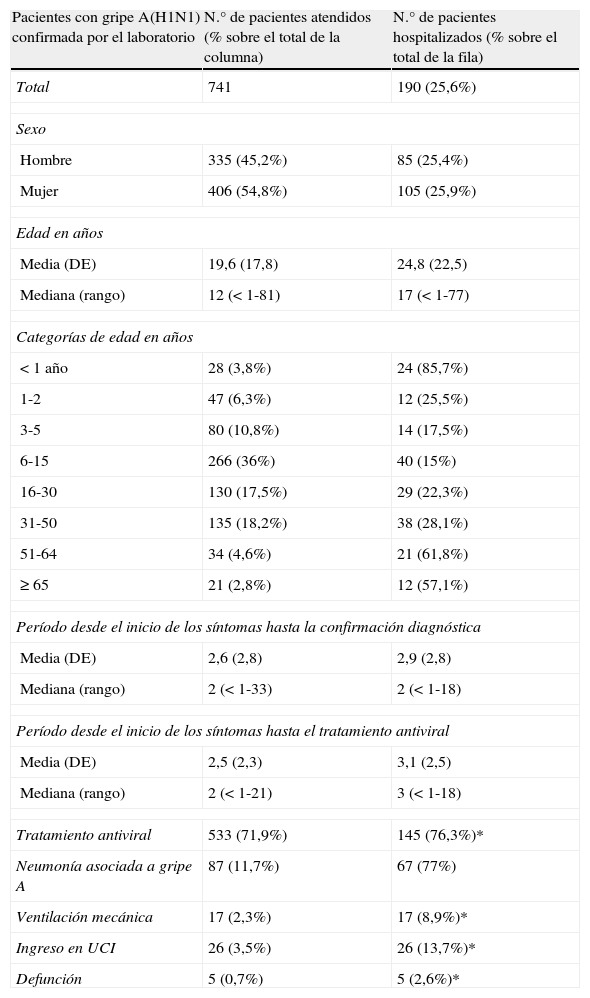
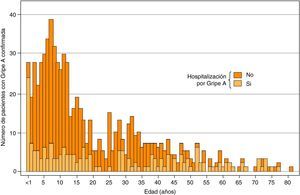
Durante el curso de la pandemia, en el HUVH se realizó la confirmación diagnóstica de 741 casos de gripe A (H1N1) 2009 (tabla 1), que representan el 31% de los casos sospechosos en los que se solicitó la prueba. Hubo 421 pacientes menores de 16 años (niños: 56,8%), y 320 de 16 y más años (adultos: 43,2%). El mayor número de casos se registró entre los 6 y 15 años, y el menor entre los de 65 y más años (fig. 2).
Características demográficas y asistenciales de los casos confirmados de gripe A atendidos en el HUVH durante la pandemia
| Pacientes con gripe A(H1N1) confirmada por el laboratorio | N.° de pacientes atendidos (% sobre el total de la columna) | N.° de pacientes hospitalizados (% sobre el total de la fila) |
| Total | 741 | 190 (25,6%) |
| Sexo | ||
| Hombre | 335 (45,2%) | 85 (25,4%) |
| Mujer | 406 (54,8%) | 105 (25,9%) |
| Edad en años | ||
| Media (DE) | 19,6 (17,8) | 24,8 (22,5) |
| Mediana (rango) | 12 (< 1-81) | 17 (< 1-77) |
| Categorías de edad en años | ||
| < 1 año | 28 (3,8%) | 24 (85,7%) |
| 1-2 | 47 (6,3%) | 12 (25,5%) |
| 3-5 | 80 (10,8%) | 14 (17,5%) |
| 6-15 | 266 (36%) | 40 (15%) |
| 16-30 | 130 (17,5%) | 29 (22,3%) |
| 31-50 | 135 (18,2%) | 38 (28,1%) |
| 51-64 | 34 (4,6%) | 21 (61,8%) |
| ≥ 65 | 21 (2,8%) | 12 (57,1%) |
| Período desde el inicio de los síntomas hasta la confirmación diagnóstica | ||
| Media (DE) | 2,6 (2,8) | 2,9 (2,8) |
| Mediana (rango) | 2 (< 1-33) | 2 (< 1-18) |
| Período desde el inicio de los síntomas hasta el tratamiento antiviral | ||
| Media (DE) | 2,5 (2,3) | 3,1 (2,5) |
| Mediana (rango) | 2 (< 1-21) | 3 (< 1-18) |
| Tratamiento antiviral | 533 (71,9%) | 145 (76,3%)* |
| Neumonía asociada a gripe A | 87 (11,7%) | 67 (77%) |
| Ventilación mecánica | 17 (2,3%) | 17 (8,9%)* |
| Ingreso en UCI | 26 (3,5%) | 26 (13,7%)* |
| Defunción | 5 (0,7%) | 5 (2,6%)* |
DE: desviación estándar; *Porcentaje sobre el total de la columna.
La mediana del tiempo desde el inicio de los síntomas hasta la confirmación diagnóstica y hasta el inicio del tratamiento antiviral fue similar, si bien el rango de días fue más extenso en el intervalo hasta la confirmación diagnóstica (tabla 1).
Solo recibió tratamiento antiviral uno de los 28 pacientes menores de un año (3,5%), en cambio lo recibió cerca del 80% de los pacientes de 1-15 años; el 67% de los de 16-50 años; el 88% de los de 51-64 años y el 90% los de más de 64 años. Oseltamivir fue el fármaco antiviral más empleado (99,8% de casos). En el 12,1% de los casos el tratamiento se inició a partir del primer día; en el 28,5% a partir del segundo, y en el 59,4% tras más días. Fueron ingresados el 24,1% de los pacientes que recibieron antivirales dentro de las primeras 48 horas, y el 30% de los que los recibieron posteriormente (p=0,136).
Presentaron neumonía en el momento de la consulta en urgencias o al ingreso el 11,7% de los pacientes.
Fueron hospitalizados el 25,6% de los casos confirmados (tabla 1); este porcentaje fue superior en los adultos respecto a los niños (31,3% versus 21,4%; p < 0,01). La mediana de la edad de los ingresados fue más elevada que la del conjunto de casos (p<0,02). El mayor porcentaje de ingresos en los niños se produjo en la categoría de edad de menores de 1 año, y en los adultos en las categorías de 51-64 años y de 65 y más años. El grupo de 6 a 15 años fue el de más casos confirmados y registró el menor porcentaje de ingresos.
No se han detectado diferencias entre los pacientes hospitalizados y los derivados a domicilio en relación a la media de días desde el inicio de los síntomas hasta el diagnóstico. En relación al período de tiempo hasta el inicio del tratamiento, la media ha sido superior en los pacientes que requirieron ingreso, aunque sin significación estadística (p=0,07).
Requirieron ingreso en UCI 26 pacientes, 4 niños y 22 adultos. De ellos, 17 fueron sometidos a ventilación mecánica (65%). Fallecieron 5 pacientes. La causa de la muerte de tres de ellos, de 12, 48 y 49 años, fue el agravamiento de una insuficiencia respiratoria aguda que complicó su enfermedad de base (trasplante de progenitores hemopoyéticos; cirrosis hepática; y adenocarcinoma de pulmón, respectivamente). Los otros dos pacientes, de 42 y 72 años, fallecieron por neumonía asociada a gripe e insuficiencia respiratoria aguda, y por ictus embólico y sepsis, respectivamente. En los hospitalizados la letalidad fue del 2,6%, sin existir diferencias por encima o por debajo de los 50 años.
Riesgo de hospitalizaciónEn las tablas 2 y 3 se muestra la distribución de las principales variables y el riesgo asociado de hospitalización para los dos grupos de edad (niños y adultos). En ambos grupos los porcentajes de hospitalización han sido muy similares según sexo.
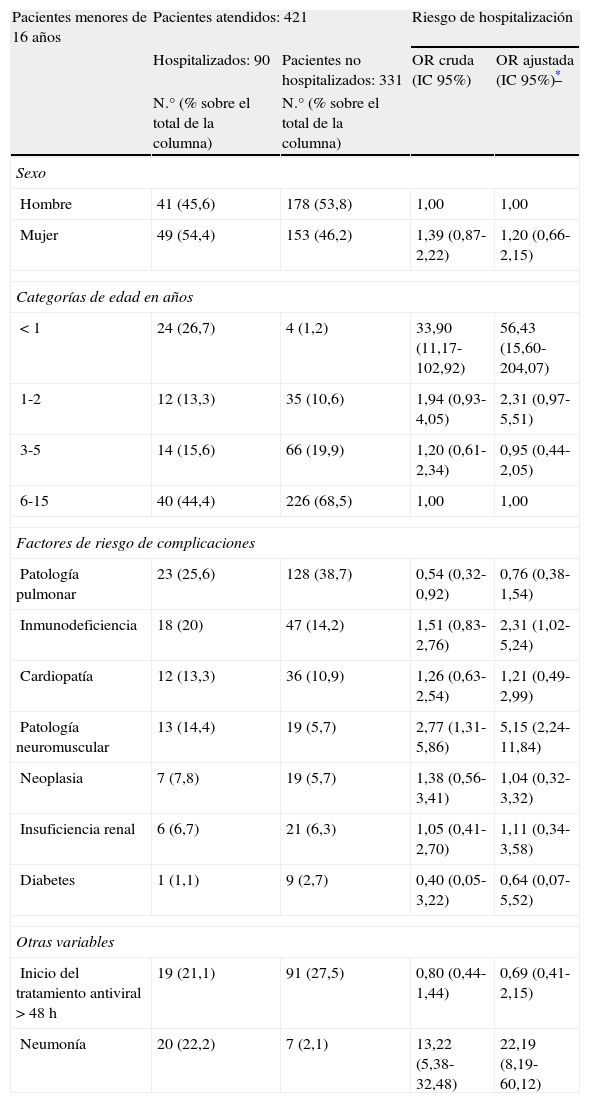
Distribución de las principales variables analizadas en los pacientes menores de 16 años y estimación del riesgo de hospitalización
| Pacientes menores de 16 años | Pacientes atendidos: 421 | Riesgo de hospitalización | ||
| Hospitalizados: 90 | Pacientes no hospitalizados: 331 | OR cruda (IC 95%) | OR ajustada (IC 95%)* | |
| N.° (% sobre el total de la columna) | N.° (% sobre el total de la columna) | |||
| Sexo | ||||
| Hombre | 41 (45,6) | 178 (53,8) | 1,00 | 1,00 |
| Mujer | 49 (54,4) | 153 (46,2) | 1,39 (0,87-2,22) | 1,20 (0,66-2,15) |
| Categorías de edad en años | ||||
| < 1 | 24 (26,7) | 4 (1,2) | 33,90 (11,17-102,92) | 56,43 (15,60-204,07) |
| 1-2 | 12 (13,3) | 35 (10,6) | 1,94 (0,93-4,05) | 2,31 (0,97-5,51) |
| 3-5 | 14 (15,6) | 66 (19,9) | 1,20 (0,61-2,34) | 0,95 (0,44-2,05) |
| 6-15 | 40 (44,4) | 226 (68,5) | 1,00 | 1,00 |
| Factores de riesgo de complicaciones | ||||
| Patología pulmonar | 23 (25,6) | 128 (38,7) | 0,54 (0,32-0,92) | 0,76 (0,38-1,54) |
| Inmunodeficiencia | 18 (20) | 47 (14,2) | 1,51 (0,83-2,76) | 2,31 (1,02-5,24) |
| Cardiopatía | 12 (13,3) | 36 (10,9) | 1,26 (0,63-2,54) | 1,21 (0,49-2,99) |
| Patología neuromuscular | 13 (14,4) | 19 (5,7) | 2,77 (1,31-5,86) | 5,15 (2,24-11,84) |
| Neoplasia | 7 (7,8) | 19 (5,7) | 1,38 (0,56-3,41) | 1,04 (0,32-3,32) |
| Insuficiencia renal | 6 (6,7) | 21 (6,3) | 1,05 (0,41-2,70) | 1,11 (0,34-3,58) |
| Diabetes | 1 (1,1) | 9 (2,7) | 0,40 (0,05-3,22) | 0,64 (0,07-5,52) |
| Otras variables | ||||
| Inicio del tratamiento antiviral > 48 h | 19 (21,1) | 91 (27,5) | 0,80 (0,44-1,44) | 0,69 (0,41-2,15) |
| Neumonía | 20 (22,2) | 7 (2,1) | 13,22 (5,38-32,48) | 22,19 (8,19-60,12) |
IC: intervalo de confianza; OR: odds ratio.
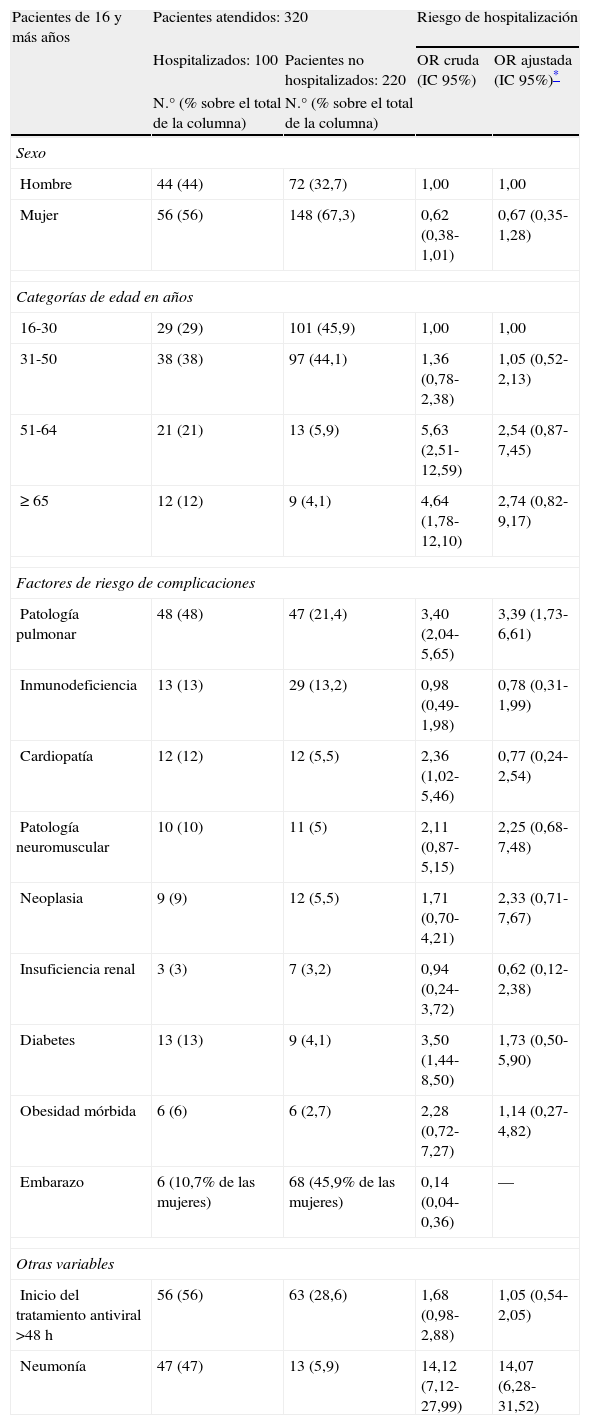
Distribución de las principales variables analizadas en los pacientes de 16 y más años y estimación del riesgo de hospitalización
| Pacientes de 16 y más años | Pacientes atendidos: 320 | Riesgo de hospitalización | ||
| Hospitalizados: 100 | Pacientes no hospitalizados: 220 | OR cruda (IC 95%) | OR ajustada (IC 95%)* | |
| N.° (% sobre el total de la columna) | N.° (% sobre el total de la columna) | |||
| Sexo | ||||
| Hombre | 44 (44) | 72 (32,7) | 1,00 | 1,00 |
| Mujer | 56 (56) | 148 (67,3) | 0,62 (0,38-1,01) | 0,67 (0,35-1,28) |
| Categorías de edad en años | ||||
| 16-30 | 29 (29) | 101 (45,9) | 1,00 | 1,00 |
| 31-50 | 38 (38) | 97 (44,1) | 1,36 (0,78-2,38) | 1,05 (0,52-2,13) |
| 51-64 | 21 (21) | 13 (5,9) | 5,63 (2,51-12,59) | 2,54 (0,87-7,45) |
| ≥ 65 | 12 (12) | 9 (4,1) | 4,64 (1,78-12,10) | 2,74 (0,82-9,17) |
| Factores de riesgo de complicaciones | ||||
| Patología pulmonar | 48 (48) | 47 (21,4) | 3,40 (2,04-5,65) | 3,39 (1,73-6,61) |
| Inmunodeficiencia | 13 (13) | 29 (13,2) | 0,98 (0,49-1,98) | 0,78 (0,31-1,99) |
| Cardiopatía | 12 (12) | 12 (5,5) | 2,36 (1,02-5,46) | 0,77 (0,24-2,54) |
| Patología neuromuscular | 10 (10) | 11 (5) | 2,11 (0,87-5,15) | 2,25 (0,68-7,48) |
| Neoplasia | 9 (9) | 12 (5,5) | 1,71 (0,70-4,21) | 2,33 (0,71-7,67) |
| Insuficiencia renal | 3 (3) | 7 (3,2) | 0,94 (0,24-3,72) | 0,62 (0,12-2,38) |
| Diabetes | 13 (13) | 9 (4,1) | 3,50 (1,44-8,50) | 1,73 (0,50-5,90) |
| Obesidad mórbida | 6 (6) | 6 (2,7) | 2,28 (0,72-7,27) | 1,14 (0,27-4,82) |
| Embarazo | 6 (10,7% de las mujeres) | 68 (45,9% de las mujeres) | 0,14 (0,04-0,36) | — |
| Otras variables | ||||
| Inicio del tratamiento antiviral >48 h | 56 (56) | 63 (28,6) | 1,68 (0,98-2,88) | 1,05 (0,54-2,05) |
| Neumonía | 47 (47) | 13 (5,9) | 14,12 (7,12-27,99) | 14,07 (6,28-31,52) |
IC: intervalo de confianza; OR: odds ratio.
Tras el ajuste logístico, en los niños la edad ha constituido un importante riesgo de hospitalización en los menores de 1 año, mientras que en los adultos no ha sido significativa ninguna categoría.
El factor de riesgo de complicaciones más prevalente en ambos grupos ha sido la patología pulmonar crónica, seguido de la inmunodeficiencia y la patología cardíaca. En conjunto, la prevalencia de factores ha sido más elevada en los niños que en los adultos (67% versus 55%, respectivamente), pero en los hospitalizados las cifras se han invertido (61% en relación al 73%), debido principalmente a que en los adultos ingresaron la mitad de los que presentaban patología pulmonar y solo el 15% en los niños. Los adultos que ingresaron presentaban en relación a los que no ingresaron una prevalencia superior o muy similar de todos los factores de riesgo, en cambio, en los niños la prevalencia fue menor en cuanto a patología pulmonar y diabetes, y superior en el resto de factores. En los niños la inmunodeficiencia y la patología neuromuscular han constituido factores asociados de forma significativa al riesgo de hospitalización, mientras que en los adultos solo la patología pulmonar. La prevalencia de factores de riesgo de complicaciones en los pacientes ingresados en UCI fue del 65,3% y en los fallecidos del 60%.
La instauración del tratamiento antiviral transcurridas 48 horas del inicio de los síntomas no ha mostrado ser un factor significativo de riesgo de hospitalización en los dos modelos logísticos. En cambio, la presencia de neumonía ha constituido un importante factor de riesgo en ambos.
Fueron atendidas 74 embarazadas que representan el 36,3% de las mujeres adultas con gripe confirmada. La mediana de edad fue de 28 años y el rango de 17 a 42 años. Ingresaron 6 (tabla 3), de las que dos requirieron ingreso en UCI. En cuanto a la presencia de factores de riesgo, 7 embarazadas padecían patología pulmonar subyacente y dos patología neuromuscular, pero ninguna de ellas fue hospitalizada.
Carga asistencialLa mediana de estancia fue de 5 días, con un rango de 1 a 184 días. En los pacientes ingresados en UCI, la mediana de estancia fue de 10 días, con un rango de 1 a 184 días.
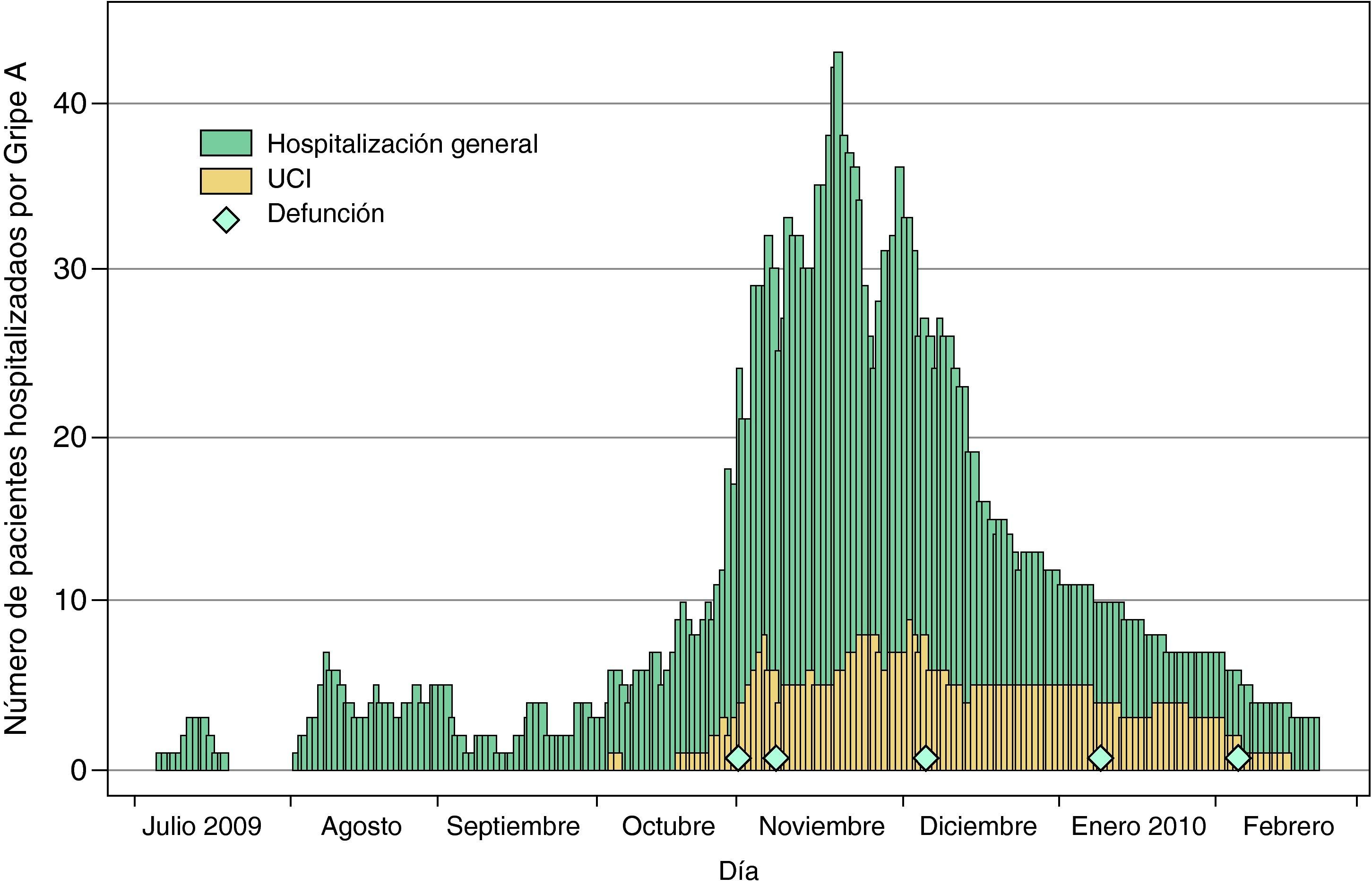
Tal como se muestra en la figura 3 hasta el día 19 de octubre no se alcanzó la cifra de 10 pacientes hospitalizados por gripe A en un mismo día. Este número fue sobrepasado a partir del día 26, alcanzándose un pico máximo el 19 de noviembre con 43 pacientes, 6 de ellos en UCI. A partir de este momento se produjo una notable disminución a la que siguió otro punto elevado, el 1 de diciembre, con 36 pacientes. En esta fecha se inició un declive abrupto que se prolongó de forma lineal en enero y febrero. Durante 46 días hubo de forma permanente 20 o más ingresados, y durante 84 días 10 o más. El 22 de febrero aún permanecían hospitalizados tres pacientes.
En UCI, a partir del 16 de agosto y durante dos meses prácticamente solo hubo un paciente diario hospitalizado; luego, en noviembre y diciembre, tras el incremento iniciado en octubre, el número de ingresados pasó a 2,14 pacientes/día. El pico máximo se registró el 3 de diciembre, con 9 pacientes.
Durante la onda pandémica la tasa de ocupación de camas del HUVH se mantuvo en su nivel habitual, superior al 90%. Se priorizaron los ingresos por gripe en los servicios de enfermedades infecciosas de adultos y de pediatría general en niños, que llegaron a incrementar hasta un tercio su dotación de camas, y en los de UCI, donde aumentó en un 10%.
DiscusiónEn los meses de octubre a diciembre de 2009 el HUVH debió hacer frente a la onda pandémica, que durante 6 semanas repercutió especialmente en los servicios de urgencias y durante 8 en los de hospitalización. Según nuestra interpretación, la primera cifra es una expresión directa de la duración del fenómeno etiológico, mientras que la segunda señala la carga hospitalaria generada, que, a su vez, es el resultado de la interacción entre la tipología de los pacientes asistidos, la gravedad del proceso y los medios curativos aplicados. El porcentaje de ingresos no registró variaciones significativas durante toda la pandemia, si bien, en los primeros meses, los criterios de ingreso establecidos en los protocolos fueron seguramente demasiado estrictos, lo que comportó sin duda un exceso de hospitalizaciones en pacientes sin criterios de gravedad.
Conforme a lo ocurrido en prácticamente todos los países15–29, gran parte de los casos eran personas jóvenes; así, el 64,1% tenía menos de 31 años. La categoría con más casos confirmados fue la de 6-15 años, probablemente debido a que este grupo por su elevada movilidad y contactos se halla más expuesto al virus, y posee una baja inmunidad cruzada por infecciones gripales previas o vacunación. La concentración inicial de la enfermedad en la población infantil y juvenil es un hecho habitual cuando aparece un nuevo virus pandémico, que en los años sucesivos pasa a afectar a grupos de mayor edad30.
La confirmación diagnóstica e ingreso se realizó de forma rápida, con una mediana de dos días desde el inicio de los síntomas, similar a la de las series de casos de California21, Reino Unido26 y EE.UU.29. Se administraron antivirales al 73% de los casos, si bien las cifras fueron más elevadas en los grupos de edad con mayores tasas de hospitalización, en los que se alcanzó el 87% observado en los casos hospitalizados de EE.UU.29. En la extensa serie de casos confirmados del hospital de Santiago de Chile se administró antivirales al 99,7%24, pero este hospital actuó a la vez como centro de recepción primaria de casos y más del 50% de los casos no tuvieron confirmación diagnóstica.
La elevada cifra global de hospitalizaciones del 25,6% de los casos confirmados, en relación por ejemplo al 2% del citado hospital de Santiago de Chile, al 4,5% de la serie de Ontario18, al 9% del informe sobre los primeros casos atendidos en Estados Unidos20, o al 17% de la serie de la Clínica Mayo en EE.UU. referida únicamente a adultos28, podría explicarse por ser un hospital de tercer nivel y de referencia en Cataluña para determinadas patologías, en especial en la población pediátrica.
La mediana de la edad de los hospitalizados fue de 17 años, y más de la mitad tenían menos de 31 años, es decir, al contrario de lo que ocurre en la gripe estacional, en la presente pandemia se ha producido una elevada morbilidad en las personas jóvenes. Es necesario señalar que según el protocolo del hospital se ingresó a casi todos los menores de un año, pero ello ha introducido un limitado sesgo en nuestros datos pues, según la literatura, en esta gripe han sido habituales unas elevadas tasas de ingreso en menores de 5 años y especialmente en menores de 1 año20,21. A partir de los 50 años ingresaron más de la mitad de los pacientes, pues de forma similar a la gripe estacional, la pandémica produce una elevada tasa de complicaciones y hospitalizaciones en las personas mayores31. Como era de esperar, la presencia de neumonía fue el principal motivo clínico de hospitalización.
Fueron admitidos en UCI el 17,3% de los casos hospitalizados, cifra que es superior a la del estudio de pacientes ingresados en el Reino Unido (13%)26, se halla cerca del punto medio de los ingresos señalado en el informe americano antes citado (9 a 31%)20, y es menor que el 25, 27 y 34% de otros estudios24,25,29, y el 44% de la Clínica Mayo28. Todas estas cifras señalan la relevancia clínica del proceso.
La letalidad global fue del 2,6%, que puede considerarse baja en relación a otras series de pacientes hospitalizados: Reino Unido, 4,5%26; EE.UU., 8%29; California y Clínica Mayo, 11%21,28 y varios países, 14-46%25. Es decir, la letalidad observada en el HUVH indica un favorable resultado en relación a la de otros hospitales, aunque las comparaciones entre centros son complejas pues existen grandes diferencias en cuanto a los grupos de edad y socioeconómicos atendidos, los protocolos aplicados, las dotaciones técnicas de la asistencia y otras variables.
En nuestra serie la prevalencia de factores de riesgo de complicaciones era más elevada en los niños que en los adultos, pero en los hospitalizados las cifras se han invertido, circunstancia indicativa de que para el ingreso de los adultos se exigió una mayor presencia de factores que para los niños. La mayoría de estudios han detectado elevadas cifras de factores en los enfermos hospitalizados, del orden de 4625, 6729, 7524 y 78%27, que en el nuestro era del 68%. La elevada prevalencia de factores en los pacientes atendidos en nuestro centro indica, por un lado, que los casos presentaban un elevado nivel de comorbilidad de base que predisponía a las complicaciones y, en otra vertiente, que la remisión de los pacientes al hospital por los centros de Atención Primaria se ciñó, según lo previsto, a los pacientes con mayor probabilidad de complicaciones. En el modelo logístico de riesgo de hospitalización de los niños resultaron significativos dos factores, la inmunodeficiencia y la patología neuromuscular, que son muy comunes en la literatura sobre la pandemia en población pediátrica32,33. En el modelo de los adultos únicamente ha sido significativo el factor más prevalente, la patología respiratoria crónica, que por lo general ocupa un lugar relevante en las series publicadas21,24,25.
En nuestro centro, la presencia de neumonía en la consulta inicial o al ingreso ha sido un factor determinante de la hospitalización, según señalan las cifras crudas y los ajustes logísticos. En cambio, el inicio del tratamiento antiviral pasadas las 48 horas del inicio de los síntomas no ha mostrado ser un factor de riesgo de hospitalización, en razón a que su efecto puede haber sido débil en relación al de los factores de riesgo generales y neumonía, a posibles sesgos de selección o de otro tipo34, y a que la efectividad del tratamiento puede mantenerse durante cierto tiempo22,35. Kaiser et al documentaron en 2003 que el tratamiento antiviral precoz reducía de forma significativa las complicaciones y el riesgo de hospitalización por gripe estacional36, y Falagas et al, en un metanálisis de 11 estudios aleatorizados mostraron que sus efectos beneficiosos eran más pronunciados en los pacientes con elevado riesgo37. En la gripe A (H1N1) 2009, múltiples estudios han señalado que la rápida iniciación de la terapia se ha asociado a mejores resultados clínicos21,22,25,26,34,35,38, sin embargo el impacto específico de los retrasos sobre el riesgo de hospitalización ha sido poco estudiado.
Las embarazadas han constituido un colectivo singular en el presente estudio. Un tercio (36,3%) de las mujeres adultas con gripe confirmada eran embarazadas, cifra importante si tenemos en cuenta que el porcentaje actual de embarazadas en Cataluña según nuestra estimación se aproxima al 5%, cifra cercana al 6% del Reino Unido26. Fueron hospitalizadas el 10,7%, que es una cifra inferior a la de la serie del Reino Unido con el 18%25 o de los EE.UU. con el 32%38. Sin duda, en nuestra área sanitaria una embarazada con gripe fue considerado una situación de riesgo para la salud y motivo de una atenta valoración, aunque en relación a la literatura24,25,38 no hemos observado un mayor porcentaje de hospitalizaciones.
En cuanto a la carga asistencial, el impacto de la onda pandémica sobre los servicios de hospitalización fue reducido, pues la cifra máxima de ingresados en un solo día fue de 43 pacientes, que en relación al total de camas del HUVH representó una pequeña fracción (4%). Aunque el aumento de camas asignado a algunos servicios clínicos para ingresar a los pacientes implicó una ligera modificación de la dotación de otros, de forma general el hospital no tuvo que modificar sus programas asistenciales habituales.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.