Introducción
Fiebre Q es el término clínico aplicado a la infección de carácter zoonótico causada por Coxiella burnetii. Esta enfermedad abarca un amplio espectro de manifestaciones, desde la presentación asintomática (el 60% de las veces) 1, hasta casos graves con compromiso orgánico importante 2. La infección aguda presenta síntomas inespecíficos como fiebre, malestar general, cefaleas y artralgias. En ocasiones, este cuadro puede acompañarse de hepatitis, o bien puede agravarse con una clínica de neumonía atípica. La principal fuente de contagio es la inhalación de aerosoles a partir de animales infectados (especialmente ganado ovino, bovino y caprino) 3. Aunque tradicionalmente ha sido considerada una enfermedad ocupacional de ambientes rurales 2, en la actualidad se han incrementado los informes de casos que viven en entornos urbanos 4.
Entre los métodos serológicos útiles para el diagnóstico de fiebre Q destacan la fijación de complemento (FC) y la inmunofluorescencia indirecta (IFI). La FC ha sido el procedimiento más común en el pasado. Sin embargo, presenta como inconveniente su falta de sensibilidad 2,5. Hoy en día la detección de IgM e IgG mediante IFI constituye el método serológico de referencia 2,5. Como una alternativa a las técnicas anteriores, se han desarrollado distintos métodos de análisis de inmunoabsorción ligada a enzimas (ELISA) 6,7 que permiten realizar un diagnóstico mediante la detección de inmunoglobulinas (IgM 8,9 o de IgG 6,10). El objetivo de este estudio es describir el rendimiento de cuatro técnicas de ELISA (2 para detección de IgM y 2 para detección de IgG frente a C. burnetii) en el diagnóstico de un brote fiebre Q ocurrido en un medio urbano.
Materiales y métodos
En marzo de 2004 se detectó un brote de fiebre Q en la Comunidad de Madrid 11 que afectó mayoritariamente a trabajadores y usuarios de un centro para discapacitados psíquicos ubicado en la capital. La investigación epidemiológica identificó como fuente de infección el contacto con animales durante una visita a una granja-escuela. En total se registraron 25 casos de infección, de los que 22 (16 de ellos sintomáticos) correspondían a personas relacionadas con el centro para discapacitados. Este centro estaba integrado por 55 personas (entre trabajadores y usuarios) y 41 de ellos habían visitado la granja-escuela. El estudio del brote en este colectivo permitió evaluar cuatro técnicas de ELISA: dos para detección de IgM (test C. burnetii IgM ELISA, Panbio, Australia, y ELISA classic C. burnetii phase II IgM, Serion, Alemania) y dos para detección de IgG (test C. burnetii IgG ELISA, Panbio y ELISA classic C. burnetii phase II IgG, Serion).
Se llevó a cabo un estudio serológico en 29 personas del centro ocupacional (24 trabajadores y 5 usuarios). La obtención de las muestras se realizó sin seleccionar a los sujetos en función de la sintomatología o la exposición. En 11 personas que presentaron síntomas (10 de ellos usuarios) no se lograron obtener muestras para serología (las alteraciones conductuales que presentaban estos pacientes por sus enfermedades de base dificultaron en gran medida la toma de muestras). Se definió como expuesto al usuario o trabajador del centro que había visitado la granja-escuela. Se procesaron 53 muestras (muestras pareadas en 24 personas y únicas en cinco). Un total de 23 de estas personas fueron expuestas y cinco de ellas sintomáticas (el tiempo entre la obtención de la primera o única muestra y la exposición osciló entre 38 y 98 días; media [M]: 47,7; desviación estándar [DE]: 16,7). En 18 expuestos se dispuso de muestras pareadas de suero (el tiempo entre la primera y la segunda muestra varió entre 8 y 25 días; M: 23,2; DE: 3,8). En los cinco expuestos sintomáticos el tiempo entre el inicio de la sintomatología y la toma de la primera o única muestra fue de 1 a 63 días (M: 21,4; DE: 24,1).
El diagnóstico de fiebre Q se realizó por IFI, y se consideraron positivos títulos iguales o mayores de 1/50. El criterio de confirmación fue la detección de IgM o la seroconversión de IgG (aumento de cuatro o más veces el título). En esta técnica se utilizaron antígenos de fase I y fase II, obtenidos del Instituto de Virología de Bratislava, Eslovaquia, y producidos a partir de la cepa Nine Mile de C. burnetii. El método serológico se llevó a cabo según se ha descrito previamente 12. Para la determinación de anticuerpos IgM, se efectuó una absorción previa de IgG (RF Absorbente, Dade Behring, Marburg, Alemania), según las indicaciones de los fabricantes.
Todas las técnicas de ELISA se realizaron siguiendo las recomendaciones de los fabricantes. Los resultados obtenidos para IgG por Panbio y Serion se expresaron como unidades de absorbancia y unidades por mililitro. Los criterios de interpretación de resultados fueron positivo o negativo (los resultados dudosos o no concluyentes se consideraron negativos). En el caso de IgM los resultados obtenidos por las dos técnicas se expresaron sólo en términos cualitativos (positivo o negativo, los resultados dudosos o no concluyentes también se consideraron negativos). Estos resultados se evaluaron en términos de sensibilidad y especificidad (muestras) y valores predictivos negativos (VPN) y positivos (VPP) (sujetos expuestos, sintomáticos o no) empleando como referencia la IFI.
La determinación de la significación estadística para la asociación entre los resultados obtenidos por IFI y los ELISA estudiados se llevó a cabo empleando el test exacto de Fisher de 2 colas. En la comparación de resultados y con el fin de eliminar las coincidencias por azar se calcularon los índices kappa (IK) (los valores de IK comprendidos en los intervalos ≤ 0,2; 0,21-0,4; 0,41-0,60; 0,61-0,80 y 0,81-1,00; se consideraron concordancias muy débiles, débiles, moderadas, buenas o muy buenas, respectivamente).
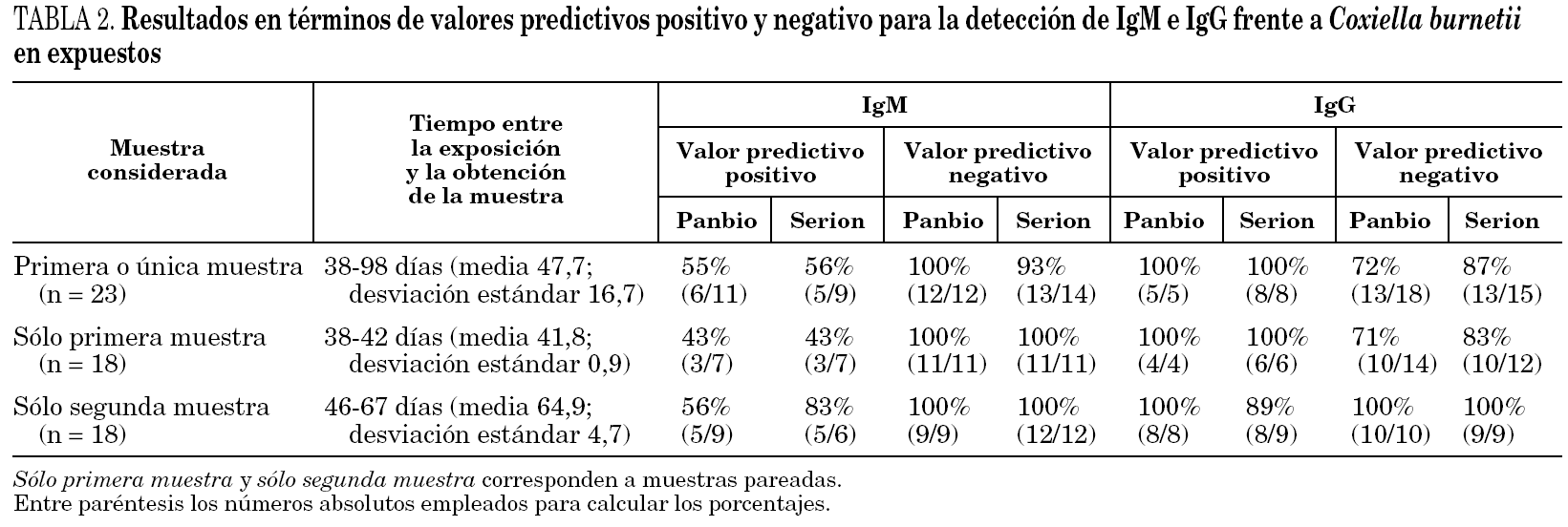
Resultados
Se confirmaron 10 casos por IFI (todos por detección de IgM y tres también por seroconversión de IgG). Todos estos casos eran expuestos y cuatro de ellos sintomáticos. Los resultados obtenidos por Panbio y Serion para IgM e IgG respecto a la IFI en las 53 muestras de suero, expresados como valores de sensibilidad, especificidad y nivel de concordancia se exponen en la tabla 1. La concordancia entre ambas técnicas de ELISA resultó buena tanto para IgM (IK = 0,715) como para IgG (IK = 0,773). La tabla 2 muestra los VPN y VPP de ambas técnicas en la identificación de IgM e IgG, en función del tiempo transcurrido entre la exposición y la toma de muestras en el grupo de 23 sujetos expuestos. En éstos, y considerando los resultados positivos obtenidos en al menos una muestra por persona (independientemente de que se tratara de la primera, segunda o única muestra), la detección de IgM por Panbio clasificó correctamente como infectados (casos de fiebre Q) a los 10 pacientes con IgM positiva por IFI y como no infectados a 9 de los 13 individuos en los que el resultado de IgM por IFI había sido negativo. Serion clasificó como casos a 9 de los 10 pacientes con IgM positiva por IFI y como no casos a 11 de los 13 individuos con IgM negativa por IFI. Teniendo en cuenta la clasificación final de los pacientes como infectados o no infectados (según los resultados de detección de IgM por IFI) los grados de sensibilidad, especificidad y valores predictivos positivo y negativo para la detección de fiebre Q aguda mediante la determinación de IgM por ELISA fueron 100, 69, 71 y 100% en el caso de Panbio y 90, 85, 82 y 92% en el caso de Serion.
La detección de IgM por ambos ELISA confirmó el diagnóstico en los 5 casos expuestos y sintomáticos (incluyendo un enfermo con dos muestras repetidamente negativas por IFI). En estos pacientes, 8 de las 9 muestras estudiadas fueron positivas para IgM, tanto por Panbio como por Serion. Sólo una muestra resultó negativa en los dos ELISA (se trató de una muestra que también había sido negativa por IFI y que se obtuvo al día siguiente del inicio de los síntomas). Un total de 4 casos (dos de ellos sintomáticos) presentaron un resultado negativo para IgM por IFI en la primera muestra y un resultado positivo en la segunda. Dos de ellos (incluyendo uno de los pacientes sintomáticos) mostraron resultados positivos para IgM por los dos ELISA ya en la primera muestra (los dos restantes fueron positivos por los ELISA sólo en la segunda). En 3 sujetos (incluyendo uno sintomático) se obtuvo por ambos ELISA un resultado negativo para IgG en la primera muestra y positivo en la segunda. Dos de estos tres individuos fueron clasificados como casos por IFI (resultados positivos para IgM en alguna muestra o seroconversión de IgG). Sin embargo, el paciente sintomático no fue diagnosticado como caso por IFI (IgM negativa en las dos muestras e IgG positiva pero sin seroconversión). Panbio detectó una seroconversión adicional de IgG en un individuo clasificado como caso por IFI (resultados positivos de IgM y seroconversión de IgG).
En los 6 individuos no expuestos (y con resultados negativos tanto para IgG como para IgM mediante IFI), Panbio detectó un resultado positivo para IgM en las dos muestras de una misma persona y un resultado positivo para IgG en la segunda muestra de un sujeto distinto. Los resultados aportados por Serion en cada una de las dos muestras de estos seis controles fueron negativos.
Discusión
Este brote es uno de los más amplios registrados en España y el mayor del que se tiene constancia en la Comunidad de Madrid. Sin embargo, las conclusiones de este trabajo se ven en gran medida limitadas por el reducido número de muestras e individuos estudiados. Las dos técnicas de ELISA mostraron buena concordancia entre sí. Esta concordancia resultó, para la detección de IgM, superior a la que presentó cada una de ellas en relación con la IFI. El valor relativamente bajo de los IK para IgM pudo ser una consecuencia del reducido número de resultados positivos de la IFI en comparación con los ELISA. Ambas ELISA fueron más sensibles que específicos y aportaron mejores VPN que VPP en la detección de IgM. Otros autores han estimado valores de sensibilidad y especificidad de Panbio para la detección de IgM del 99 y 88%, respectivamente 8. Nuestros resultados confirman la elevada sensibilidad de esta técnica. No obstante, su especificidad se mostró inferior en el presente estudio. Por el momento, no se dispone de información relativa a la utilidad de Serion en la detección de IgM. Según nuestros datos, esta técnica fue más homogénea que Panbio, con valores de sensibilidad y especificidad próximos al 90%. Dada su sensibilidad y VPN, ambas técnicas pueden resultar útiles en brotes como métodos de cribado de IgM. Su empleo inicial podría reducir en gran medida el número de muestras que confirmar por IFI. Por otra parte, la menor especificidad de los dos ELISA para IgM, podría deberse en realidad a una menor sensibilidad de la IFI. No obstante, la posibilidad de aparición de resultados falsos positivos es evidente (uno de los individuos no expuestos presentó dos resultados positivos para IgM mediante el ELISA de Panbio). En cuanto a la IgG, tanto Panbio como Serion se revelaron muy específicos. Además, sus VPP resultaron buenos. En el caso de Panbio, nuestros resultados coinciden con los publicados previamente 10. Serion fue algo más sensible que Panbio. Sin embargo, la sensibilidad de los dos métodos se situó por debajo del 90%. Por este motivo, e inversamente a lo que ocurre con la detección de IgM, el uso de estas técnicas para el filtrado inicial de muestras podría ser cuestionable. La explicación de la variación de los valores predictivos en función del tiempo resulta complicada. En los sujetos expuestos el valor predictivo positivo para IgM de ambas técnicas de ELISA parece aumentar al considerar los resultados de las muestras obtenidas más tardíamente (la segunda muestra de individuos con muestras pareadas). Quizás esto se deba a una demora en la detección de IgM por IFI (fallos en muestras más tempranas). El valor predictivo negativo se mantuvo bueno a lo largo del tiempo. A la inversa, en el caso de IgG el valor predictivo negativo de los dos métodos de ELISA parece elevarse con el tiempo. En este caso el valor predictivo negativo se mantuvo bueno y estable (en Serion disminuyó a cifras próximas al 90%). Estos hechos podrían justificarse por una menor capacidad de detección de IgG por los ELISA en las etapas más iniciales de la infección.
Agradecimientos
Al doctor Fernando de Ory, del Centro Nacional de Microbiología por su colaboración en el diagnóstico diferencial del brote y a las doctoras Alicia Téllez y Raquel Escudero por sus comentarios en el trabajo. Este estudio se ha realizado, en parte, mediante la financiación de la Red Temática de Investigación Cooperativa del FIS EBATRAG (G03/057). La descripción epidemiológica del brote será publicada en breve en la revista Medicina Clínica.
Correspondencia: Dr. J.C. Sanz.
Laboratorio Regional de Salud Pública.
General Oraa, 15. 28006 Madrid. España.
Correo electrónico: juan.sanz@salud.madrid.org
Manuscrito recibido el 27-4-2005; aceptado el 10-6-2005.