La proctitis ulcerosa (PU) constituye un cuarto de los casos de colitis ulcerosa (CU), con características clínicas, evolutivas y terapéuticas diferenciales. Nuestro objetivo fue describir la utilización de recursos terapéuticos y sanitarios en pacientes con PU en remisión clínica.
Material y métodosEstudio observacional retrospectivo en el que se incluyó a pacientes con PU en seguimiento en nuestro centro dentro del período 1989-2014. Se registraron las características y evolución clínicas, los tratamientos utilizados y las diferentes galénicas para el mantenimiento de la remisión de la enfermedad.
ResultadosSe incluyó a 101 pacientes con PU, con una mediana de seguimiento de 8 años (IIC: 3-14). El tratamiento de mantenimiento más utilizado fue la mesalazina tópica (89%), mayoritariamente en forma de supositorios. Un 55% de los pacientes siguieron en algún momento mesalazina oral. El 33% siguieron tratamiento combinado con mesalazina oral y tópica, el 12% utilizaron corticoides tópicos para el mantenimiento y solo el 3% requirieron tiopurinas. El 10% de los pacientes consultaron alguna vez al Servicio de Urgencias y solo el 4% requirió ingreso hospitalario por actividad de la PU durante el seguimiento. Ninguno de ellos precisó colectomía.
ConclusionesLa mesalazina tópica constituye la terapia de mantenimiento más empleada en la PU en nuestra práctica clínica, lo que indica una buena aceptación por parte de los pacientes y un elevado grado de confianza por los médicos prescriptores. La PU se asocia a una baja utilización de recursos sanitarios, pero serían necesarios estudios de su impacto en la calidad de vida.
In population-based studies, ulcerative proctitis (UP) accounts for more than 25% of ulcerative colitis (UC) patients and presents distinctive clinical outcomes and therapeutic approaches as compared to left-sided and extensive UC. Our aim was to describe the different therapeutic approaches and health resources used in patients with UP in clinical remission.
Material and methodsWe performed a retrospective observational study including patients with UP that were followed in our Hospital Universitari Germans Trias i Pujol between 1989-2014. Clinical information and the different treatments for the maintenance of remission were recorded, including galenical formulation.
ResultsA total of 101 patients with UP were included. Median time of follow up was 8 years (IQR 3-14). Most patients were treated with topical mesalazine (especially suppositories) (89%); followed by oral mesalazine (55%). The 33% of patients underwent combined therapy with oral and topical mesalazine. Another 12% were treated with topical steroids for maintenance therapy and 3% of patients required thiopurines. The 10% of patients attended to Emergency Service and 4% were hospitalized for disease activity within follow-up. None of them required colectomy.
ConclusionsTopical mesalazine is the most used maintenance treatment in UP patients in our clinical practice, suggesting both a good acceptance by patients and a high degree of confidence for doctors. UP is associated with a low requirement of health resources, although studies focused on the quality of life are needed.
La colitis ulcerosa (CU) es una enfermedad crónica caracterizada por la inflamación de la mucosa cólica. Según la clasificación de Montreal1, se define como proctitis ulcerosa (PU) aquella forma de presentación cuya afectación endoscópica se limita al recto. En los estudios de cohortes poblacionales más recientes, la PU constituye aproximadamente un tercio de los casos de CU2,3 y presenta implicaciones pronósticas claramente diferenciales respecto a la colitis izquierda o extensa, fundamentalmente con relación a un menor riesgo de brotes graves, necesidad de tratamiento con corticoides sistémicos, hospitalización, colectomía o desarrollo de displasia o cáncer colorrectal (CCR)4–6.
Con relación al tratamiento de mantenimiento, los aminosalicilatos (5-ASA) constituyen el fármaco más comúnmente utilizado (como en el resto de formas de CU), si bien en el caso de la PU, raramente se requerirá de inmunosupresores o agentes biológicos, dada la baja probabilidad de requerir tratamiento con corticoides sistémicos. En este sentido, y dadas las características farmacocinéticas y farmacodinámicas de los 5-ASA, el tratamiento tópico presenta una clara ventaja sobre el tratamiento oral al obtener concentraciones en mucosa rectal mucho más elevadas7,8. Por el contrario, existe la posibilidad de progresión proximal de la CU9, lo que, unido a la hipotética menor comodidad del tratamiento tópico, podría justificar una mayor utilización del tratamiento oral de mantenimiento en estos pacientes.
Con estas premisas, el objetivo de nuestro estudio es describir la utilización de las diferentes galénicas disponibles para el tratamiento de mantenimiento de la PU en la práctica clínica y describir la evolución clínica a largo plazo.
Pacientes y métodosSe trata de un estudio retrospectivo y observacional, realizado en el Servicio de Aparato Digestivo del Hospital Universitari Germans Trias i Pujol (Badalona). Se incluyó a pacientes mayores de 18 años identificados a partir del registro del Estudio Nacional en Enfermedad Inflamatoria intestinal sobre Determinantes genéticos y Ambientales (ENEIDA) local, diagnosticados de CU por criterios clínicos, endoscópicos e histológicos, con una extensión máxima limitada al recto (sin constatarse en ningún momento de su evolución progresión proximal de la enfermedad), en seguimiento en nuestro centro a partir de mayo de 1989.
Se registraron las características demográficas, clínicas y evolutivas, así como los fármacos y galénicas utilizados durante el seguimiento para el mantenimiento de la remisión de la enfermedad y los efectos adversos asociados. Se especificó el uso de recursos sanitarios incluyendo el número de colonoscopias y las hospitalizaciones durante el seguimiento. Se definió tratamiento de mantenimiento como aquel que se utilizó al menos 3 meses consecutivos durante los periodos de remisión clínica. Se definió la actividad clínica de la enfermedad según el índice de Mayo parcial (puntuación de >1, con sangrado rectal). Se excluyó a aquellos pacientes que presentaron progresión proximal de la enfermedad (a colitis izquierda o extensa) en algún momento de la evolución. El periodo de seguimiento finalizó en la última visita realizada en nuestro centro, ya fuera por pérdida de seguimiento o por finalización de la recogida de datos (diciembre de 2014).
El registro ENEIDA fue aprobado por el Comité de Ética de nuestro centro con fecha 22 de diciembre de 2006 (referencia: EO-06-031). Se obtuvo el consentimiento informado de todos los pacientes incluidos.
Análisis estadísticoSe realizó un análisis descriptivo de las variables estudiadas con el paquete estadístico SPSS versión 20.0 (SPSS, Inc, Chicago, IL, EE. UU.). Los resultados se expresan como números absolutos, frecuencias o medianas (intervalo intercuartil, IIC).
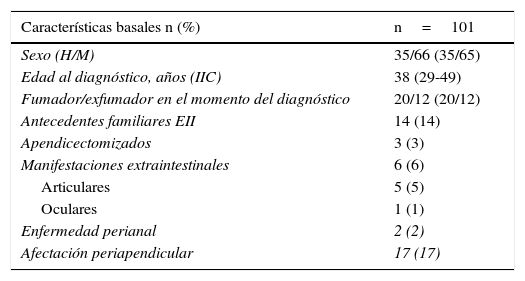
ResultadosDe un total de 687 pacientes con CU incluidos en el registro ENEIDA local, 101 (15%) presentaron una extensión máxima confirmada limitada al recto, sin evidencia de progresión proximal en ningún momento del seguimiento, y con una tasa relativamente inferior respecto a los estudios poblacionales descritos. Hubo predominio de mujeres (65%) y hasta en un 17% de los casos presentaron afectación periapendicular en el momento del diagnóstico. Las características basales de los pacientes se describen en la tabla 1. La mediana de seguimiento desde el diagnóstico fue de 8 años (IIC: 3-14).
Características basales de los pacientes
| Características basales n (%) | n=101 |
|---|---|
| Sexo (H/M) | 35/66 (35/65) |
| Edad al diagnóstico, años (IIC) | 38 (29-49) |
| Fumador/exfumador en el momento del diagnóstico | 20/12 (20/12) |
| Antecedentes familiares EII | 14 (14) |
| Apendicectomizados | 3 (3) |
| Manifestaciones extraintestinales | 6 (6) |
| Articulares | 5 (5) |
| Oculares | 1 (1) |
| Enfermedad perianal | 2 (2) |
| Afectación periapendicular | 17 (17) |
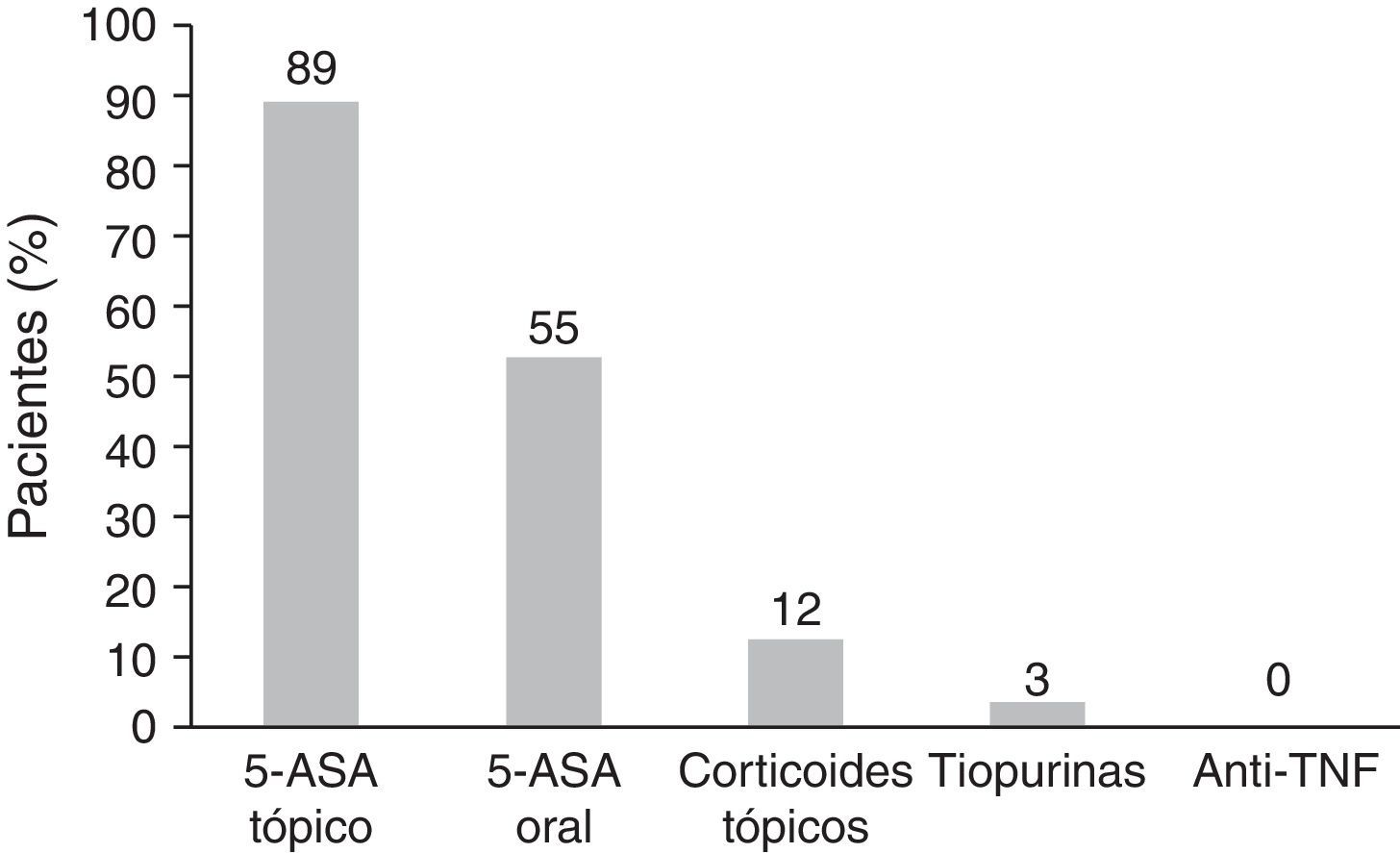
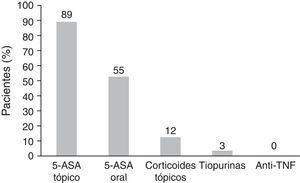
Un 89% de los pacientes fue tratado en algún momento del seguimiento con 5-ASA tópico, en monoterapia, mayoritariamente (92%) en forma de supositorio, con una mediana de tiempo de tratamiento de 40 meses (IIC: 14-115). La posología más frecuentemente prescrita fue 500mg/48 h (51%), el 40% restante recibió dosis superiores a 500mg/24 h, 1g/24h, 1g/48h (21, 9 y 10%, respectivamente) y un 9% realizó tratamiento con 500mg/72h. Solo un 6% de los pacientes cambiaron la galénica del 5-ASA tópico inicialmente prescrita.
El 52% de los pacientes realizó tratamiento con 5-ASA oral en algún momento del seguimiento (19% en monoterapia, 33% en tratamiento combinado). La dosis continuada que se utilizó durante un mayor intervalo de tiempo fue >2g/día (mediana de tiempo en tratamiento con 5-ASA oral >2g: 36 meses [IIC: 0-73] vs. <2g: 4 meses [IIC: 0-32]). En el caso del 5-ASA oral, en el 16% de los pacientes se cambió la galénica con el objetivo de optimizar la adherencia al tratamiento.
Por otra parte, un 12% de los pacientes utilizaron corticoides tópicos para el mantenimiento y 3 pacientes requirieron terapia con tiopurinas por intolerancia a 5-ASA o por corticodependencia. Ninguno precisó tratamiento con anti-TNF (fig. 1).
El tratamiento con 5-ASA tópico se retiró únicamente a 2 pacientes. En uno de ellos, por intolerancia gastrointestinal y en el otro fue suspendido de forma provisional tras una reacción cutánea inicialmente atribuida a alergia al 5-ASA, descartada después mediante pruebas cutáneas y test de exposición, por lo que se pudo reintroducir sin complicaciones (caso ya publicado)10. Un paciente que requirió tiopurinas presentó trombocitopenia grave que obligó a suspender el tratamiento.
El tiempo máximo en remisión continuada fue de 48 meses (IIC: 22-118 meses); un 49% de los pacientes presentó, al menos, una recidiva durante el seguimiento. Las recidivas fueron más frecuentes en aquellos pacientes bajo tratamiento con 5-ASA combinado oral y tópico (50%), seguido de los que utilizaban tratamiento oral (40%) y tratamiento tópico (35%). No se apreció significación estadística en el riesgo de recidiva ni en el tratamiento prescrito.
La utilización de recursos sanitarios fue escasa, pues únicamente un 10% de los pacientes consultaron alguna vez al Servicio de Urgencias y tan solo un 4% requirió ingreso hospitalario por actividad de la PU durante el seguimiento. Ninguno de ellos precisó colectomía. En el 46% de los pacientes se realizó al menos una colonoscopia durante el seguimiento. En las endoscopias de control de 5 pacientes se objetivó la existencia de adenomas esporádicos (de localización proximal al recto); tan solo uno presentó displasia y ninguno fue diagnosticado de CCR.
Finalmente cabe destacar que hasta un 36% de los pacientes refirieron estreñimiento significativo en el seguimiento. El 75% de estos requirió tratamiento médico con laxantes: plantago ovata fue el más utilizado.
DiscusiónLa PU, aunque se incluye habitualmente dentro del conjunto de pacientes con CU, presenta peculiaridades en cuanto a sus manifestaciones clínicas, requerimientos terapéuticos y pronóstico, claramente diferenciales respecto al resto de las formas fenotípicas de CU. Globalmente su prevalencia se estima en alrededor de un tercio de los casos de CU. En nuestra cohorte, sin embargo, tan solo el 15% de los pacientes con CU presentaron tanto al diagnóstico como durante su evolución una afectación solo rectal. Probablemente, esto se deba, entre otras causas, a que estos pacientes son derivados con menor frecuencia a centros de referencia de EII dada su evolución más benigna y a la exclusión de nuestro estudio de aquellos pacientes que presentaron progresión proximal en algún momento del seguimiento.
El 5-ASA constituye la terapia de elección para el mantenimiento de la remisión en CU tanto en aquellos en los que se ha inducido la remisión con 5-ASA como con corticoides de acción tópica o sistémica11. Es un fármaco con buen perfil de seguridad y generalmente bien tolerado. En los pacientes con PU, dada la localización y extensión de la enfermedad, el uso de 5-ASA tópico permite optimizar la eficacia del fármaco, garantizando, así, la liberación directamente sobre la mucosa afecta. Son varios los estudios que demuestran la efectividad del 5-ASA tópico frente a placebo recogida en varias revisiones sistemáticas12–16. Por ello, según la guía clínica de GETECCU sobre tratamiento de la CU elaborada con la metodología GRADE17, se recomienda como terapia de elección en aquellos pacientes con PU que hayan presentado previamente un brote tratado con 5-ASA (oral o tópico) o bien con corticoides de acción tópica. En nuestra población, a excepción de 3 pacientes que requirieron uso de tiopurinas, la mayoría fueron controlados con 5-ASA. El tratamiento de elección fue el 5-ASA tópico, utilizado en algún momento del seguimiento hasta en un 89% de los pacientes. Ello demuestra una buena aceptación por parte del médico prescriptor y por el paciente.
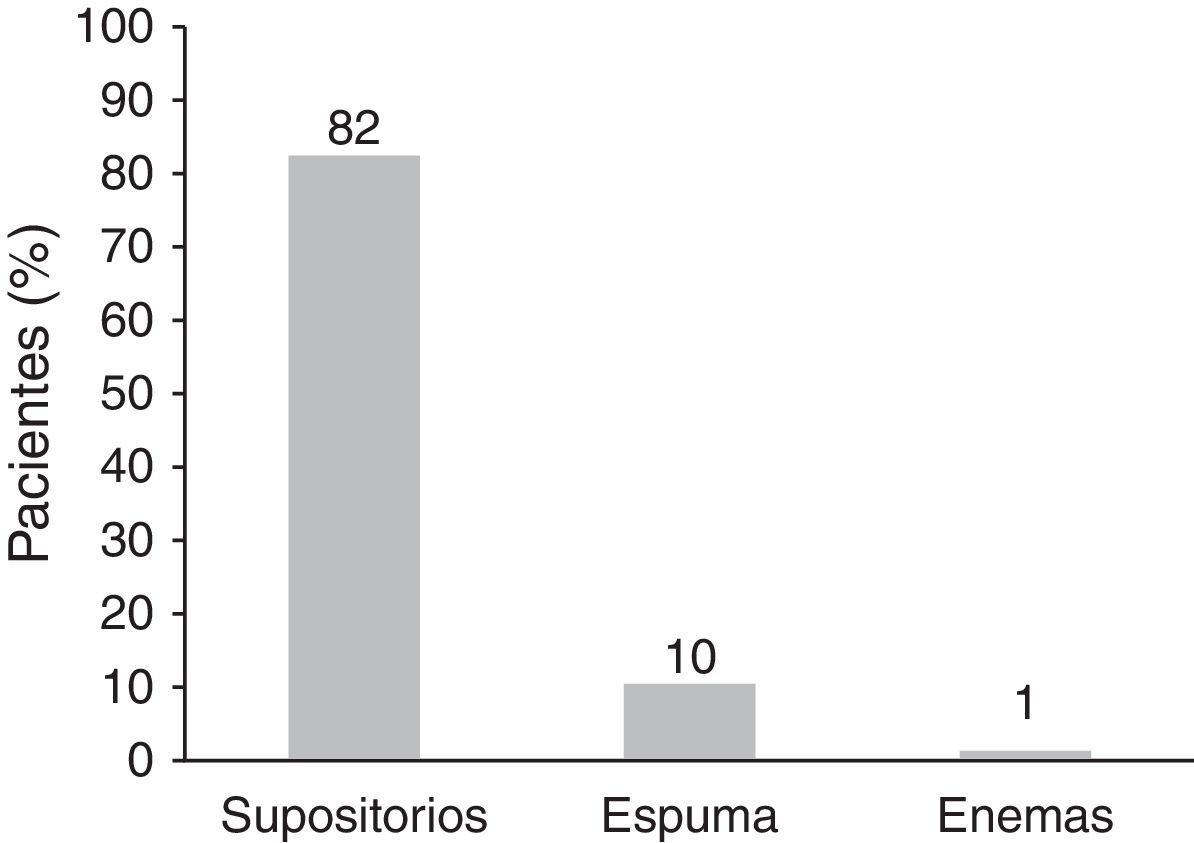
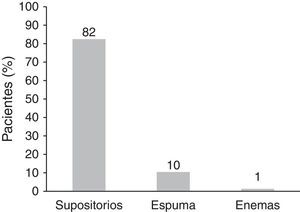
En cuanto a la galénica, las distintas formulaciones de 5-ASA tópico de las que disponemos (supositorios, espuma y enema) se adaptan a las diferentes localizaciones de CU: se liberan exclusivamente en el recto los supositorios, hasta el sigma la espuma y hasta el ángulo esplénico los enemas18. Por ello, y junto con una mayor aceptación por parte del paciente debido a su mejor tolerancia y comodidad, la galénica más utilizada en la PU son los supositorios; como en nuestro estudio, que alcanza cifras del 92% frente a las otras formulaciones (fig. 2).
Respecto a la posología, en nuestra población la pauta de dosificación más prescrita de 5-ASA en forma de supositorios fue 500mg/48h hasta en un 51% de los casos. No hay un consenso claro sobre la dosis óptima, aunque sí se recomienda una dosis mínima de 1g 2 o 3 veces por semana17. Asimismo, se aconseja prolongar el tratamiento de mantenimiento durante 6 meses, en el caso de un primer brote y, si se presentan resistencia o recidivas frecuentes, mantenerlo de manera indefinida. Según las últimas recomendaciones de GETECCU sobre el uso e indicaciones del tratamiento tópico en pacientes con CU19 parece razonable realizar en formas de CU distales un tratamiento diario en aquellos pacientes que presenten recidivas frecuentes y reservar el tratamiento «intermitente» en aquellos en remisión prolongada, que previamente no hayan presentado brotes graves y hayan mostrado una respuesta rápida y eficaz al tratamiento. En nuestra población, la mayoría recibió tratamiento de mantenimiento con 5-ASA tópico durante algún periodo del seguimiento, incluyendo los pacientes que lo realizaron de manera indefinida o intermitente, y a los que se les retiró por remisión clínica prolongada o cambio a otros tratamientos, con una tasa de recidiva en este grupo del 35%.
En cuanto a la controversia sobre el uso de 5-ASA oral o tópico, los estudios disponibles demuestran una mayor eficacia para las formulaciones tópicas14,20. A pesar de la evidencia descrita, algunos autores señalan que en la práctica clínica el 5-ASA tópico se infrautiliza21, probablemente por reticencia del paciente a la vía de administración y por su preferencia por la vía oral. De hecho, en nuestra población casi un 20% de los pacientes llegaron a utilizar 5-ASA oral en monoterapia y un 33% de forma combinada en algún momento del seguimiento, sin presentar intolerancia al tópico. Sin embargo, cabe destacar que un 17% de los pacientes presentaban afectación periapendicular en el diagnóstico y esto podría haber incrementado el uso del 5-ASA oral por parte del médico prescriptor22. A pesar de presentar una menor concentración en el recto que las formulaciones tópicas, las diferentes galénicas de administración oral, mediante distintas formas de liberación específicas, pueden aumentar la concentración del 5-ASA en el colon distal. Así pues, podría estar indicado como terapia combinada en aquellos pacientes no respondedores a la terapia tópica o como alternativa en pacientes con mala tolerancia al tratamiento vía rectal23.
Por otra parte, un 12% de los pacientes siguió tratamiento con corticoides tópicos durante periodos prolongados en algún momento del seguimiento. A pesar de no existir evidencia suficiente para recomendar su uso como terapia de mantenimiento, se sabe que son efectivos para inducir la remisión, con superioridad frente al placebo24. Además, presentan una baja incidencia de efectos secundarios atribuida a su baja biodisponibilidad sistémica, particularmente la budesonida tópica, por lo que en casos seleccionados se podría plantear su asociación en aquellos pacientes con falta de eficacia o respuesta parcial al 5-ASA tópico19.
Disponemos de poca evidencia sobre la eficacia de los inmunosupresores y agentes anti-TNF en el tratamiento de las proctitis. Su uso supone un riesgo por los efectos secundarios y un coste añadido, por lo que es fundamental una valoración adecuada de la falta de respuesta al 5-ASA, insistiendo en la adherencia de los pacientes, especialmente de las formas de presentación tópicas.
Los pacientes con PU presentan un curso más benigno que las formas más extensas6, lo que debería suponer una menor utilización de recursos sanitarios. Este aspecto queda claramente demostrado en nuestro estudio, en el que se ha constatado una baja tasa de atención en urgencias, hospitalización y colectomía. Por otra parte, no se detectó ningún caso de CCR en los pacientes que se realizaron colonoscopia durante el seguimiento (46%). La extensión de la enfermedad es un factor de riesgo para el desarrollo de CCR, por lo que los pacientes con PU presentan un riesgo similar al de la población general25. Por tanto, esto no significa que estos pacientes no deban seguir cribado alguno para CCR, sino que deben seguir el cribado de CCR de la población general una vez se ha constatado que no ha existido progresión proximal en los primeros 8 años desde el diagnóstico26. De hecho, en nuestra cohorte se detectaron adenomas esporádicos, que demostraron que la aparición de neoplasias cólicas es posible también en esta población, aunque suela depender de la vía adenoma-carcinoma y no de la de la inflamación27.
Aunque los pacientes con PU gocen de un mejor pronóstico y requieran de una menor utilización de recursos sanitarios en comparación con las formas izquierdas o extensas de CU, existen pocos datos acerca del impacto sobre su calidad de vida. En nuestro estudio evaluamos una situación clínica que nos pareció frecuente en el seguimiento de estos pacientes como es el desarrollo de estreñimiento, registrado hasta en un 30% de los casos de nuestra cohorte. Se ha postulado que la aparición de estreñimiento en los pacientes con PU probablemente sea debida a la fibrosis del recto, que se produce como consecuencia de la inflamación crónica por la enfermedad28. Esto favorecería una disminución de la complianza rectal y una deficiente evacuación de las heces. En nuestro centro, el laxante más comúnmente utilizado en estos pacientes fue plantago ovata. Esto obedece a diversas razones. En primer lugar, se ha descrito que los pacientes con CU presentan una disminución de la síntesis de ácidos grasos de cadena corta por parte de la microbiota intestinal, por lo que un suplemento de fibra soluble podría facilitar el aumento de su síntesis29. Por otro lado, un estudio controlado y aleatorizado realizado en el seno de GETECCU demostró que el plantago ovata es igual de efectivo que el tratamiento con 5-ASA para la prevención de la recidiva clínica en pacientes con CU en remisión clínica30.
En conclusión, los pacientes con PU requieren una utilización limitada de recursos sanitarios, si bien sería recomendable evaluar de forma específica cuál es el impacto de su enfermedad en su calidad de vida. Los supositorios de 5-ASA constituyen el tratamiento más comúnmente utilizado en el mantenimiento de la PU, lo que indica que tanto prescriptores como pacientes se sienten cómodos con su eficacia y administración.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflictos de interésT. L., M. M, E. C. y E. D. han recibido ayudas para la asistencia a cursos o congresos o pagos por conferencias de FAES Farma, Shire, Tillots o Ferring. M. C. y N. C. recibieron ayudas para la asistencia a cursos de FAES Farma.