Introducción y objetivo: Valorar la erradicación o disminución en el tamaño de las várices gástricas con el uso de N-butil-2-cianocrilato, como medida de profilaxis primaria.
Material y métodos: En el Centro Médico Nacional 20 de Noviembre se llevó a cabo un estudio de cohorte, en pacientes con hipertensión portal de diversa etiología, con várices gástricas grandes (> 10 mm), sin hemorragia previa; a quienes se les aplicó N-butil-2-cianocrilato con seguimiento a un año. Se evaluaron dos grupos: los que lograron la erradicación y los que persistieron con várices > 5 mm. Se evaluó también el número total de sesiones necesarias para lograr el objetivo.
Resultados: El tipo predominante de várices gástricas fueron las GOV1 (42.9%). La erradicación de las várices gástricas se logró en el 77.8% y 33.3% a los seis y 12 meses, respectivamente (p=0.000). Por otro lado, el estado basal de las várices esofágicas al ingreso del estudio se mantuvo en el 82.1% vs 71.4% a los seis y 12 meses, respectivamente (p=0.001). El número de sesiones de N-butil-2-cianocrilato se relacionó significativamente con la erradicación y el tamaño de las várices gástricas de forma inversamente proporcional, mostró que a mayor número de sesiones requeridas, menor tasa de erradicación alcanzada (p=0.039). Durante el seguimiento a un año, no hubo ningún evento de hemorragia.
Conclusiones: El uso de N-butil-2-cianocrilato como profilaxis primaria de várices gástricas es una medida útil para disminuir el tamaño variceal, y con ello el riesgo del primer evento de hemorragia, al aumentar el intervalo de tiempo libre de várices gástricas.
Introduction and aim: To evaluate the eradication or reduction in the size of gastric varices using N-butyl-2-cyanoacrylate, as a measure of primary prophylaxis.
Material and methods: In the "C.M.N. 20 de Noviembre" was conducted a cohort study in patients with portal hypertension of diverse etiology, with large gastric varices (> 10 mm) without prior bleeding, to whom we applied N-butyl-2-cyanoacrylate with one-year follow-up. We studied two groups: those who achieved eradication and those who persisted with gastric varices > 5 mm. We also evaluated the total number of sessions needed.
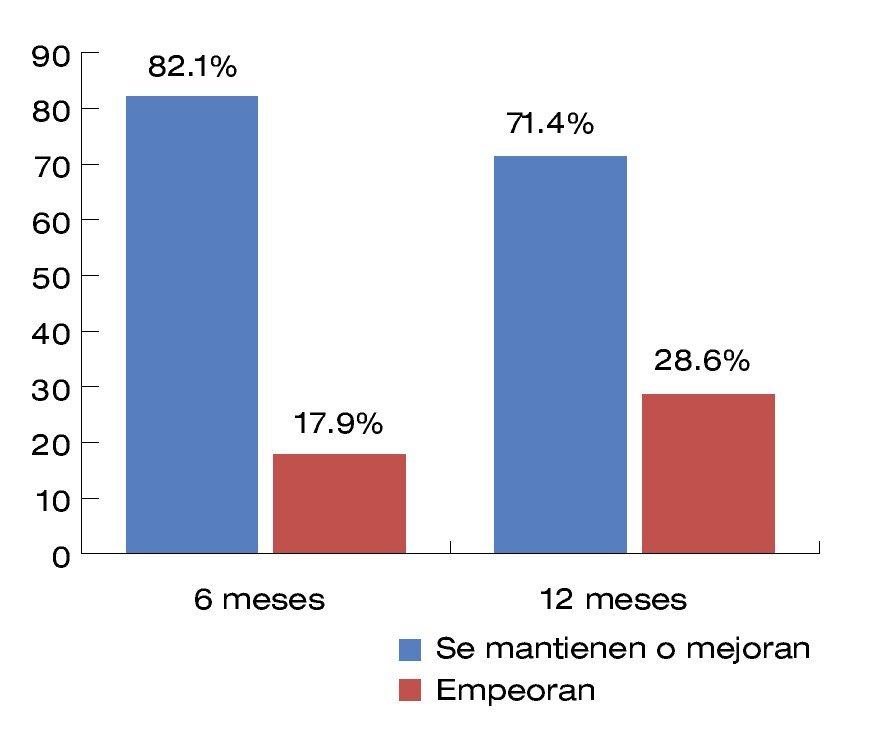
Results: The predominant type of gastric varices was GOV1 (42.9%). The eradication of gastric varices was achieved in 77.8% and 33.3% at 6 and 12 months respectively (p=0.000). On the other hand, the baseline of esophageal varices at study entry remained at 82.1% vs 71.4% at six and 12 months respectively (p=0.001). The number of sessions of N-butyl-2-cyanoacrylate was inversely associated with eradication and gastric varices size, showed that the greater number of sessions required, lower eradication rate achieved (p=0.039). During one-year follow up, there was any bleeding event.
Conclusions: The use of N-butyl-2-cyanoacrylate as primary prophylaxis of gastric varices is useful to decrease variceal size and the risk of first bleeding event.
Introducción
Las várices gástricas se encuentran en el 20% de los pacientes con hipertensión portal.1 La hemorragia por várices gástricas es mucho más severa, requiere de un mayor número de transfusiones, además de tener una mayor mortalidad cuando se compara con la hemorragia secundaria a várices esofágicas.1-3 La mortalidad del primer evento de hemorragia variceal es tan alta, como del 20% en las primeras seis semanas de la hemorragia inicial.2,3 Las várices gástricas pueden estar asociadas a várices esofágicas (várices esofagogástricas tipo 1 (GOV1), a lo largo de la curvatura menor; o a lo largo del fondo, tipo 2 (GOV2), o bien, presentarse aisladas en el fondo (IGV1) o en sitios ectópicos en el estómago o en la primera porción duodenal (IGV2).1 La incidencia de hemorragia variceal secundaria a várices IGV1 y GOV2 es más frecuente y profusa (78% y 54%, respectivamente), cuando se compara con la secundaria a várices GOV1 (28%).1 En presencia de factores que indican riesgo alto de hemorragia, la probabilidad de sangrado variceal es tan alta como del 65%.4,5
Hay pocos datos respecto a la profilaxis de la hemorragia variceal gástrica.6 El tratamiento profiláctico debe basarse en la incidencia de hemorragia y su mortalidad, tomando en cuenta el tamaño y localización de las várices gástricas, el grado de disfunción hepática y otros factores. Generalmente los pacientes con várices gástricas quienes también tienen várices esofágicas, están en tratamiento con betabloqueadores no selectivos para reducir la incidencia del primer evento de hemorragia variceal esofágica. Si este tratamiento también puede prevenir el sangrado de las várices gástricas no es del todo conocido.7,8
Dado la alta tasa de hemorragia y la menor tasa de resangrado, la obturación variceal gástrica con inyección de N-butil-2-cianocrilato es usado como tratamiento de primera línea para várices gástricas sangrantes y en la profilaxis secundaria de las mismas.9-15
Su papel en la profilaxis primaria de hemorragia variceal gástrica no se ha evaluado extensamente. Se publicó en el año 2011 un estudio que valoró el uso de N-butil-2-cianocrilato como profilaxis primaria para hemorragia variceal gástrica, comparándolo con el uso de betabloqueadores, con resultados muy favorables para su uso en este ámbito.16
El uso de inyección de N-butil-2-cianocrilato para la profilaxis primaria de várices gástricas aún no se recomienda, aunque se empieza a utilizar para esos fines. Dado los antecedentes mencionados, en el Hospital se inició el tratamiento con N-butil-2-cianocrilato como medida profiláctica primaria en todos aquellos pacientes con hipertensión portal y várices gástricas grandes, con la finalidad de disminuir el tamaño variceal y con ello evitar o retrasar el primer evento de hemorragia variceal, y así la mortalidad asociada.
El objetivo del presente estudio fue valorar la tasa de erradicación o disminución en el tamaño de las várices gástricas con el uso de N-butil-2-cianocrilato, como medida de profilaxis primaria.
Material y métodos
En el Centro Médico Nacional (C.M.N.) 20 de Noviembre del ISSSTE, se llevó a cabo un estudio de cohorte en pacientes con diagnóstico de hipertensión portal de etiología diversa, con várices gástricas grandes (> 10 mm), que se sometieron a la aplicación de N-butil-2-cianocrilato por vía endoscópica, con seguimiento a un año.
Los criterios de inclusión fueron todos aquellos pacientes cirróticos admitidos en el C.M.N. 20 de Noviembre de mayo de 2010 a mayo de 2012, portadores de várices gástricas GOV1, GOV2 e IGV1, con tamaño > 10 mm, sin hemorragia previa. En caso de presentar várices esofágicas y gástricas, se dio tratamiento a ambas. El estudio se aprobó por el comité de ética y se obtuvo el consentimiento informado de todos los pacientes.
Los criterios de exclusión fueron el antecedente de hemorragia variceal previa, várices gástricas previamente tratadas, hipertensión portal no secundaria a cirrosis, hemorragia en el momento de la endoscopia, alergia al esclerosante o al lipiodol, encefalopatía hepática grado III-IV, síndrome hepatorrenal, niveles séricos de bilirrubina > 10mg/dL, falla cardiorrespiratoria, edad > 75 años, embarazo y pacientes sin firma previa de consentimiento informado.
Una vez ingresados al estudio, los pacientes fueron evaluados y estuvieron en seguimiento por un periodo mínimo de un año, con revisiones mensuales durante los primeros seis meses y posteriormente, dependiendo de la evolución y respuesta al tratamiento cada dos a tres meses.
El tamaño de las várices gástricas se midió con respecto al diámetro de la punta del endoscopio utilizado, el cual es de 9.8 mm. Se evaluó también la presencia o no de várices esofágicas y de gastropatía portal. Para la realización del estudio endoscópico se utilizó lidocaína en spray en dosis de 100 mg, y en algunos casos sedación con midazolam y propofol.
El sangrado variceal se definió como presencia de hematemesis y/o melena con requerimiento de transfusión de dos concentrados eritrocitarios o descenso de tres mg/dL de la hemoglobina basal sin transfusión previa. La evidencia de hemorragia variceal gástrica incluyó presencia de hemorragia en chorro o en capa durante la endoscopia, o coágulos adheridos a las várices.
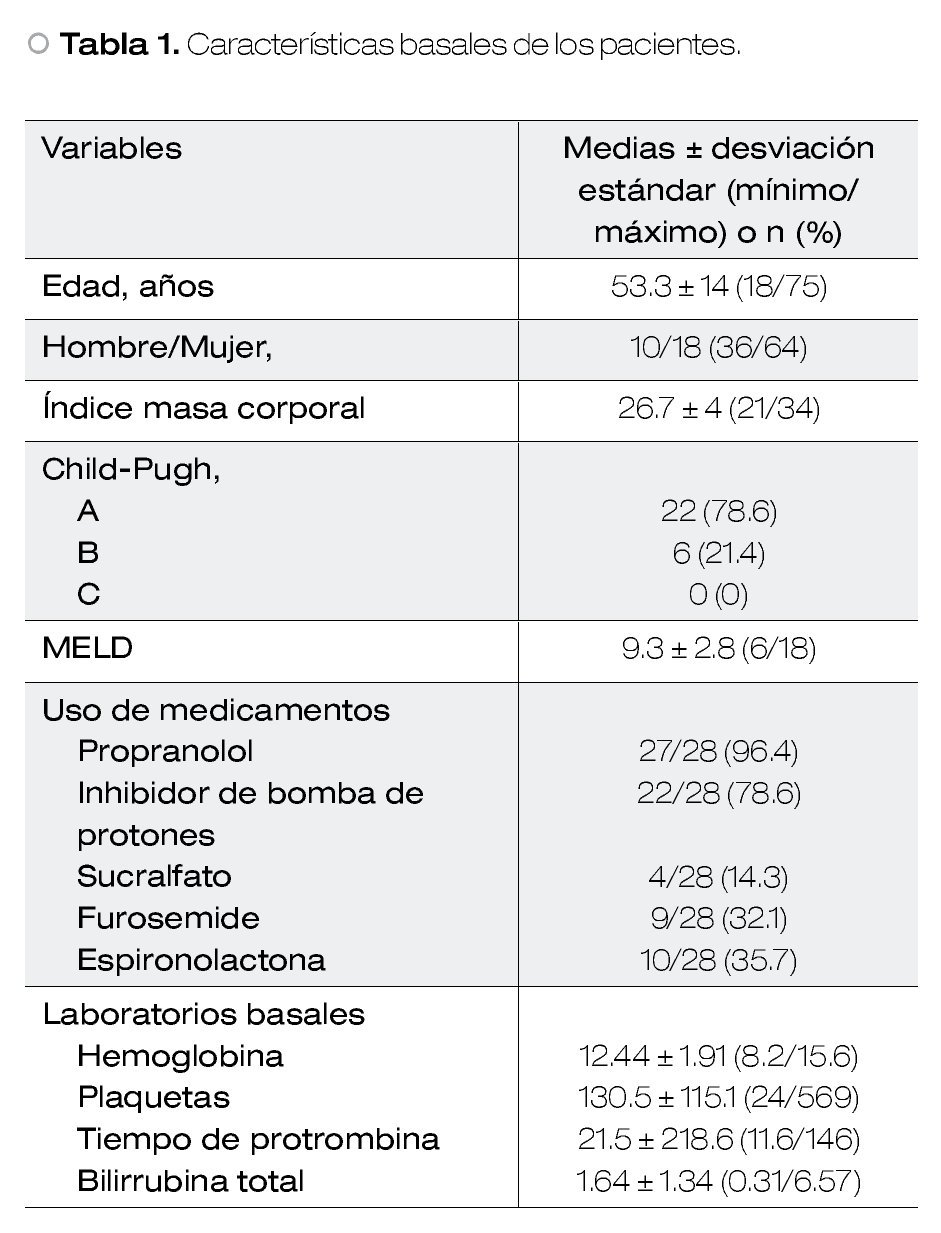
Todos los pacientes tratados en el Servicio llegaron ya referidos con el diagnóstico de cirrosis. Se les calculó el puntaje de Child-Pugh-Turcotte al momento del ingreso y el MELD.
Para valorar las várices gástricas se tomó en cuenta el tamaño, > 10 mm y su localización. En el seguimiento se distribuyeron en dos grupos, los pacientes con várices gástricas erradicadas por completo y aquellos con várices > 5 mm. Para valorar las várices esofágicas se utilizó la clasificación de Dagradi y se dividieron en dos grupos: ausencia y presencia de las mismas. Asimismo, se utilizaron dos grupos para valorar el número de aplicaciones necesarias para la erradicación; el primer grupo de una a dos sesiones y el segundo más de dos intervenciones. Todos los pacientes se evaluaron a los seis y 12 meses.
Técnica de inyección de cianocrilato
La inyección de N-butil-2-cianocrilato se aplicó intravaricealmente, se utilizó un endoscopio GIF H150 y un catéter inyector, con una aguja de 4 mm de longitud y calibre 23 G. Antes de introducir el endoscopio, se impregnaba con aceite vegetal para evitar que el cianocrilato lo dañara. Ya en la cavidad gástrica y con las várices localizadas, se pasó por el canal de trabajo 5 mL de aceite vegetal, para protección del mismo. Posteriormente se procedió a inyectar lipiodol bajo control fluoroscópico, una vez corroborado el sitio correcto de inyección se pasó el N-butil-2-cianocrilato, hasta dos dosis como máximo (2 mL). Todo el estudio se siguió mediante fluoroscopía.
Análisis estadístico
Las variables numéricas continuas son expresadas como promedios y desviaciones estándar. Las variables categóricas se manejaron como frecuencias. Para las comparaciones entre el estado de las várices gástricas basal vs seis y 12 meses, se realizó ji cuadrada de McNemar. Se hizo una comparación entre dos grupos, mayor de dos sesiones y menor de dos sesiones, para comparar la evolución de las várices gástricas y las várices esofágicas a los seis y 12 meses utilizando ji cuadrada de McNemar. Finalmente, se realizó un modelo de regresión logística para identificar variables predictoras de éxito para erradicación de várices gástricas.
Resultados
Entre mayo del 2010 y mayo del 2012 en el Servicio de Endoscopia, fueron atendidos 288 pacientes con diagnóstico de cirrosis con hipertensión portal por diversas causas; fueron excluidos 253 y solamente 35 se incluyeron en el estudio, de éstos, cinco eran foráneos y no concluyeron su seguimiento; uno rehusó participar y otro abandonó el estudio.
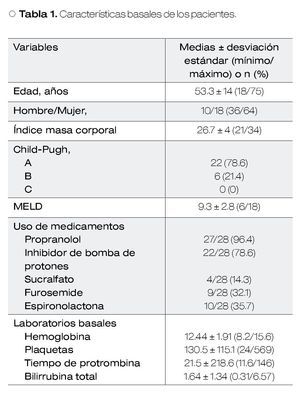
En el análisis se incluyeron 28 pacientes cuyas características basales se muestran en la Tabla 1. En el 75% de los pacientes la etiología más común de cirrosis fue no infecciosa, y de éstas, la criptogénica encabezó la lista. El 25% restante la causa de cirrosis fue infección por virus de hepatitis C. Además, el 60.7% del total de la muestra tenían várices esofágicas erradicadas.
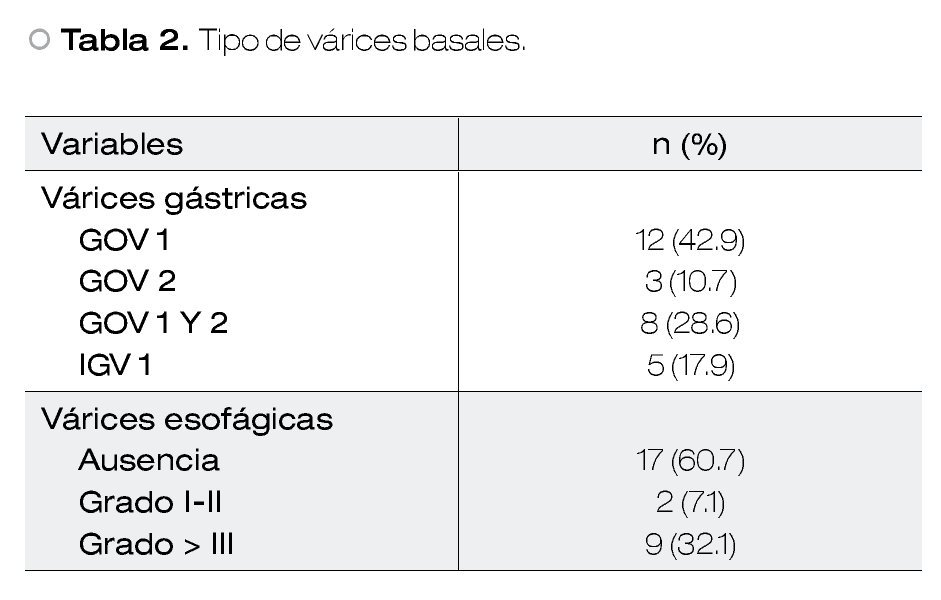
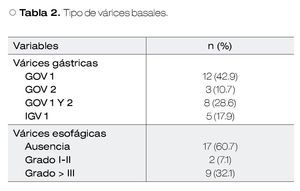
El tipo predominante de várices gástricas fueron GOV1 en 42.9% (Tabla 2).
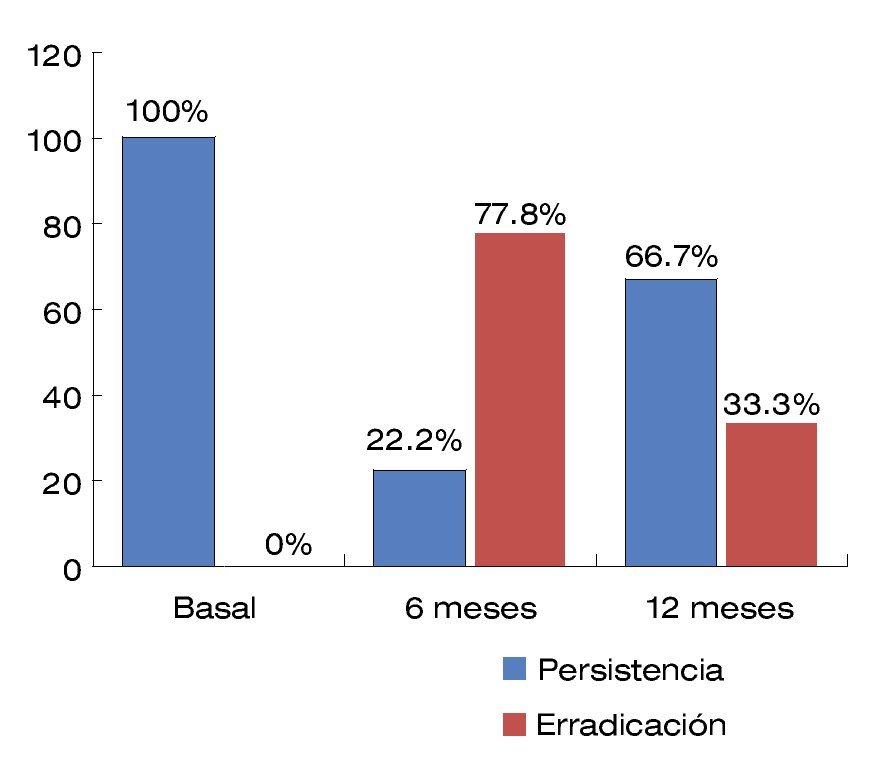
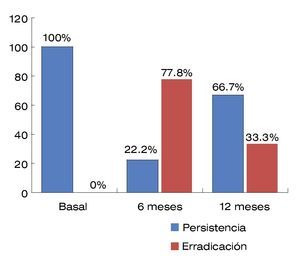
Cuando se comparó el tamaño de las várices gástricas basal y posterior a la aplicación de la sustancia esclerosante a los seis y 12 meses, se encontró el siguiente comportamiento mostrado en la Figura 1.
| Figura 1. Comportamiento de várices gástricas posterior a la aplicación de N-butil-2-cianocrilato.
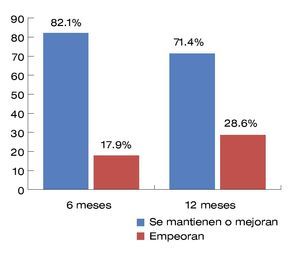
Con respecto a las várices esofágicas, se observó el comportamiento de las mismas a los seis y 12 meses posterior a las sesiones de N-butil-2-cianocrilato (Figura 2).
| Figura 2.Comportamiento de várices esofágicas con respecto a su estado basal.
Del total de pacientes que se incluyeron en el estudio, el 60.7% requirió un máximo de dos sesiones para lograr el objetivo.
El número de aplicaciones de N-butil-2-cianocrilato no tuvo relación estadísticamente significativa
con el comportamiento de las várices esofágicas a los seis y 12 meses, sin embargo, si la tuvo respecto a la erradicación y tamaño de las várices gástricas, con relación inversamente proporcional, mostrando que entre mayor fue el número de sesiones requeridas, el porcentaje de erradicación fue menor (77.8% con una a dos sesiones vs 22.2% con más de dos sesiones) con una p=0.039.
Finalmente, utilizando el modelo de regresión logística no se encontraron variables estadísticamente significativas que pudieran predecir el éxito de la aplicación de N-butil-2-cianocrilato en el tamaño variceal, únicamente se observaron tendencias como la edad y la hemoglobina basal que pudieran influir en el resultado, pero deberá contarse con una muestra más grande y hacer el seguimiento por mayor tiempo.
Es importante mencionar que ninguno de los pacientes incluidos en el estudio presentó hemorragia variceal durante el seguimiento. Hubo un solo paciente que falleció por causas ajenas a la patología de base.
En todos los pacientes intervenidos se vigiló la presencia de eventos adversos, ya descritos para la aplicación del medicamento. Dichos eventos se buscaron en cada visita, y se instruyó al paciente para que en caso de presentar algún síntoma relacionado lo reportara con el investigador. Los eventos adversos que se reportaron, todos sin consecuencias clínicas, fueron: dolor en nueve pacientes (32%), hemorragia durante la aplicación en seis pacientes (21%) y migración del material a los campos pulmonares sin traducción clínica en un paciente (3%).
Discusión
La hemorragia variceal gástrica se caracteriza por ser mucho más severa, con importante pérdida sanguínea, elevada mortalidad, además de mayor dificultad para su manejo, cuando se compara con la hemorragia de várices esofágicas. Es por ello, que es importante identificar qué pacientes están en alto riesgo de hemorragia; en algunas ocasiones observamos las manchas rubíes y moradas, como las que se aprecian en las várices esofágicas, con inminencia de hemorragia.
Como se ha mostrado ya en estudios previos, el N-butil-2-cianocrilato es muy efectivo para la profilaxis secundaria de hemorragia variceal gástrica. Asimismo, recientes estudios muestran que la esclerosis de várices gástricas es una medida terapéutica útil como profilaxis primaria, ya que disminuye la incidencia de hemorragia variceal y por lo tanto la mortalidad por estos eventos. En base a ello, quisimos ver cuál era el comportamiento del tamaño variceal con las sesiones de cianocrilato aplicadas y su relación con el primer episodio de hemorragia. Dado los hallazgos, parece ser un método prometedor como profilaxis primaria de várices gástricas. Sin embargo, para poder afirmar esto con certeza, se requieren ensayos clínicos controlados que demuestren los hallazgos.
Se observó que la presencia de dolor durante el estudio se relaciona con la extravasación de la sustancia y la cantidad acumulada, esto se evita con el control fluoroscópico, además de poder apreciar cuando el esclerosante emigra a lugares distantes del sitio de aplicación.
Consideramos que es un procedimiento que se relaciona directamente con la experiencia del endoscopista.
En conclusión, el uso de N-butil-2-cianocrilato como profilaxis primaria de várices gástricas, es una medida útil para disminuir el tamaño variceal y el riesgo de un primer evento de hemorragia.
Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Financiamiento
Los autores no recibieron ningún patrocinio para llevar a cabo este estudio.
Correspondencia:
Dra. Mónica Valdivia Balbuena.
C.M.N. 20 de Noviembre del ISSSTE, Servicio de Endoscopia. Félix Cuevas 540, Colonia del Valle, Delegación Benito Juárez, C.P.
03229. México D.F., México.
Teléfono: 5200 3442.
Correo electrónico: monivalbal@hotmail.com