Existe una importante proporción de pacientes en tratamiento con anticoagulantes o antiagregantes plaquetarios que requieren procedimientos endoscópicos electivos o de urgencia. Es deseable que los endoscopistas tengan conocimiento de la farmacología básica de los antitrombóticos, sus indicaciones, las condiciones que definen el riesgo de trombosis al suspender el tratamiento y el riesgo de sangrado de los procedimientos endoscópicos. La importancia de este conocimiento radica en la optimización de los desenlaces de tromboembolismo y hemorragia, por lo que el objetivo de esta revisión es mostrar la evidencia sobre las recomendaciones para llevar a cabo un procedimiento endoscópico seguro en pacientes que se encuentran bajo tratamiento antitrombótico.
A significant proportion of patients treated with anticoagulants or platelet aggregation inhibitors may require elective or urgent endoscopic procedures. It is desirable that endoscopists have knowledge of the basic pharmacology of antithrombotic agents and their indications, as well as the risk of thrombosis after discontinuation of therapy and the risk of bleeding due to endoscopic procedures. The importance of this information lies in optimising the outcomes of thromboembolism and bleeding. The aim of this review is to present the evidence on the recommendations to conduct a safe endoscopic procedure in patients on antithrombotic treatment.
La enfermedad cardiovascular es la principal causa de muerte en todo el mundo1, por lo que una importante proporción de la población se encuentra bajo tratamiento antitrombótico con anticoagulantes o antiagregantes plaquetarios. Los pacientes en tratamiento antitrombótico que requieren de un procedimiento endoscópico necesitan de un manejo especial e individualizado, valorando el balance entre la urgencia del procedimiento, el riesgo endoscópico de sangrado y el riesgo tromboembólico por la interrupción de los medicamentos.
Este artículo presenta la evidencia sobre las recomendaciones para llevar a cabo un procedimiento endoscópico seguro en pacientes bajo tratamiento con anticoagulantes o inhibidores de la agregación plaquetaria.
Epidemiología del uso de antitrombóticosEl 70% de los pacientes con enfermedad cardiovascular son usuarios de aspirina, el 18% utilizan doble antiagregante plaquetario y el 6% la combinación de aspirina con un anticoagulante oral. La mitad de los pacientes que no toman aspirina se encuentra en tratamiento con algún anticoagulante oral u otro antiplaquetario2.
En EE. UU. se ha calculado que para el año 2030 el 40.5% de la población presentará al menos una forma de enfermedad cardiovascular por lo que se espera el incremento del uso de antitrombóticos, así como el aumento de desenlaces hemorrágicos3.
FarmacodinamiaLos fármacos antitrombóticos incluyen los anticoagulantes y antiplaquetarios. Para realizar un manejo adecuado de los pacientes bajo estos tratamientos es necesario conocer su farmacodinamia.
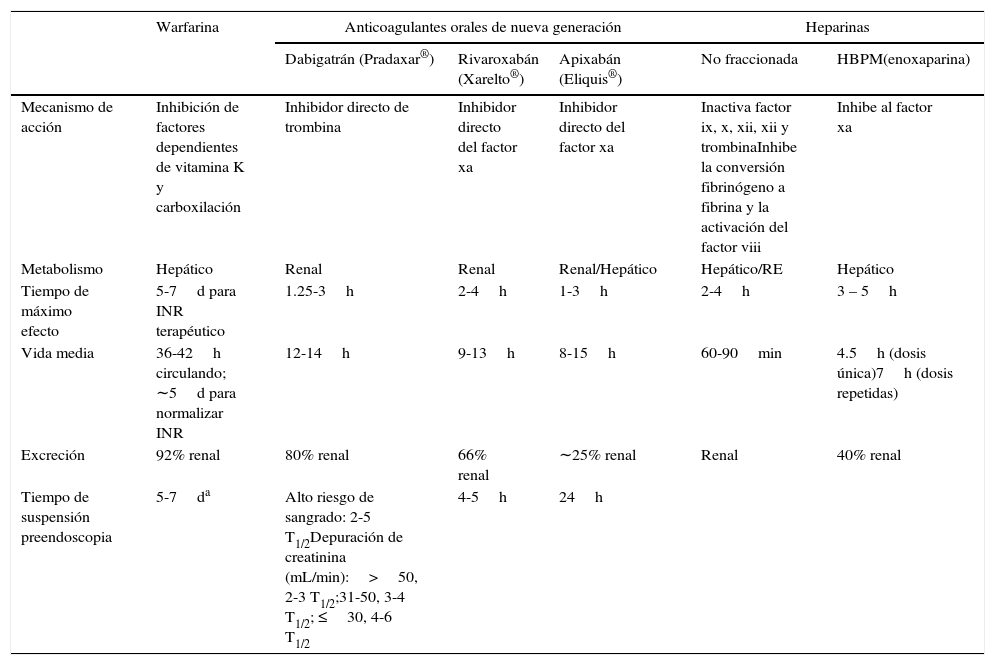
AnticoagulantesLos anticoagulantes tienen efecto a diferentes niveles de la cascada de la coagulación (tabla 1). Los anticoagulantes orales pueden ser inhibidores directos de trombina (dabigatrán, ximelagatrán), inhibidores directos del factor x activado (apixabán, rivaroxabán, darexabán, edoxabán) o pueden inhibir la gamma-carboxilación y los factores dependientes de la vitamina K –II,VIII, IX y X– (warfarina)4. La heparina no fraccionada y la heparina de bajo peso molecular se unen a la antitrombina iii aumentando su actividad con la consecuente inhibición de varios factores de la coagulación5.
Farmacodinamia de anticoagulantes
| Warfarina | Anticoagulantes orales de nueva generación | Heparinas | ||||
|---|---|---|---|---|---|---|
| Dabigatrán (Pradaxar®) | Rivaroxabán (Xarelto®) | Apixabán (Eliquis®) | No fraccionada | HBPM(enoxaparina) | ||
| Mecanismo de acción | Inhibición de factores dependientes de vitamina K y carboxilación | Inhibidor directo de trombina | Inhibidor directo del factor xa | Inhibidor directo del factor xa | Inactiva factor ix, x, xii, xii y trombinaInhibe la conversión fibrinógeno a fibrina y la activación del factor viii | Inhibe al factor xa |
| Metabolismo | Hepático | Renal | Renal | Renal/Hepático | Hepático/RE | Hepático |
| Tiempo de máximo efecto | 5-7d para INR terapéutico | 1.25-3h | 2-4h | 1-3h | 2-4h | 3 – 5h |
| Vida media | 36-42h circulando; ∼5d para normalizar INR | 12-14h | 9-13h | 8-15h | 60-90min | 4.5h (dosis única)7h (dosis repetidas) |
| Excreción | 92% renal | 80% renal | 66% renal | ∼25% renal | Renal | 40% renal |
| Tiempo de suspensión preendoscopia | 5-7da | Alto riesgo de sangrado: 2-5 T1/2Depuración de creatinina (mL/min):>50, 2-3 T1/2;31-50, 3-4 T1/2; ≤30, 4-6 T1/2 | 4-5h | 24h | ||
HBPM: heparina de bajo peso molecular; INR: índice internacional de normalización; RE: reticuloendotelial; T1/2: vida media.
Fuente: Alberca-de-las-Parras et al.31.
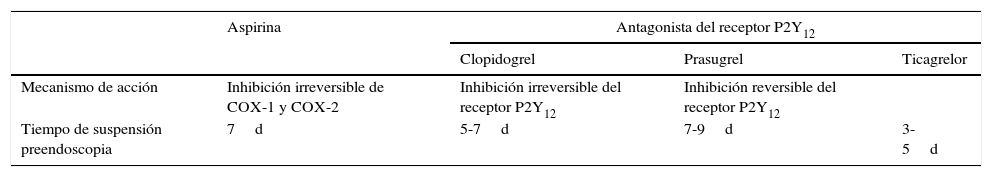
Las plaquetas expresan en su superficie diferentes receptores que son susceptibles de inhibición (tabla 2). La aspirina inhibe al receptor de tromboxano. El receptor ADP (P2Y12) es el blanco de las tienopiridinas (clopidogrel, cangrelor, elinogrel, prasugrel, ticagrelor y ticopidine).
Farmacodinamia de inhibidores de agregación plaquetaria
| Aspirina | Antagonista del receptor P2Y12 | |||
|---|---|---|---|---|
| Clopidogrel | Prasugrel | Ticagrelor | ||
| Mecanismo de acción | Inhibición irreversible de COX-1 y COX-2 | Inhibición irreversible del receptor P2Y12 | Inhibición reversible del receptor P2Y12 | |
| Tiempo de suspensión preendoscopia | 7d | 5-7d | 7-9d | 3-5d |
COX: ciclooxigenasa.
Las indicaciones del uso de aspirina incluyen6:
- -
Prevención primaria de infarto agudo de miocardio o enfermedad vascular cerebral con riesgo mayor al 10% a 5 años
- -
Prevención secundaria de evento cardioembólico
El tratamiento con doble antiagregante plaquetario (aspirina+tienopiridina) está indicado en6:
- –
Angina inestable o infarto agudo de miocardio sin elevación de segmento ST sin intervención coronaria percutánea (máximo 12 meses)
- –
Después de infarto agudo de miocardio con elevación del segmento ST (al menos 14 días)
- –
Colocación de stent coronario: aspirina por tiempo indefinido y tienopiridina hasta 12 meses en caso de stent no medicado, y al menos 12 meses en caso de stent medicado.
Indicaciones de anticoagulación con warfarina7:
- –
Tromboembolismo venoso
- –
Síndrome de anticuerpos antifosfolípidos
- –
Fibrilación auricular
- –
Cardioversión
- –
Enfermedad valvular y colocación de prótesis valvulares
Así como se han establecido las indicaciones de los antitrombóticos, también se ha evaluado el riesgo tromboembólico al suspender el tratamiento. De acuerdo al diagnóstico de base de cada paciente, el riesgo tromboembólico puede ser bajo o alto (tabla 3), por lo que se debe evaluar el riesgo-beneficio de suspender la terapia por la realización de algún procedimiento8.
Tabla 3.Riesgo de complicaciones tromboembólicas de condiciones basales al suspender el tratamiento antitrombótico
Bajo riesgo tromboembólico• FA no complicada y no valvular• Remplazo valvular mecánico en posición aórtica• Remplazo valvular biológico• Trombosis venosa profunda Alto riesgo tromboembólico• Stent coronario liberador de fármaco colocado≤12 meses (terapia dual)• Stent coronario metálico≤6 meses (terapia dual)• PCI después de infarto de miocardio• Antecedente de oclusión del stent• FA con enfermedad valvular• FA con algún factor de riesgo (enfermedad valvular con prótesis, FE<35%, hipertensión, edad>75 años, diabetes, antecedente de EVC o ataque isquémico transitorio)• Remplazo valvular mecánico en posición mitral• Remplazo valvular mecánico en cualquier posición con el antecedente de un evento tromboembólico• Estados hipercoagulantes• Antecedente de EVC isquémico o ataque isquémico transitorio recientes• Antecedente de tromboembolismo venoso reciente EVC: enfermedad vascular cerebral; FA: fibrilación auricular; FE: fracción de expulsión; PCI: intervención coronario percutánea.
Riesgo alto: mayor al 5% por año.
Fuente: Abraham6.
Se ha reportado que el riesgo absoluto de un evento embólico para pacientes en los que la warfarina se interrumpe durante 4-7días es de aproximadamente un 1%9,10, mientras que el riesgo a mayor plazo depende de la enfermedad de base (tabla 3).
Desenlaces hemorrágicos secundarios al uso de antitrombóticosEl tracto gastrointestinal es una fuente común de hemorragia mayor entre los pacientes con antitrombóticos. El uso de estos medicamentos con la combinación de factores específicos como la edad avanzada, el sexo femenino, el antecedente de úlcera péptica, la presencia de comorbilidades, el choque cardiogénico y la falta de coprescrición de un inhibidor de bomba de protones se ha asociado con el incremento de riesgo de sangrado11,12. Las tasas de hemorragia con aspirina se han reportado a 28días del 0.6% y a 12 meses del 3.8%. En el caso de la terapia dual (aspirina más alguna tienopiridina) la tasa a 28 días es del 0.6% y a un año del 4.8%. El riesgo de HGI con triple terapia es del 5.1% a 12 meses13. Por otro lado, la incidencia de hemorragia con el uso de warfarina se ha reportado entre el 1-3% por persona-año14,15. Se ha reportado que el número necesario para dañar al utilizar alguna combinación de fármacos antitrombóticos es importante sobre todo para el caso de HGI baja, con cifras de 15-23. El número necesario para dañar para el desenlace de HGI alta va de 52 a 93, para transfusión de 16 a 51 y para hospitalización se reporta de 34 a 5716.
El impacto de la HGI debe ser resaltado, ya que paradójicamente estos pacientes presentan complicaciones trombroembólicas que afectan su supervivencia. Los pacientes con HGI presentan mayor proporción de trombosis del stent coronario, infarto de miocardio, mortalidad de origen cardíaco y mortalidad por cualquier causa a 30 días y a un año17. La mortalidad hospitalaria secundaria a eventos cardiovasculares trombóticos puede ser hasta del 4.1%, mientras que la mortalidad derivada de la HGI se ha reportado como del 0.15%11.
La HGI originada en pacientes bajo tratamiento antitrombótico también dificulta los procedimientos endoscópicos y puede propiciar eventos adversos o no planeados. Los eventos adversos se pueden considerar como leves si conllevan a procedimientos incompletos, necesidad de segunda endoscopia, transfusiones, requerimiento de radiología intervencionista, estancias hospitalarias cortas no planeadas y tratamientos intervencionistas de lesiones producidas. Los eventos adversos de moderada gravedad pueden ser un internamiento por 4-10 noches, la necesidad de cirugía o alguna incapacidad permanente. Los desenlaces graves son la estancia prolongada en la unidad de terapia intensiva o la muerte6.
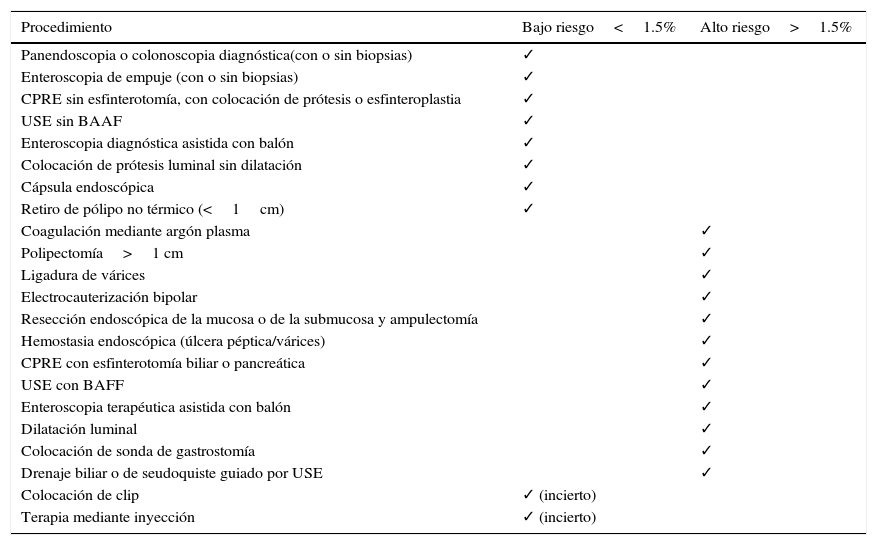
Riesgo hemorrágico de los procedimientos endoscópicos y recomendacionesEl riesgo de hemorragia de los procedimientos endoscópicos se clasifican en bajo o alto de acuerdo a un punto de corte del 1.5% de probabilidad de hemorragia (tabla 4)4.
Probabilidad (riesgo) estimada de hemorragia postendoscopia
| Procedimiento | Bajo riesgo<1.5% | Alto riesgo>1.5% |
|---|---|---|
| Panendoscopia o colonoscopia diagnóstica(con o sin biopsias) | ✓ | |
| Enteroscopia de empuje (con o sin biopsias) | ✓ | |
| CPRE sin esfinterotomía, con colocación de prótesis o esfinteroplastia | ✓ | |
| USE sin BAAF | ✓ | |
| Enteroscopia diagnóstica asistida con balón | ✓ | |
| Colocación de prótesis luminal sin dilatación | ✓ | |
| Cápsula endoscópica | ✓ | |
| Retiro de pólipo no térmico (<1cm) | ✓ | |
| Coagulación mediante argón plasma | ✓ | |
| Polipectomía>1 cm | ✓ | |
| Ligadura de várices | ✓ | |
| Electrocauterización bipolar | ✓ | |
| Resección endoscópica de la mucosa o de la submucosa y ampulectomía | ✓ | |
| Hemostasia endoscópica (úlcera péptica/várices) | ✓ | |
| CPRE con esfinterotomía biliar o pancreática | ✓ | |
| USE con BAFF | ✓ | |
| Enteroscopia terapéutica asistida con balón | ✓ | |
| Dilatación luminal | ✓ | |
| Colocación de sonda de gastrostomía | ✓ | |
| Drenaje biliar o de seudoquiste guiado por USE | ✓ | |
| Colocación de clip | ✓ (incierto) | |
| Terapia mediante inyección | ✓ (incierto) |
BAAF: biopsia por aspiración de aguja fina; CPRE: colangiopancreatografía retrógrada endoscópica; USE: ultrasonido endoscópico.
Fuente: Abraham6 y Committee ASoP8.
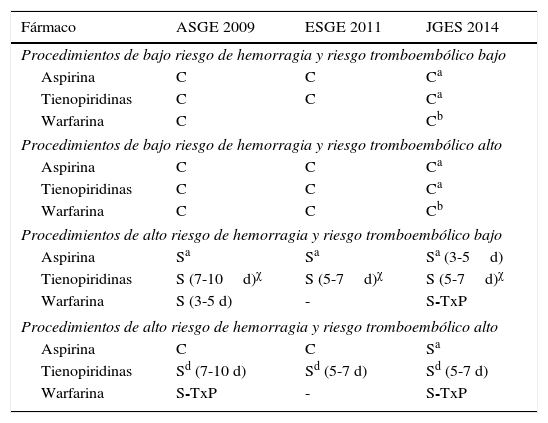
Diferentes organizaciones, incluyendo la Sociedad Americana de Endoscopia Gastrointestinal (ASGE)7, la Sociedad Europea de Endoscopia Gastrointestinal (ESGE)18 y la Sociedad japonesa de Endoscopia Gastroenterológica (JGES)19, han emitido recomendaciones respecto al uso de fármacos antitrombóticos en pacientes que requieren de un procedimiento endoscópico (tabla 5).
Recomendaciones sobre el uso de fármacos antitrombóticos en pacientes programados para procedimientos endoscópicos
| Fármaco | ASGE 2009 | ESGE 2011 | JGES 2014 |
|---|---|---|---|
| Procedimientos de bajo riesgo de hemorragia y riesgo tromboembólico bajo | |||
| Aspirina | C | C | Ca |
| Tienopiridinas | C | C | Ca |
| Warfarina | C | Cb | |
| Procedimientos de bajo riesgo de hemorragia y riesgo tromboembólico alto | |||
| Aspirina | C | C | Ca |
| Tienopiridinas | C | C | Ca |
| Warfarina | C | C | Cb |
| Procedimientos de alto riesgo de hemorragia y riesgo tromboembólico bajo | |||
| Aspirina | Sa | Sa | Sa (3-5d) |
| Tienopiridinas | S (7-10d)χ | S (5-7d)χ | S (5-7d)χ |
| Warfarina | S (3-5 d) | - | S-TxP |
| Procedimientos de alto riesgo de hemorragia y riesgo tromboembólico alto | |||
| Aspirina | C | C | Sa |
| Tienopiridinas | Sd (7-10 d) | Sd (5-7 d) | Sd (5-7 d) |
| Warfarina | S-TxP | - | S-TxP |
ASGE: Sociedad Americana de Endoscopia Gastrointestinal; C: continuar; ESGE: Sociedad Europea de Endoscopia Gastrointestinal; JGES: la Sociedad japonesa de Endoscopia Gastroenterológica; S: suspender; TxP: terapia de puente.
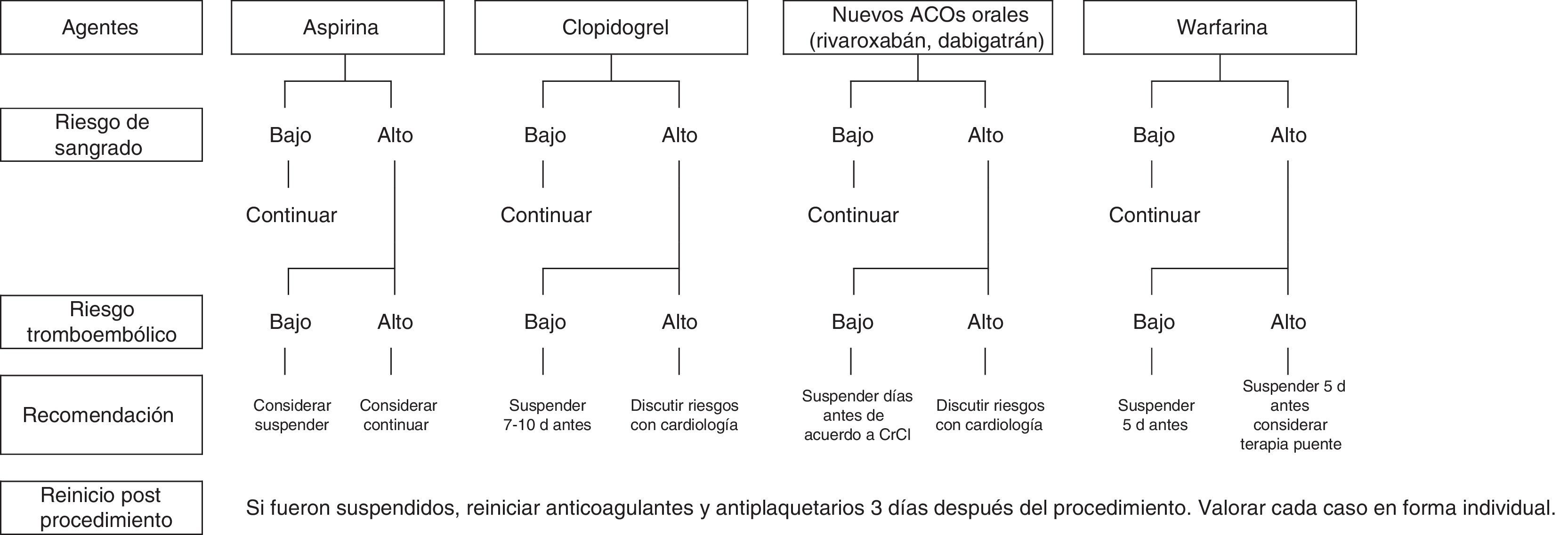
Existen varios escenarios que contemplan el riesgo de hemorragia por el procedimiento endoscópico y el riesgo tromboembólico al suspender los antitrombóticos (fig. 1).
Algoritmo de manejo de pacientes en tratamiento con antitrombóticos.
Modificada de Gorospe y Oxentenko29. Las decisiones se basan en el riesgo tromboembólico y de sangrado.
En general, en los procedimientos con bajo riesgo de hemorragia en pacientes con bajo o alto riesgo tromboembólico el tratamiento tromboembólico se puede continuar durante el procedimiento endoscópico. La ASGE, ESGE y la JGES recomiendan que los fármacos continúen en pacientes sometidos a procedimientos de diagnóstico sin biopsia de la mucosa; sin embargo si se requiere tomar una biopsia, la incidencia de sangrado no es significativamente mayor al comparar a pacientes que suspenden la terapia antitrombótica vs. los que no lo hacen (0.35 vs. 0.14%, p=0.38)20.
En procedimientos con alto riesgo hemorrágico y riesgo tromboembólico bajo se recomienda suspender el tratamiento tromboembólico.
En el caso de alto riesgo hemorrágico y tromboembólico, la ASGE y la ESGE recomiendan que el tratamiento continúe únicamente con aspirina. Se recomienda que los procedimientos electivos en este grupo de pacientes se retrasen hasta concluir la terapia. Antes de modificar cualquier tratamiento se debe considerar la indicación y los factores de riesgo tromboembólico para limitar las consecuencias de suspender los fármacos.
En el caso de síndromes coronarios agudos se han establecidos períodos de mayor riesgo de tromboembolismo, durante los cuales suspender la terapia dual con aspirina y tienopiridina incrementa el riesgo de oclusión del stent, infarto de miocardio y la mortalidad en un 50%6:
- –
90 días después de síndrome coronario agudo (independientemente del tratamiento con fármacos o con intervención coronaria percutánea)
- –
30-45 días después de la colocación de stent no medicado
- –
3-6 meses después de la colocación de stent medicado
Durante estos períodos se debe evitar suspender el tratamiento dual. Como se explicó anteriormente, un procedimiento endoscópico de bajo riesgo de hemorragia se puede realizar sin suspender el tratamiento dual. En caso de requerirse de un procedimiento endoscópico con alto riesgo de hemorragia, la tienopiridina se suspende solo por 5-7 días mientras que la administración de aspirina debe continuar21.
En el caso de los usuarios de warfarina, la hemostasia endoscópica se puede realizar con INR de 1.5-2.7, por lo que el tratamiento endoscópico urgente puede no posponerse22; sin embargo se debe ser muy cuidado con esta indicación y evaluar la urgencia real.
Nuevos anticoagulantes oralesLos nuevos anticoagulantes incluyen a los inhibidores directos del factor xa o de la trombina. Estos medicamentos se encuentras disponibles para su administración oral, subcutánea o intravenosa. Los anticoagulantes orales directos actualmente aprobados y disponibles en México incluyen el dabigatrán, el rivaroxabán y el apixabán. Para limitar el riesgo, los anticoagulantes orales deben ser suspendidos durante al menos 3 vidas medias antes del procedimiento endoscópico, pero el tiempo se debe ampliar de acuerdo a la función renal y al riesgo de sangrado del procedimiento (tabla 1)23.
Los procedimientos urgentes por sangrado activo deben ser manejados mediante la suspensión del anticoagulante, transfusión y tratamiento endoscópico o radiológico para realizar hemostasia. En caso de indicación de una colangiopancreatografía de urgencia se colocará una prótesis sin realizar esfinterotomía23.
Terapia puenteEl empleo de terapia puente (bridging therapy) está indicado solo en aquellos pacientes con alto riesgo de hemorragia y alto riesgo tromboembólico. Se puede realizar con heparina no fraccionada o con heparina de bajo peso molecular7,24. Esta indicación se basa en las recientes publicaciones sobre una posible relación con el incremento del riesgo de sangrado.
Las principales indicaciones para el uso de terapia puente son25:
- •
Portadores de válvulas protésicas. Reemplazo valvular mitral, 2 o más válvulas mecánicas, reemplazo de válvula aórtica bivalva o reemplazo valvular aórtico con otros factores de riesgo.
- •
Fibrilación auricular no valvular. Con antecedente de evento embólico, trombo intracardíaco, puntaje de CHADS2Score mayor o igual a 4.
- •
Tromboembolismo venoso. En 3 meses previos o trombofilia severa (deficiencia de proteína C, proteína S o antitrombina; síndrome antifosfolípidos; homocigoto para factor v de Leiden; homocigoto para la mutación del gen de protrombina G20210A; o componente heterocigoto para los 2 genes).
El protocolo de la terapia puente consiste en suspender la warfarina 5 días antes del procedimiento endoscópico, vigilar el valor de INR hasta ser<2.5 para iniciar heparina no fraccionada o heparina de bajo peso molecular, administrando la última dosis al 50% y de acuerdo a la vida media de la heparina. La heparina de bajo peso molecular se reinicia al lograr el control hemostático y se suspende al alcanzar un rango terapéutico de INR con la administración de warfarina25.
La utilización de la terapia puente debe ser individualizada ya que un metaanálisis ha demostrado que la terapia puente con heparina incrementa en forma global el riesgo de sangrado clínicamente relevante, sin aumentar significativamente el riesgo de eventos tromboembólicos26, y un ensayo clínico aleatorizado realizado en pacientes con fibrilación auricular demostró que la interrupción del anticoagulante oral previo a una cirugía o procedimiento electivo (50% de los procedimientos fueron endoscópicos) no es inferior a la terapia puente con heparina de bajo peso molecular para la prevención de tromboembolismo arterial y que disminuye en forma significativa el riesgo de sangrado; sin embargo, cabe destacar que la mayor parte de los procedimientos realizados en dicho estudio eran de bajo riesgo de hemorragia27.
Ante la evidencia mencionada se podría limitar el uso de terapia puente a aquellos casos donde exista un alto riesgo de tromboembólico y el procedimiento a realizar sea de bajo riesgo hemorrágico. En caso contrario se podrá recomendar suspender el anticoagulante oral antes del procedimiento y reiniciarlo en el momento en que sea segura la hemostasia.
Manejo de evento agudoLos pacientes bajo tratamiento antitrombótico que presentan un evento agudo de HGI con compromiso hemodinámico, disminución mayor o igual a 2g de hemoglobina o signos clínicamente evidentes de HGI (melena, hematemesis, posos de café, hematoquecia) requieren un procedimiento endoscópico de urgencia. En el manejo de estos pacientes debe considerarse lo siguiente6:
- 1.
El riesgo de sangrado del procedimiento endoscópico empleado para hemostasia (tabla 4). Debe considerarse que los procedimientos endoscópicos para hemostasia son maniobras que conllevan un alto riesgo de sangrado posprocedimiento. La magnitud es de al menos>1.5%, sin embargo este riesgo puede ser aún mayor en los contextos de coagulopatía preexistente (no inducida por medicamentos) y comorbilidades asociadas, como disfunción renal, hepática y/o presencia de cáncer.
- 2.
Manejo de antiplaquetarios en sangrado. La decisión de modificar el tratamiento con inhibidores de la agregación plaquetaria debe basarse en el conocimiento de la farmacología, mecanismo de acción, indicación, consecuencias del evento tromboembólico y la presencia de factores de riesgo tromboembólico. No se conoce con exactitud el riesgo de realizar un procedimiento endoscópico hemostático en pacientes que toman estos medicamentos o en quienes es necesario reiniciarlos a la brevedad. En el caso del tratamiento con aspirina no existe un incremento del riesgo de sangrado posprocedimiento asociado, pero en pacientes de alto riesgo cardiovascular su suspensión incrementa la mortalidad a 30 días. En los casos de HGI severa se puede requerir la resucitación agresiva con volumen, el uso de inotrópicos y la transfusión de plaquetas para promover la hemostasia endoscópica, radiológica o quirúrgica.
- 3.
Manejo de anticoagulantes en sangrado. La heparina no fraccionada presenta un riesgo de sangrado menor al 3%. Las heparinas de bajo peso molecular tienen un menor riesgo de sangrado. Se ha establecido el tiempo necesario de suspensión para la pérdida del efecto anticoagulante (tabla 1). El riesgo de sangrado asociado a warfarina está determinado por la intensidad del efecto anticoagulante, las características basales del paciente y la duración del tratamiento. En el 93% de los casos el INR disminuye a menos de 1.5 después de 5 días de suspensión del medicamento. La reversión del efecto se consigue con la transfusión de plasma fresco congelado y/o vitamina K. Parece ser que la normalización del INR no es estricta, ya que la hemostasia endoscópica puede llevarse a cabo en forma segura en pacientes con INR hasta de 2.7 y las tasas de resangrado son similares con y sin reversión de la anticoagulación; sin embargo se debe tomar con reserva esta información y tratar de alcanzar un INR por debajo de 1.523.
- 4.
Manejo de nuevos anticoagulantes. El momento para suspender estos medicamentos antes del procedimiento endoscópico está determinado por la vida media, la tasa depuración de creatinina y el riesgo de sangrado. Es primordial la resucitación agresiva con volumen preendoscópica, ya que estos medicamentos son eliminados en su mayoría por vía renal. En caso necesario deberá considerarse la administración de factor vii activado, o concentrado de complejo de protrombina (activados o no). El concentrado de complejo de protrombina activado es el agente más efectivo para revertir el efecto de dabigatrán, mientras que los concentrados de complejo de protrombina no activados son más útiles para revertir los agentes anti-factor xa. Por otro lado, también existen nuevos agentes para reversión de efecto anticoagulante. El idarucizumab es anticuerpo monoclonal humanizado que expresa un fragmento de un anticuerpo específico que tiene alta afinidad por el dabigatrán casi inmediatamente (en 5min)28. El peroesphera es una pequeña molécula catiónica, sintética, soluble en agua, que se une en forma no covalente a las heparinas no fraccionada y de bajo peso molecular, pero están pendientes los estudios para determinar su eficacia23,29.
Al menos un 20% de los pacientes que presentan una HGI no reinicia el tratamiento con aspirina o tienopiridina después del alta hospitalaria; este porcentaje aumenta al 40% entre los pacientes con anticoagulantes orales17.
En general se recomienda que el tratamiento antitrombótico se reinicie en cuanto se tenga control hemostático, en la mayoría de los casos el mismo día del procedimiento. Si no hay seguridad del control hemostático se requerirá de una valoración individualizada. En los casos con requerimiento de doble antiagregación plaquetaria siempre se debe continuar con la aspirina mientras que la tienopiridina será suspendida 5-7 días antes del procedimiento y se reiniciará una vez que se logre la hemostasia; sin embargo no hay que olvidar que durante los períodos de alto riesgo tromboembólico se debe evitar suspender el tratamiento dual30.
En el caso de anticoagulación con warfarina la ASGE recomienda que se inicie dentro de las 24h siempre y cuando sea seguro. En general, se considera seguro iniciar la heparina de bajo peso molecular 48h después del procedimiento (si se ha alcanzado la hemostasia), pero puede hacerse en las primeras 24h si se trata de un procedimiento de baja probabilidad de hemorragia, o hasta las 72h en el caso de procedimientos de alto riesgo7.
ConclusionesLa prevalencia del uso de antitrombóticos claramente se está incrementando de manera que con mayor frecuencia nos enfrentaremos sus efectos secundarios. Por otro lado, estos pacientes no están exentos de requerir algún tratamiento endoscópico por alguna causa diferente a hemorragia, por lo que es muy importante que los endoscopista tengan el conocimiento de cómo actuar. Lo ideal sería que los cambios del tratamiento antitrombótico se realicen de acuerdo al riesgo tromboembólico por suspender dichos fármacos y al riesgo de hemorragia a causa de los procedimientos, y esta decisión debería ser tomada en conjunto por el cardiólogo y el endoscopista; sin embargo no siempre será posible, por lo cual se espera que el endoscopista comience a adquirir los conocimientos sobre el tema con la finalidad de evitar desenlaces no deseados.
FinanciamientoLos autores no recibieron patrocinio para llevar a cabo este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.