INTRODUCCIÓN
Enfermedad inflamatoria intestinal (EII) es un término general que se aplica a un grupo de enfermedades inflamatorias crónicas de etiología desconocida que afectan al tubo digestivo.
La EII crónica puede dividirse en 2 grupos principales, la colitis ulcerosa (CU) y la enfermedad de Crohn (EC). La CU afecta exclusivamente al colon, con mayor o menor extensión; la lesión se limita a la mucosa y la submucosa de forma continua. Por el contrario, la EC puede afectar a cualquier parte del tubo digestivo, desde la boca al ano; las lesiones son segmentarias y transmurales, y pueden afectar a todas las capas de la pared intestinal. De ahí su tendencia a la fistulización.
La incidencia en España de CU es de 8 por 100.000 habitantes/año y la de EC, de 5,5 por 100.000 habitantes/año1. Alrededor de un 25% de los pacientes se diagnostican en la infancia o la adolescencia.
El tratamiento de estas entidades incluye una combinación de terapias nutricionales, farmacológicas y quirúrgicas que habrán de individualizarse.
En esta revisión se ha realizado una actualización sobre el soporte nutricional basado en la evidencia en la EII. Para ello se realizó una búsqueda bibliográfica en MEDLINE (1981-2004) y la Cochrane Library de ensayos clínicos aleatorizados y metaanálisis que incluyan las palabras clave inflammatory bowel diseases, Crohn disease, colitis, ulcerative y malnutrition, enteral nutrition, parenteral nutrition, glutamine, fiber, prebiotics y probiotics. Se limitó la búsqueda a artículos publicados en lengua inglesa y española. Se completa con la revisión manual de las citas relevantes y revisiones aparecidas en la bibliografía de los artículos seleccionados.
¿ES FRECUENTE LA MALNUTRICIÓN EN LOS PACIENTES CON ENFERMEDAD INFLAMATORIA INTESTINAL?
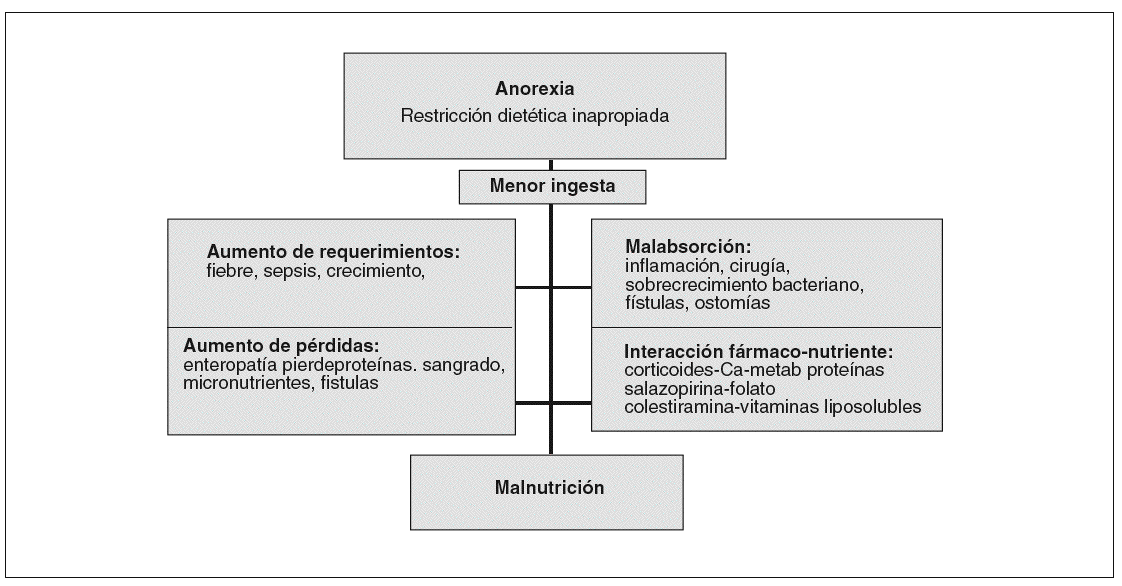
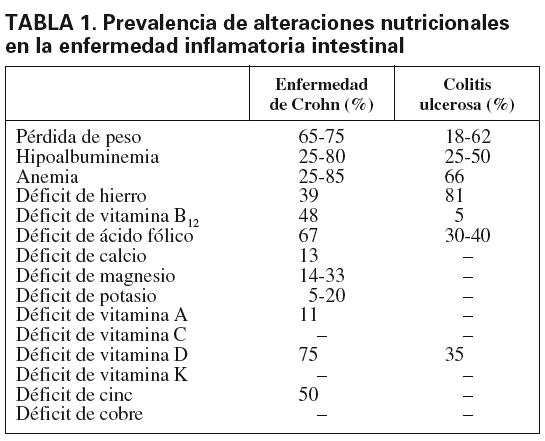
Los pacientes con EII presentan un amplio espectro de alteraciones nutricionales, desde malnutrición energético-proteínica, malnutrición proteica y deficiencias de micronutrientes (tabla 1)2. En general, estas alteraciones ocurren con más frecuencia en los pacientes con EC, en los brotes moderados-graves y en los enfermos hospitalizados3. La etiopatogenia de la malnutrición es multifactorial (fig. 1). Esta malnutrición originará importantes repercusiones para el enfermo (alteraciones en la composición corporal, pérdida de peso, retraso de crecimiento y de la maduración sexual en los niños y adolescentes, cuadros clínicos por deficiencia de micronutrientes, inmunosupresión, etc.), al tiempo que puede influir negativamente en el curso de la enfermedad (alteraciones en la cicatrización, atrofia vellositaria, mayor morbilidad operatoria, etc.)4.
Fig. 1. Etiopatogenia de la malnutrición en la enfermedad inflamatoria intestinal.
La Sociedad Americana de Nutrición Parenteral y Enteral (ASPEN) considera que los pacientes con EII están en riesgo de desnutrición, por lo que se les debería realizar un cribado nutricional a todos ellos para identificar a los pacientes que requieran una valoración nutricional formal que permita desarrollar un tratamiento nutricional adecuado (grado de recomendación B)5.
¿EN QUÉ CIRCUNSTANCIAS Y QUÉ TIPO DE SOPORTE NUTRICIONAL DEBERÍA UTILIZARSE EN LOS PACIENTES CON ENFERMEDAD INFLAMATORIA INTESTINAL?
Dada la alta prevalencia de malnutrición en estos enfermos, en muchas ocasiones será necesario instaurar un soporte nutricional. Siguiendo las recomendaciones de la ASPEN, son candidatos a recibir un soporte nutricional artificial los pacientes con malnutrición grave, los pacientes con malnutrición moderada que no realicen una ingesta oral adecuada y los enfermos con brotes graves de la enfermedad que podrían originar malnutrición a corto plazo (5-7 días) si no se instaura un adecuado soporte nutricional4,6.
Los objetivos del tratamiento nutricional que se han propuesto en la EC han sido5:
Revertir la malnutrición.
Como tratamiento primario para alcanzar la remisión clínica y disminuir la resección quirúrgica.
En el preoperatorio en pacientes con malnutrición.
Revertir el retraso de crecimiento de los niños.
Facilitar la curación de las fístulas enterocutáneas.
En los pacientes con síndrome de intestino corto.
En los pacientes con CU, el soporte nutricional se ha utilizado para intentar alcanzar la remisión clínica evitando la necesidad de cirugía5. En cuanto al tipo de soporte nutricional (enteral o parenteral) en los pacientes con EC no se ha demostrado que el reposo intestinal mejore el curso de la enfermedad. En estudios prospectivos que comparan la evolución de los pacientes tratados con reposo intestinal más nutrición parenteral (NP) frente a nutrición enteral (NE), el porcentaje de remisiones clínicas fue similar en ambos grupos7,8. La NE estaría contraindicada en pacientes con EC que presenten fístulas yeyunales de alto flujo, obstrucción intestinal, íleo paralítico, sepsis intraabdominal, hemorragia digestiva grave o perforación intestinal. En todos estos casos se debería utilizar NP.
Tampoco en los estudios publicados en pacientes con CU parece que el reposo intestinal produzca remisiones clínicas y/o evite la colectomía en estos enfermos. Dos estudios controlados realizados en pacientes con brotes graves de CU demostraron que el reposo intestinal más NP, en comparación con la dieta oral normal, no influyó en el curso clínico de los pacientes tratados con corticoides9,10. En un estudio controlado que comparó la evolución de los pacientes con CU grave con corticoides que recibieron NE con los tratados con NP y reposo digestivo, no se observaron diferencias en el curso clínico ni en la necesidad de cirugía, pero sí hubo mayor número de infecciones y de complicaciones relacionadas con el tratamiento nutricional en los que recibieron NP11. Por tanto, en los pacientes con CU la NP sólo debería reservarse para los pacientes que no toleren la NE o en los que ésta esté contraindicada (megacolon tóxico, íleo paralítico, hemorragia digestiva, obstrucción intestinal, perforación intestinal).
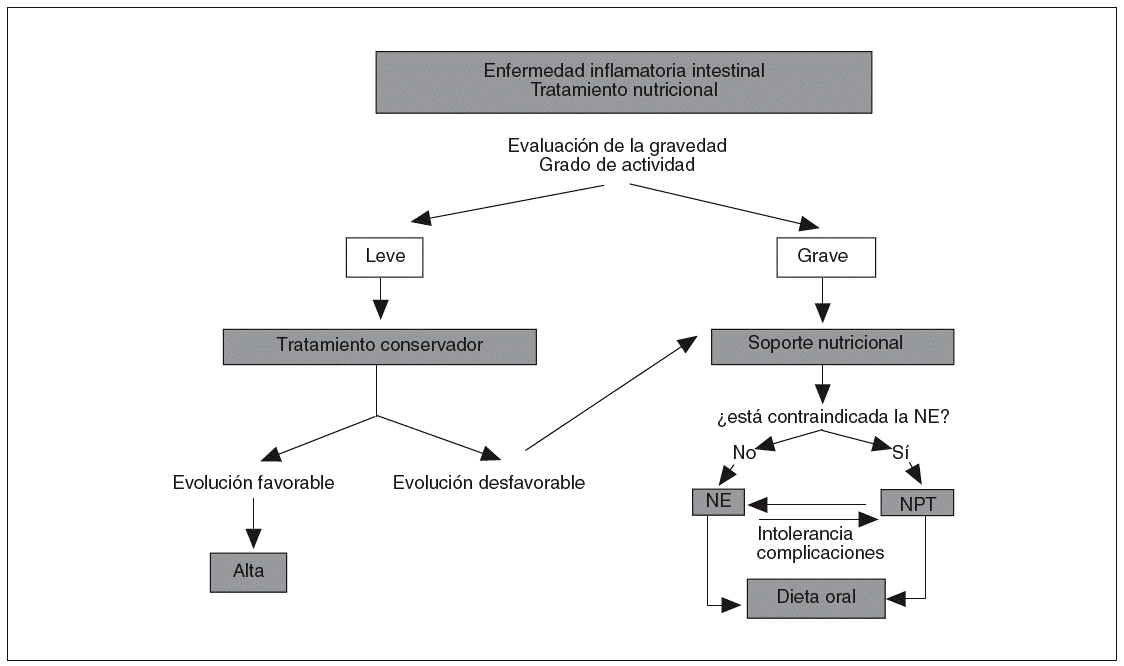
Por tanto, en los pacientes con EII en los que esté indicado iniciar un soporte nutricional se debería utilizar la NE (por vía oral o por sonda) (fig. 2). La NP sólo deberá utilizarse en los pacientes en que esté contraindicada la NE o no sea bien tolerada5 (grado de recomendación B).
Fig. 2. Algoritmo del soporte nutricional en la enfermedad inflamatoria intestinal NE: nutrición enteral; NPT: nutrición parenteral total.
¿QUÉ TIPO DE FÓRMULA DE NUTRICIÓN ENTERAL DEBERÍA EMPLEARSE EN ESTOS PACIENTES?
Se han publicado numerosos estudios aleatorizados que comparan la utilidad de las dietas elementales frente a las no elementales (peptídicas o poliméricas) para inducir la remisión12-21 en los pacientes con EC. Asimismo, se han realizado 3 metaanálisis que evalúan los resultados de estos estudios22-24. En todos ellos no se encontraron diferencias significativas entre las dietas elementales y no elementales para inducir la remisión en pacientes con EC (tabla 2) (grado de recomendación A).
Las dietas elementales produjeron la remisión en el 65% de los casos, frente al 61% en las dietas no elementales22.
La mayoría de autores recomienda que, dado que las dietas poliméricas son mejor toleradas por su menor osmolaridad y permiten aportar mayor cantidad de nitrógeno, deberían utilizarse en la mayoría de los casos, y reservar las dietas elementales o peptídicas para los pacientes que no toleren de forma adecuada las dietas poliméricas o que presenten gran alteración de la función intestinal.
Además, no deberían utilizarse fórmulas enterales con lactosa o con un elevado contenido en sacarosa u otros disacáridos debido al riesgo de inducir diarreas.
Las dietas enterales podrán administrarse por vía oral o por sonda nasogástrica. Cuando se emplea esta última es preferible la infusión continua y con bomba peristáltica para una mejor tolerancia de la dieta. En los pacientes que adquieran NE de forma prolongada (> 4-6 semanas) se deberán utilizar accesos enterales permanentes, como la gastrostomía endoscópica percutánea25.
¿ESTÁ INDICADA LA NUTRICIÓN ENTERAL COMO TRATAMIENTO PRIMARIO EN LA ENFERMEDAD INFLAMATORIA INTESTINAL?
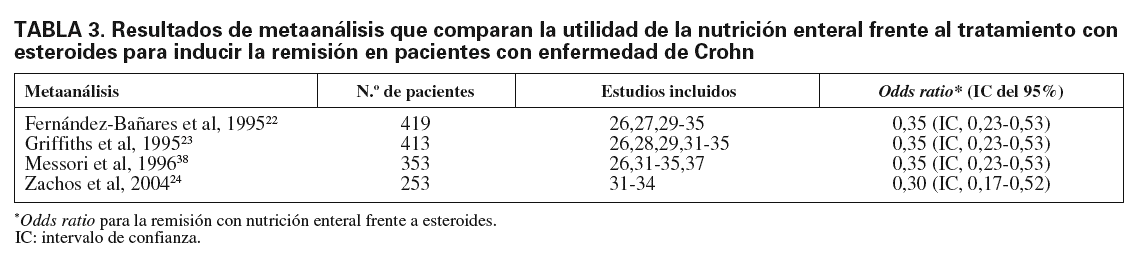
En la EC la NE podría tener un efecto antiinflamatorio y se ha sugerido que podría ser útil para controlar los brotes de actividad de esta enfermedad. En numerosos estudios aleatorizados se ha estudiado la eficacia de la nutrición enteral frente al tratamiento esteroideo para inducir la remisión en pacientes con EC26-37. Además, se han publicado 4 metaanálisis en los que se concluye que el tratamiento con corticoides es superior a la NE como tratamiento primario de la EC22-24,38 (tabla 3).
El tratamiento con esteroides induce un porcentaje de remisiones del 80%, frente al 60% en la NE22. Por tanto, la NE no debería utilizarse como tratamiento primario de elección en los pacientes con EC5 (grado de recomendación A).
No obstante, es de señalar que el porcentaje de remisiones con la NE es superior al esperado con un placebo (alrededor del 20-30% en la mayoría de las series).
Los mecanismos por los que la NE puede tener un efecto terapéutico en estos pacientes son desconocidos. Las hipótesis iniciales sugerían que la antigenicidad de las proteínas de la dieta podría ser responsable del inicio de la respuesta inflamatoria. Sin embargo, en ninguno de los metaanálisis realizados se encontraron diferencias en el porcentaje de remisiones cuando se utilizaron dietas elementales o no elementales (poliméricas o peptídicas)22-24. Más recientemente, se ha señalado que la composición lipídica de estas dietas podría desempeñar un papel importante para inducir la remisión en estos pacientes39.
Por todo ello, la NE sólo estaría indicada como tratamiento primario de la EC en los pacientes en que exista contraindicación para el tratamiento con esteroides. Éste podría ser el caso de los niños y los adolescentes en fase de crecimiento y en la osteoporosis notoria, sobre todo si se trata de brotes de actividad leve o moderada.
¿SON ÚTILES ALGUNOS NUTRIENTES ESPECÍFICOS EN LOS PACIENTES CON ENFERMEDAD INFLAMATORIA INTESTINAL?
Tipo de grasa
Entre los mecanismos patogénicos responsables de la utilidad de la NE como tratamiento primario en los pacientes con EC, se ha sugerido que el tipo de grasa podría desempeñar un papel importante39,40. En un metaanálisis se observó que el número de remisiones es mayor en los estudios que utilizan dietas con un menor contenido en triglicéridos de cadena larga (TCL), sin bien eran estudios con pocos pacientes41. También en un estudio reciente aleatorizado con dieta enteral en pacientes con EC activa la tasa de remisiones fue inversamente proporcional al contenido en TCL de la dieta42. Sin embargo, los resultados de otros estudios no apoyan esta conclusión. Un estudio aleatorizado y controlado reciente en que se comparaban 2 dietas poliméricas con un 35% de grasa pero con diferente contenido en TCL (un 5% de las calorías totales frente a un 30%) produjo unas tasas de remisiones similares, un 26 y un 33%, respectivamente, si bien la mitad de los pacientes no toleraron la dieta, y las tasas de remisiones (por intención de tratar) fueron muy bajas, similares a los de un placebo43.
En cuanto a los triglicéridos de cadena media (TCM), no parece que disminuyan la eficacia de la NE como tratamiento en la EC41. Khoshoo et al obtuvieron respuestas similares en adolescentes con EC con una dieta peptídica con un 9% de las calorías totales en forma de grasa (de las cuales el 45% eran TCM) y con un 33% de grasa (de las cuales el 70% eran TCM)44. Más recientemente, Sakurai et al obtuvieron respuestas alrededor del 70% utilizando dieta elemental baja en grasa (el 1,5% grasa) o dieta con hidrolizado de proteínas con el 25% de grasa, en su mayoría TCM45.
En la revisión sistemática de la biblioteca Cochrane sobre la NE como tratamiento primario en EC se hizo un subanálisis con los ensayos que comparaban dietas bajas en grasa (< 20 g/1.000 kcal) frente a altas en grasas (> 20 g/1.000 kcal), y no se encuentran diferencias estadísticamente significativas (odds ratio [OR] = 1,05; intervalo de confianza [IC] del 95%, 0,45-2,45)24. Tampoco en otro subanálisis, en que se comparaban las dietas muy bajas en grasa (< 3 g/1.000 kcal) frente a las ricas en grasa, se obtuvieron diferencias significativas (OR = 2,03; IC del 95%, 0,65-6,29)24.
Más recientemente, el interés se ha centrado en el tipo de grasa (poliinsaturada *6, *3, monoinsaturada), ya que podría modular la respuesta inflamatoria a través de la síntesis de eicosanoides y de citocinas. Las dietas ricas en ácido linoleico (*6), precursor del ácido araquidónico, podrían aumentar la respuesta inflamatoria en estos pacientes debido a la producción de prostaglandinas y leucotrienos proinflamatorios. Aunque en un principio se pensaba que la utilización de dietas ricas en grasa monoinsaturada podría ser beneficiosa en relación con dietas con gran contenido en ácido linoleico, en un estudio aleatorizado y multicéntrico reciente no se observó dicho beneficio46. El porcentaje de remisiones en el grupo tratado con dieta rica en ácido oleico fue del 20%, frente al 52% en el grupo tratado con dieta rica en ácido linoleico, siendo el contenido total de grasa similar en ambas dietas.
Los ácidos grasos poliinsaturados *3 se han utilizado en los pacientes con EII ya que son precursores de eicosanoides con un menor efecto inflamatorio que los derivados del ácido araquidónico. Los aceites de pescado son ricos en *3 aunque su tolerancia no es buena, a menos que se utilicen en cápsulas con cubierta entérica para disminuir los efectos indeseables de halitosis, pirosis, flatulencia y diarrea.
Los resultados del tratamiento con estos ácidos grasos en pacientes con EII se han revisado recientemente y varían dependiendo de si los pacientes se encontraban o no en remisión, según la dosis, la forma de administración, etc.47
En el estudio de Beluzzi et al48, la utilización de aceites de pescado con cubierta entérica 2,7 g/día en pacientes con EC en remisión produjo una menor tasa de recaídas al año de tratamiento comparado con el grupo placebo. Sin embargo, en un estudio también aleatorizado con 5 g/día de aceite de pescado no se confirmó la disminución de las recaídas al año de tratamiento49. En otro estudio, la administración de 3,2 g/día de *3 no afectó el grado de actividad en pacientes con EC50.
En adultos con CU leve-moderada, en 4 estudios con dosis de ácidos grasos *3 entre 2,7 y 5,4 g/día demostraron una modesta mejoría clínica y una disminución de los requerimientos de esteroides51-54. Salvo el estudio de Loeschke et al55, la mayoría de trabajos no han mostrado efectos beneficiosos en pacientes con CU en remisión53,56,57.
Con los resultados actuales no existe una evidencia científica fuerte para apoyar el uso de dietas pobres en grasa en estos pacientes, aunque probablemente su tolerancia clínica sea mejor. Por otro lado, los estudios actuales tampoco parecen apoyar que el ácido linoleico de las dietas tenga un efecto perjudicial en esta enfermedad, en relación con otras grasas, si bien son necesarios más estudios. El efecto de los ácidos grasos poliinsaturados de la serie *3 en el tratamiento de los pacientes con EII requiere de nuevos estudios.
Glutamina
Es un aminoácido semiesencial que se considera el combustible de elección del enterocito. Tiene un papel importante en el mantenimiento de la integridad de la mucosa y de la barrera intestinal. En el 50% de los pacientes con EC se ha descrito un aumento en la permeabilidad intestinal que podría ser importante en la patogenia de la enfermedad.
En un estudio con pacientes con EII activa tratados con NP la suplementación con glutamina previno el incremento de la permeabilidad intestinal a la lactulosa y manitol en el período postoperatorio58.
En un estudio aleatorizado en pacientes con EC con aumento de la permeabilidad intestinal, la suplementación con glutamina oral (21 g/día) durante 4 semanas no mostró diferencias significativas en la permeabilidad de la membrana intestinal, en la actividad de la enfermedad ni en el estado nutricional respecto al grupo control59. En otro estudio aleatorizado en niños con EC activa con dieta enteral polimérica frente a dieta enteral polimérica enriquecida en glutamina, no se observaron diferencias en el número de remisiones (OR = 0,64; IC del 95%, 0,10-4,11)60.
Con los resultados actuales no parece que la suplementación con glutamina sea eficaz para inducir la remisión en pacientes con EC activa (grado de recomendación B).
Fibra y prebióticos
El concepto de fibra incluye un conjunto de sustancias con diferentes características en cuanto a fermentabilidad, solubilidad, viscosidad, etc., que tienen como denominador común que escapan a la digestión de las enzimas digestivas humanas. Dentro del concepto de fibra total se incluyen la fibra dietética (polisacáridos no almidónicos y la lignina) y la fibra funcional (almidón resistente, fructooligosacáridos, galactooligosacáridos, disacáridos). En algunas de estas fibras funcionales se ha demostrado ya un efecto prebiótico en el hombre, es decir, que serían fibras fermentables capaces de estimular de forma selectiva el crecimiento de ciertas bacterias del colon beneficiosas para la salud del huésped. Entre ellas se encuentran los fructooligosacáridos y los galactooligosacáridos61.
Una de las teorías sobre la patogenia de la EII se basa en que en estos pacientes se produciría una activación de la respuesta inmune e inflamatoria iniciada por un factor medioambiental, que podrían ser las propias bacterias de la flora intestinal. En este sentido, se sabe que el número de bacterias adheridas a la mucosa intestinal es superior en los pacientes con EII que en los sujetos normales, y es mayor según la gravedad de la enfermedad, predominando algunos géneros, como Proteobacteria, Enterobacteria, Bacteroides o Prevotella62.
Algunos tipos de fibra podrían tener un efecto antiinflamatorio a través de diferentes mecanismos, como la acidificación del pH intestinal, en producción de ácidos grasos de cadena corta (AGCC), principalmente butirato, y modificaciones de la flora intestinal con incremento de la proporción de bacterias acidolácticas. La acidificación del contenido del colon se debe a la producción de ácido láctico y de AGCC. El butirato es el AGCC considerado como combustible principal del colonocito. Además de actuar como sustrato energético para el colonocito, el butirato podría disminuir la inflamación mediante la inhibición de la activación del factor nuclear kappa B (NF*B), inhibiendo la producción de citocinas proinflamatorias.
Por otro lado, los cambios en la flora bacteriana inducidos por los prebióticos puede también disminuir la inflamación, debido a que favorecen el crecimiento de bacterias acidolácticas, Lactobacillus y Bifidobacterium.
Otra teoría sobre la patogenia de la CU sería que en estos pacientes existiría una deficiencia en la oxidación del butirato y que este defecto podría corregirse con niveles suprafisiológicos de AGCC en el colon63. En esta línea, los ensayos clínicos publicados sugieren que la administración tópica de AGCC podría ser útil como tratamiento primario y/o coadyuvante en pacientes con CU distal con afección leve-moderada64.
El efecto de la fibra fermentable (como fuente de AGCC) también se ha estudiado en estos pacientes. En un estudio controlado y aleatorizado se comparó el efecto de las semillas de Plantago ovata con el tratamiento estándar con mesalamina como terapia de mantenimiento en pacientes con CU en remisión, no encontrándose diferencias en la tasa de recaídas al año de tratamiento entre ambos grupos65.
En otro estudio aleatorizado y doble ciego realizado en pacientes con CU activa en que se comparaba una dieta enteral polimérica estándar con otra enriquecida con hidrolizado de goma guar, se observó una mejoría más notoria en las biopsias de colon de los pacientes tratados con la dieta enriquecida en fibra guar66.
En un estudio controlado y aleatorizado, la ingestión de inulina (24 g/día) durante 3 semanas disminuyó significativamente la inflamación endoscópica e histológica de la mucosa de los pacientes con reservorio ileal (pouchitis)67.
En un estudio abierto, el tratamiento con un preparado prebiótico de cebada germinada produjo una disminución de los índices de actividad clínica y endoscópica de la CU en pacientes con brotes de actividad leve-moderada que recibían su tratamiento antiinflamatorio habitual68.
A la vista de los resultados actuales es probable que algunas fibras fermentables resulten eficaces en el tratamiento de pacientes con EII con afección colónica y/o en enfermos con pouchitis, aunque se necesitan más estudios controlados y de mayor muestra para comprobar su utilidad en este tipo de enfermos.
Probióticos
Los probióticos son microorganismos viables no patógenos que confieren efectos beneficiosos para el huésped mejorando el balance microbiológico de la microflora intestinal69. Incluyen las especies bacterianas Lactobacilli, Bifidobacteria, cocos grampositivos y enterococos, levaduras (Saccharomyces boulardii) y hongos (Aspergillus orizae).
Son varias las líneas de evidencia que relacionan a la EII con modificaciones en la microflora intestinal70. Los mecanismos por los que los probióticos podrían ser útiles en estos pacientes serían: a) compitiendo con los microorganismos patógenos por un limitado número de receptores presentes en la superficie del epitelio; b) por inmunomodulación y/o estimulación de la respuesta inmune del tejido linfoide asociado al intestino y a las células epiteliales; c) mediante la actividad antimicrobiana y la supresión del cre0cimiento de patógenos; d) mejorando la barrera intestinal, y e) induciendo la apoptosis de células T en la mucosa intestinal71.
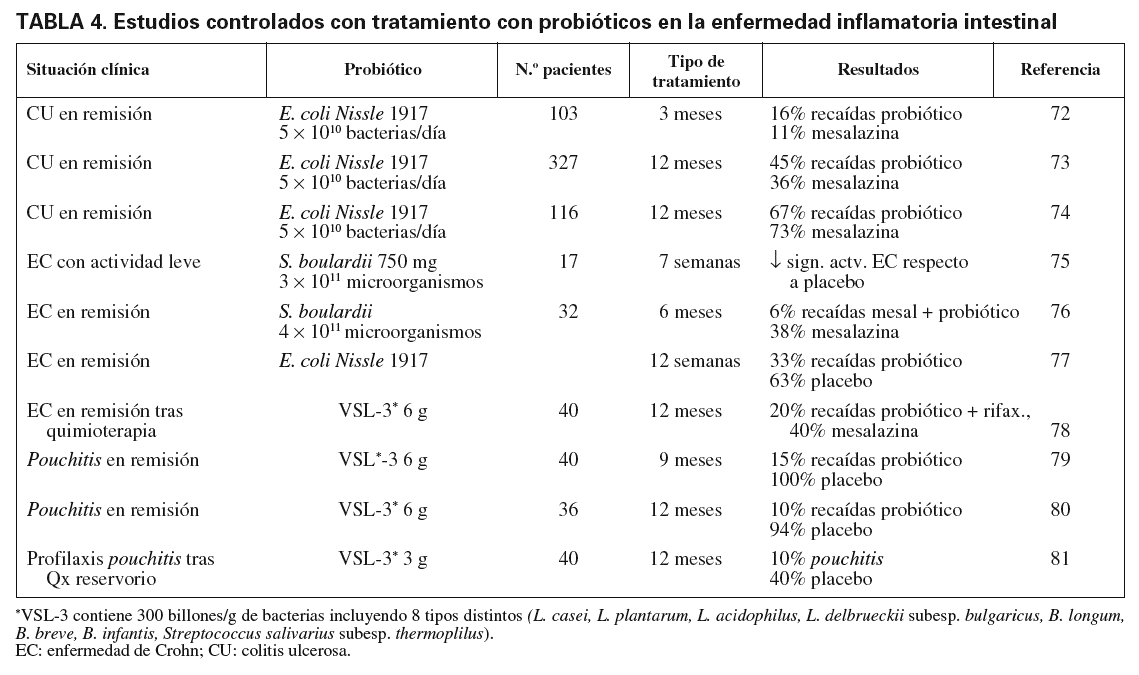
Sin embargo, no todos los probióticos tienen efectos terapéuticos similares. En pacientes con EII, de los muchos candidatos estudiados hasta el momento actual, sólo una cepa específica, Escherichia coli Nissle 1917, la levadura Saccharomyces boulardii y una mezcla de 8 bacterias diferentes (L. acidophilus, L. delbrueckii, L. plantarum, L. casei, B. infantis, B. longum, B. breve y S. salivarius) (VSL-3) han demostrado efectos terapéuticos convincentes en estudios controlados72-82. En una reciente revisión se comentan las principales áreas en que estos probióticos se han utilizado en pacientes con EII83, que se resumen en la tabla 4.
En pacientes con CU se han utilizado como tratamiento de mantenimiento tras la remisión, y se han obtenido unas tasas de recaídas muy similares a la mesalazina72-74, si bien en uno de estos estudios la tasa de recaídas fue muy elevada en ambos grupos (el 67% probiótico y el 73% mesalazina), similar a la que se encontraría con un placebo, lo que indicaría que ambos tratamientos en este estudio fueron igualmente ineficaces74.
En la EC se han hecho estudios en pacientes con enfermedad leve75, como tratamiento de mantenimiento tras la remisión76,77 y en la profilaxis de recurrencias tras la cirugía78 (tabla 4). Aunque los resultados son satisfactorios, es necesario realizar más estudios para comprobar su utilidad en este tipo de pacientes. En la actualidad está en marcha un protocolo para el estudio de los probióticos como tratamiento de mantenimiento tras la remisión en pacientes con EC por la biblioteca Cochrane84.
El área en la que los probióticos están despertando un mayor interés es el tratamiento de la pouchitis o inflamación del reservorio ileal en pacientes con anastomosis ileoanal. Este tratamiento incluye la administración de antibióticos durante la fase aguda (metronidazol, ciprofloxacino) que deberían interrumpirse posteriormente para evitar la aparición de resistencias. Los probióticos (VSL-3) se han utilizado con éxito en el mantenimiento de la remisión tras el tratamiento con antibióticos en estos pacientes79,80. Asimismo, este preparado también parece eficaz en la profilaxis de la pouchitis tras la realización de un reservorio ileoanal81.
En una revisión sistemática de la biblioteca Cochrane se concluye que la solución probiótica oral VSL-3 parece ser un tratamiento eficaz para el mantenimiento de la remisión en pacientes con pouchitis crónica tras la inducción de la remisión con antibióticos (OR = 205; IC del 95%, 9,89-4.247)85.
Con los estudios actuales se puede concluir que la utilización de probióticos en el tratamiento de mantenimiento y en la prevención de la pouchitis postoperatoria presenta un grado de recomendación A o B. En cuanto a la utilización de probióticos en el tratamiento de la CU y la EC, sólo presenta actualmente un grado de recomendación B o C.
Se necesitan más ensayos clínicos controlados para investigar algunos problemas no resueltos en relación cotante de prebióticos, simbióticos o antibióticos. zación por separado o asociando varias cepas, así como el uso concomi