El tratamiento con bomba infusora de insulina trata de mejorar el control glucémico y disminuir el riesgo de hipoglucemia en diabetes tipo 1.
ObjetivoValorar las concentraciones de glucosa intersticial y la duración y los síntomas de las hipoglucemias e hiperglucemias con el uso de un monitor continuo de glucosa en niños y adolescentes con diabetes mellitus tipo 1 tratados con infusión de insulina, así como la tolerancia de esta prueba en estos pacientes.
Pacientes y métodoSe estudia a 13 pacientes (4 varones) con diabetes mellitus tipo 1 tratados con infusor de insulina, edad 10,6±3,5 (intervalo, 3,2-13,6) años; tiempo de evolución de la diabetes mellitus, 5,0± 3,2 años; tiempo de tratamiento con bomba, 12,0±4,6 meses; dosis de insulina, 0,99±0,19U/kg/día, y último valor de glucohemoglobina, 7,1±0,8. Se utilizó el sistema CGMS de Minimed durante 72h.
ResultadosEl sensor no fue tolerado por el niño preescolar de 3 años. La concentración de glucosa intersticial captada por el sensor fue 187±40mg/dl. El tiempo en hipoglucemia (menor de 70mg/dl) fue del 3,6% ± 5,6% del total y el tiempo en hiperglucemia (mayor de 180 mg/dl) fue del 47,3% ± 17,4% del total. En ningún caso se detectaron hipoglucemias subclínicas.
ConclusionesLos niños y adolescentes con infusor de insulina muestran un perfil de glucosa intersticial muy irregular y no consiguen la normoglucemia. Nuestros pacientes conservan la sintomatología de alarma frente a la hipoglucemia y en general toleran bien el CGMS.
Insulin pump therapy aims to improve glycemic control and decrease the risk of hypoglycemia in type 1 diabetes.
ObjectiveTo evaluate interstitial glucose levels and the frequency, duration and symptoms of hypo- and hyperglycemia through the use of a continuous glucose monitoring system (GGMS) in children and adolescents with insulin pump-treated type 1 diabetes, and to determine whether this monitoring method is well tolerated by these patients.
Patients and methodThirteen patients (4 boys) with insulin pump-treated type 1 diabetes mellitus were monitored. Age was 10.6±3.5 (range, 3.2-13.6) years, diabetes duration was 5.0±3.2 years, pump therapy duration was 12.0±4.6 months, insulin dose was 0.99 ± 0.19 U/kg/day, and last hemoglobin A1c level was 7.1% ± 0.8%. The Minimed CGMS was used for 72 hours.
ResultsA 3-year-old preschool child did not tolerate the CGMS. Interstitial glucose concentration was 187±40 mg/dl. Hypoglycemia (below 70mg/dl) accounted for 3.6% ± 5.6% of total time, while hyperglycemia (above 180 mg/dl) occurred 47.3% ± 17.4% of the time. No asymptomatic hypoglycemia episodes were detected.
ConclusionsInsulin pump-treated children and adolescents showed an irregular interstitial glucose level and did not achieve normoglycemia. In our patients, adrenergic symptoms of hypoglycemia were preserved and the CGMS was generally well tolerated.
El tratamiento con infusión continua, que es el más cercano a lo fisiológico de los disponibles, trata de mejorar el control glucémico y disminuir el riesgo de hipoglucemia en diabetes mellitus tipo 1. Sin embargo, incluso en pacientes adecuadamente entrenados y motivados, no es tan eficaz como el páncreas sano.
Los resultados obtenidos con esta terapia en niños y adultos con diabetes mellitus tipo 1 se reflejan en un metaanálisis que incluye 52 estudios y 1.547 pacientes y concluye que la bomba infusora mejora muy discretamente el control glucémico (la glucohemoglobina baja en promedio un 0,4%)1. En los estudios pediátricos aleatorizados publicados posteriormente no llega a demostrarse beneficio en el control frente al tratamiento multidosis2-5. En nuestra experiencia, la única variable que mejoró significativamente tras la instauración de la bomba fue la satisfacción de los niños y sus padres con el tratamiento6.
El objetivo de nuestro estudio es valorar las concentraciones de glucosa intersticial y la duración y los síntomas de las hipoglucemias e hiperglucemias con el uso de un monitor continuo de glucosa en el espacio intersticial en niños y adolescentes con diabetes mellitus tipo 1 tratados con bomba de insulina, así como la tolerancia de estos pacientes a esta prueba.
PACIENTES Y MÉTODOSe estudia a 13 pacientes (4 varones) con diabetes mellitus tipo 1 tratados con bomba de insulina, con una media ± desviación típica de edad de 10,6 ± 3,5 (intervalo, 3,2-13,6) años; 4 de ellos prepúberes (de 3, 7, 8 y 10 años de edad). El tiempo de evolución de la diabetes mellitus era 5,0 ± 3,2 años; el tiempo de tratamiento con bomba, 12 ± 4,6 meses; la dosis de insulina, 0,99 ± 0,19 U/kg/día; el último valor de glucohemoglobina, 7,1% ± 0,8%; el valor previo al inicio del infusor fue 7,6 ± 1. Las indicaciones de la terapia con infusión fueron hipoglucemias inadvertidas en los niños prepúberes y mal control metabólico (glucohemoglobina mayor del 7,5%) en los púberes. En todos los casos realizaban previamente tratamiento multidosis con 3 dosis de insulina NPH y 3 o 4 de análogo lispro al día; eran familias muy motivadas y cumplidoras de las recomendaciones, tanto antes como después del inicio de la terapia infusora.
Para la monitorización continua de glucosa se utilizó el sistema CGMS® de Minimed, que es con el que se ha realizado la mayoría de los trabajos publicados. Fue aprobado para uso clínico por la FDA en 1999 y por la Dirección General de Farmacia de España en 2001. Estudios previos demuestran una correlación alta entre sus glucemias y las determinadas por los autoanálisis capilares, del orden de 0,91, con diferencias medias con respecto a los valores plasmáticos de entre el 12 y el 21%, que aumenta hasta el 40% en hipoglucemia7-12. Una limitación de este método es su baja reproducibilidad; según estudios en que los pacientes llevaron simultáneamente 2 sensores, hay que contar con una media de error cercana al 10%7 y con que en un 7% de las mediciones la diferencia será mayor del 50%13. La tasa de mal funcionamiento se sitúa entre el 18 y el 28%11.
El CGMS obtiene el valor medio de glucosa intersticial cada 5min, con un total de 288 mediciones al día. Este valor presenta un retraso respecto al plasmático de unos 13min. Las lecturas del sensor tienen que ser calibradas con las determinaciones capilares, y se precisan al menos 4 en 24h.
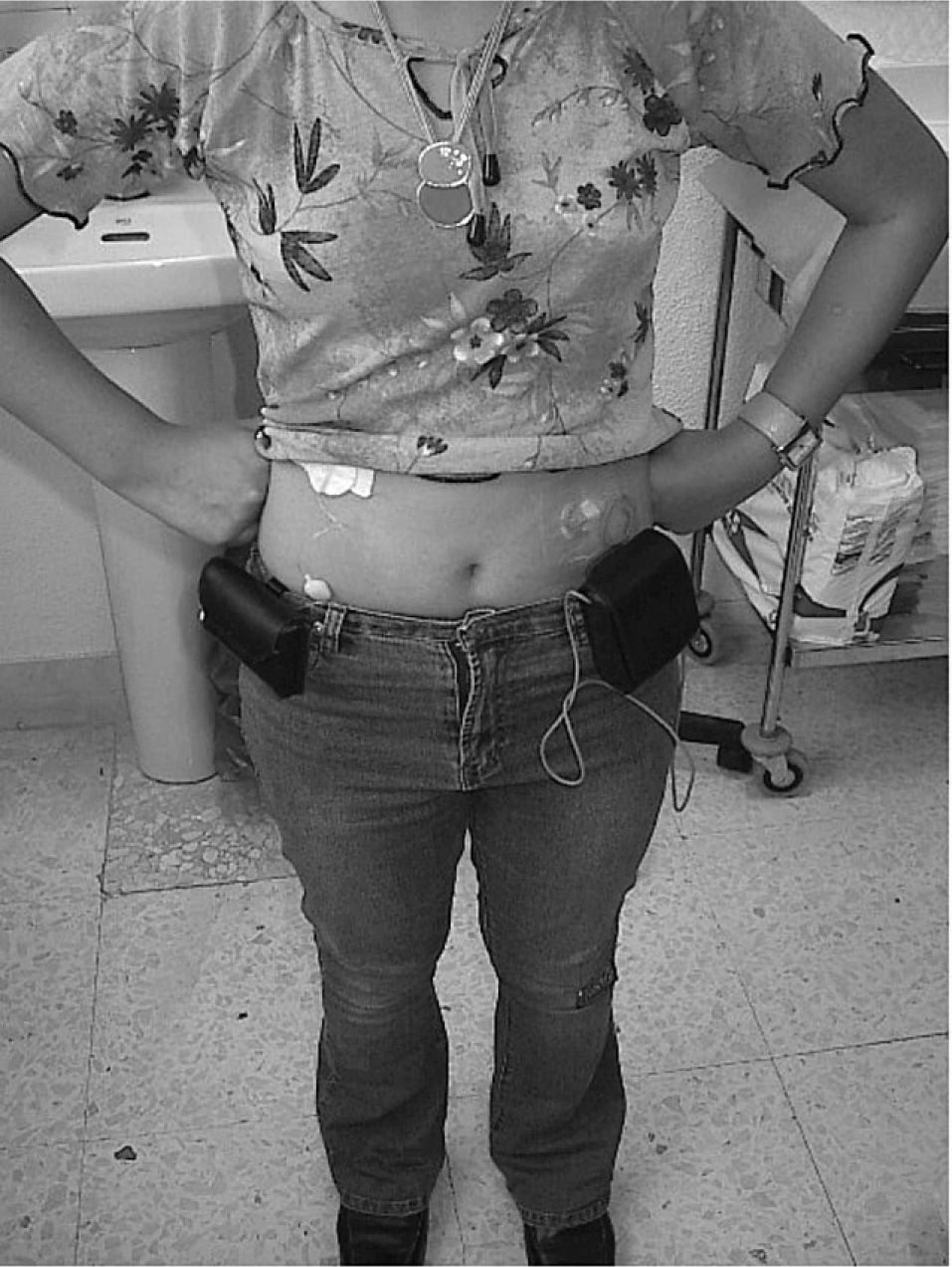
Se citó a los pacientes los miércoles a las 13.00h para insertarles el sensor, siempre a más de 10cm de la bomba de insulina (fig. 1). El mismo investigador colocó y retiró el sensor en todos los casos. Los pacientes y sus familiares eran informados sobre el manejo del monitor y se les daba un cuadernillo con horario donde debían anotar: administración de insulina, glucemia capilar, raciones de hidratos ingeridos, actividad física, síntomas y otras eventualidades. Disponían de un teléfono de 24h para consultar problemas técnicos. Se les indicó mantener la monitorización un mínimo de 72h, hasta el sábado, y que intentaran realizar todas sus actividades cotidianas, con los cambios de ritmo propios al inicio del fin de semana. Se les animó a participar proponiéndoles que la monitorización ayudaría a reajustar las dosis de insulina y mejorar así el control metabólico, a detectar hipoglucemias inadvertidas y a comprender la fisiología del metabolismo hidrocarbonado, aumentando la motivación.
El estudio cumple la normativa de Helsinki sobre estudios en humanos, y cuenta con la aprobación del Comité Ético del centro y con el consentimiento informado de los padres y los pacientes mayores de 12 años.
RESULTADOSEl sensor no fue tolerado por el preescolar de 3 años que lo dobló y se lo arrancó a las 7h de su inserción. Los niños mayores toleraron bien la prueba y completaron las 72h, aunque ninguno de ellos se prestara a repetirla en un segundo tiempo. Dos monitorizaciones debieron suspenderse por errores continuos en la calibración y fueron realizadas en otra semana.
En los 12 pacientes que completaron el estudio, la concentración de glucosa intersticial captada por el sensor fue 187 ± 40mg/dl, y el de glucemia capilar, 178 ± 23mg/dl, con un número de determinaciones glucémicas capilares de 5,5 ± 0,8. En los días de cambio de catéter las concentraciones de glucosa intersticial fueron de 166 ± 33mg/dl; en los días segundos de uso del catéter, 194 ± 59mg/dl, y en los días terceros, 214 ± 88mg/dl.
El tiempo en hipoglucemia (menor de 70mg/dl) fue el 3,6% ± 5,6% del total, lo que supone 0,7 episodios por paciente y día con una duración media de 1,2h. El 25% fue durante el sueño y el resto se relacionó directa o indirectamente con ejercicio físico. Todas las hipoglucemias captadas por el sensor se acompañaron de sintomatología y fueron reconocidas adecuadamente por los pacientes.
El tiempo en hiperglucemia (mayor de 180mg/dl) fue el 47,3% ± 17,4% del total, lo que supone 2,6 episodios por paciente y día, con una duración media de 4,3h. La mayor parte (46%) fue posprandial: un 25% fue de más de 2h de duración, atribuidas a mal cálculo de los bolos, y un 21%, picos hiperglucémicos autolimitados a la primera hora tras la ingesta interpretados como debidos a la rápida absorción de carbohidratos en relación con la acción de la insulina. Otras causas de hiperglucemia fueron los problemas de catéter (20%) (que se solucionaron al cambiarlo) y la inactividad física (sin adecuación correcta de la dosis basal) (19%).
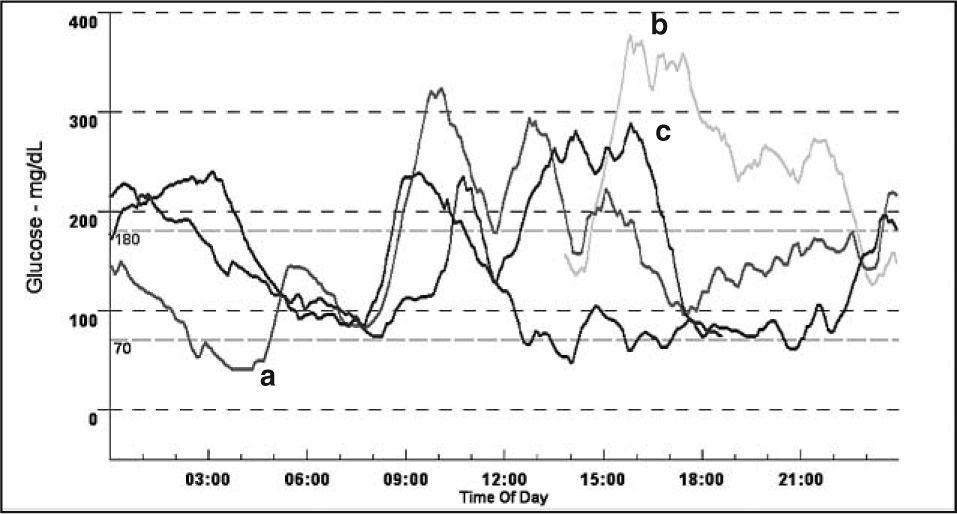
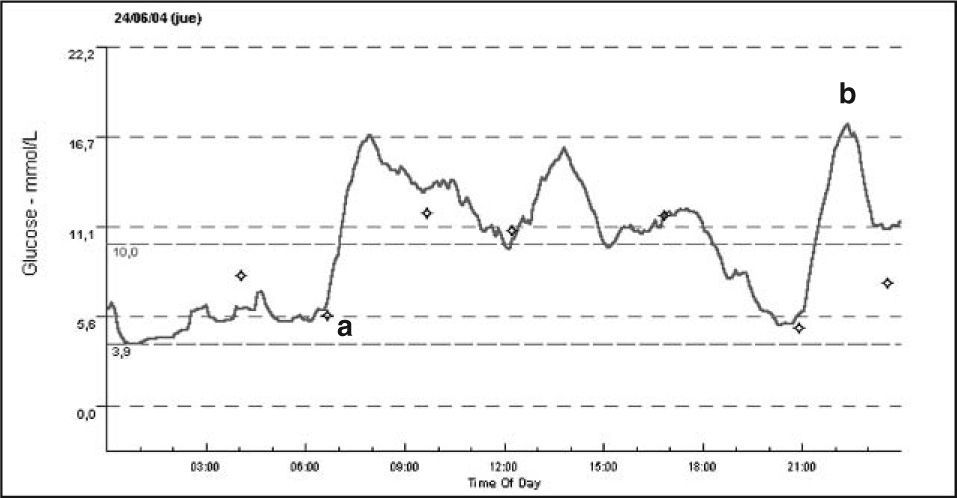
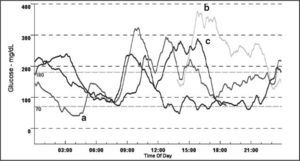
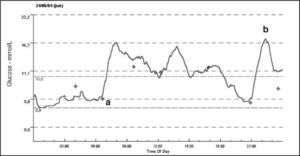
Los perfiles de glucosa intersticial fueron, en todos los casos, muy irregulares y poco reproducibles de unos días a otros, como se muestra en las figuras 2 y 3, en las que se señalan algunas hipoglucemias e hiperglucemias y su causa.
Monitorización continua de glucosa en un varón de 8 años, última glucohemoglobina, del 6,7%. Cada línea representa la glucemia de un día; llama la atención su gran irregularidad durante todo el día y de unos días a otros. Hipoglucemia sintomática a las 4 de la madrugada una noche (a). Hiperglucemia por falta de ejercicio la tarde en que inició la monitorización (b). Hiperglucemias posprandiales por ingesta de azúcares rápidos (c).
En la siguiente revisión trimestral en consulta, la concentración de glucohemoglobina era similar a la previa a la monitorización, del 7,4% ± 1,2%.
DISCUSIÓNEn niños tratados con bomba de insulina el CGMS parece ser aceptablemente tolerado. Hay referencias de su utilización primero en mayores de 8 años7 y posteriormente en preescolares de hasta 2 años, sin ningún efecto adverso14,15.
Con respecto a las concentraciones de glucosa obtenidas en la monitorización, igual que en nuestros niños, en otras series las medias son superiores al intervalo normal, con una buena correlación con las capilares15. Se ha preconizado que con bomba mejoran con respecto al tratamiento multidosis, pero en estudios que comparan con el momento previo a su instauración, esta mejoría está sesgada por la gran motivación que acompaña al inicio de una terapia16. Sin embargo, en un ensayo cruzado, aleatorizado, en que los 2 grupos de niños realizan durante 3,5 meses los 2 tratamientos, bomba y multidosis, las concentraciones de glucosa fueron similares17.
La exploración de hipoglucemias subclínicas es una aplicación interesante de esta prueba18. Se ha advertido que el sensor podría sobrestimar la frecuencia de hipoglucemias, como se ha visto al detectarlas en sujetos sanos10,19, así como su duración, pues la glucosa intersticial puede seguir baja tras la recuperación de la glucemia como consecuencia de la redistribución de glucosa a los órganos7,10,19,20. En nuestra serie estos fenómenos no han ocurrido y el escaso tiempo que los pacientes pasan en hipoglucemia apoya la utilidad de la infusión continua en su prevención.
Con respecto a las hiperglucemias, las posprandiales son las más importantes15. Esto tiene una importante implicación clínica por el papel que desempeñan en el desarrollo de complicaciones vasculares21.
La cuestión que se plantea actualmente es si la monitorización continua permitiría mejorar la glucohemoglobina a largo plazo. Los primeros estudios en niños propugnan mejorías de entre el 0,2 y el 1,5% tras las intervenciones terapéuticas guiadas por el sensor22-24, aunque es difícil separar la repercusión de un seguimiento médico más estrecho en los pacientes25. En estudios aleatorizados la mejoría es muy pequeña, del orden del 0,3%26 o ninguna27, con respecto al grupo que sólo tiene información del glucómetro.
Los niños muestran una inestabilidad glucémica independiente de la modalidad terapéutica utilizada, como demuestra un estudio que compara la monitorización con bomba y multidosis, en niños de 3 a 16 años, y obtiene similares glucemias medias, excursiones hipoglucémicas e hiperglucémicas en amplitud y número y diferencias de unos días a otros28. Incluso en un trabajo en que los niños utilizan semanalmente un monitor continuo a tiempo real durante 4 semanas y cambian su dosificación en función de su información, tampoco se consigue la normoglucemia: la glucemia media baja de 167 a 155mg/dl y el número de episodios de hipoglucemia e hiperglucemia disminuye solamente alrededor de una tercera parte de la primera a la cuarta semana29.
Podemos concluir que, a pesar de un adecuada motivación y la correcta aplicación del tratamiento, los niños y adolescentes con infusión continua de insulina muestran un perfil de glucosa intersticial muy irregular y sólo la mitad del tiempo consiguen la normoglucemia. Esta realidad deben conocerla los pacientes candidatos a esta terapia y sus familias para evitar falsas expectativas. Por otra parte, nuestros niños conservan la sintomatología de alarma ante la hipoglucemia y, en general, toleran bien la monitorización continua de glucosa.