Evaluar si el tratamiento con levotiroxina mejora la capacidad funcional en pacientes con insuficiencia cardíaca crónica clase funcional i-iii de la New York Heart Association e hipotiroidismo subclínico.
MétodosSe incluyeron 163 pacientes ambulatorios con insuficiencia cardíaca crónica estable y con un mínimo de seguimiento de 6 meses. Se realizó un examen clínico y se solicitaron pruebas de laboratorio que incluyeron hormonas tiroideas, ecocardiograma con doppler, ventriculografía radioisotópica y un estudio Holter. La capacidad funcional se evaluó por medio de una caminata de 6min. Se detectaron los pacientes con hipotiroidismo subclínico que recibieron tratamiento sustitutivo y, una vez con valores normales de tirotropina (TSH), se les realizó una nueva caminata de 6min. Se registraron los metros recorridos en cada prueba y se analizó la diferencia de los metros caminados en cada paciente.
ResultadosObservamos una prevalencia de hipotiroidismo subclínico del 13% en pacientes con insuficiencia cardíaca. Mientras se encontraban hipotiroideos, los metros recorridos fueron de 292±63, y una vez alcanzados valores normales de TSH, de 350±76. La diferencia en metros fue de 58±11 (p<0,011). Los pacientes con valores normales de TSH no mostraron diferencias significativas entre las 2 pruebas.
ConclusionesLos pacientes con insuficiencia cardíaca crónica e hipotiroidismo subclínico, una vez eutiroideos, mejoraron de forma significativa su rendimiento físico.
To assess whether levothyroxine treatment improves functional capacity in patients with chronic heart failure (New York Heart Association class i-iii) and subclinical hypothyroidism.
MethodsOne hundred and sixty-three outpatients with stable chronic heart failure followed up for at least 6 months were enrolled. A physical examination was performed, and laboratory tests including thyroid hormone levels, Doppler echocardiogram, radionuclide ventriculography, and Holter monitoring were requested. Functional capacity was assessed by of the 6-min walk test. Patients with subclinical hypothyroidism were detected and, after undergoing the s6-min walk test, were given replacement therapy. When they reached normal thyrotropin (TSH) levels, the 6-min walk test was performed again. The distance walked in both tests was recorded, and the difference in meters covered by each patient was analyzed.
ResultsPrevalence of subclinical hypothyroidism in patients with heart failure was 13%. These patients walked 292±63m while they were hypothyroid and 350±76m when TSH levels returned to normal, a difference of 58±11m (P<.011). Patients with normal baseline TSH levels showed no significant difference between the 2 6-min walk tests.
ConclusionsPatients with chronic heart failure and subclinical hypothyroidism significantly improved their physical performance when normal TSH levels were reached.
El síndrome de insuficiencia cardíaca (IC) es altamente complejo y se inicia con una alteración de la función ventricular, diastólica y/o sistólica, pero posteriormente genera e involucra alteraciones bioquímicas, metabólicas, hormonales y neurohormonales1. Se reconoce la relación existente entre las hormonas tiroideas, el corazón y el sistema vascular periférico; las hormonas tiroideas tienen acciones relevantes sobre el corazón y la circulación, generan múltiples cambios incluyendo alteraciones hemodinámicas y efectos mediados sobre las células cardíacas a través de la expresión génica2–4.
El hipotiroidismo subclínico (HS) es una alteración bioquímica frecuente, definida por elevación de la tirotropina (TSH) con niveles circulantes de hormonas tiroideas normales para el rango de referencia5. No existe aún un consenso a nivel internacional para establecer el punto de corte a partir del cual considerar como patológico el valor de TSH. En el registro National Health and Nutrition Examination Survey III se evaluó una muestra de individuos aparentemente sanos y eutiroideos, con anticuerpos antitiroideos negativos. En esta población, la mediana de concentración de TSH fue de 1,39μUI/l, con un rango de referencia para el 95% de las muestras entre 0,45 y 4,12μUI/l6. Estos valores se han tomado como referencia para establecer el punto de corte de normalidad de la TSH en un consenso sobre el diagnóstico y tratamiento del HS7. Sin embargo, la Academia Nacional de Bioquímica Clínica de los Estados Unidos ha sugerido como límites de referencia normales los valores que oscilan entre 0,4 y 2,5μUI/l5, mientras que la Asociación Americana de Endocrinólogos Clínicos estableció dichos valores entre 0,3 y 3,0μUI/l8.
La prevalencia de HS en la población general es del 1 al 11%, alcanzando el 20% en las mujeres mayores de 60 años6,9–12. Aún resta por determinar la relevancia clínica del HS; estos pacientes presentan un aumento en los niveles de lipoproteína de baja densidad, de prevalencia de afección coronaria y de enfermedad arterial periférica13,14. Las alteraciones tiroideas en la IC se asocian con una peor clase funcional y una función ventricular más deteriorada. Por ello, además de los métodos convencionales, podría ser útil evaluar la función tiroidea, ya sea para la evolución o el pronóstico de los pacientes con IC15. Por estos motivos, parecería recomendable el uso de tratamiento sustitutivo hormonal en pacientes con HS y, a su vez, la determinación periódica del perfil tiroideo en la IC aportaría valiosa información para su estratificación pronóstica.
Dado que existen controversias sobre qué hacer con este tipo de pacientes en cuanto al tratamiento sustitutivo, el objetivo del presente estudio fue evaluar si en el subgrupo de pacientes con IC e HS la corrección del perfil hormonal se traduce en una mejoría de la capacidad funcional medida a través de una caminata de 6min.
Material y métodosEstudio de intervención, prospectivo, abierto y de individuo como propio control, que incluyó a pacientes ambulatorios consecutivos de 2 centros. Después de aceptar su intervención en el estudio y cumplidos los requisitos para estudios clínicos del Departamento de Investigación y Docencia del Hospital Militar Central, que incluyó la firma de un consentimiento informado, se incluyeron los pacientes con IC, quienes debían completar un mínimo de 6 meses de seguimiento, encontrarse estables por lo menos durante un mes y recibir dosis óptimas –o las máximas toleradas– de inhibidores de la enzima convertidora de la angiotensina ii o antagonistas del receptor 1 de la angiotensina ii, betabloqueantes y espironolactona.
Los criterios para ser incluidos en el estudio fueron: edad>21 años, diámetro diastólico del ventrículo izquierdo>55mm y fracción de eyección<35%. Los criterios de exclusión fueron: pacientes con indicación de cirugía por cualquier causa, miocardiopatías de origen valvular e hipertrófica, aquellos bajo tratamiento con amiodarona, los que presentaban arritmia ventricular compleja, los que tenían antecedentes de muerte súbita y/o síncope de probable origen arrítmico, los portadores de cardiodesfibrilador implantable, y aquellos con incapacidad motora para realizar la caminata de 6min.
Se sometió a cada participante a un examen clínico y se le realizó: electrocardiograma, ecocardiograma bidimensional con doppler, ventriculografía radioisotópica, un estudio Holter de 24h, y a los pacientes con etiología isquémica, un estudio de perfusión miocárdica. Además, se solicitó analítica de sangre que incluyó la determinación de TSH, triyodotironina y tiroxina libre realizada por inmunoanálisis de electroquimioluminiscencia, siendo los intervalos de referencia para TSH de 0,27-4,2μUI/l, para triyodotironina de 0,8-2,0ng/ml y para tiroxina libre de 0,7-1,7ng/dl.
Se definió el HS como la elevación de la TSH en 2 determinaciones consecutivas de laboratorio con valores por encima del percentil 95 según el registro National Health and Nutrition Examination Survey III (4,12μUI/l), con niveles circulantes de hormonas tiroideas dentro de los valores normales. La capacidad funcional se evaluó con la prueba de caminata de 6min. Una vez incluidos se detectó a los pacientes con HS, que fue confirmado con una segunda determinación bioquímica a los 2 meses. Se realizó la primera caminata de 6min a todos los pacientes. Tras reposo de 15min, un mismo operador determinó la presión arterial en posición de sedestación con esfigmógrafo calibrado y la frecuencia cardíaca. Posteriormente, se les indicó que caminaran durante 6min a la mayor velocidad posible en un pasillo de 30m. Una vez finalizada, se controlaron las mismas variables.
Los pacientes con IC e HS fueron remitidos al Servicio de Endocrinología y evaluados por un endocrinólogo, quien indicó el tratamiento sustitutivo del HS. A los pacientes sin HS se los citó para una segunda caminata de 6min a los 30 días de la primera, y a los que fueron medicados para su HS se les programó la segunda prueba 30 días después de haberse corroborado que estuvieran con valores de TSH normalizados. Se registraron los metros recorridos en cada una de las pruebas y se analizó la diferencia de los metros caminados en cada paciente. Como medida de seguridad, a todos los participantes del grupo con HS se les solicitó un nuevo Holter de 24h a los 30 días de estar recibiendo el tratamiento hormonal sustitutivo.
Análisis estadísticoLas variables continuas paramétricas se expresaron como media±desviación estándar o como mediana±intervalo intercuartílico, y las no paramétricas como razones o porcentajes, según el caso.
Para las variables continuas, tras comprobar la normalidad de las distribuciones muestrales mediante la prueba de Shapiro-Wilk, y, eventualmente, procurar la normalización mediante las transformaciones correspondientes (transformación logarítmica), las comparaciones intragrupo se realizaron mediante la prueba t de Student para datos apareados y las comparaciones entre grupos mediante la prueba t de Student para muestras paralelas. En el caso de distribuciones claramente no normales se recurrió a métodos no paramétricos para su análisis estadístico inferencial (test de proporciones).
Se consideró indicativo de significación estadística un valor de p, bilateral, igual o menor de 0,05. De acuerdo con los datos muestrales del laboratorio, el número de pacientes a incluir para detectar una variación con el tratamiento igual o mayor al 20% de los valores de referencia de la caminata, con un error alfa<0,05 y un poder≥90%, se calculó en 20 individuos.
ResultadosLa población total del grupo con IC estuvo formada por 163 pacientes y se observó una prevalencia de HS del 13% (IC 95% 7,8-18,2%).
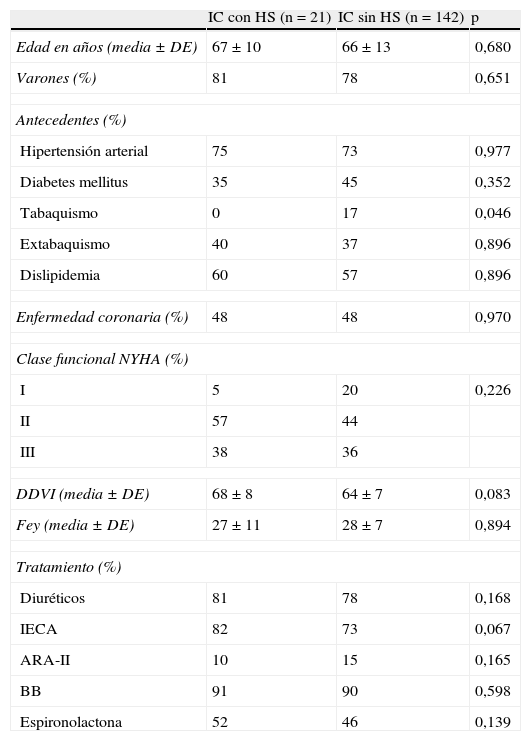
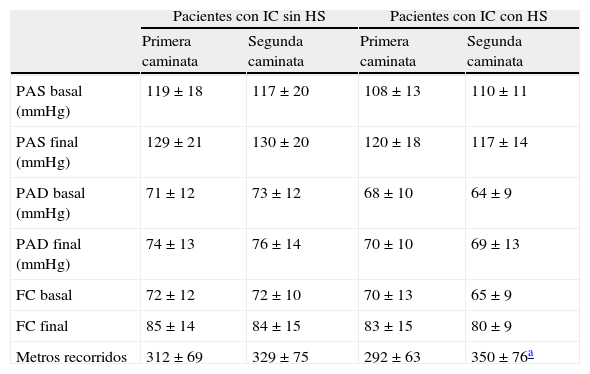
Las características de los subgrupos de IC sin HS (n=142) y con HS (n=21) pueden observarse en la tabla 1. Como puede apreciarse en la tabla 2, no hubo diferencias significativas en la frecuencia cardíaca, la presión arterial sistólica ni la presión arterial diastólica entre la primera la y segunda caminata, en ninguno de los 2 grupos. Dichas variables tampoco difirieron de forma significativa entre ambos grupos en cada una de las caminatas. En el grupo con HS se observó un aumento significativo en los metros caminados en la segunda prueba (58m; p<0,011), mientras que el grupo sin HS experimentó un aumento menor de un tercio, no significativo, en la distancia recorrida (17m; p=0,20).
Características clínicas de los pacientes con insuficiencia cardíaca con y sin hipotiroidismo subclínico
| IC con HS (n=21) | IC sin HS (n=142) | p | |
| Edad en años (media±DE) | 67±10 | 66±13 | 0,680 |
| Varones (%) | 81 | 78 | 0,651 |
| Antecedentes (%) | |||
| Hipertensión arterial | 75 | 73 | 0,977 |
| Diabetes mellitus | 35 | 45 | 0,352 |
| Tabaquismo | 0 | 17 | 0,046 |
| Extabaquismo | 40 | 37 | 0,896 |
| Dislipidemia | 60 | 57 | 0,896 |
| Enfermedad coronaria (%) | 48 | 48 | 0,970 |
| Clase funcional NYHA (%) | |||
| I | 5 | 20 | 0,226 |
| II | 57 | 44 | |
| III | 38 | 36 | |
| DDVI (media±DE) | 68±8 | 64±7 | 0,083 |
| Fey (media±DE) | 27±11 | 28±7 | 0,894 |
| Tratamiento (%) | |||
| Diuréticos | 81 | 78 | 0,168 |
| IECA | 82 | 73 | 0,067 |
| ARA-II | 10 | 15 | 0,165 |
| BB | 91 | 90 | 0,598 |
| Espironolactona | 52 | 46 | 0,139 |
ARA II: antagonistas del receptor AT1 de la angiotensina ii; BB: betabloqueantes; DDVI: diámetro diastólico ventricular izquierdo; DE: desviación estándar; Fey: fracción de eyección; HS: hipotiroidismo subclínico; IC: insuficiencia cardíaca; IECA: inhibidores de la enzima convertidora de la angiotensina ii; NYHA: New York Heart Association.
Características de las variables analizadas en los 2 grupos en ambas caminatas de 6 minutos
| Pacientes con IC sin HS | Pacientes con IC con HS | |||
| Primera caminata | Segunda caminata | Primera caminata | Segunda caminata | |
| PAS basal (mmHg) | 119±18 | 117±20 | 108±13 | 110±11 |
| PAS final (mmHg) | 129±21 | 130±20 | 120±18 | 117±14 |
| PAD basal (mmHg) | 71±12 | 73±12 | 68±10 | 64±9 |
| PAD final (mmHg) | 74±13 | 76±14 | 70±10 | 69±13 |
| FC basal | 72±12 | 72±10 | 70±13 | 65±9 |
| FC final | 85±14 | 84±15 | 83±15 | 80±9 |
| Metros recorridos | 312±69 | 329±75 | 292±63 | 350±76a |
FC: frecuencia cardíaca; HS: hipotiroidismo subclínico; IC: insuficiencia cardíaca; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
La mediana de TSH inicial en el subgrupo con HS (21 pacientes) fue de 6,25μUI/l (5,12-14,46), y tras el tratamiento con levotiroxina, de 2,53μUI/l (2,03-3,69) (p<0,0001). La mediana de tiempo que necesitaron los pacientes con HS para normalizar los valores de TSH fue de 36 días (mínimo 28 días, máximo 45 días); en este grupo, la segunda caminata se realizó con una mediana de 43 días (mínimo 35 días, máximo 52 días), la dosis media de levotiroxina utilizada fue de 86,90±32,22mcg/día (mediana de 75mcg/día, rango intercuartílico de 75-100) y no se observaron efectos colaterales de la terapia sustitutiva.
DiscusiónLas alteraciones de la función tiroidea son muy frecuentes en los pacientes con IC. El interés por el rol de las hormonas tiroideas en la IC ha aumentado nuevamente en los últimos años debido al conocimiento de sus efectos sobre la contractilidad y relajación del corazón, por hallazgos experimentales que apoyan sólidamente la hipótesis de que las funciones de las hormonas tiroideas son importantes en la preservación de la anatomía y función cardíaca bajo condiciones fisiológicas y de anormalidad, y, por último, a la evidencia de que mínimas alteraciones en la función de las hormonas tiroideas están asociadas a un peor pronóstico evolutivo16–20. Es frecuente ver en la práctica diaria una cantidad importante de pacientes con IC que a su vez presentan HS, por este motivo, la idea de nuestro trabajo fue ver qué sucedía en estos pacientes en relación con la capacidad funcional si la alteración bioquímica era corregida, y no se decidió una dosis estándar de levotiroxina ya que el objetivo era el eutiroidismo independientemente de la dosis. Observamos que el tratamiento con levotiroxina en los pacientes con IC e HS aumenta significativamente la capacidad funcional medida en metros a través de una caminata de 6min al compararlo con un grupo de pacientes con IC sin HS. Si bien es posible esperar una mejoría en el rendimiento cuando una prueba se realiza más de una vez –por la familiarización del paciente con la misma–, como se puede observar en la tabla 2 el aumento en el grupo con IC y sin HS fue menor de un tercio del experimentado por los pacientes con IC e HS (17 vs. 58m). La reducción de la resistencia vascular sistémica observada por la administración de hormona tiroidea podría ser útil para poder mejorar la función cardíaca sin generar costo en el consumo de oxígeno, ya que actúa disminuyendo la poscarga por un efecto vasodilatador. Además, esta reducción de la resistencia vascular sistémica disminuye la presión arterial diastólica, aumentando así el volumen minuto. Este incremento del volumen minuto sostiene un aumento del índice metabólico basal y del consumo de oxígeno, el cual incrementa la liberación de este a la periferia. Estos hallazgos podrían explicarse por la redistribución del flujo sanguíneo a los músculos esqueléticos a través de la vasodilatación, o por la mejoría del metabolismo muscular por acción local de la T4, la cual estimula la síntesis proteica, las enzimas mitocondriales y el intercambio de fibras rápidas a fibras lentas, situación similar a la que ocurre con el entrenamiento físico12,21.
Varios estudios han investigado el impacto del HS en pacientes con IC. Sin embargo, los resultados muchas veces han sido contradictorios; por ejemplo, Rodondi et al. presentaron un seguimiento a 4 años de pacientes con HS y observaron que a partir del valor de 7μUI/l hubo un aumento de los eventos asociados con IC comparado con los participantes eutiroideos22. Silva-Tinoco et al., en un estudio prospectivo que incluyó pacientes con IC eutiroideos que luego desarrollaron HS, observaron un mal pronóstico y un incremento de las hospitalizaciones comparados con los que persistieron eutiroideos23. Por el contrario, Frey et al. recientemente mostraron en una cohorte con seguimiento promedio de 3 años que el HS no implica peor pronóstico evolutivo ni mayor riesgo de mortalidad24.
En relación con el tratamiento sustitutivo con hormonas tiroideas en la IC, el tema ha sido evaluado en estudios con reducido tamaño muestral, pero hay un fuerte argumento en favor del tratamiento debido a que los defectos en la expresión genética de los pacientes con IC son similares a los encontrados en los pacientes con hipotiroidismo, siendo estas alteraciones reversibles con el tratamiento sustitutivo21,25–29.
Se ha postulado que las alteraciones tiroideas son un mecanismo de adaptación o de mala adaptación al incremento del catabolismo que existe en los pacientes con IC avanzada, pero se desconoce hasta la actualidad el papel del HS. Independientemente de las consideraciones en cuanto a que pueda ser un mecanismo adaptativo o mal adaptativo o eventualmente una comorbilidad, lo que está claro es que el porcentaje de pacientes con HS no es despreciable, y si bien por definición es una alteración bioquímica asintomática, en la práctica diaria se observa que esto no es así y, según la literatura, entre un 25 y un 50% de los pacientes con HS presentan algún síntoma explicado por este trastorno.
En el presente estudio se observó una prevalencia de HS del 13% (IC 95% 7,8-18,2%), con una mediana de TSH de 6,25μUI/l, en una población mayoritariamente masculina, y si bien es cierto que el método utilizado en el trabajo no es el ideal para evaluar la respuesta al tratamiento con levotiroxina, se observa una mejoría en los metros caminados una vez eutiroideos. Observamos que si existe un buen control de los pacientes, el tratamiento sustitutivo no se asocia con efectos colaterales relevantes; además, el mismo se asoció con una mejoría significativa en la capacidad funcional. Por ello, creemos conveniente incorporar la determinación de hormonas tiroideas de forma rutinaria en este grupo de pacientes.
El presente estudio muestra algunas limitaciones. Si bien la muestra es pequeña, el porcentaje de pacientes con HS es acorde con anteriores publicaciones. El diseño del trabajo, al no ser aleatorizado, no es el ideal para evaluar la respuesta al tratamiento. Se decidió llevar a cabo el estudio mediante el diseño de individuo como propio control ya que la realización de este tipo de estudio requiere de una población menor, y como el reclutamiento de pacientes se realizaría solo en 2 centros y en un plazo estipulado no mayor a 2 años, intuimos que sería el diseño más propicio para concretar los objetivos del estudio. La naturaleza abierta del estudio puede dificultar su conducción, pero son riesgos que hemos debido asumir para aprovechar el relativo número limitado de casos y no privar del tratamiento a algunos enfermos.
La caminata de 6min es un método controvertido dado que algunos de los trabajos que la han utilizado, así como los resultados de la misma, han sido heterogéneos en cuanto a las características de las poblaciones estudiadas, el tratamiento en curso y la técnica utilizada en la realización de la prueba; a pesar de esto, en la Sección de Insuficiencia Cardíaca de nuestro hospital, la utilizamos desde hace más de 15 años como un método complementario de rutina para pacientes con IC. La caminata de 6min es un método fácilmente realizable, seguro y de bajo costo. La subjetividad de la prueba se puede minimizar cuando la misma es realizada por el mismo operador y estimulando al paciente mientras la realiza, lo cual la hace bastante confiable; así, numerosos estudios previos y de grandes dimensiones la han utilizado como método para evaluar la capacidad funcional de este tipo de pacientes y, en muchos de ellos, se ha correlacionado mejor que con la ergometría con consumo de oxígeno, respecto de la aparición de eventos futuros30.
Concluimos que los pacientes con IC que presentaban HS, una vez tratados con levotiroxina mejoraron de forma significativa su rendimiento físico medido mediante una caminata de 6min, lo cual justificaría el cribado rutinario de hormonas tiroideas, especialmente si este grupo de pacientes tratados de forma óptima no mejora su capacidad funcional.
Conflicto de interesesLos autores declaran no tener ningún conflicto de interés.
Los autores agradecen especialmente a las Sras. Eleonora Vanasco y Alicia Aubry la corrección del manuscrito.