Desde el primer artículo en el año 2006 de Epstein1, varias publicaciones han puesto de relieve la relación entre el tratamiento prolongado con inhibidores de la bomba de protones (IBP) y la existencia de hipomagnesemia. Aunque el número de casos descrito hasta la actualidad es muy pequeño, podría tratarse de un efecto adverso más frecuente de lo esperado teniendo en cuenta el gran número de personas que reciben este tratamiento. Presentamos el caso de un paciente con hipomagnesemia refractaria al tratamiento con suplementos orales que ha revertido tras la retirada del tratamiento con omeprazol.
Paciente de 65 años ingresado después de sufrir un episodio de convulsiones tónico-clónicas generalizadas. Entre sus antecedentes personales destaca: HTA en tratamiento con doxazosina y valsartan/hidroclorotiazida, epilepsia focal criptogenética diagnosticada en 2005 tratada con levetirazetam y flutter auricular (anticoagulado con warfarina). Reflujo gastroesofágico en tratamiento con 20mg de omeprazol desde hace 20 años.
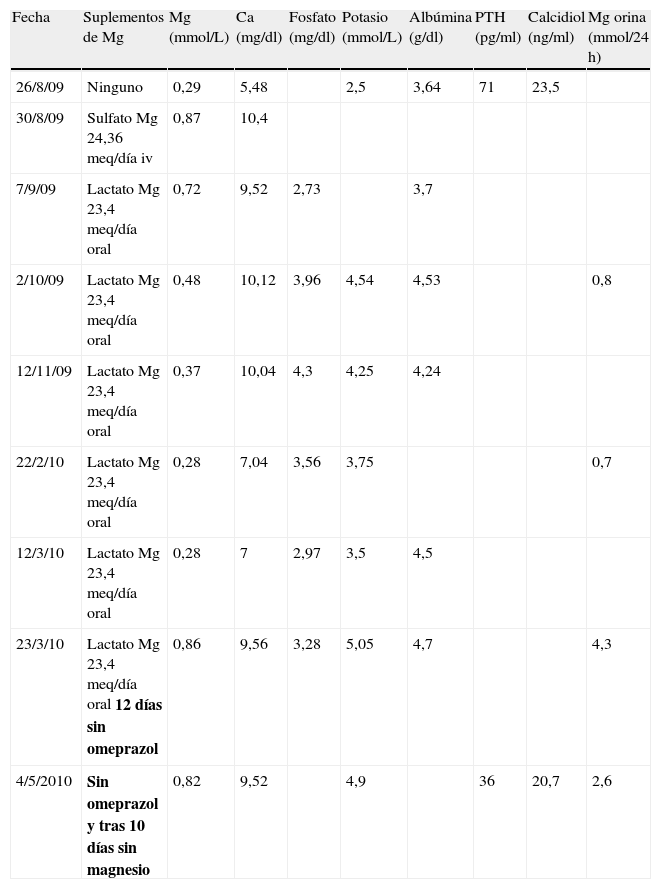
Al ingreso se le detectaron niveles plasmáticos muy disminuidos de calcio, magnesio y potasio, por lo que se inició tratamiento con suplementos de magnesio por vía endovenosa y posteriormente por vía oral. Los 3 primeros días también recibió suplementos de calcio y potasio. Los niveles de magnesio se normalizaron con el aporte endovenoso, pero posteriormente fueron disminuyendo progresivamente hasta llegar a niveles plasmáticos similares a los iniciales a pesar de un elevado aporte oral (tabla 1). Se evaluaron las pérdidas urinarias de magnesio objetivando valores muy bajos, lo que sugería que la hipomagnesemia guardaba relación con un defecto en la absorción. El paciente refería una ingesta equilibrada, no consumía etanol ni laxantes. Se descartó enfermedad celíaca e insuficiencia pancreática. Se intentó sustituir el lactato magnésico por pidolato pero se retiró por intolerancia. También se suspendió el tratamiento con hidroclorotiazida sin que presentara mejoría analítica. Después de revisar la literatura se decidió suspender el tratamiento con omeprazol y sustituirlo por ranitidina, objetivándose la normalización de los niveles de calcio y magnesio en el plazo de 12 días. Posteriormente se han retirado los suplementos orales y el paciente mantiene el magnesio plasmático dentro de la normalidad.
Evolución de los parámetros analíticos
| Fecha | Suplementos de Mg | Mg (mmol/L) | Ca (mg/dl) | Fosfato (mg/dl) | Potasio (mmol/L) | Albúmina (g/dl) | PTH (pg/ml) | Calcidiol (ng/ml) | Mg orina (mmol/24 h) |
| 26/8/09 | Ninguno | 0,29 | 5,48 | 2,5 | 3,64 | 71 | 23,5 | ||
| 30/8/09 | Sulfato Mg 24,36 meq/día iv | 0,87 | 10,4 | ||||||
| 7/9/09 | Lactato Mg 23,4 meq/día oral | 0,72 | 9,52 | 2,73 | 3,7 | ||||
| 2/10/09 | Lactato Mg 23,4 meq/día oral | 0,48 | 10,12 | 3,96 | 4,54 | 4,53 | 0,8 | ||
| 12/11/09 | Lactato Mg 23,4 meq/día oral | 0,37 | 10,04 | 4,3 | 4,25 | 4,24 | |||
| 22/2/10 | Lactato Mg 23,4 meq/día oral | 0,28 | 7,04 | 3,56 | 3,75 | 0,7 | |||
| 12/3/10 | Lactato Mg 23,4 meq/día oral | 0,28 | 7 | 2,97 | 3,5 | 4,5 | |||
| 23/3/10 | Lactato Mg 23,4 meq/día oral 12 días sin omeprazol | 0,86 | 9,56 | 3,28 | 5,05 | 4,7 | 4,3 | ||
| 4/5/2010 | Sin omeprazol y tras 10 días sin magnesio | 0,82 | 9,52 | 4,9 | 36 | 20,7 | 2,6 |
Revisando el historial del paciente no hemos podido encontrar ninguna determinación de calcio ni de magnesio previa al ingreso referido, por tanto, desconocemos el momento en el que ha comenzado a presentar estas alteraciones.
ComentarioEl magnesio es el cuarto catión más abundante en el organismo y el segundo en el medio intracelular. El 99% del magnesio corporal se encuentra en el espacio intracelular, principalmente en el tejido óseo (60%) seguido por el músculo esquelético (20%). El magnesio extracelular supone únicamente un 1% del total y circula en el plasma principalmente de forma libre (60%) con un 30% unido a proteínas plasmáticas y un 10% en forma de sales minerales.
Los niveles plasmáticos de magnesio se mantienen en condiciones normales entre 0,66 y 1,05mmol/l y están influenciados por el balance entre la absorción intestinal y la excreción renal.
La absorción del magnesio se produce fundamentalmente en el yeyuno proximal y en el ileon. En una dieta promedio se ingieren unos 360mg diarios de los cuales solo se absorbe un 50%. Además, en el intestino delgado se secretan diariamente hacia la luz intestinal 40mg de magnesio de los cuales 20mg son reabsorbidos en el colon y en el recto2. La absorción de magnesio en el tubo digestivo se produce a través de 2 mecanismos diferenciados. El primero y principal es un proceso activo y saturable que se realiza a través del canal de magnesio Transient Receptor Potential Melastatin 6 (TRPM6)3. Este receptor también se encuentra en el túbulo distal renal favoreciendo la reabsorción del magnesio que no ha sido asimilado en el asa de Henle. El 90% de la absorción intestinal se produce por esta vía. El segundo mecanismo es pasivo y no saturable y se realiza a través de la ruta paracelular. El 80% del magnesio plasmático es filtrado por el glomérulo del cual el 95% es reabsorbido por la nefrona (60-70% en asa de Henle, 15-25% en túbulo proximal y 5-10% en túbulo distal).
En la tabla 2 se enumeran las diferentes causas de hipomagnesemia; generalmente el diagnóstico diferencial suele ser sencillo ya que la mayoría de estos procesos son fácilmente reconocibles.
Causas de hipomagnesemia
| • Causas de hipomagnesemia |
| –Disminución de ingesta |
| • Desnutrición |
| • Alcoholismo |
| • Nutrición parenteral prolongada |
| –Redistribución |
| • Síndrome de hueso hambriento |
| • Síndrome de realimentación |
| • Tratamiento de la cetoacidosis diabética |
| –Pérdidas gastrointestinales |
| • Diarrea |
| • Resecciones intestinales |
| • Hipomagnesemia con hipocalcemia secundaria (HHS): mutación gen TRPM6 |
| –Pérdidas renales |
| • Varias alteraciones tubulares (Gitelman, Bartter III) |
| • Fármacos (diuréticos) |
Desde el año 2006 varias publicaciones han descrito casos aislados o pequeñas series de pacientes con hipomagnesemia severa refractaria al tratamiento oral en relación con el uso prolongado de IBP4–9. En total se han publicado 14 casos, lo que supone una incidencia muy baja si se tiene en cuenta la amplia utilización de estos fármacos en la población. No obstante, podríamos estar únicamente detectando un pequeño porcentaje ya que no se suele medir el magnesio plasmático de forma rutinaria y la sintomatología que presentan los pacientes puede ser poco florida.
El mecanismo por el que se produce esta alteración no ha sido dilucidado, no obstante, parece claro que se trata de un defecto de absorción, ya que la excreción urinaria de magnesio está disminuida en la práctica totalidad de los pacientes. Un dato común en la mayoría de los casos es el uso previo prolongado durante años de los IBP lo que sugiere que debe existir una depleción crónica de los depósitos corporales antes de la aparición del cuadro clínico. Otros fármacos capaces de producir hipomagnesemia lo hacen a través de un aumento de la excreción urinaria de magnesio.
Cundy y Dissanayake4 sugieren que existe un fallo en el mecanismo activo de absorción permaneciendo indemne el sistema pasivo no saturable, ya que describen una corrección parcial con dosis muy elevadas de suplementos de magnesio por vía oral. Estos autores además llevaron a cabo un test de infusión de magnesio por vía venosa a 2 pacientes demostrando que, por un lado, existe una depleción severa de magnesio y que, por otro lado, la excreción urinaria se mantiene extremadamente baja hasta que los niveles plasmáticos superan un nivel de 1,0mmol/l, reforzando la tesis de que existe un defecto de absorción con mecanismos compensatorios renales.
Puesto que la hipomagnesemia asociada a los IBP es un efecto no muy frecuentemente descrito hasta la actualidad, se cree que puede existir una susceptibilidad genética para desarrollar esta complicación y se plantea que mutaciones del gen TRPM6 pueden estar implicadas en la patogénesis sin que se haya publicado nada a este respecto.
Probablemente se trata de un efecto clase, ya que se ha descrito no solo con omeprazol sino también con esomeprazol, pantoprazol y lansoprazol7, mientras que el uso de ranitidina no se asocia con este fenómeno.
En estudios previos no se había observado ningún efecto de los IBP sobre la absorción de magnesio a corto plazo10. Esto puede estar relacionado con la necesidad de tratamientos prolongados para presentar estas alteraciones o con la escasa probabilidad de que aparezca este fenómeno. El problema en nuestro paciente no llegó a ser evidente hasta que transcurrieron 15 años de tratamiento con omeprazol.
Este defecto es claramente reversible y los niveles de magnesio vuelven a la normalidad unos días después de la retirada de los IBP, como ocurre en nuestro caso.
En resumen, los IBP pueden producir hipomagnesemia refractaria a la suplementación oral. En el diagnóstico diferencial de la hipomagnesemia debe tomarse en consideración este hecho sobre todo cuando no existen otras causas aparentes que la produzcan.