La ginecomastia se define como una proliferación benigna del tejido mamario en el varón y aparece como resultado de un disbalance entre la actividad estrogénica y la androgénica1. Puede deberse a una disminución en la producción de andrógenos, un aumento en la de estrógenos o a un aumento de la conversión periférica de precursores androgénicos. El bloqueo de receptores androgénicos y la unión aumentada de andrógenos a su proteína transportadora (SHBG) son otros posibles mecanismos2.
Entre sus causas menos frecuentes se encuentran los tumores testiculares, responsables aproximadamente del 2% de los casos de ginecomastia3. Se presenta un caso de ginecomastia secundaria a producción de gonadotropina coriónica (HCG) por un tumor testicular de células germinales.
Paciente varón de 27 años sin antecedentes de interés salvo fumador de 10 cigarrillos e intervenido de septoplastia. Acudió a consulta por ginecomastia bilateral dolorosa de tres meses de evolución. En la anamnesis no refería clínica de hipogonadismo asociada, modificaciones del peso corporal, empleo de fármacos ni productos cosméticos, o consumo de drogas. No había antecedentes familiares de interés.
A la exploración física se observó un fenotipo masculino normal, con adecuada distribución del vello corporal. El peso era 71,7kg y la talla 1,71 m (índice de masa corporal 25kg/m2) y la tensión arterial normal (130/80mmHg). Se palpaba aumento de tejido glandular mamario bilateral, grado II, simétrico, sin nódulos y sin secreción a la expresión. No se palpaba bocio y la auscultación cardiopulmonar era normal. El abdomen era blando y depresible, sin masas ni visceromegalias. Ambos testes se encontraban en bolsa escrotal, siendo el derecho de 25 cc y el izquierdo de 15-20 cc. No se palpaban masas testiculares.
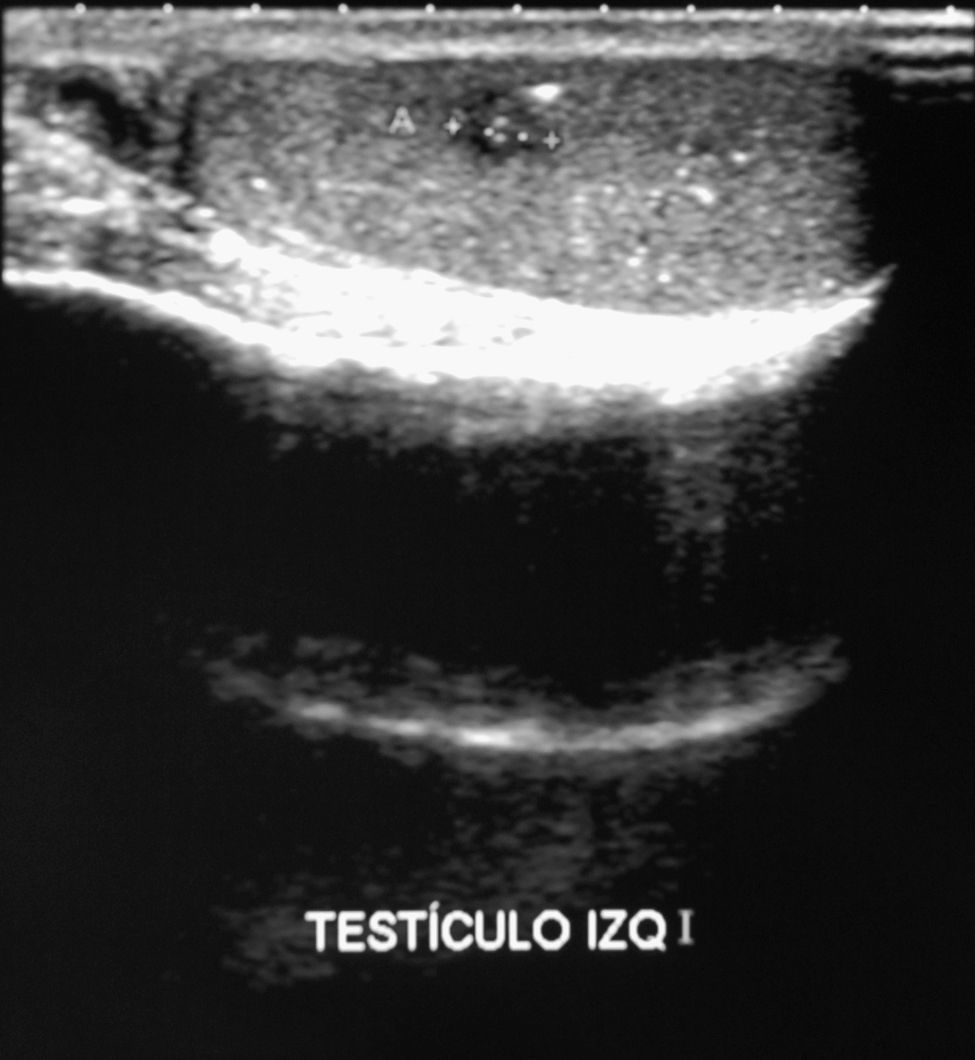
Ante ginecomastia bilateral de aparición reciente sin causa identificable se solicitó analítica que mostró concentraciones de HCG 27.703 UI/L (normal inferior a 2,5 UI/L), LH 16,2 UI/L (normal 0,87-7,6) FSH inferior a 0,1 UI/L (normal 0,7-11,1); estradiol 143 ng/L (normal 0-80); testosterona libre 53 ng/L (normal 8,8-27). El resto de analítica general, hormonas tiroideas y alfa fetoproteina fueron normales. Se solicitó ecografía testicular que describió teste derecho normal y teste izquierdo con hipogenicidad difusa, con múltiples imágenes hiperecogénicas dispersas en relación a microlitiasis. En zona media de teste izquierdo area hipoecoica de 6mm con márgenes mal definidos (fig. 1). Dilatación del plexo pampiniforme izquierdo en relación con varicocele. La radiografía de tórax fue normal.
Se derivó al paciente a urología realizándose orquiectomía transinguinal izquierda más colocación de prótesis testicular, sin incidencias. El TC toraco-abdómino-pélvico no mostró adenopatías ni lesiones sugestivas de enfermedad metastásica.
La anatomía patológica fue informada como tumor quemado de testículo asociado a neoplasia germinal intratubular con borde quirúrgico libre de lesión. Área blanquecina compatible con cicatriz, asociada a lesión granulomatosa con abundante reacción histiocitaria, sin células tumorales residuales, por lo que no fue posible un diagnóstico anatomopatológico definitivo. No infiltración vascular aparente. Hiperplasia de células de Leydig y litiasis intratubular.
En análisis de control tras la intervención quirúrgica, las concentraciones de HCG persistían elevadas (83.117 UI/L), por lo que se decidió en sesión multidisciplinar la necesidad de iniciar quimioterapia. Al proceder el paciente de otra comunidad autónoma, prefería continuar el tratamiento en su ciudad de origen, por lo que se contactó con su hospital de referencia para su traslado.
La ginecomastia aparece como resultado de un disbalance entre estrógenos y andrógenos. La ginecomastia fisiológica es muy frecuente en el período neonatal, la adolescencia y en varones de entre 50 y 80 años y se resuelve de forma espontánea en la mayoría de los casos1. En adultos, las causas más frecuentes se atribuyen a la persistencia de ginecomastia puberal, fármacos o a ginecomastia idiopática. Otros trastornos como la cirrosis hepática, insuficiencia renal, malnutrición, hipogonadismo o hipertiroidismo se asocian a ginecomastia4.
Entre las múltiples causas de ginecomastia patológica en adultos jóvenes se encuentran las de causa tumoral, fundamentalmente secundarias a tumores testiculares, bien por producción de HCG en tumores de células germinales o por secreción de estrógenos en tumores de células de Leydig5. Otros tumores que se han asociado a ginecomastia incluyen los adrenocorticales feminizantes y neoplasias con producción ectópica de HCG (pulmón, gástrico, renal, etc.)1.
Los tumores testiculares son las neoplasias sólidas más frecuentes en varones de entre 15 y 35 años. Los tumores de células germinales constituyen el 95% de los cánceres testiculares y la ginecomastia está presente en el 2,5-6% de los casos6. Ésta se asocia a la producción de HCG por focos de coriocarcinoma o células trofoblásticas en el tumor, y se considera un signo de mal pronóstico7.
Entre los tumores de células germinales se distinguen dos categorías principales: los seminomas y los no seminomatosos. Los seminomas constituyen el 50% de los tumores de células germinales y habitualmente al diagnóstico están localizados en testículo. Los marcadores tumorales son normales aunque la HCG puede estar levemente aumentada (generalmente por debajo de 100 UI/L). Los tumores no seminomatosos aparecen en pacientes más jóvenes, suelen estar constituidos por dos o más subtipos histológicos y hasta el 80-85% presentan concentraciones de HCG o alfafetoproteína elevadas. La variante histológica más agresiva es el coriocarcinoma, que rara vez aparece como componente único, pero está presente en el 10% de los tumores mixtos. En estos, la HCG es generalmente superior a 1.000 UI/L.
Ecográfícamente los tumores seminomatosos suelen aparecer como lesiones hipoecoicas bien definidas, mientras que los no seminomatosos son típicamente heterogéneos, con calcificaciones, áreas quísticas y márgenes irregulares8.
El tratamiento recomendado es la orquiectomía inguinal radical, lo que permite el diagnóstico histológico y el control local de la enfermedad. La evaluación radiológica mediante TC abdomino-pélvico está recomendada7,8 ya que las metástasis regionales aparecen con mayor frecuencia en ganglios retroperitoneales. Si se sospechase afección pulmonar debe realizarse TC torácico. Aunque los marcadores tumorales (HCG y alfafetoproteía) son útiles en el diagnóstico de los tumores testiculares y tienen valor pronóstico, su mayor utilidad es para el seguimiento de la enfermedad tras el tratamiento primario9.
Los valores de HCG y las características ecográficas del tumor en este paciente apuntaban a un tumor germinal no seminomatoso, aunque la anatomía patológica no fue concluyente por tratarse de un tumor «quemado», hecho relativamente frecuente en tumores testiculares. Tras el tratamiento quirúrgico, el paciente mantuvo concentraciones elevadas de HCG, por lo que se decidió realizar tratamiento con quimioterapia. No disponemos de datos posteriores al tratamiento quimioterápico, ya que este se realizó en otra comunidad autónoma.
En la mayoría de los pacientes que se presentan con ginecomastia, la historia clínica y exploración física permite el diagnóstico etiológico2. Las pruebas de función hepática, renal y tiroidea son útiles para excluir patología a dichos niveles. Cuando la ginecomastia es de origen reciente, sobre todo en el adulto joven, deben realizarse determinaciones de HCG, LH, testosterona, estradiol y prolactina salvo que la causa sea aparente tras una cuidadosa historia clínica y exploración física que incluya exploración testicular1. Hay que tener presente que en determinados casos, los tumores testiculares pueden no ser evidentes a la palpación10. Un diagnóstico precoz de estos casos, aunque infrecuentes, es esencial para un tratamiento temprano y un mejor pronóstico.