El cáncer diferenciado de tiroides es la neoplasia endocrina mas frecuente. El tratamiento con radioyodo es una pieza importante del tratamiento.
ObjetivoAnalizar los efectos de esta terapia sobre la función ovárica y reproductiva en las pacientes tratadas con I131.
Material y métodoSe realizó un análisis retrospectivo de los datos de 202 mujeres afectas de cáncer diferenciado de tiroides y tratadas con I131 en nuestro servicio entre 1985–2008. Se recogieron datos acerca de la edad de la menopausia de las pacientes y de sus madres y hermanas, historia menstrual, fertilidad y patología neonatal.
Resultados34 mujeres alcanzaron la edad de menopausia durante su seguimiento, con una edad media de 49,94±3,45 años mientras que en madres y hermanas fue de 49,20±5,37 y 48,73±3,74 años, respectivamente. Tres de estas pacientes presentaron oligoamenorrea transitoria. Ninguna tuvo infertilidad ni alteraciones en la descendencia.
ConclusionesEn nuestra serie no se halló un adelanto significativo de la edad de la menopausia respecto a sus familiares de primer grado ni una incidencia significativa de patología neonatal, infertilidad y/o alteraciones menstruales.
Differentiated thyroid cancer (DTC) is an increasingly frequent endocrinological disease. Radioiodine is a key component of treatment.
ObjectiveTo analyze the effects of I131 therapy on ovarian and reproductive function.
Material and methodsWe retrospectively analyzed data from 202 women treated with radioiodine for DTC in our service from 1985–2008. Data on age at menopause in patients and their mothers and sisters, menstrual history, fertility and neonatal abnormalities were collected.
ResultsMenopause occurred in 34 patients at follow-up. The mean age at menopause in patients was 49.94±3.45 while that in their mothers and sisters was 49.20±5.37 and 48.73±3.74 years, respectively. Three patients had transient amenorrhea. No infertility or neonatal alterations were found.
ConclusionsIn our series, menopause did not occur earlier in patients than in their first degree relatives. No significant alterations in neonatal health, fertility or menstruation were found.
La incidencia en mujeres de cáncer diferenciado de tiroides (CDT) en nuestro país, según los datos del Ministerio de Sanidad y Consumo publicados en el año 2004, es de 424 nuevos casos al año por cada 100.000 mujeres menores de 50 años, lo que supone la neoplasia endocrina mas frecuente en este grupo poblacional1.
Dentro del abordaje multidisciplinar de esta enfermedad el tratamiento con I131, supone uno de los pilares principales junto a la cirugía, dada su capacidad para actuar sobre las células que no han podido ser eliminadas mediante la intervención quirúrgica o sobre la enfermedad residual. Esta terapia puede asociarse con algunos efectos adversos incluyendo el deterioro transitorio o definitivo de la función ovárica y su repercusión cardiovascular, metabólica y ósea para esta población a largo plazo. La capacidad reproductiva (esterilidad transitoria o permanente), así como la posible morbi-mortalidad neonatal o teratogenicidad son otras potenciales complicaciones de esta terapia2–4.
Sin embargo, existen pocos datos acerca de un posible adelanto en la edad de menopausia en pacientes que recibieron tratamiento con I131. En una revisión reciente sobre los efectos del I131 sobre la función ovárica y su potencial efecto teratogénico realizado por Sawka et al5 se identificaron solo 2 estudios6,7 en los que se investigó dicha precocidad y sólo uno mostró datos significativos a favor de una menopausia ligeramente precoz en relación con la dosis administrada de I1317.
El objetivo de nuestro trabajo fue revisar la edad de menopausia de las pacientes que se habían tratado previamente con I131 así como otras alteraciones de la función reproductiva que pudieran ser atribuibles a dicha terapia.
Material y métodoEn el presente estudio se recogieron y analizaron retrospectivamente datos acerca de 202 mujeres a las que se les practicó tiroidectomía total y posterior tratamiento con I131 en nuestro centro entre los años 1985 y 2008. De ellas, se incluyeron en el estudio 89 que habían recibido el tratamiento antes de los 50 años cuando mantenían una ciclicidad menstrual normal. Treinta y cuatro de estas pacientes habían alcanzado la menopausia, definida esta como la ausencia de menstruación de, al menos, un año de duración sin otras causas para la misma. El grupo control lo conformaban las madres y hermanas de las pacientes siempre que no hubieran recibido tratamiento con I131 o tuvieran antecedentes de ooforectomía, histerectomía o alteraciones menstruales previas. No hemos registrado pérdidas en el seguimiento de las 89 pacientes consideradas.
Se recogió la edad a la que recibieron el primer tratamiento con I131, la edad de menopausia, así como si presentaron alteraciones menstruales antes y después de la administración de I131, infertilidad, número de hijos nacidos antes y después de recibir el tratamiento, salud de los hijos, características histológicas del cáncer, número de tratamientos y dosis total administrada de I131 en mCi. La recogida de datos tuvo un carácter retrospectivo, siendo sus fuentes la historia clínicas y la realización de un cuestionario telefónico. Se respetaron las normas de buena práctica clínica de nuestro centro.
El tratamiento con I131 fue realizado mayoritariamente en situación de hipotiroidismo (retirándose el tratamiento sustitutivo con levotiroxina durante 4 semanas y exigiéndose una TSH mínima de 30mU/ml) o tras estímulo con TSH recombinante (una inyección de 0,9mg de rTSH los días 1 y 2, administrando la dosis de I131 requerida el 3.er día y obteniendo imágenes el 5.° día), mediante este protocolo la TSH mínima exigida fue de 80mU/ml. De las 34 pacientes incluidas en el análisis final, 33 recibieron el tratamiento en situación de hipotiroidismo.
El análisis estadístico de los datos se realizó bajo soporte informático del paquete estadístico SPSS versión 15.0. Las estadísticas descriptivas se presentan como media±desviación estándar si la distribución era normal y, como mediana para variables cualitativas. La comparación entre variables se llevo a cabo mediante U de Mann-Whitney. Se consideró estadísticamente significativo un valor de p<0,05.
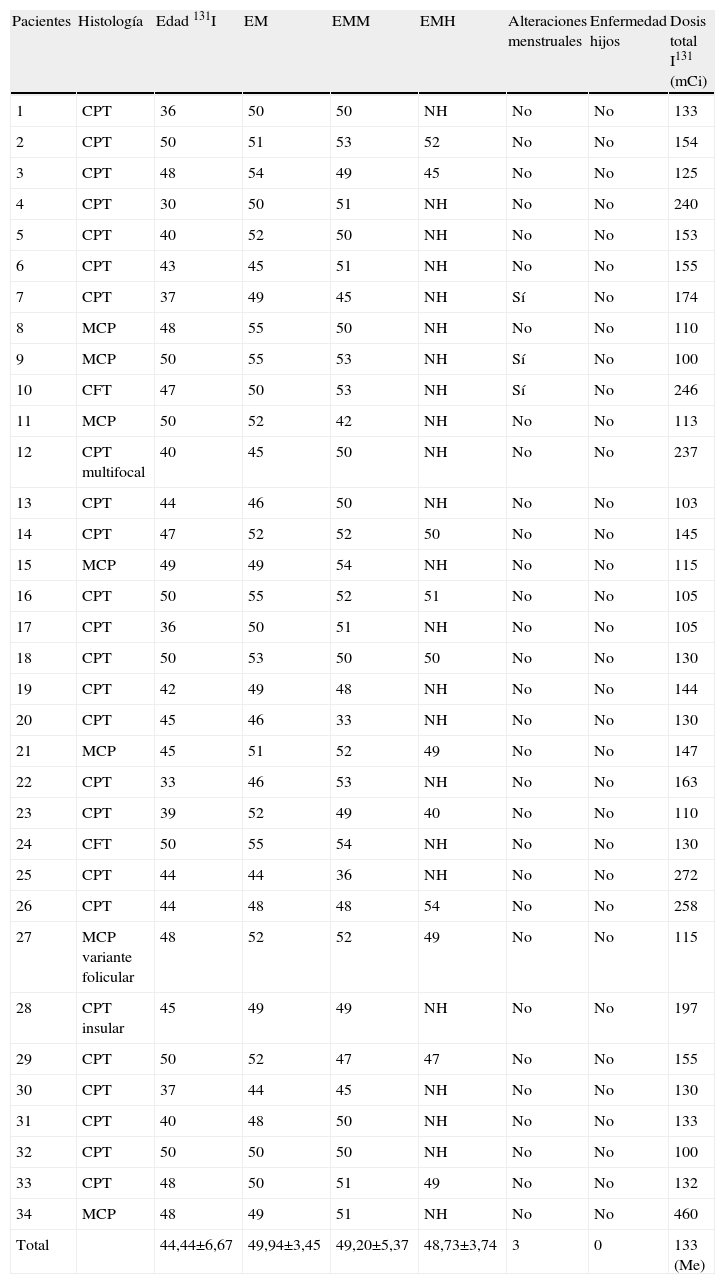
ResultadosLas características particulares de las pacientes así como el estudio histológico y la dosis de I131 acumulada aparecen recogidos en la tabla 1.
Características de las pacientes afectas de carcinoma diferenciado de tiroides
| Pacientes | Histología | Edad 131I | EM | EMM | EMH | Alteraciones menstruales | Enfermedad hijos | Dosis total I131 (mCi) |
| 1 | CPT | 36 | 50 | 50 | NH | No | No | 133 |
| 2 | CPT | 50 | 51 | 53 | 52 | No | No | 154 |
| 3 | CPT | 48 | 54 | 49 | 45 | No | No | 125 |
| 4 | CPT | 30 | 50 | 51 | NH | No | No | 240 |
| 5 | CPT | 40 | 52 | 50 | NH | No | No | 153 |
| 6 | CPT | 43 | 45 | 51 | NH | No | No | 155 |
| 7 | CPT | 37 | 49 | 45 | NH | Sí | No | 174 |
| 8 | MCP | 48 | 55 | 50 | NH | No | No | 110 |
| 9 | MCP | 50 | 55 | 53 | NH | Sí | No | 100 |
| 10 | CFT | 47 | 50 | 53 | NH | Sí | No | 246 |
| 11 | MCP | 50 | 52 | 42 | NH | No | No | 113 |
| 12 | CPT multifocal | 40 | 45 | 50 | NH | No | No | 237 |
| 13 | CPT | 44 | 46 | 50 | NH | No | No | 103 |
| 14 | CPT | 47 | 52 | 52 | 50 | No | No | 145 |
| 15 | MCP | 49 | 49 | 54 | NH | No | No | 115 |
| 16 | CPT | 50 | 55 | 52 | 51 | No | No | 105 |
| 17 | CPT | 36 | 50 | 51 | NH | No | No | 105 |
| 18 | CPT | 50 | 53 | 50 | 50 | No | No | 130 |
| 19 | CPT | 42 | 49 | 48 | NH | No | No | 144 |
| 20 | CPT | 45 | 46 | 33 | NH | No | No | 130 |
| 21 | MCP | 45 | 51 | 52 | 49 | No | No | 147 |
| 22 | CPT | 33 | 46 | 53 | NH | No | No | 163 |
| 23 | CPT | 39 | 52 | 49 | 40 | No | No | 110 |
| 24 | CFT | 50 | 55 | 54 | NH | No | No | 130 |
| 25 | CPT | 44 | 44 | 36 | NH | No | No | 272 |
| 26 | CPT | 44 | 48 | 48 | 54 | No | No | 258 |
| 27 | MCP variante folicular | 48 | 52 | 52 | 49 | No | No | 115 |
| 28 | CPT insular | 45 | 49 | 49 | NH | No | No | 197 |
| 29 | CPT | 50 | 52 | 47 | 47 | No | No | 155 |
| 30 | CPT | 37 | 44 | 45 | NH | No | No | 130 |
| 31 | CPT | 40 | 48 | 50 | NH | No | No | 133 |
| 32 | CPT | 50 | 50 | 50 | NH | No | No | 100 |
| 33 | CPT | 48 | 50 | 51 | 49 | No | No | 132 |
| 34 | MCP | 48 | 49 | 51 | NH | No | No | 460 |
| Total | 44,44±6,67 | 49,94±3,45 | 49,20±5,37 | 48,73±3,74 | 3 | 0 | 133 (Me) |
CFM: carcinoma folicular de tiroides; CPT: carcinoma papilar de tiroides; Edad 131I: edad en ańos al primer tratamiento con 131I; EM: edad en ańos de la menopausia de la paciente; EMM: edad en ańos de la menopausia de la madre de la paciente; EMH: edad en ańos de la menopausia de la hermana de la paciente; MCP: microcarcinoma papilar; NH: la paciente no tiene hermana; NM: no ha alcanzado menopausia.
La edad media de las pacientes en el momento del tratamiento fue de 44,44±6,67 años, mientras que la edad media en la que alcanzaron la menopausia fue de 49,94±3,45 años. Diez pacientes no tenían hermanas y en otros 13 casos estas no habían presentado la menopausia. De las 11 pacientes cuyas hermanas presentaban menopausia, 5 tenían más de una hermana con dicha condición por lo que se realizó la media de las edades de menopausia.
La mayoría de los estudios histológicos de los tumores encontrados correspondió con carcinomas papilares (92,9%) distinguiéndose entre ellos 7 microcarcinomas (25% del total de pacientes), 2 variantes foliculares (7,1% del total de pacientes), una variante insular (3,6% del total de pacientes) y un tumor multifocal (3,6% del total de pacientes). Dos pacientes presentaron carcinoma folicular (7,1%).
El número medio de veces que se trataron con I131 fue de 1,31±0,79 veces, siendo la mediana de las dosis administradas de 133mCi (RI: 48mCi), 5 mujeres recibieron 2 veces el tratamiento (dosis media de 250,6mCi) y una de ellas 4 veces (460mCi) En el caso de las 7 pacientes afectas de microcarcinoma papilar recibieron tratamiento con I131 por presentar anticuerpos antitiroglobulina en 4 casos y por la existencia de afectación ganglionar en el resto.
La edad media de la menopausia materna fue de 49,20±5,37 y no difirió significativamente de la de las pacientes (p=0,55). Tampoco encontramos diferencias significativas cuando se comparó con la edad media de la menopausia que se pudo recoger en las hermanas: 48,73±3,74 años (p=0,64).
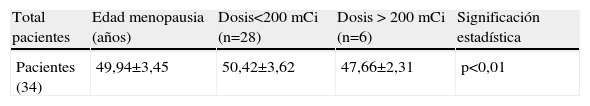
Se analizó la media de edad de menopausia en función de la dosis total de I131 recibida (tabla 2); separando las pacientes en función de haber recibido uno o más tratamientos con I131 (nivel de corte 200mCi). Las pacientes que recibieron menos de 200mCi (n=28) presentaban una edad media a la menopausia de 50,42±3,62 años (diferencia no significativa) y las pacientes que recibieron 200mCi o más de radioyodo (n=6) mostraron una edad media de menopausia de 47,66±2,31 años (p<0,01).
Edad de menopausia de las pacientes en función de la dosis de 131I recibida
| Total pacientes | Edad menopausia (años) | Dosis<200 mCi (n=28) | Dosis > 200 mCi (n=6) | Significación estadística |
| Pacientes (34) | 49,94±3,45 | 50,42±3,62 | 47,66±2,31 | p<0,01 |
EMM: edad de menopausia de madres de pacientes; EMP: edad media de menopausia de pacientes.
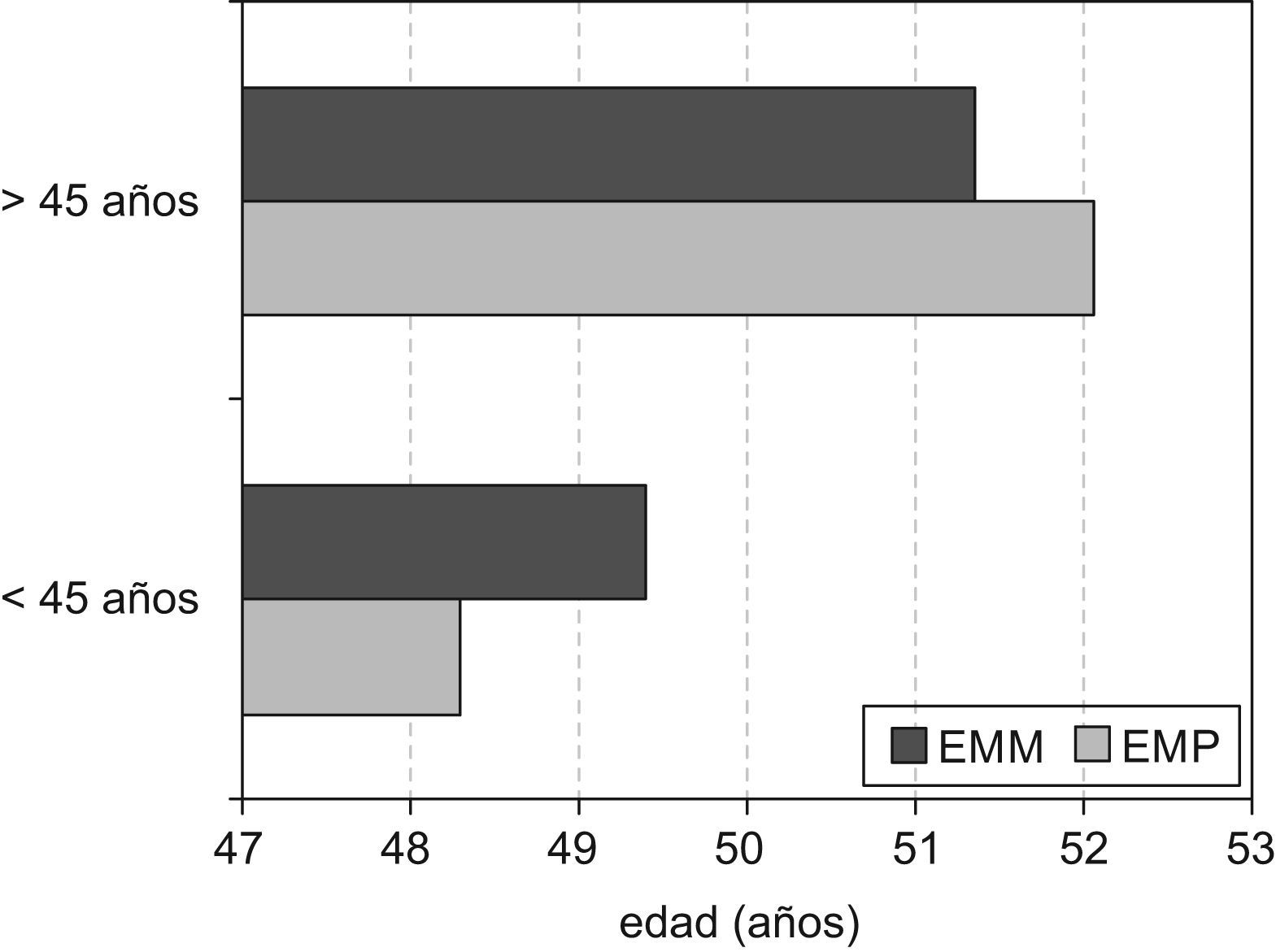
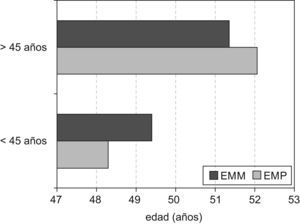
Por otro lado, se estableció comparación entre la edad media de menopausia de las pacientes y la de sus madres en función de la edad a la que recibieron el primer tratamiento (fig. 1). No se realizó comparación con las hermanas debido al pequeño tamaño muestral. Así mismo se eliminaron los datos de aquellas pacientes cuyas madres presentaron menopausia precoz. Las pacientes que en el momento de recibir I131 por primera vez tenían 45 años o menos (mediana de edad) presentaron un adelanto en la edad de menopausia de 1,14 años respecto a sus madres, lo que supone un adelanto promedio del 2%. En el segundo grupo, las pacientes mayores de 45 años en el momento del tratamiento alcanzaron la menopausia de media 0,72 años después que sus madres. La comparación no mostró diferencias estadísticamente significativas.
El número medio de hijos fue de 2,35 por paciente, de ellos, uno nació después de haber recibido tratamiento materno con 240mCi de I131. Ninguno presentó complicaciones obstétricas ni enfermedades congénitas. Ocho pacientes (8,89%) de las 89 analizadas presentaron alteraciones menstruales transitorias (dentro del primer año) tras el tratamiento.
DiscusiónAl igual que en la mayoría de las series recogidas en la revisión sistemática llevada a cabo por Sawka et al5 no se ha registrado en la nuestra un descenso en la edad de menopausia de las pacientes tratadas con I131, comparado con nuestro grupo control, aunque si con respecto a los datos de la población general española, donde la edad media de la menopausia se sitúa en los 51,7 años8. Estos datos son discordantes con respecto a los obtenidos en los estudios de Souza Rosario et al7 y Cecarelli et al6 en los que se evidenciaba una discreta disminución en la edad de menopausia de las mujeres tratadas con I131 respecto a otra población no sometida a este tratamiento. A diferencia de otros trabajos, nosotros hemos considerado como grupo control la muestra formada por las madres y hermanas de las pacientes en vez de la de un subgrupo de pacientes o la correspondiente a población general en base a la buena concordancia de base genética y epidemiológica9,10.
En el estudio de Cecarelli et al6, la reducción en la edad de la menopausia de las pacientes no estaba relacionada con la dosis de I131 recibida a diferencia del trabajo de Souza Rosario et al7 en el que se objetiva una asociación dosis-dependiente para la misma.
En nuestro trabajo nosotros si hemos encontrado una discreta pero significativa disminución en la edad de la menopausia en las pacientes que recibieron dosis de I131 mayores de 200mCi lo que refleja una mayor probabilidad de fallo ovárico relacionado con la dosis de I131. A priori, este discreto adelanto de la menopausia podría ser el resultado del daño ovaricoinducido por el I131 contribuyendo a acelerar el proceso natural de atresia folicular que conduce a la misma; y en definitiva, a señalar la necesidad de un mayor seguimiento de las complicaciones de la menopausia precoz en estas pacientes, especialmente de la enfermedad osteoporótica y cardiovascular.
Al igual que en el trabajo de Cecarelli et al6, en el presente estudio no hemos encontrado relación entre una edad avanzada en el primer tratamiento y un mayor adelanto en la edad de la menopausia. Nuestros datos muestran un adelanto no significativo en la menopausia sólo en el grupo que recibió tratamiento a una menor edad. Estos resultados no permiten extraer conclusión alguna debido al reducido tamaño muestral que encontramos al dividir los datos en 2 grupos (menores y mayores de 45 años), así como al hecho de que cuatro de las 6 pacientes que fueron sometidas a 2 o más tratamientos tenían menos de 45 años al recibir la primera dosis con el consiguiente aumento de irradiación ovárica.
No se registraron datos de infertilidad, malformaciones congénitas o enfermedad neonatal en esta serie lo que está acorde con el resto de series consultadas11–14.
La frecuencia de alteraciones menstruales tras el tratamiento fue algo menor que en la otras series consultadas3,6 debido probablemente al pequeño tamaño muestral y a que la mayoría recibió dosis no muy elevadas de I131. Al igual que en estos estudios estas alteraciones fueron transitorias resolviéndose entre 3–6 meses después del tratamiento, y se presentaron en mujeres mayores de 35 años en el momento de recibir I131.
La disparidad en las edades de las pacientes, así como el pequeño tamaño muestral, son las principales limitaciones de nuestro trabajo por lo que se hacen necesarios nuevos estudios prospectivos que recojan de manera sistemática y en cantidad suficiente datos acerca de la influencia del I131 sobre la función ovárica. En nuestra opinión la edad de menopausia de los familiares de primer grado debería considerarse en futuros estudios.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.