INTRODUCCIÓN
El aumento de la secreción de somatotropina u hormona de crecimiento (growth hormone [GH]) se debe, en la gran mayoría de los casos, a tumores de la adenohipófisis, el 85% de los cuales son macroadenomas, y ocasiona el cuadro clínico de la acromegalia cuando se presenta en adultos o el gigantismo cuando se presenta en niños antes del cierre de las epífisis óseas. En un 20-30% de los casos estos tumores son secretores también de prolactina.
Clínicamente, el diagnóstico se basa en las manifestaciones típicas de la enfermedad tanto a nivel central, por el efecto compresivo del tumor, como a nivel periférico, por los efectos del exceso de secreción de GH, no obstante, como el proceso clínico es insidioso, el estudio bioquímico es de gran importancia para el diagnóstico temprano de la enfermedad. La correcta evaluación clínica del paciente confirmada mediante pruebas bioquímicas, pruebas de imagen (resonancia o tomografía de la región selar) o campimetría son, en general, suficientes para el diagnóstico.
Para una correcta evaluación bioquímica de la patología asociada al aumento de secreción de GH es necesario tener en cuenta que la acción de la hormona sobre el crecimiento está mediada por unas proteínas de bajo peso molecular denominadas factores de crecimiento insulinoides (IGF) y, en consecuencia, el estudio conjunto del eje GH-IGF facilitará el diagnóstico de este tipo de enfermedad.
SOMATOTROPINA
La GH se secreta de forma pulsátil por las células somatotropas de la adenohipófisis. En la sangre circulan varias formas moleculares, entre ellas, la más abundante es una cadena polipeptídica de 191 aminoácidos de 22 kDa. Otras formas que se han descrito son: la de 176 aminoácidos de 20 kDa, formas acídicas y desaminadas, dímeros, trímeros, oligómeros y fragmentos de 17 y 12 kDa. El gen se sitúa en el brazo largo del cromosoma 17 en una región denominada "clúster del gen de la GH" en el que se combinan 5 genes de los cuales sólo uno, el denominado GH1, codifica para la hormona que circula en sangre y el resto se expresan en la placenta.
La secreción de GH está regulada principalmente por 2 péptidos hipotalámicos, uno estimulador denominado somatoliberina (GHRH) y otro inhibidor, la somatostatina. Estos péptidos, a su vez, se liberan bajo la influencia de diferentes neurotransmisores y hormonas, como los glucocorticoides, los estrógenos, las hormonas tiroideas, etc. Se ha descrito, también, un potente estimulador de la secreción de GH de origen gástrico, denominado ghrelina, cuyo papel en la fisiopatología del crecimiento está en estudio.
La GH actúa sobre las células que poseen receptores específicos. Sus acciones son variadas, sobre el crecimiento induciendo la síntesis del factor de crecimiento insulinoide de tipo 1 (IGF1) tanto a nivel local de cartílago de crecimiento como a nivel general, sobre todo en el hígado, y metabólicas, principalmente anabolizantes, que dependen tanto del tejido diana como del tiempo de exposición de estos tejidos a la hormona. Los efectos agudos de la hormona son similares a los de la insulina, mientras que la exposición prolongada provoca efectos diabetogénicos. El gen del receptor se sitúa en el brazo corto del cromosoma 5.
En la sangre, la GH circula unida a 2 proteínas de transporte: una específica de alta afinidad de aproximadamente 65 kDa, denominada proteína enlazante de la somatotropina (GHBP), que se corresponde con el dominio extracelular del receptor de la hormona y transporta aproximadamente la mitad de la forma de 22 kDa, y otra de baja afinidad que se une, sobre todo, a la forma de 20 kDa1.
MÉTODOS DE ANÁLISIS DE SOMATOTROPINA
Para cuantificar la GH se utilizan métodos de inmunoanálisis que pueden emplear anticuerpos mono o policlonales en la reacción antígeno-anticuerpo (tabla 1). Los más usados son los métodos no competitivos que miden la molécula de GH inmunorreactiva mediante 2 anticuerpos, uno que fija la molécula llamado captador y otro que es el que da la señal susceptible de ser cuantificada denominado marcador o trazador. Se ha descrito, además, un método funcional (Ligand Immuno-Functional Assay) que mide la molécula biológicamente activa capaz de unirse al receptor2. En este método se utilizan: a) un anticuerpo específico frente a uno de los sitios de unión de la GH al receptor; b) GHBP recombinante, que se unirá a la GH, y c) un anticuerpo anti-GHBP marcado que es el que proporciona la señal que se mide. Conceptualmente, éste sería el método más idóneo pero no está todavía automatizado y su uso no está extendido3.
Sensibilidad
Los métodos utilizados actualmente tienen mayor capacidad de detección de la molécula a concentraciones bajas. Los inmunoanálisis competitivos (RIA), suelen tener un límite de detección de 1 µg/l (equivalente a ng/ml), mientras que los métodos no competitivos inmunoquimioluminométricos llegan a detectar niveles incluso de 0,01 µg/l.
Variabilidad de los resultados
Del mismo modo, los coeficientes de variación intra e interseriales se han ido reduciendo hasta límites inferiores al 5% en algunos casos.
No obstante, siguen dándose discrepancias notables cuando se analizan las mismas muestras por diferentes métodos. Los resultados que se obtienen pueden variar sustancialmente dependiendo del inmunoanálisis que se utilice en el laboratorio, por lo que es imprescindible que la comunicación entre el bioquímico y el endocrinólogo sea fluida a la hora de informar e interpretar los resultados que se obtienen.
Se han señalado diversas razones para explicar las discordancias entre laboratorios:
a) La heterogeneidad de la propia molécula. No todos lo métodos que se utilizan detectan las mismas formas moleculares de GH, que ya se han mencionado, por lo tanto, se introduce un factor importante de variabilidad en los resultados. Se ha propuesto, para intentar paliar este problema, que los reactivos contengan anticuerpos dirigidos únicamente contra la forma de 22 kDa4.
b) Tipo de anticuerpos anti-GH. Metodológicamente, al utilizar anticuerpos monoclonales se ha ganado en especificidad pero, paralelamente, estos métodos son capaces de detectar menos formas moleculares de GH dependiendo de la especificidad de los anticuerpos que se utilizan.
c) La utilización de diferentes estándares. Actualmente se están utilizando 3 estándares internacionales como referencia para la calibración de los distintos métodos analíticos. Los dos últimos estándares establecidos (WHO 88/624 y 98/574) se obtienen mediante técnica de recombinación de ADN que, aunque presentan la dificultad respecto a los estándares obtenidos de hipófisis humana (WHO 80/505) de que sólo contienen la forma molecular de 22 kDa, tienen la gran ventaja de que su producción es prácticamente ilimitada3. Cuando sea necesaria la conversión de las unidades de expresión de los resultados hay que considerar que el factor de conversión varía con relación al estándar que se utilice para la calibración; por ejemplo, para convertir µg/l a mU/l el factor es 2,6 cuando los calibradores utilizados están estandarizados frente al estándar internacional 80/505, mientras que para el 98/574 el factor es 3.
d) La interferencia de la proteína enlazante de la GH. Se ha descrito que en los análisis no competitivos el aumento progresivo de las concentraciones de GHBP conlleva una disminución gradual de las de GH pudiendo llegar a recuperaciones del 75%, mientras que en los análisis competitivos se han encontrado valores falsamente elevados5,6.
Estabilidad de la muestra
En sangre recogida en tubos sin anticoagulante es estable durante 1 día a temperatura ambiente. La muestra recomendada es suero y se debe procesar antes de 24 h si se conserva a temperatura ambiente, antes de 8 días conservada a 4-8 ºC y antes de 3 meses si se guarda a -20 ºC7.
DIAGNÓSTICO BIOQUÍMICO
Determinación aislada de somatotropina
Aunque se ha descrito que la medida basal de la concentración de GH es útil para el seguimiento de la acromegalia8, una determinación aislada, en general, carece de valor ya que presenta problemas de especificidad diagnóstica. Se han encontrado valores elevados en varias situaciones clínicas que no se corresponden con un aumento continuado de secreción y en situaciones de estrés. Además, como la secreción de GH es pulsátil, los "picos" fisiológicos que se producen pueden inducir a dificultades de interpretación de los resultados analíticos porque la concentraciones que se alcanzan se pueden solapar con las que se encuentran en pacientes acromegálicos y, a la inversa, pueden encontrarse valores de GH dentro del intervalo de referencia, o en el límite superior, en algunos pacientes afectados de acromegalia o gigantismo.
Sin embargo, la medida de la concentración basal de GH se utiliza para descartar el diagnóstico de acromegalia cuando se valora conjuntamente con la cuantificación de IGF1. Se ha establecido, por consenso, que si se encuentran concentraciones de GH inferiores a 0,4 µg/l9, o 0,3 µg/l si se utilizan inmunoanálisis de alta sensibilidad analítica10, junto con valores de IGF1 dentro del intervalo de referencia, considerados en función de la edad y el sexo, el diagnóstico de acromegalia es extremadamente improbable.
Asimismo, concentraciones muy elevadas de GH junto con valores de IGF1 también por encima del intervalo de referencia hacen muy probable el diagnóstico.
Sobrecarga oral de glucosa
Debido a la falta de especificidad de la determinación aislada de GH, se han utilizado pruebas funcionales para establecer el diagnóstico bioquímico de la enfermedad; de todas ellas, actualmente se considera que la prueba de la sobrecarga oral de glucosa (SOG) es la que proporciona el mejor rendimiento diagnóstico.
La prueba se fundamenta en que, en personas no afectadas por la enfermedad, el aumento de la concentración de glucosa en sangre provoca la supresión de la secreción de GH, posiblemente por aumento de la secreción de somatostatina por el hipotálamo, mientras que en pacientes acromegálicos este efecto no se produce e, incluso, puede observarse un aumento de secreción.
Procedimiento clínico
La prueba debe realizarse con el paciente en ayunas, en reposo y sin estrés.
Se realiza administrando por vía oral 75 g de glucosa y midiendo las concentraciones plasmáticas de GH en los tiempos 0, 30, 60, 90 y 120 min, aunque se ha descrito también un procedimiento con una determinación única de GH a los 120 min que podría ser tan útil como la curva completa11.
Interpretación
En personas no afectadas por la enfermedad, la ingesta oral de glucosa suele provocar una disminución de la concentración de GH en suero hasta límites indetectables, entre 30-120 min después de la administración. Para intentar descartar acromegalia se han establecido valores de corte o discriminación, de modo que, si el resultado obtenido en algún punto de la curva se sitúa por debajo de ellos es improbable el diagnóstico de acromegalia.
Se consideraron como valores discriminantes las concentraciones inferiores a 1 µg/l9,12 (pero a medida que los métodos analíticos han ido consiguiendo mayor sensibilidad se ha sugerido la necesidad de redefinirlos. Así, para inmunoanálisis de alta sensibilidad se ha propuesto utilizar valores mucho más bajos de entre 0,14 y 0,42 µg/l10,13-16
A la hora de interpretar los resultados hay que tener en cuenta variables como el sexo, la edad o el índice de masa corporal y hacer una cuidadosa historia clínica para detectar diversas enfermedades, como diabetes mal controlada, consumo de opiáceos, enfermedad hepática o renal y anorexia nerviosa que pueden producir resultados falsos positivos10. Por otra parte, no cabe duda de que la evaluación de los resultados se ha de considerar en función del método analítico utilizado17. Para evitar todas estas dificultades y establecer el diagnóstico bioquímico de la enfermedad, es importante que los resultados de esta prueba sean considerados conjuntamente con los de IGF1. En una revisión de trabajos publicados16 se sugiere que cuando se combinan el hallazgo de valores de GH inferiores a 0,25 µg/l, obtenidos en algún punto de la curva mediante métodos de alta sensibilidad, con valores de IGF1 dentro del intervalo de referencia establecido por edad y sexo, es extremadamente improbable el diagnóstico de acromegalia.
Secreción integrada de hormona de crecimiento
El estudio de la secreción de GH espontánea mediante la toma de muestra a lo largo de 3 o de 24 h se ha utilizado, también, para el diagnóstico de acromegalia. No obstante, por la complejidad del procedimiento que necesita ingreso hospitalario, su elevado coste y porque parece demostrado en algunos trabajos que los resultados que se obtienen en pacientes con acromegalia activa pueden solaparse con los de personas no afectadas por la enfermedad, no se recomienda la utilización de esta prueba que, en todo caso, quedaría reservada para el campo de la investigación o en aquellos pacientes en los que se encuentran resultados discordantes entre otras pruebas diagnósticas o en los que no pueden utilizarse los protocolos habituales18.
Para la interpretación de los resultados, se calcula el valor promedio de todas las concentraciones obtenidas en las diferentes muestras considerándose que el hallazgo de resultados inferiores a 2,5 µg/l son poco indicativos de acromegalia19.
Pruebas de estimulación
Se han utilizado pruebas de estimulación de la secreción de GH con protirelina (TRH), gonadorelina (GnRH) y somatorelina (GHRH), pero actualmente no se recomiendan para el diagnóstico porque no ofrecen ventajas respecto a la SOG9.
FACTOR DE CRECIMIENTO INSULINOIDE DE TIPO 1
Los factores de crecimiento insulinoides (IGF) son los principales mediadores de la acción de la GH y tienen un efecto de retrocontrol sobre la secreción de la hormona tanto en la hipófisis como en el hipotálamo. Son 2 péptidos, el IGF de tipo 1 (IGF1) y el IGF de tipo 2 (IGF2), de un peso molecular de alrededor de 7 kDa que se sintetizan en los tejidos y, sobre todo, en el hígado. El IGF2 parece tener más importancia durante el período fetal, mientras que el IGF1 se correlaciona mejor con la secreción de GH después del nacimiento. El 75% del IGF1 circula en la sangre unido, en un complejo ternario de 150 kDa, a 2 proteínas: a) la isoforma 3 de la proteína enlazante de los factores de crecimiento insulinoides (insulin-like growth factor binding protein-3 o IGFBP3), que pertenece a una gran familia de proteínas de transporte de la que se conocen 6 isoformas numeradas de 1 a 6, y b) la denominada subunidad ácido-lábil (ALS). La secreción de los componentes de este complejo ternario está regulada, aunque no exclusivamente, por la acción de la GH, por lo que se ha descrito que pudieran tener cierta importancia en el diagnóstico de la acromegalia20.
El estudio de las concentraciones de IGF1, en función de intervalos de referencia establecidos por edad y sexo, es de gran utilidad para el diagnóstico y el seguimiento de los pacientes con acromegalia. Los valores de IGF1 aumentan tempranamente en la enfermedad y no suelen alterarse en otros procesos patológicos, distintos a la acromegalia, que cursan con aumento de la secreción de GH (tabla 2). Por otra parte, las concentraciones de IGF1 son más estables que las de GH a lo largo del día, lo que permite una mejor interpretación de los resultados obtenidos en condiciones basales.
Es importante también señalar que en algunos estudios se ha demostrado que valores de IGF1 claramente elevados pueden ser diagnósticos de acromegalia incluso en pacientes con concentraciones de GH basales y tras sobrecarga de glucosa dentro de los valores de referencia14. Finalmente, la determinación de IGF1 es de vital importancia cuando se utiliza el bloqueo de los receptores de GH en el tratamiento de la acromegalia, ya que se ha demostrado que en estos pacientes es el principal marcador de actividad de la enferme dad20,21.
OTRAS DETERMINACIONES BIOQUÍMICAS
Como ya se ha mencionado, los tumores productores de GH suelen secretar también prolactina y se han encontrado valores elevados de esta hormona en un 36% de los pacientes acromegálicos22; por lo tanto, es recomendable medir la concentración de dicha hormona en sangre. Del mismo modo, por el efecto compresivo del tumor, pueden estar alterados los demás ejes hipotalamohipofisarios, que deberían estudiarse en este tipo de pacientes mediante la determinación basal concomitante de hormonas hipofisarias y periféricas o, en los casos que fuera necesario, la prueba de estimulación múltiple o megatest.
En la acromegalia activa pueden encontrarse, también, variaciones en otras pruebas bioquímicas, como modificación de los marcadores de la homeostasis del calcio23, o alteración de la prueba de tolerancia oral a la glucosa.
CONCLUSIONES
Para el diagnóstico bioquímico de los pacientes en los que se sospecha un exceso de secreción de somatotropina es necesaria una estrecha colaboración entre el endocrinólogo y el bioquímico clínico. Las pruebas bioquímicas iniciales que se utilizan son las determinaciones basales de GH e IGF1; si los resultados de éstas no son concluyentes se debe realizar la prueba de sobrecarga oral de glucosa, que también debe valorarse junto con la determinación de IGF1.
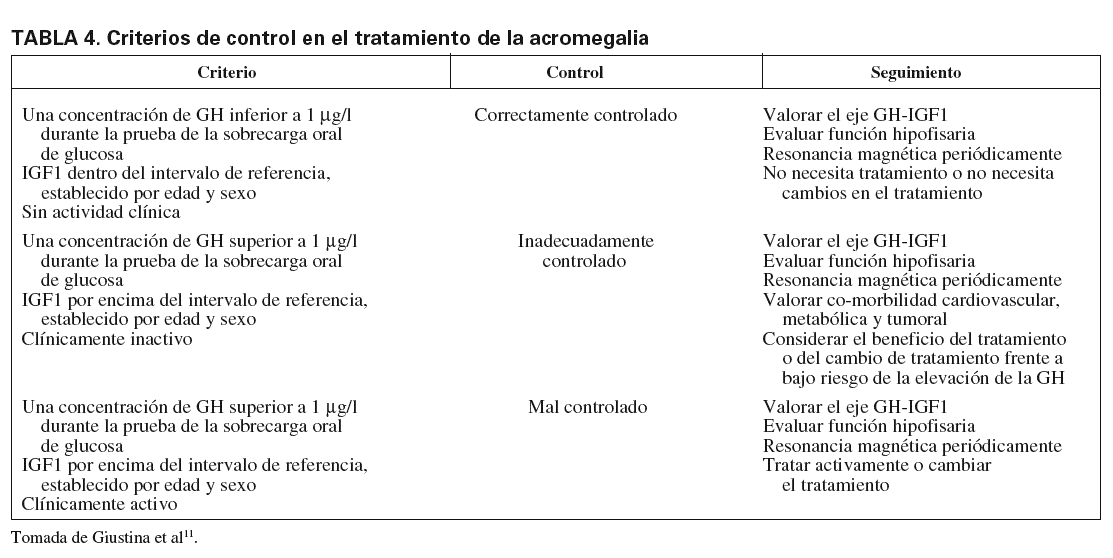
Respecto a los valores discriminantes que se aplican en la determinación de GH, el consenso al que se llegó en el año 20009 y que se describe en las tablas 3 y 4, ha sido puesto en entredicho12, y será necesario establecer un nuevo acuerdo teniendo en cuenta la sensibilidad y la especificidad analíticas de los nuevos inmunoanálisis.
Desde el punto de vista analítico, será preciso disminuir la variabilidad de los resultados homogeneizando tanto los estándares como el tipo de anticuerpos que se utilizan en los métodos de determinación.