La tiroiditis inducida por amiodarona (TIA) es una entidad clínica frecuente, con distintas formas de presentación, respuesta variable al tratamiento, y que puede ser potencialmente fatal.
MétodosSe presentan tres pacientes con fibrilación auricular, que desarrollaron una TIA tras al menos 36 meses de exposición al fármaco. El hipertiroidismo asociado no respondió a la terapia farmacológica convencional, conllevando un empeoramiento franco de la cardiopatía de los pacientes, lo que motivó la indicación de tiroidectomía total, previa instauración de una terapia basada en la combinación de dexametasona 8-12mg/día iv, tionamidas 45mg/día vo, beta-bloqueantes, junto perclorato potásico 0,8-1g/día vo. Dos pacientes normalizaron las hormonas tiroideas periféricas tras 12 y 32 días de terapia combinada.
ConclusiónLa combinación de tionamidas y perclorato potásico es una alternativa terapéutica eficaz en la TIA tipo I en pacientes refractarios a terapia convencional. Debe valorarse su empleo en pacientes con TIA mixta o etiología no aclarada.
Amiodarone-induced thyrotoxicosis (AIT) is a common clinical disorder that may be life threatening and whose clinical manifestations and response to treatment may vary among patients.
MethodsWe present three patients treated with amiodarone for atrial fibrillation who developed AIT at least 36 months after beginning the treatment. Thyrotoxicosis worsened the underlying cardiac disorders and was resistant to treatment based on the combination of dexamethasone 8-12mg/day i.v., thioamides 45mg/day p.o., beta blockers and potassium perchlorate at doses of 800 to 1000mg per day p.o. Two of the patients attained sustained euthyroidism after 12 and 32 days of combined treatment, while the third required total thyroidectomy.
ConclusionThe combination of thioamides with potassium perchlorate is an appropriate form of therapy for AIT in patients resistant to thioamides. The use of this combination should be evaluated in patients with mixed AIT or AIT of unclear etiology.
La amiodarona es un fármaco antiarrítmico eficaz, que presenta complicaciones tiroideas en un 15% de los pacientes1. Puede manifestarse como hipotiroidismo o como tirotoxicosis. Existen dos tipos de tiroiditis inducidas por amiodarona (TIA), TIA tipo I consistente en un aumento de síntesis de hormonas tiroideas, y la TIA tipo II caracterizada por una inflamación de la glándula tiroides con destrucción de folículos tiroideos y salida al torrente sanguíneo de hormonas tiroideas preformadas2,3. La diferenciación entre ambas entidades y su abordaje terapéutico es complejo. Presentamos tres casos clínicos de pacientes con TIA resistentes a terapia antitiroidea convencional que precisaron tratamiento adyuvante con perclorato potásico, con distintos grados de respuesta clínica, previo a tratamiento definitivo con tiroidectomía total.
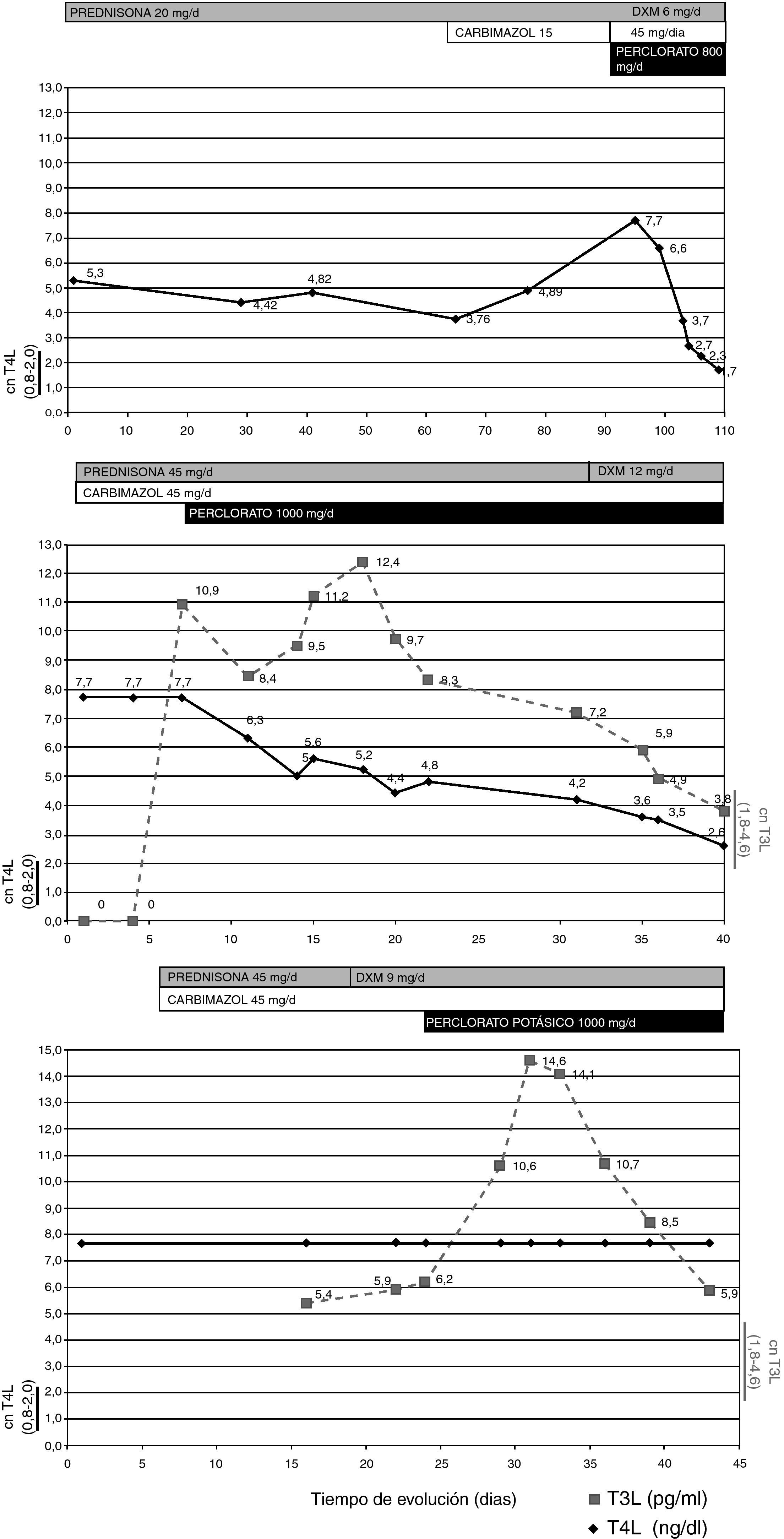
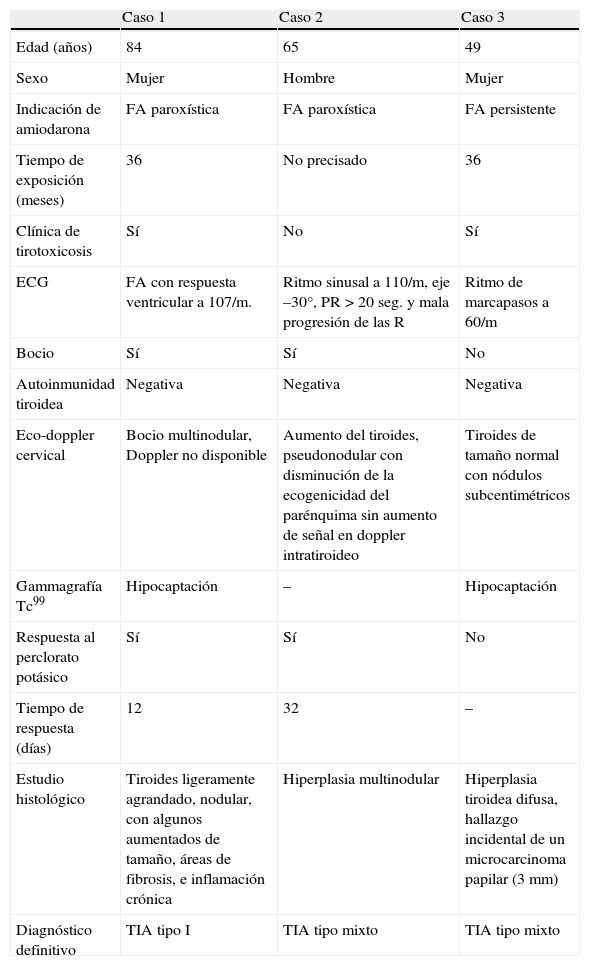
Las características clínicas y el tipo de tratamiento instaurado, junto a las variaciones en las concentraciones plasmáticas de hormonas tiroideas periféricas en cada uno de los casos quedan representados en la tabla 1 y fig. 1.
Características clínicas de los pacientes.
| Caso 1 | Caso 2 | Caso 3 | |
| Edad (años) | 84 | 65 | 49 |
| Sexo | Mujer | Hombre | Mujer |
| Indicación de amiodarona | FA paroxística | FA paroxística | FA persistente |
| Tiempo de exposición (meses) | 36 | No precisado | 36 |
| Clínica de tirotoxicosis | Sí | No | Sí |
| ECG | FA con respuesta ventricular a 107/m. | Ritmo sinusal a 110/m, eje –30°, PR>20 seg. y mala progresión de las R | Ritmo de marcapasos a 60/m |
| Bocio | Sí | Sí | No |
| Autoinmunidad tiroidea | Negativa | Negativa | Negativa |
| Eco-doppler cervical | Bocio multinodular, Doppler no disponible | Aumento del tiroides, pseudonodular con disminución de la ecogenicidad del parénquima sin aumento de señal en doppler intratiroideo | Tiroides de tamaño normal con nódulos subcentimétricos |
| Gammagrafía Tc99 | Hipocaptación | – | Hipocaptación |
| Respuesta al perclorato potásico | Sí | Sí | No |
| Tiempo de respuesta (días) | 12 | 32 | – |
| Estudio histológico | Tiroides ligeramente agrandado, nodular, con algunos aumentados de tamaño, áreas de fibrosis, e inflamación crónica | Hiperplasia multinodular | Hiperplasia tiroidea difusa, hallazgo incidental de un microcarcinoma papilar (3 mm) |
| Diagnóstico definitivo | TIA tipo I | TIA tipo mixto | TIA tipo mixto |
ECG: electrocardiograma; FA: fibrilación auricular; TIA: tiroiditis inducida por amiodarona.
Mujer de 84 años, que consultó en hospital de área por astenia, disnea a mínimos esfuerzos, palpitaciones e insomnio. Como antecedentes, la paciente refería episodio de fibrilación auricular (FA) paroxística tres años antes, requiriendo cardioversión eléctrica. Instaurándose tratamiento con amiodarona (200mg/día) y acenocumarol. El electrocardiograma (ECG) evidenció una FA con respuesta ventricular elevada (105 l/m), objetivándose en los estudios de función tiroidea una TSH<0,03 mU/L (v-n- 0,38-4,84), T4 Libre (T4L) 4,42 ng/dl (v-n- 0,8-2,0). Se inició tratamiento con prednisona 30mg/día, asociado a acenocumarol, y se suspendió la amiodarona. Tras un mes de tratamiento glucocorticoideo sin respuesta bioquímica se asoció carbimazol 15mg/día y propranolol 20mg/8h. Tras tres meses de terapia la paciente presentaba clínica franca de tirotoxicosis, disnea de reposo y pérdida ponderal progresiva de 5kg de peso. Ante la ausencia de respuesta se consultó con nuestro servicio decidiéndose ingreso hospitalario para tratamiento definitivo con tiroidectomía total. A la exploración física presentaba bocio grado 1 de consistencia aumentada y textura nodular, una frecuencia cardíaca de 107/m, arrítmica (peso 52,8kg, talla: 1,60 m, índice de masa corporal 20,62kg/m2), ingurgitación yugular, edemas bimaleolares y pretibiales con fóvea. El estudio de función tiroidea objetivó una TSH inferior a 0,03 mU/L, T4L: superior a 7,7 ng/dl, T3 libre (T3L) 4,6 pg/ml (v.n. 1,8-4,6). Se instauró una terapia de preparación rápida para cirugía indicando un esquema terapéutico basado en perclorato potásico 800mg/día vo, dexametasona (DXM) 2mg/8h iv, carbimazol 45mg/día y propranolol 40mg/día vo. Se inició tratamiento con digoxina manteniendo acenocumarol por parte de cardiología. Tras 12 días de tratamiento con este esquema, la paciente presentó una completa normalización de las hormonas tiroideas periféricas, procediéndose a tiroidectomía total. La paciente fue diagnosticada de tiroiditis inducida por amiodarona tipo I.
Caso 2Varón de 65 años, que ingresó a cargo de cardiología por angina de reposo y taquicardia sinusal, con PR largo para ajuste de tratamiento. Antecedentes de diabetes mellitus tipo 2, dislipemia, hipertensión arterial e insuficiencia renal crónica leve. Cardiopatía isquémica crónica con revascularización previa (hacía 12 años) con doble bypass, y angor de reposo de 4 meses de evolución, que motivó la colocación de 4 stents e implante de células madre y revascularización transmiocárdica con láser. Asimismo había recibido tratamiento con amiodarona durante varios años por episodios de FA paroxística, habiéndose retirado hacía dos meses. La ecocardiografía mostró un ventrículo izquierdo (VI) dilatado, función sistólica (FS) intensamente deprimida, aquinesia de segmentos septales y anterior, con hipoquinesia del resto. El estudio de función tiroidea reveló una TSH inferior a 0,03 mU/L, T4L superior a 7,7 ng/dl y T3L 12,8 ng/dl, motivo por el que se consultó a nuestro departamento. El paciente no refería clínica de tirotoxicosis, sin embargo había perdido 15kg en los últimos dos meses. A la exploración, el paciente presentaba una tensión arterial de 120/80 mmHg, FC 96/m, no presentaba bocio, signos de oftalmopatía, ni temblor distal. Se instauró carbimazol 45mg/día y prednisona 45mg/día. Tras 7 días de tratamiento, el paciente presentaba una T4L superior a 7,7 ng/dl y T3L 10,9 ng/dl, junto episodios de repetición de síndrome coronario agudo, indicándose tratamiento definitivo mediante tiroidectomía total. Se continuó tratamiento con carbimazol 45mg/día, dexametasona 12mg/día vo y se añadió perclorato potásico 1.000mg/día vo. Tras 32 días con este esquema terapéutico se obtuvo la normalización de las concentraciones plasmáticas de T3L, practicándose la intervención quirúrgica sin incidencias. El diagnóstico fue de hipertiroidismo primario grave inducido por amiodarona de tipo mixto. Tras 12 meses de seguimiento el paciente no ha vuelto a presentar sintomatología cardíaca.
Caso 3Mujer de 49 años, que consultó en cardiología de forma ambulatoria por clínica de 2-3 semanas de evolución de astenia intensa, anorexia y disnea. Presentaba antecedentes de miocardiopatía dilatada idiopática de 4 años de evolución (insuficiencia cardíaca [IC] grado II de la NYHA), junto FA persistente diagnosticada hacía tres años en tratamiento con acenocumarol y amiodarona, y portadora de desfibrilador automático implantable y marcapasos unicameral por taquicardia ventricular polimorfas con resincronización cardíaca, por bloqueo auriculoventricular de alto grado hacía 3 años. El estudio de función tiroidea reveló TSH inferior a 0,03 mU/L y T4L superior a 7,7 ng/dl. Se suspendió la amiodarona, se inició tratamiento con betabloqueantes (bisoprolol 2,5mg/día) y se intensificó el tratamiento diurético. En este momento se solicitó valoración ambulatoria por nuestro departamento. A la exploración la paciente presentaba una FC de 60/m, auscultación cardíaca rítmica con un soplo sistólico panfocal, un tiroides de tamaño normal y consistencia aumentada y sin signos de IC. Se instauró tratamiento con carbimazol 45mg/día y prednisona 45mg/día vo. Tras 15 días de tratamiento, las concentraciones de hormonas tiroideas permanecían elevadas, presentando la paciente signos francos de IC descompensada, con edemas bimaleolares, por lo que se decidió ingreso hospitalario para tratamiento definitivo con tiroidectomía total. Se inició una pauta intensiva con DXM 8mg/día iv, metimazol 45mg/día y perclorato potásico 1.000mg/día vo. La paciente no respondió al tratamiento instaurado, con empeoramiento progresivo de los signos de IC y aparición de miopatía esteroidea. Pese a la persistencia de la tirotoxicosis, dada la mala evolución clínica de la paciente se procedió a la tiroidectomía total a los 25 días del ingreso sin complicaciones perioperatorias inmediatas. El diagnóstico definitivo fue de hipertiroidismo primario grave inducido por amiodarona de tipo mixto.
La amiodarona es un fármaco antiarrítmico muy eficaz de clase III, con un alto contenido en yodo en su molécula, es muy lipofílica con un amplio volumen de distribución y una vida media prolongada, superior a 40 días4. La disfunción tiroidea, puede presentarse desde el inicio del tratamiento hasta varios años después1,5.
La presentación clínica de la TIA es similar a la de otras causas de tirotoxicosis, no obstante esta clínica puede enmascararse parcialmente por el efecto betabloqueante de la amiodarona y su inhibición de los receptores nucleares de T31,6. La diferenciación entre ambos tipos de TIA es difícil, admitiéndose la existencia de tipos mixtos, como en dos de los casos reportados7. La presencia de autoanticuerpos positivos, aumento del tamaño tiroideo, nódulos tiroideos en la ecografía y fundamentalmente un aumento de la vascularización en la eco-Doppler tiroidea serían sugestivos de TIA tipo I. En ambos casos, en la gammagrafía suele haber hipocaptación dada la saturación por yodo de la glándula, sólo la inusual presencia de hipercaptación sugiere TIA tipo I. El hallazgo de IL-6 elevada, está presente en TIA tipo II2,8.
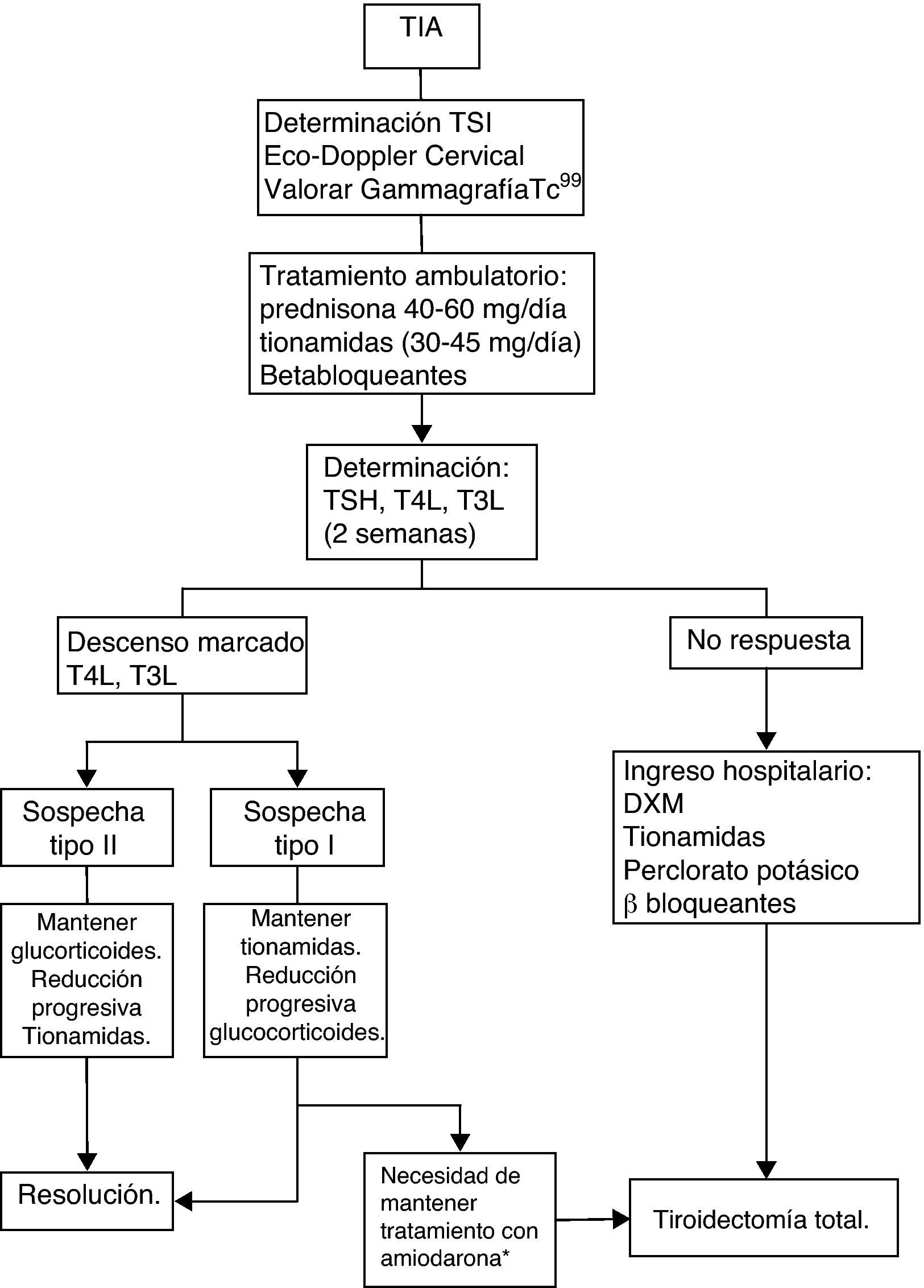
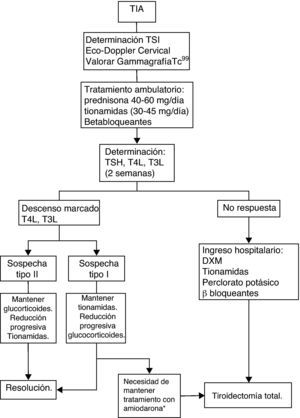
El tratamiento de la TIA tipo I son las tionamidas, este grupo farmacológico inhibe la síntesis de T4 y T3 al interferir en la organificación del yodo1,5,8, la respuesta suele ser más lenta y a más altas dosis que en otras causas de hipertiroidismo con una dosis inicial de metimazol 30-45mg/día. El abordaje terapéutico de la TIA tipo II, consiste en la administración de glucocorticoides por su efecto antiinflamatorio y estabilizador de membrana. No obstante, en la práctica clínica se aconseja iniciar terapia combinada con glucocorticoides y tionamidas, dada la existencia de tipos mixtos de hipertiroidismo, la dificultad de distinguir ambas entidades de forma inicial y la necesidad de un abordaje terapéutico agresivo con normalización rápida de la función tiroidea en estos pacientes con cardiopatía subyacente (fig. 2). En los casos de TIA refractaria se aconseja asociar perclorato potásico2.
El perclorato potásico, es un polvo cristalino blanco o incoloro soluble en agua, que se usa conjuntamente con tionamidas para el tratamiento de las tiroiditis inducidas por yodo. Esta molécula reduce la captación y concentración de yodo y de otros aniones en la glándula tiroidea, mediante la inhibición competitiva de mecanismo de transporte activo (bomba Na+-I+). Así mismo, produce una liberación rápida del yodo acumulado en los folículos tiroideos9. Está indicada para tratar el las TIA tipo I en ausencia de respuesta a tionamidas, ya que aumenta la sensibilidad frente a los fármacos antitiroideos convencionales, también podría ser útil en la TIA mixta o de etiología no aclarada. En trabajos como el de Martino et al10 en pacientes con TIA, sólo en los individuos tratados con una combinación de perclorato potásico (1g/día) y tionamidas (metimazol 40mg/d) se consiguió controlar la tirotoxicosis en la totalidad de los casos, siendo además el tiempo requerido hasta alcanzar el eutiroidismo menor. Estos resultados fueron confirmados por otros estudios, alcanzando el eutiroidismo con la terapia combinada en un periodo de 2-5 semanas11,12. El principal inconveniente de este tratamiento es su toxicidad, como efectos secundarios algunos pacientes presentan náuseas y vómitos, habiéndose descrito la aparición de fiebre y exantemas. Su uso prolongando puede ocasionar efectos adversos graves (anemia aplásica, agranulocitosis, leucopenia, pancitopenia y síndrome nefrótico), por lo que deben realizarse controles hematológicos frecuentes durante el tratamiento. Trotter13 comparó la toxicidad del perclorato y las tionamidas, objetivando agranulocitosis en 0,3% de 1.200 pacientes tratados con perclorato y en 0,94% de 1.0131 pacientes tratados con tionamidas. La incidencia de eventos adversos por perclorato fue del 2-3%, subiendo al 16-18% cuando la dosis era superior a 1g/día13. La descripción en la literatura de 7 casos de anemia aplásica disminuyó el empleo de esta molécula, si bien en todos ellos la dosis era superior a 1g/día y la duración del tratamiento hasta la aparición de los efectos secundarios fue de 2 a 6 meses9. Estos hallazgos justifican que en adultos se aconseje la administración de una dosis diaria de 600mg a 1g vía oral, fraccionada en 3 o 4 tomas, como tratamiento inicial, con una dosis de mantenimiento entre 200 y 500mg/día en varias tomas, y durante un período de tiempo limitado1,14. La retirada de este fármaco está recomendada una vez alcanzado el eutiroidismo, alrededor de las 6 semanas de tratamiento, teniendo en cuenta que una retirada más precoz está relacionada con un alto riesgo de recidiva9.
La indicación o no de supresión del tratamiento con amiodarona es controvertida, los riesgos potenciales y beneficios de su retirada deben ser discutidos conjuntamente con cardiología, su vida media larga no condiciona un efecto beneficioso inmediato y su retirada puede exacerbar la sintomatología de tirotoxicosis por su efecto beneficioso al bloquear el paso de T4 a T3, receptores β adrenérgicos y de T3. Existen diversos estudios en los que la suspensión del fármaco o su mantenimiento no condicionan diferencias en el curso clínico de la TIA15. Nuestra experiencia aboga por la retirada de la amiodarona una vez que se haya controlado la fase inicial de tirotoxicosis franca, siempre que no sea imprescindible para el control de la arritmia1.
En pacientes con tirotoxicosis por exceso de yodo (TIA tipo I) refractarias a terapia convencional, el uso de perclorato potásico junto a tionamidas es una alternativa terapéutica segura y eficaz. En pacientes con formas mixtas la respuesta clínica es variable, sin embargo, su instauración precoz debe plantearse en pacientes con comorbilidades asociadas, dada la morbi-mortalidad potencial de la TIA en pacientes con cardiopatía establecida.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.