INTRODUCCIÓN
El embarazo ectópico representa la implantación de una gestación fuera de la cavidad uterina1. Esta situación patológica se conoce desde el siglo xvii, y presenta una incidencia aproximada de 11-18 casos por cada 1.000 partos1.
Sin lugar a dudas, esta implantación gestacional patológica representa una de las complicaciones más graves del embarazo, y su incidencia se ha visto incrementada notoriamente en los últimos 20 años2,3. Entre los factores etiologicos que se han asociado a este incremento de embarazos ectópicos destacan las lesiones tubáricas secundarias a salpingitis causadas por enfermedades de transmisión sexual (enfermedad pélvica inflamatoria)3, el uso de dispositivos intrauterinos2, el tabaco4 y el empleo de técnicas de reproducción asistida5.
Tres grandes avances diagnósticos han contribuido de forma espectacular a establecer diagnósticos cada vez más tempranos y precisos: la introducción de la ecografía vaginal, la cuantificación de la gonadotropina coriónica humana (hCG) y el empleo de la laparoscopia diagnóstica2. Gracias a estos avances diagnósticos, hemos cambiado nuestra visión clínica de esta afección, desde una situación potencialmente peligrosa para la vida de la paciente a una situación de menor gravedad6,7. Así, la frase de Louis M. Hellmn2 "en una paciente con sospecha de embarazo ectópico nunca dejes que se ponga el sol sin practicarle una laparotomía" ha caído en desuso.
Por otro lado, la introducción de metotrexato para el tratamiento médico del embarazo ectópico ha supuesto una autentica revolución en el enfoque terapéutico de esta enfermedad8,9.
Estos avances suponen todo un reto para el clínico a la hora de enfocar el tratamiento de una gestación ectópica. En primer lugar, hay que decidir si tratar o no el embarazo ectópico (tratamiento expectante). En caso de que se decida instaurar tratamiento, hay que valorar si éste debe ser radical o, por el contrario, debe ser conservador (médico o quirúrgico).
Todos estos avances diagnósticos y terapéuticos han supuesto una autentica revolución en la visión actual del clínico del embarazo ectópico. En el presente estudio se pretende analizar la evolución en la incidencia de esta enfermedad, los factores etiológicos relacionados, el diagnóstico y el enfoque terapéutico en la última década.
MATERIAL Y MÉTODOS
Se ha llevado a cabo un estudio retrospectivo entre enero de 1992 y diciembre de 2001 de las gestaciones ectópicas en nuestro centro (Hospital Clínico Universitario). En todos los casos el diagnóstico inicial de gestación ectópica se estableció de forma no invasiva, empleando la clínica, la ecografía vaginal y la cuantificación de la hCG, tal y como se ha descrito previamente10.
Hasta el año 1996 las opciones terapéuticas emplea-das en nuestro centro eran el tratamiento expectante o el quirúrgico (radical o conservador).
El tratamiento expectante se aplica a las pacientes asintomáticas diagnosticadas de embarazo ectópico por ecografía Doppler transvaginal, que asocian cifras bajas de hCG (< 1.000 mU/ml), que además disminuyen progresivamente en los días posteriores11,12.
El tratamiento quirúrgico se emplea en las pacientes sintomáticas y/o hemodinámicamente inestables, así como en aquellas que presentaban cifras altas de hCG (> 1.000 mU/ml) o en aquellas cuya cuantificación sérica de la hCG, aun siendo baja, ascendía progresivamente2.
A todas las pacientes susceptibles de tratamiento quirúrgico se les ofrece la posibilidad de un tratamiento quirúrgico conservador (salpingotomía lineal) o bien un tratamiento radical (salpingectomía), empleando la vía laparoscópica o la laparotómica.
En todas las pacientes tratadas mediante una técnica quirúrgica conservadora se realiza un control seriado poscirugía de la hCG hasta su negativización2.
Desde 1997 y tras la aprobación por parte del comité ético del hospital, se introdujo la opción de una terapéutica médica con el empleo de metotrexato sistémico2,8. Inicialmente, los criterios de inclusión para el tratamiento médico con metotrexato de una gestación ectópica fueron: paciente hemodinámicamente estable (ausencia de hemorragia activa), imagen ecográfica de menos de 3,5 cm, ausencia de frecuencia cardíaca fetal en caso de presencia de botón embrionario, hCG sérica inferior a 3.000 mU/ml, hemograma, y funciones hepática y renal normales2.
En las pacientes susceptibles de tratamiento médico con metotrexato se empleó una dosis única de 50 mg/m2, administrada por vía intramuscular. Tras el día de la administración del metotrexato (día 0), se determinaba la hCG sérica en los días quinto y décimo, y a partir de ahí de forma semanal. Si no se apreciaba una disminución de, al menos, un 15% en las cifras séricas de hCG a los 10 días, se administraba una nueva dosis de metotrexato, proceso que se repetía hasta comple-tar un máximo de 3 dosis. Asimismo, a las pacientes se les administraban 30 mg de ácido fólico diario (2 comprimidos de 15 mg). Si la paciente estaba clínicamente estable, era controlada ambulatoriamente hasta la negativización de la hCG sérica (< 15 mU/ml).
Si tras un máximo de 3 dosis de metotrexato no se apreciaba una disminución de las cifras séricas de hCG, y/o la paciente pasaba a estar sintomática y/o hemodinámicamente inestable, se pasaba a un abordaje quirúrgico.
Con el paso de los años, y al ganar experiencia tanto en nuestro grupo como a escala internacional13,14, las cifras iniciales de hCG dejaron de tener valor para decidir si la paciente era tratada con una terapia médica (metotrexato sistémico). Asimismo, la presencia de frecuencia cardíaca fetal en el botón embrionario dejó de ser una contraindicación absoluta para el empleo del metotrexato sistémico15.
En el presente estudio, en todos los casos de gestaciones ectópicas acaecidas en nuestro centro en la última década, hemos analizado las siguientes variables: número de embarazos ectópicos/número de partos año, edad de las pacientes, paridad, factores etiológicos relacionados con el embarazo ectópico, amenorrea y clínica en el momento del diagnóstico, hallazgos ecográficos, cifra de hCG en el ingreso, y porcentaje de tratamientos expectante, médico o quirúrgico. En caso de tratamiento médico con metotrexato sistémico se evaluó también el número de dosis de metotrexato necesarias para solucionar el embarazo ectópico, días hasta la negativización de la hCG, porcentaje de casos que precisaron cirugía tras iniciar el tratamiento médico, complicaciones del tratamiento con metotrexato sistémico.
El estudio estadístico se realizó con el test de ANOVA y el independent sample T-test. El análisis fue reali-zado empleando el Statistical Package for Social Science (SPSS 9.0 Inc., Chicago, IL) y se consideró una p < 0,05 como estadísticamente significativa.
RESULTADOS
Durante la década estudiada (enero de 1992-diciembre de 2001) han ocurrido 280 gestaciones ectópicas, lo que representa el 18,5 de todos los partos (n = 15.132) atendidos en nuestro centro durante este período.
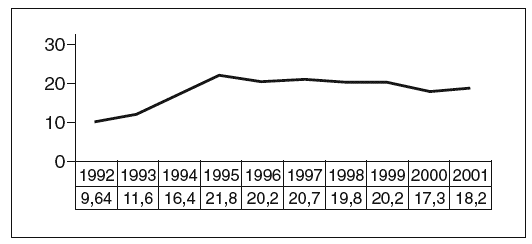
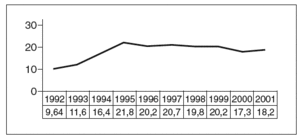
Cuando se analiza la incidencia de gestaciones ectópicas desglosadas por años se observa una diferencia estadísticamente significativa (p < 0,05) entre la incidencia de embarazos ectópicos antes de diciembre de 1994 y los años posteriores, si bien desde el año 1995 hasta el año 2001 la incidencia fue similar en todos los años estudiados (p > 0,05) (fig. 1).
Fig. 1. Incidencia de gestaciones ectópicas por años.
La edad de las pacientes que presentaron una gestación ectópica osciló entre 18 y 43 años (media, 31 años; mediana, 32 años). Sólo el 25% de las pacientes de nuestro centro tenía más de 35 años. La gestación ectópica tubárica (98,6%) representó la variedad clínica más frecuente de forma estadísticamente significativa (p < 0,05). Hubo, además, 2 gestaciones ectópicas cervicales (0,7%), una gestación ectópica ovárica (0,35%) y un embarazo ectópico cornual (0,35%). Hay que destacar, también, la presencia de 2 embarazos heterotópicos (gestación intrauterina junto con gestación extrauterina); en ambos casos el embarazo ectópico fue de localización tubárica.
Respecto a factores de riesgo presentes en las pacientes con embarazo ectópico, sólo 61 pacientes (21,8%) no presentaron ningún factor de riesgo. Entre las restantes 219 pacientes (78,2%) concurrieron 1 o más factores de riesgo (p < 0,05). El factor encontrado con más frecuencia en nuestras pacientes fue el tabaco (> 10 cigarrillos/día), presente en el 47,8% de las pacientes con algún factor de riesgo (p < 0,05). En segundo lugar, destaca la cirugía pélvica o abdominal, presente en el 22,3% de las pacientes con factores de riesgo. En tercer lugar, se encuentran las infecciones genitales debidas a enfermedades de transmisión sexual (ETS), presentes en el 12,9% de las pacientes con antecedentes de riesgo. Otros factores presentes fueron: llevar implantado un DIU (7,2%), haber seguido terapias de reproducción asistida (TRA) (16,7%) y haber presentado un embarazo ectópico previo (8,4%).
Cuando se valoró la evolución de los diferentes factores de riesgo en esta última década, se observó que el tabaco representaba el factor más frecuente en todos los años, y su incidencia no variaba (un 50% de los casos en el año 1992 y el 50% en el año 2001). Respecto a los otros factores implicados, es destacable una disminución significativa (p < 0,05) en los casos relacionados con infecciones genitales debidas a ETS (un 20% en el año 1992 y un 6,2% en el año 2001). Por el contrario, se observa un aumento significativo (p < 0,05) de los casos relacionados con TRA (un 0% casos en el año 1992 y un 12,5% en el año 2001).
Es reseñable que los 2 heterotópicos y los 2 ectópicos cervicales se produjeron en pacientes sometidas a técnicas de fertilización in vitro, con transferencia intrauterina de embriones. En 104 casos (37,1%) la gestación ectópica ocurrió en pacientes nuligestas. En los restantes 176 casos (62,9%) la gestación ectópica ocurrió en pacientes que habían gestado previamente (p < 0,05). En este grupo de pacientes, la media de gestaciones previas al ectópico fue de 1,9 (rango, 1-7 gestaciones). El porcentaje de pacientes con problemas de infertilidad ($ 3 abortos) fue del 2,8%.
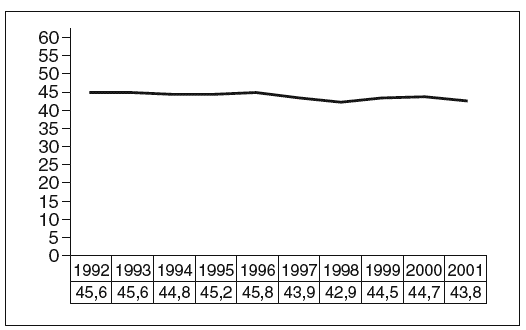
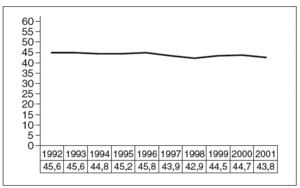
La aplicación de las diferentes técnicas diagnósticas en el campo de la gestación ectópica pone de manifiesto que realizamos el diagnóstico prácticamente con la misma edad gestacional en el año 2001 (amenorrea media, 43,8 días; rango, 38-50 días) que en el año 1992 (amenorrea, 45,6 días; rango, 40-53 días) (p > 0,05). La figura 2 representa la evolución en términos de edad gestacional en el momento del diagnóstico durante esta última década.
Fig. 2. Evolución en términos de edad gestacional en el momento del diagnóstico.
La presentación clínica del embarazo ectópico pone de manifiesto que sólo 8 (2,8%) de todos los casos se presentaron como un cuadro de shock hipovolémico. Entre los restantes 272 (97,2%) casos, el síntoma más frecuente fue el dolor abdominopélvico (un 71,9% de las pacientes lo presentó), seguido de la metrorragia (un 58,2% de los casos). Sólo el 42% de las pacientes presentaba la tríada clínica clásica de dolor, amenorrea y metrorragia.
En esta última década estudiada, no hemos tenido ninguna muerte materna relacionada con una gestación ectópica.
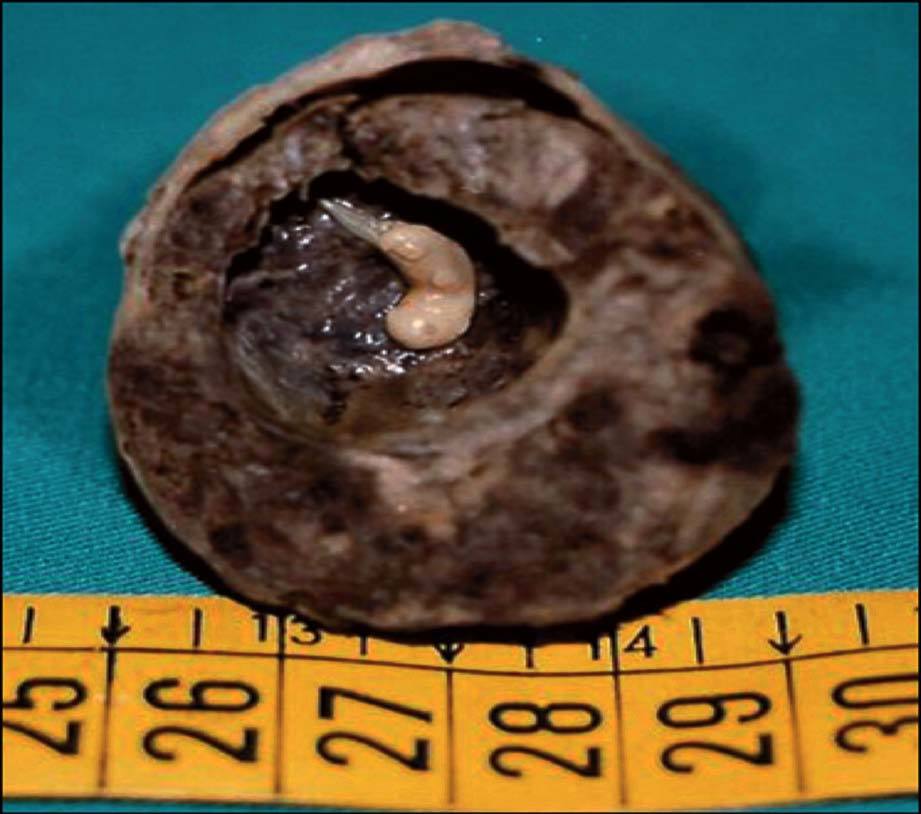
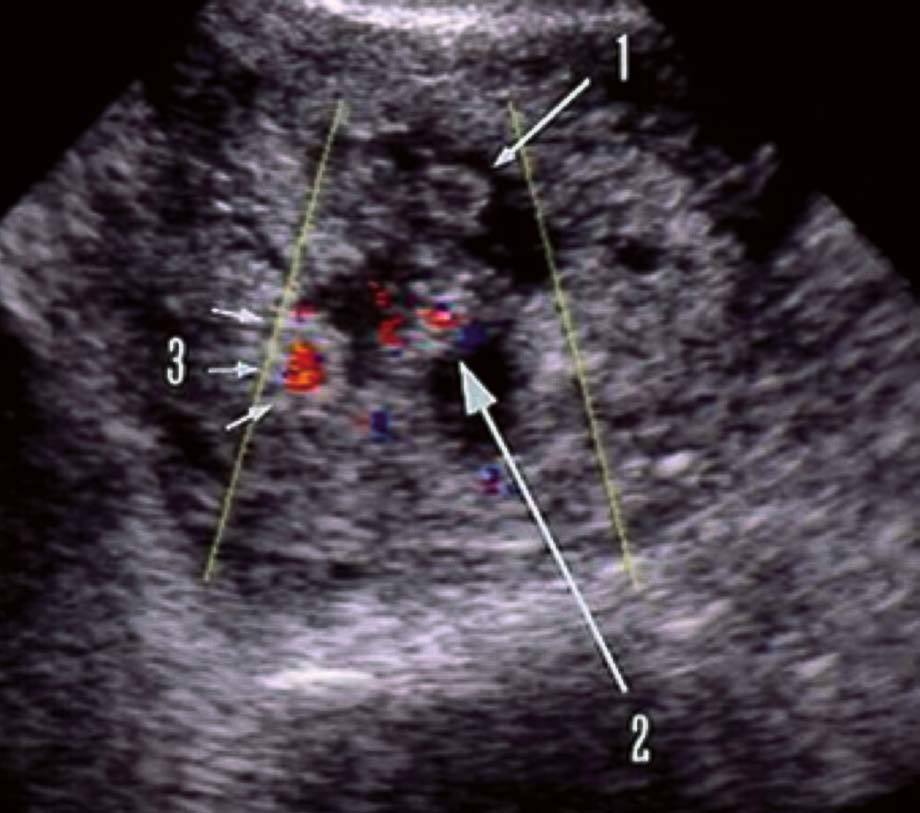
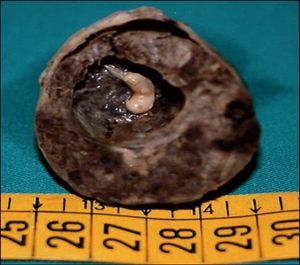
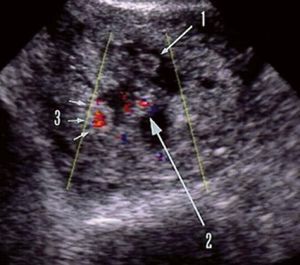
Todas las pacientes fueron sometidas a un estudio ecográfico transvaginal y en el 87,7% de los casos se identificó una masa anexial anormal sugestiva de gestación ectópica. En los demás casos (12,3%) el estudio ecográfico no identificó el embarazo ectópico, sólo refería ausencia de gestación intrauterina. Sólo en 12 casos (el 4,3% de todos los casos) se observó la presencia de un embrión con frecuencia cardíaca fetal positiva (fig. 3). Asimismo, el estudio ecográfico puso de manifiesto la presencia de hemoperitoneo (líquido en el saco de Douglas positivo) en el 50,7% de los casos.
Fig. 3. Embrión con frecuencia cardíaca fetal positiva.
Las cifras de hCG en el ingreso fueron inferiores a 1.000 mU/ml en el 16% de las pacientes, de 1.000 a 3.000 mU/ml en el 65% de los casos y superiores a 3.000 en el 19% de los casos.
Durante estos 10 años el porcentaje de embarazos ectópicos tratados exitosamente de forma expectante ha permanecido estable, lo que representa el 10,7% de todos nuestros casos. Por tanto, el 67% de los ectópicos etiquetados inicialmente de involutivos no requirió tratamiento, mientras que el 33% requirió de tratamiento médico o quirúrgico.
Un total de 214 casos fueron tratados quirúrgicamente mediante laparotomía o bien mediante laparoscopia. En 95 casos (un 33,9% de los casos tratados quirúrgicamente) se realizó un tratamiento conservador (salpingotomía), dado que la paciente deseaba conservar su fertilidad. En 75 de estos casos se realizó un control histerosalpingográfico de la permeabilidad tubárica, que fue positivo en la trompa tratada quirúrgicamente en 63 pacientes (84%).
Desde 1997, y tras la introducción del tratamiento médico con metotrexato, hemos observado un incremento significativo (p < 0,05) de los casos tratados de forma no invasiva mediante un tratamiento médico (del 13,9% de los casos en 1997 al 28,1% en 2001). Por consiguiente, hemos notado una disminución significativa (p < 0,05) de los ectópicos tratados quirúrgicamente (del 75,1% de los casos en 1997 al 59,4% en 2001).
Por tanto, desde 1997 hemos tratado 36 casos de gestaciones ectópicas con metotrexato sistémico. Sólo en 4 de los 36 casos (11%) se requirió cirugía tras el tratamiento médico inicial. En los restantes casos se requirió una media de 28 días (rango, 17-42) hasta la negativización de la hCG. Es destacable que la cifra de hCG aumenta durante los primeros días tras la administración del metotrexato (quinto días posmetotrexato).
En 12 pacientes se realizó un control histerosalpingográfico de la permeabilidad tubárica tras el tratamiento médico con metotrexato, y se observó permeabilidad en la trompa afectada en 10 de los 12 casos (83,3%). Por tanto, al comparar la permeabilidad tubárica tras el tratamiento médico o quirúrgico conservador, no hemos apreciado diferencias significativas (p > 0,05).
DISCUSIÓN
En la mayoría de los países industrializados la frecuencia de gestaciones ectópicas se ha triplicado en los últimos 20 años1,2. Sin embargo, su incidencia parece haberse estabilizado en la década de 19903,15,16.
El presente estudio confirma esta tendencia, ya que si bien encontramos un incremento significativo de ectópicos entre el inicio de la década de 1990 (enero de 1991 a diciembre de 1994) con respecto a los años posteriores, desde enero de 1995 a diciembre de 2001 la incidencia de gestaciones ectópicas se estabilizó. Esto supone que, en la actualidad, la incidencia de gestaciones ectópicas en nuestro centro se sitúe en un 18,5 partos, cifra similar a la presentada por estudios recientes3.
El embarazo ectópico es una enfermedad multifactorial16. Entre los factores de riesgo se pueden diferenciar 2 grandes grupos:
1. Factores de riesgo potencialmente accesibles y, por tanto, susceptibles de modificarse mediante medidas de prevención: secuelas de infecciones genitales debidas a ETS, iatrogenia (TRA) y tabaco.
2. Factores de riesgo poco accesibles y, por tanto, difícilmente modificables por las medidas de prevención: cirugía pélvica, antecedentes de embarazo ectópico, edad materna, etc.
En el presente estudio se ha comprobado que la mayoría de las pacientes con gestaciones ectópicas (78,2%) presentaban uno o varios factores de riesgo. Asimismo, llama poderosamente la atención que el factor de riesgo relacionado con más frecuencia fue el tabaco y que su relación con el ectópico no se ha visto modificada en la última década. Teniendo presente que en la actualidad se considera que el tabaco es la causa del 20% de los ectópicos1,4,16 y que puede modificarse, se debería hacer un esfuerzo para concienciar a las mujeres de suspender el consumo de tabaco durante el período concepcional.
Otro dato interesante del presente estudio es la disminución significativa de ectópicos relacionados con las secuelas de ETS en la última década en nuestro medio. Esto probablemente guarda relación con las campañas de prevención del sida mediante el empleo de métodos barrera (preservativo) y, por consiguiente, otras ETS16.
Debe, asimismo, llamarse la atención al aumento significativo de embarazos ectópicos relacionados con las TRA. Estudios previos han demostrado que una mujer sometida a TRA tiene un riesgo 3 veces mayor de presentar un embarazo ectópico que la población general17-19. Además, en nuestro centro hemos pasado de aproximadamente 100 ciclos de inducción de la ovulación en el año 1991 a más de 1.000 en 2001. Todo esto permite comprender el aumento de embarazos ectópicos relacionados con las TRA en esta última década.
Estudios previos han planteado que la gestación ectópica es 5 veces más frecuente en mujeres mayores de 35 años16. En nuestro estudio, sin embargo, sólo el 25% de las pacientes eran mayores de 35 años. Es importante destacar que la relación con la edad está basada únicamente en la exposición más larga a los factores de riesgo, por lo que en la actualidad este factor es discutido16.
La forma clínica más frecuente de gestación ectópica fue el embarazo tubárico (el 98,6% de los casos), en consonancia con estudios previos, lo que demuestra que la localización tubárica es la más frecuente con diferencia20,21. La mayoría de las formas poco frecuentes de embarazos ectópicos (heterotópicos, cervicales, etc.) descritas en el presente estudio ocurrieron en pacientes sometidas a TRA. Esto es consecuente con publicaciones previas sobre formas infrecuentes de embarazos ectópicos en TRA, donde se demuestra un aumento de formas hasta ahora inusuales de estos embarazos entre estas pacientes22,23.
Los antecedentes obstétricos como paridad o pérdidas gestacionales precoces espontáneas (> 3 abortos) no guardaron ninguna relación con la génesis del embarazo ectópico, lo que concuerda con estudios previos en los que no se demostró relación alguna entre los antecedentes obstétricos y la paridad16,24. El único antecedente obstétrico relacionado con los embarazos ectópicos es la práctica de una interrupción voluntaria del embarazo25, aunque los resultados de este estudio son contradictorios y no se han confirmado posteriormente16.
El gran abanico de formas de presentación clínica del embarazo ectópico dificulta su diagnóstico. Así, la tríada clínica clásica de amenorrea, dolor abdominal y metrorragia no está siempre presente26. De este modo, por ejemplo, la amenorrea no es siempre reconocida por la paciente, ya que las metrorragias asociadas al embarazo ectópico con frecuencia se confunden con menstruaciones "raras"26. Sin embargo, el desarrollo de técnicas inmunológicas (cuantificación sérica de hCG) y el perfeccionamiento de la ecografía vaginal han permitido establecer diagnósticos cada vez más precisos y tempranos26.
Pese a todos los avances mencionados anteriormente, nuestro estudio demuestra que los embarazos ectópicos se diagnostican prácticamente en la misma edad gestacional en la actualidad que hace 10 años, lo que, a nuestro entender, tiene una explicación sencilla: la gran mayoría de los embarazos ectópicos son diagnosticados en urgencias cuando la paciente consulta por presentar alguna clínica que considera anómala en el primer trimestre de su gestación. Por otro lado, las gestaciones con controles más precisos (p. ej., pacientes de reproducción asistida) son susceptibles de diagnósticos más tempranos.
El embarazo ectópico representa la primera causa de mortalidad materna durante el primer trimestre de gestación en los países industrializados27,28. Afortunadamente, en esta última década no hemos tenido ninguna muerte materna relacionada con una gestación ectópica. Además, sólo 8 de los 280 ectópicos (2,8%) cursaron con un cuadro de shock hipovolémico.
La clínica por la que consultó la paciente con más frecuencia fue el dolor abdominal (71,9%), seguido de la metrorragia (58,2%). Sólo el 42% de nuestras pacientes cumplía la tríada clínica clásica de dolor, amenorrea y metrorragia. Todos estos datos son similares a los presentados en estudios previos3,7,26.
El diagnóstico de la gestación ectópica se ha beneficiado de los progresos recientes de la ecografía vaginal. Tal y como se ha apuntado previamente, la mayoría de las situaciones actuales de diagnóstico del embarazo ectópico no se corresponden con la tríada clínica clásica. Así, se ha desarrollado una nueva aproximación semiología basada en una tríada clínica-biológica-ecográfica.
Los estudios ecográficos vaginales nos han permitido identificar el 87,7% de los embarazos ectópicos como una masa anexial anómala. En el 12,3% el embarazo ectópico se identificó por la ausencia de gestación intrauterina junto con el análisis bioquímico (hCG) y la clínica. Sólo en un 4,3% visualizamos una frecuencia cardíaca fetal positiva en la gestación ectópica. Estos datos permiten entender la ecografía como un arma imprescindible en el diagnóstico del embarazo ectópico, tal y como apuntan todos los estudios en este campo29-31.
Otro de los avances de los últimos años que han contribuido al diagnóstico del embarazo ectópico ha sido la determinación sérica de la hCG32. Es importante destacar que esta determinación realmente adquiere valor al combinarla con la ecografía33,34, dado que la determinación aislada de hCG no permite diferenciar el embarazo ectópico de gestaciones intrauterinas en las primeras semanas de gestación32. En nuestro estudio el 65% de las gestaciones presentó en el momento del diagnóstico una cifra de hCG entre 1.000 y 3.000 mU/ml, dato similar al presentado por publicaciones anteriores35. Asimismo, cuando las cifras de hCG son bajas (< 1.000 mU/ml), la combinación de los datos ecográficos y clínicos, y la curva evolutiva de la hCG permite identificar los embarazos ectópicos involutivos, que no precisan tratamiento, de los evolutivos, que sí lo precisan34.
Desde 1955 en que Lund36 describió que un porcentaje de embarazos ectópicos involucionaban espontáneamente, se abrió la puerta al tratamiento expectante de la gestación ectópica. En nuestra casuística el 10% de los embarazos ectópicos fueron susceptibles de un tratamiento expectante. Hay que destacar, además, que las cifras de embarazos involutivos han permanecido estables en esta década en nuestro centro.
Es evidente que el desarrollo de las técnicas diagnósticas ha permitido visualizar embarazos ectópicos que hasta fechas recientes pasaban inadvertidos. Asimismo, la actitud expectante permite evitar cualquier tratamiento (tanto quirúrgico como médico) en embarazos ectópicos que cursen con cifras bajas de hCG (< 1.000 mU/ml), que además presentan una regresión espontánea en los días siguientes.
Diversos estudios prospectivos han permitido confirmar que entre el 10 y el 20% de todos los embarazos ectópicos evolucionan hacia la regresión espontánea sin necesidad de tratamiento37-39. Además, del 60 al 70% de los embarazos ectópicos que cursaron inicialmente de forma asintomática y con cifras baja de hCG permitieron una actitud de abstención terapéutica. Todos estos estudios reflejan, por tanto, datos similares a los encontrados en el presente estudio.
La decisión entre adoptar un tratamiento quirúrgico conservador o radical en casos de embarazos ectópicos, es un viejo dilema que todavía hoy tiene cierta vigencia40. El primer tratamiento que se empleó en un embarazo ectópico fue radical (salpinguectomía), justificado por el hecho de que durante una época esta afección suponía un gran riesgo vital. Sin embargo, a partir de los años cincuenta apareció el tratamiento quirúrgico conservador, dado que los avances diagnósticos permitían detectar esta enfermedad antes de la rotura tubárica40.
En la actualidad, se puede realizar un tratamiento conservador en la gran mayoría de las pacientes, con excepción de los casos en que la alteración tubárica no permita una correcta cicatrización. Nosotros practicamos siempre la salpingotomía (donde no se sutura la trompa) dado que estudios previos demostraron que ésta, no sólo no mejoraba la cicatrización tubárica, sino que por el contrario podía favorecer las adherencias y la alteración de la luz tubárica41.
Es importante destacar que, en nuestra experiencia, el factor que marca fundamentalmente la realización de una cirugía conservadora es el deseo de la paciente de mantener su fertilidad. Así, muchas de nuestras pacientes solicitan una cirugía radical (salpinguectomía) asociada a una esterilización contralateral. En este sentido, el Colegio Americano de Obstetra-Ginecólogos (ACOG) sólo aconseja la cirugía conservadora en los casos de pacientes que deseen mantener su fertilidad42.
La experiencia obtenida de diversos estudios prospectivos internacionales señala que la posibilidad de recidiva de un embarazo ectópico es similar si se ha practicado una cirugía unilateral radical (salpinguectomía) o conservadora (salpingotomía); ésta se sitúa entre un 7 y un 8% de los casos43-45.
En 1982, Tanaka et al46 describieron el primer caso de tratamiento médico con metotrexato de un embarazo ectópico por vía sistémica. Este fármaco es un antagonista del ácido fólico por inhibición estequiométrica de la enzima dihidrofolato reductasa, y así conlleva una carencia de tetrahidrofolato47. A escala celular, el metotrexato utiliza el sistema de transporte activo de membrana de los folatos reducidos y desarrolla su acción principalmente en co del embarazo ectópico ha experimentado un auge progresivo desde el año 1997; actualmente cerca del 30% de los embarazos ectópicos se tratan mediante el empleo de metotrexato sistémico en nuestro centro. Estos datos son consecuentes con la experiencia internacional, que señala que entre el 30 y el 40% de los embarazos ectópicos deberían ser susceptibles de tratamiento médico con metotrexato sistémico2,3,14.
Sólo el 11% de los casos tratados en nuestro centro con metotrexato sistémico requirieron un posterior tratamiento quirúrgico. Estas cifras son similares a las presentadas en estudios previos2,3,14. Además, en nuestra experiencia, el tiempo medio para la negativización de la hCG tras la administración de metotrexato sistémico fue de 28 días, dato similar al presentado en otros estudios9.
Consideramos que actualmente el tratamiento médico del embarazo ectópico con metotrexato nos ayuda a solucionar cerca del 40% de todos los ectópicos y posiblemente la línea futura es el empleo del metotrexato vía oral. Así, ya hay estudios preliminares que demuestran buenos resultados con el empleo oral de metotrexato en esta enfermedad48,49.
En la actualidad, tal y como hemos reflejado anteriormente, ante el diagnóstico de un embarazo ectópico, el clínico debe inicialmente plantearse si tratarlo o no y en caso de decidir tratarlo plantear un tratamiento médico o quirúrgico. Así, tal y como apuntaban Balasch y Barri, en 19942, el embarazo ectópico se ha convertido en un verdadero dilema para el clínico. El presente estudio, creemos, nos ayudará a entender mejor esta enfermedad y ver su evidente evolución en esta última década.