En procedimientos quirúrgicos de las regiones supraclaviculares y laterales cervicales, así como en cirugías cardíacas y mediastínicas, la función diafragmática puede comprometerse desde la base del riesgo de lesión del nervio frénico y/o la raíz C4. Son escasas las publicaciones que tratan la estimulación intraoperatoria de estas estructuras nerviosas para evaluar su funcionalidad y, en nuestro conocimiento, hasta ahora no se ha hipotetizado acerca de si es posible reducir las tasas de lesión situadas en hasta el 26% en algunos estudios de cirugía cardíaca.
Describimos la técnica empleada para la monitorización neurofisiológica del nervio frénico. Asimismo, se discute su utilidad y ventajas respecto a otras técnicas.
Concluimos que con la incorporación creciente de la monitorización neurofisiológica intraoperatoria en los últimos años, es posible su aplicación al nervio frénico en los procedimientos en los que se considere que existe riesgo de lesión del mismo y, con ella, puede ser factible la reducción de las tasas de lesión iatrógena.
In surgical procedures of the supraclavicular and lateral cervical regions, as well as in cardiac and mediastinal surgeries, diaphragm function can be compromised by the risk of injury to the phrenic nerve and/or the C4 root. There are few publications that treat the intraoperative stimulation of these nerve structures to evaluate their functionality and, to our knowledge, until now it has not been hypothesized about whether it is possible to reduce the injury rates, which reach 26% in some cardiac surgery studies.
We describe the technique used for the neurophysiological monitoring of the phrenic nerve. Also, its usefulness and advantages over other techniques are discussed.
We conclude that, with the increasing incorporation in recent years of intraoperative neurophysiological monitoring, its application to the phrenic nerve is possible in procedures with a risk of injury and, thus, the reduction of iatrogenic injury rates may be feasible.
La función diafragmática puede comprometerse durante procedimientos quirúrgicos en las inmediaciones del nervio frénico (NF) y/o de la raíz C4 desde la base del riesgo de su lesión, a menudo de forma inadvertida. Dichas estructuras, con frecuencia, son difíciles de localizar; además, su visualización directa, aunque es de gran ayuda en un intento de preservarlas, no garantiza el respeto de su funcionalidad, ya que diferentes mecanismos como la tracción, sujeción, contusión, compresión, el daño térmico, o incluso la presión de vacío, pueden producir su lesión aun con preservación macroscópica de la integridad neural (grados I a IV de la clasificación de lesión nerviosa periférica de Sunderland1).
Son escasas las publicaciones que tratan la estimulación intraoperatoria del NF para evaluar la continuidad de la vía nerviosa. Además, algunos métodos propuestos de comprobación de la subsecuente contracción diafragmática son subjetivos, como la palpación de la región subcostal en hipocondrio ipsilateral2, o indirectos, a través de artefactos registrados en la capnografía3,4 y curvas de presión-tiempo del respirador4.
La monitorización neurofisiológica intraoperatoria (MNIO) ha experimentado un crecimiento exponencial en los últimos 20 años. Se ha convertido en una herramienta objetiva y útil, cuyo principal objetivo es la prevención de daño neurológico; prácticamente, es aplicable a cualquier estructura nerviosa, central o periférica, que pueda ponerse en riesgo durante un determinado procedimiento quirúrgico y el NF no debe suponer una excepción. A continuación, describimos la técnica empleada para la monitorización neurofisiológica de este nervio.
TécnicaLa MNIO del NF puede realizarse en aquellos procedimientos quirúrgicos donde, a criterio del cirujano, exista riesgo de lesión del mismo, en especial en cirugías cardíacas, mediastínicas, a nivel supraclavicular, así como en regiones cervicales, sobre todo en caso de vaciamientos ganglionares laterales; en estas últimas regiones anatómicas, la MNIO puede extenderse a la raíz C4.
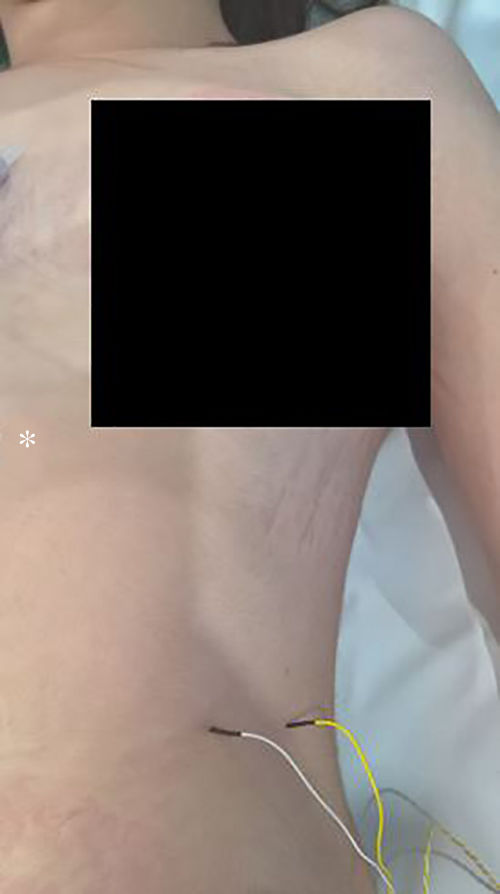
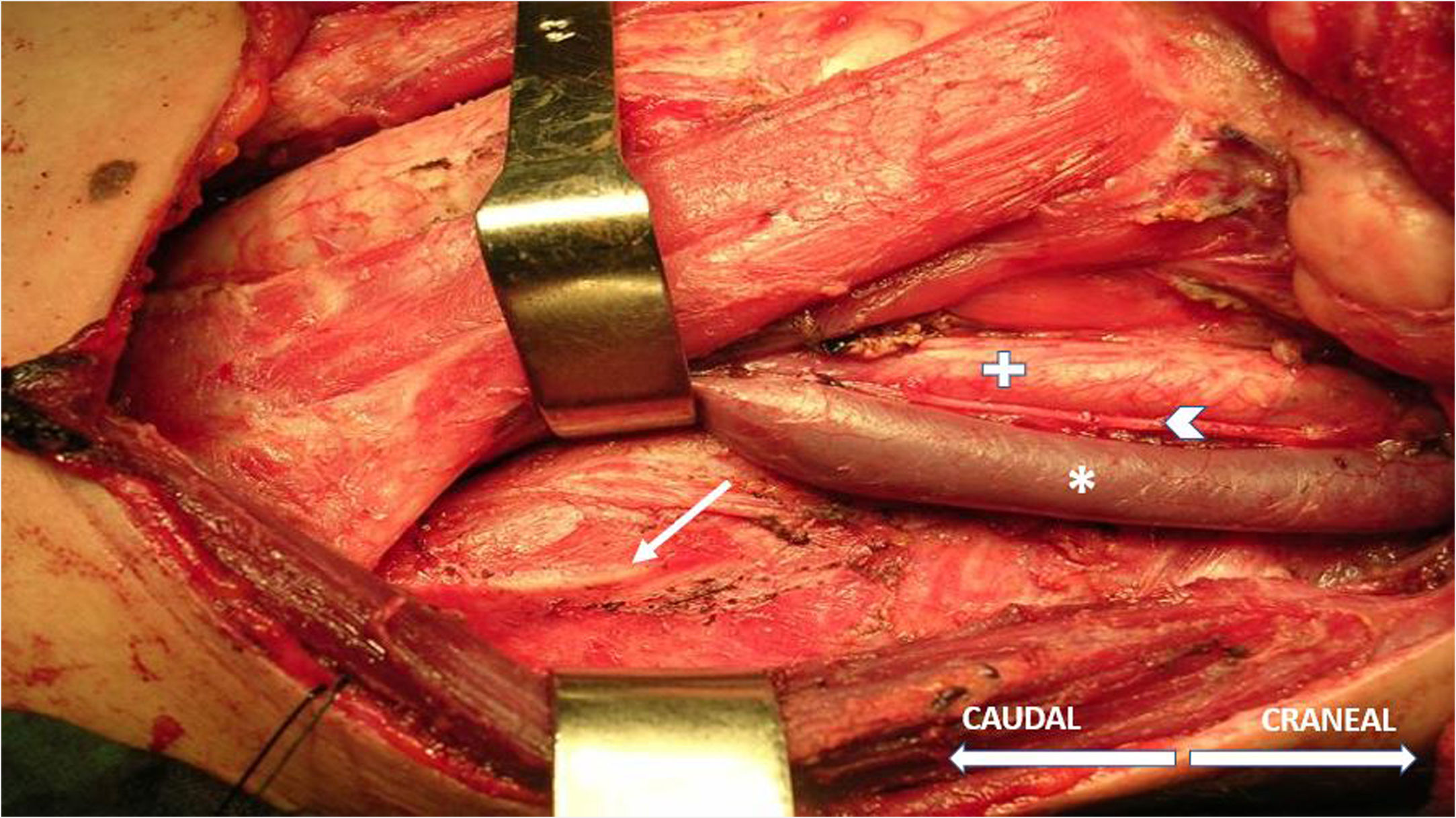
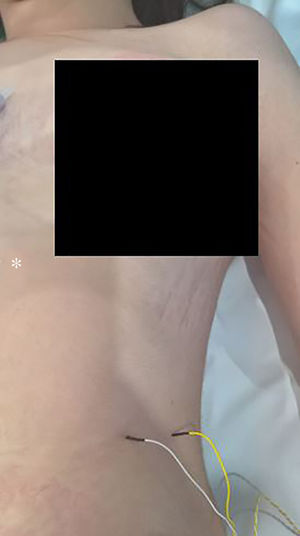
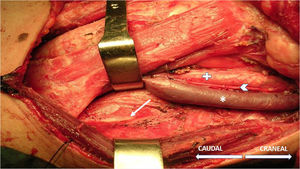
La técnica comienza, tras la inducción anestésica, con la palpación del 7.o u 8.o espacios intercostales, situados a unos 16cm siguiendo el margen costal desde la punta de la apófisis xifoides5. En ese punto se insertan los electrodos de aguja de registro: el activo, en línea medioclavicular, adyacente a la articulación costocondral; y el de referencia, lateral a unos 2cm, en línea axilar anterior (fig. 1); se coloca un electrodo más de tierra en la apófisis xifoides, y se comprueba que las impedancias no superen los 5kΩ. El estímulo sobre el NF y/o raíz C4 se realiza, de forma intermitente, con una sonda monopolar manejada por el cirujano a intensidades habituales de 2-3mA (3pulsos/s; duración del estímulo: 200ms) para el mapeo por zonas en su identificación (fig. 2) y a 1-1,5mA, una vez localizado, para valorar su funcionalidad cuando se considere oportuno. En cirugías cardíacas y mediastínicas, además es posible la colocación de electrodos de aguja adicionales de estímulo en la fosa supraclavicular (borde posterior del esternocleidomastoideo con el cátodo a 3cm de la clavícula y el ánodo 2cm superior al primero5), lo que permite una estimulación más continuada del NF (1,5pulsos/s; duración del estímulo: 50ms; intensidad supramáxima con ajuste a partir de unos 10mA), a criterio del neurofisiólogo, en especial tras maniobras de riesgo en sus proximidades, y que posibilita conocer el momento de la lesión en caso de producirse.
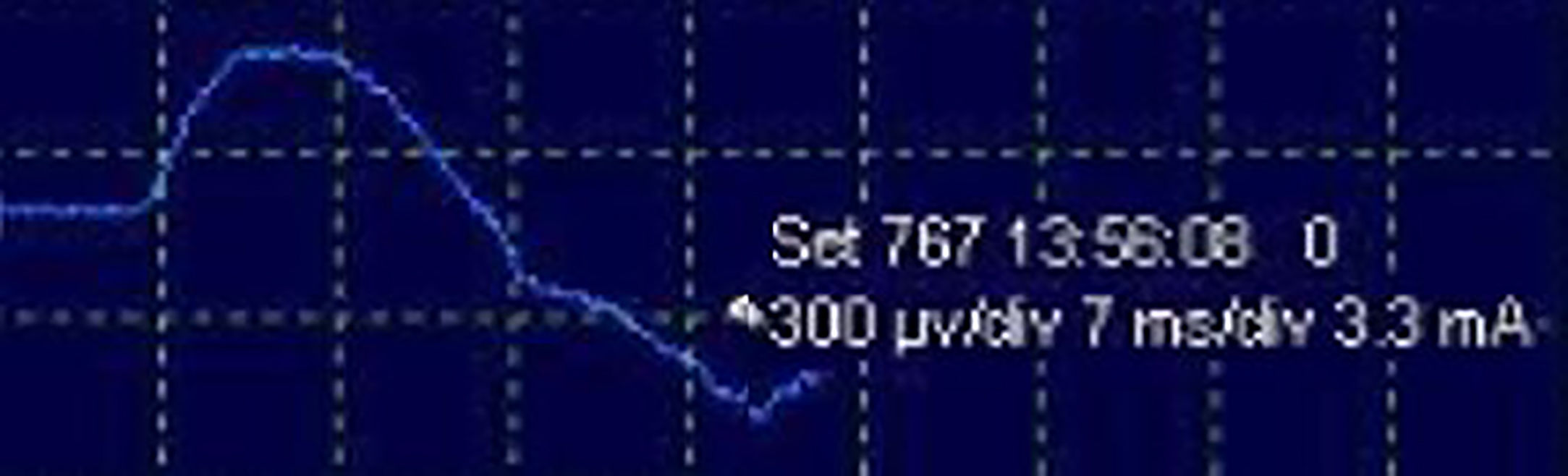
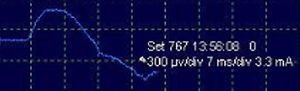
Tras el estímulo de la vía nerviosa en cualquier punto (NF-raíz C4), ya sea en sus modalidades intermitente (filtros: de baja frecuencia, 20Hz; de alta, 3kHz) o continua (filtros: de baja frecuencia, 10Hz; de alta, 1kHz), se obtiene el potencial de acción muscular compuesto (PAMC) del NF (fig. 3) con una amplitud media, por lo general, superior a 300μV (la latencia es variable según en qué punto de la vía nerviosa se realice el estímulo; alrededor de 6,5ms desde niveles más proximales, en cuello5). La dinámica de trabajo durante la MNIO consiste en detectar cambios neurofisiológicos significativos (disminución en >50% de amplitud y/o aumento de >10% de la latencia del PAMC basal), correlacionarlos con las maniobras quirúrgicas de riesgo que han podido producirlos y alertar al cirujano en ese caso, quien tomará las precauciones oportunas en un intento de revertirlos para minimizar, así, la posibilidad de déficit neurológico postoperatorio. Si se detectase interrupción en la transmisión del estímulo a lo largo de la vía nerviosa, lográndose desencadenar un PAMC con estímulo más distal (indicativo de lesión segmentaria), sería posible mediante mapeo, desde niveles distales hacia proximales, localizar el punto exacto de la lesión con el fin de intentar su reparación en caso de apreciarse solución de continuidad en dicho punto.
Para poder aplicar la técnica existen una seria de puntos a tener en cuenta, algunos comunes a cualquier otro procedimiento de MNIO, como son la estrecha colaboración y adecuada comunicación con el equipo quirúrgico y el anestesista; este último, además, debe emplear un régimen de anestesia total intravenosa y evitar la administración de relajantes musculares, ya que interfieren en el registro del PAMC, así como, en la medida de lo posible, otros agentes tales como gases halogenados6. Un aspecto particular de dificultad técnica ocurre en aquellos pacientes con sobrepeso u obesos, con abdómenes voluminosos, que dificultan un acercamiento adecuado de los electrodos de registro al diafragma, una vez insertados; esto puede resolverse, al menos parcialmente, con la utilización de electrodos de aguja de mayor longitud y/o aumentando la sensibilidad en la adquisición del PAMC. Este problema no existe en cirugías cardíacas en las que es el cirujano quien inserta, e incluso sutura directamente, los electrodos en el diafragma.
DiscusiónLa mayor parte de publicaciones acerca de la estimulación del NF son relativas al tratamiento de pacientes con hipoventilación alveolar central (por ejemplo, tras lesión medular cervical alta) como alternativa a la ventilación mecánica; básicamente, se trata del implante quirúrgico de un electrodo en el NF, en cuello o tórax, que tras el estímulo eléctrico del mismo causa la contracción diafragmática7,8. Sin embargo, son pocos los grupos de estudio que han intentado la estimulación eléctrica intraoperatoria del NF y/o la raíz C4, con la finalidad de valorar su integridad funcional durante el curso de diferentes procedimientos quirúrgicos2-4 y solamente uno con metodología similar a la que proponemos nosotros9. En ninguno de ellos se hipotetiza acerca de si es posible reducir las tasas de lesión del NF, situadas en hasta el 26% en algunos estudios de cirugía cardíaca9,10.
La lesión bilateral del NF genera un importante trastorno respiratorio restrictivo, con habitual necesidad de ventilación mecánica no invasiva11, mientras que la lesión unilateral, en general, tiende a ser bien tolerada2, en especial en ausencia de comorbilidad. No obstante, la pérdida de tono muscular de un hemidiafragma es suficiente para alterar la presión diferencial entre los compartimentos abdominal y torácico, lo que genera una reducción del volumen de este último y que puede empeorar aún más por la migración superior del contenido abdominal, sobre todo durante la posición de decúbito supino12. Así, pueden coexistir ortopnea y reflujo gastroesofágico asociados a diversos grados de disnea y trastorno respiratorio del sueño con relación al déficit restrictivo13. Cabe destacar que, en caso de lesión iatrógena, dicha sintomatología será más relevante por iniciarse en el periodo postoperatorio inmediato de un procedimiento quirúrgico mayor, habiéndose constatado asociación con mayores tasas de atelectasias, neumonías, derrames pulmonares, así como dificultad en el destete del respirador y estancias más prolongadas en la UCI10.
En la evaluación de la función de una vía nerviosa susceptible de lesión durante un determinado procedimiento quirúrgico, sin duda la MNIO constituye el método de elección, ya que los parámetros que proporciona son objetivos, reproducibles y cuentan, por lo general, con valores normativos establecidos cuya desviación significativa de los mismos definirá la anormalidad. Además, en el caso concreto de la raíz C4 y/o el NF, el registro de su PAMC dota a la técnica de mayor precisión con respecto a otras descritas, en las que los métodos de comprobación de la contracción diafragmática, por ser subjetivos (palpación de la región subcostal en hipocondrio ipsilateral2) o indirectos (a través de artefactos registrados en la capnografía3,4 y curvas de presión-tiempo del respirador4), presentan, presumiblemente, tasas más elevadas de falsos negativos y positivos, respectivamente.
Por otro lado, durante la MNIO, dado que la adquisición e interpretación de las señales se produce en tiempo real, en caso de detectar cambios neurofisiológicos (tras descartar que estén en relación con la administración de fármacos y comprobar la adecuada integridad del sistema), muchos de ellos reversibles, se puede establecer una correlación con las maniobras quirúrgicas de riesgo, con alta sensibilidad y especifidad6, lo que posibilita una toma de decisiones con el fin de evitar déficit neurológico postoperatorio. Si a pesar de todo esfuerzo dicho objetivo principal no se consiguiese, la MNIO también permite una primera aproximación fisiopatológica (lesión probablemente desmielinizante/axonal o mixta; completa/incompleta), debiéndose confirmar todo ello, en última instancia y en un segundo tiempo, mediante estudio con electroneurografía y electromiografía del NF y diafragma, respectivamente10,13; todo ello es fundamental, tanto para emitir un pronóstico del déficit (grado, transitorio/permanente) como para complementar el soporte documental de la MNIO en caso de litigio, algo cada vez más en boga. Otras ventajas teóricas son la ayuda en la localización y disección del NF, de especial importancia si el motivo de la intervención es una lesión neoformativa que distorsiona la normal anatomía, se trata de una reintervención o el paciente ha recibido radioterapia previamente. Asimismo, desde la base de lo previo, puede facilitar una mayor radicalidad de la intervención, si se precisa.
Probablemente, el principal factor limitante en la aplicación de la NMIO del NF y/o raíz C4 sea la accesibilidad a un adecuado equipo de monitorización y, sobre todo, la presencia de un neurofisiólogo clínico en el quirófano con experiencia en MNIO, no disponible siempre. No obstante, los procedimientos quirúrgicos donde tiene cabida la técnica descrita, habitualmente, tienen lugar en hospitales de tercer nivel, que cuentan con los recursos comentados. En cuanto a las limitaciones técnicas, la más importante se sitúa con relación a la necesidad de evitar el uso de relajantes musculares (al menos durante el curso del procedimiento, tras la intubación); si esto no es posible con un adecuado régimen de anestesia total intravenosa, y aumentos puntuales en su profundidad en caso de que el paciente se mueva o sea dificultosa la disección de planos musculares, los relajantes musculares a utilizar deberán ser los de vida media más corta. En ese caso, mientras dure su efecto, no será posible el registro de un óptimo PAMC del NF.
Concluimos que con la incorporación creciente en los últimos años de la MNIO, en el momento actual no ya solo como apoyo en la prevención de daño neurológico en procedimientos traumatológicos y neuroquirúrgicos exclusivamente, es posible la MNIO del NF en los procedimientos en los que se considere que existe riesgo de lesión del mismo. Asimismo, puede ser factible la reducción de las tasas de su lesión iatrógena. No obstante, dicha afirmación requiere ser comprobada, y en ese caso cuantificada, en futuros estudios prospectivos. En ese sentido, en el momento actual estamos diseñando un estudio en el seno de cirugías cardíacas, procedimientos con altas tasas de lesión del NF, para establecer mayores conclusiones al respecto.
FinanciaciónEl trabajo reflejado en este manuscrito no ha recibido financiación.
Conflicto de interesesLos autores declaramos que no existe conflicto de intereses alguno asociado con esta publicación.