Las nauseas y vómitos postoperatorios no han recibido el suficiente interés hasta la fecha. Se han considerado molestias inherentes e inevitables tras muchas intervenciones quirúrgicas. Sin embargo, esta desagradable complicación tiene un manejo que puede resultar eficaz. Para ello hay que valorar adecuadamente el riesgo y actuar en consecuencia. Existe una amplia variedad de opciones profilácticas disponibles relacionadas con la técnica anestésica, además del oportuno tratamiento antiemético. En este artículo se revisan los factores de riesgo y se efectúan una serie de recomendaciones operatorias y postoperatorias.
There still appears to be insufficient interest in the management of postoperative nausea and vomiting. They are considered as inherent and inevitable discomforts after surgical operation. However, this disagreeable complication can be effectively managed. To do this, the risk must be suitably assessed and acted on accordingly. There are a wide variety of prophylactic options available associated with the anaesthetic technique, as well as appropriate anti-emetic treatment. In this article, the risk factors are reviewed and series of operative and postoperative recommendations are made.
Los síntomas más comunes y desagradables en el postoperatorio son las náuseas y vómitos (NVPO), junto con el dolor. Las NVPO se presentan en aproximadamente el 30% de los pacientes adultos, alcanzando a más del 70% de los considerados de «alto riesgo», durante las primeras 24h1. El vómito incrementa el riesgo de aspiración y se puede asociar a evisceración, dehiscencia de sutura anastomótica y otros riesgos. Las NVPO contribuyen a retrasar el alta de Reanimación y, además, son motivo de retraso o reingreso hospitalario tras el alta de cirugía mayor ambulatoria. Resulta fundamental plantear un enfoque multimodal del problema.
El manejo debe comenzar ya en el periodo preoperatorio con la evaluación del riesgo de NVPO y la planificación de estrategias para reducirlo. Los pacientes con riesgo considerable deben recibir profilaxis farmacológica, porque una vez que las NVPO surgen, no resultará fácil suprimirlas.
Factores de riesgoEl riesgo de sufrir NVPO se relaciona con tres grupos de factores dependientes de: paciente, técnica anestésica y tipo de cirugía1.
- a.
Relacionados con el paciente.
- •
Sexo femenino.
- •
No fumador.
- •
Antecedentes de NVPO o cinetosis.
Otros posibles factores de riesgo de menor entidad son: bajo riesgo ASA, historia de migraña y ansiedad preoperatoria.
- •
- b.
Relacionados con la anestesia.
- •
Uso de anestésicos volátiles.
- •
Empleo de óxido nitroso.
- •
Anestesia balanceada frente a anestesia total intravenosa.
- •
Dosis de neostigmina mayor de 2,5mg.
- •
Utilización de opiáceos intra y postoperatorios.
Otros posibles factores de riesgo de menor consideración son: anestesia general frente a regional y opiáceos de larga duración frente a corta duración.
- •
- c.
Relacionados con la cirugía.
- •
Duración del procedimiento. Se considera que cada 30min de incremento del tiempo quirúrgico aumentará el riesgo en un 60%, sobre el valor basal estimado2.
- •
Otros posibles factores de riesgo menos determinantes son: cirugía intraabdominal, laparoscopia, ortopédica, tiroidea, neurocirugía, cirugía de mama, maxilofacial, otorrinológica y ginecológica. También se pueden considerar como riesgo la restricción de fluidos perioperatoria y la administración de cristaloides frente a coloides.
Debemos aclarar que el conocimiento general de tales factores de riesgo no tiene una aplicación clínica concreta. Para tratar de evitar las NVPO es preciso seleccionar y estratificar los factores más influyentes mediante un sistema de puntuación que permita precisar lo más exactamente posible la magnitud del riesgo al que nos enfrentamos. La precisión de un sistema de puntuación de las NVPO debe fundamentarse en su capacidad para discriminar adecuadamente entre pacientes que podrían sufrir o no las NVPO; la forma más correcta de probarlo es mediante el cálculo del área bajo la curva denominada «ROC»3.
Se han validado ocho sistemas de puntuación aunque, dadas las amplias diferencias en la potencia estadística de los predictores empleados, no sorprende que, como ha observado Gang1 en su fundamental revisión, dichos sistemas de predicción muestren una seguridad tan solo moderada, con curvas ROC que oscilan entre 0,56 y 0,78. En cualquier caso y pese a sus lógicas limitaciones los distintos sistemas evaluados han probado su eficacia para reducir la incidencia de NVPO.
¿Cuál es el mejor sistema de puntuación? La mayoría de ellos han procurado la máxima simplificación posible, por lo que no debemos buscar el de mayor potencia estadística sino el más práctico a la hora de aplicarlo en clínica, pues se ha demostrado que a la postre la capacidad discriminativa de la mayoría de los sistemas es similar4. Por su seguridad predictiva y facilidad de aplicación existe el consenso generalizado entre los expertos de que los mejores indicadores son los propuestos por Apfel5 y Koivuranta6, para los adultos, y el de Eberhart7, para los niños.
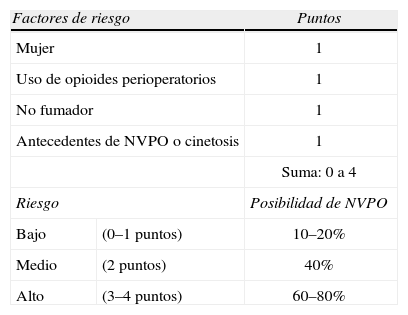
Apfel5 plantea un sistema con cuatro variables, con una potencia discriminativa (área bajo la curva ROC) de 0,69 y que son, ordenadas según su mayor odds ratio: mujer (3,55 [IC 95% 2,46–5.149]), uso perioperatorio de opiáceos (2,10 [IC 95% 1,42–3,10]), no fumador (2,05 [IC 95% 1,49–2,82]) y antecedentes de NVPO o cinetosis (1,91 [1,35–2,70]). Los odds ratio representan el cociente entre el número de veces que ocurre el suceso frente a cuantas veces no ocurre. En la práctica, con la puntuación obtenida según la tabla 1, se determina la probabilidad de riesgo de NVPO.
Koivuranta6, por su parte, formula otro sistema, esta vez con cinco variables, con una potencia discriminativa de 0,71 y que se ordenan, según su influencia en: mujer, antecedentes de NVPO, duración de la cirugía, no fumador e historia de cinetosis. El riesgo en función de la puntuación obtenida con este sistema no muestra porcentajes, para cada grupo, muy diferentes a los esperados por la escala de Apfel; con todo, el sistema de este último es el más empleado para valorar el riesgo de NVPO.
Resulta evidente que determinados factores de riesgo relacionados con el paciente y con la anestesia influyen en la aparición de NVPO. Sin embargo, la contribución a estas escalas del tipo de cirugía es controvertida8. De hecho, solo tres de las ocho publicadas lo incluyen como factor de riesgo. En un reciente artículo, Ruiz9 concluye que el tipo de cirugía, cuando se ordena anatómicamente, se asocia con una mayor necesidad de antieméticos en reanimación. Las categorías anatómicas más afectadas fueron: neurocirugía, cabeza y cuello y cavidad abdominal. No obstante, el estudio ha sido criticado en cuanto a su metodología10.
Manejo perioperatorioLa naturaleza multifactorial de las NVPO requiere un tratamiento con enfoque multimodal. Así, además del uso profiláctico de antieméticos, podemos adoptar distintas medidas no farmacológicas, de diversa índole, que minimizan el riesgo.
Los factores relacionados con el paciente no son, obviamente, modificables; tampoco cabe hacer mucho con los que dependen de la cirugía. Por el contrario, sí pueden resultar provechosas medidas que cambien el manejo anestésico perioperatorio que, si bien no eliminarán el riesgo de NVPO, contribuirán a reducirlo. Existen evidencias de mayor o menor grado de las siguientes acciones2,8:
- •
Uso de ansiolíticos preoperatorios (III B).
- •
Hidratación adecuada (III A), con preferencia de los coloides sobre los cristaloides (III A).
- •
La anestesia regional tiene ventajas sobre la general (IV A).
- •
En caso de anestesia general, se recomienda la endovenosa total con propofol (I A).
- •
Evitar anestésicos potencialmente emetizantes como: óxido nitroso (II A), agentes inhalatorios (I A), etomidato y ketamina (V).
- •
Disminuir las dosis de opioides intraoperatorios (II A) y postoperatorios (IV A).
- •
Reducir la dosis de neostigmina (<2,5mg) (V).
En cuanto al tratamiento farmacológico, se ha comprobado que los tres antieméticos usados con más frecuencia: ondansetrón (4mg), dexametasona (4mg) y droperidol (1,25mg), muestran una eficacia antiemética similar y cada uno, de forma independiente, reduce el riesgo de NVPO en un 25% aproximadamente8.
El bajo coste y excelente perfil de seguridad que exhiben tanto el droperidol como la dexametasona, hacen que su combinación resulte una estrategia de valioso coste-eficacia, por lo que no sorprende que la adición del ondansetrón obtenga tan solo un pequeño incremento de beneficio cuando se administra a pacientes con riesgo alto de NVPO11.
De todos los 5-HT3 antagonistas, el ondansetrón es el más utilizado. Se ha demostrado que todos ellos tienen la misma potencia antiemética. La dosis profiláctica que se recomienda para el ondansetrón es de 4mg, comprobándose que resulta más eficaz si se administra al final de la cirugía12. La dosis recomendada de dexametasona para la profilaxis es de 4mg, tras la inducción anestésica, no habiéndose observado efectos secundarios con esta dosis13. En cuanto al droperidol, se administra a dosis de 0,625 a 1,25mg, al final de la cirugía. Su uso ha sido cuestionado durante algunos años al haberse relacionado con alteraciones electrocardiográficas e incluso muerte súbita. Sin embargo, a las dosis empleadas como antiemético, no ha podido relacionarse con ningún problema cardiaco. Incluso recientemente se ha postulado como antiemético de primera elección14–16.
Conviene, para finalizar, mencionar el papel de un fármaco todavía muy extendido en la profilaxis y tratamiento de las NVPO: la metoclopramida. Pues bien, se ha evidenciado que a la dosis habitual (10mg) no tiene mayor efecto que un placebo17.
¿Cuál es la estrategia más eficaz para el abordaje multimodal de las NVPO? Disponemos de múltiples guías y protocolos que han obtenido diferente éxito de implantación. Tal vez las tres más reconocidas sean las de la American Society of Anesthesiologist (ASA)18, la American Society of Perianesthesia Nurses (ASPAN)19 y la Society of Ambulatory Anesthesia (SAMBA)15. Consideramos que esta última es la más completa. Sus recomendaciones se sustancian en los siguientes pasos:
- 1.
Identificar a los pacientes con riesgo de NVPO. Ya hemos discutido las peculiaridades de las escalas más empleadas; lo importante es recurrir siempre a la misma. La escala de Apfel es la más utilizada en la actualidad5.
- 2.
Reducir los factores de riesgo. Las acciones más prácticas se relacionan con la anestesia por su diversidad de técnicas, muchas veces electivas. Las que tienen la eficacia más probada son: la anestesia regional o en su defecto general con propofol en perfusión, evitar el óxido nitroso y los anestésicos inhalatorios y disminuir los opioides intraoperatorios, asociando AINE para reforzar la analgesia.
- 3.
Administrar profilaxis farmacológica en pacientes con moderado o alto riesgo. Se ha demostrado que el empleo de múltiples antieméticos de características farmacológicas diferentes tiene un beneficio acumulativo. En efecto, la adición de un 2.o o 3.o antiemético reduce sustancialmente las NVPO: un 37% con sólo uno de ellos, 28% con dos y 22% con tres. La combinación de droperidol y dexametasona disminuye la incidencia de NVPO a la mitad, frente al 15% con un solo fármaco8.
- 4.
Tratar las NVPO. Es recomendable recurrir a un antiemético diferente al empleado en la profilaxis. En aquellos pacientes que no han recibido profilaxis, está indicado el ondansetrón, administrado a dosis inferiores a las de la profilaxis (1mg)20. Como alternativa, disponemos del droperidol (0,625mg) o la dexametasona (2–4mg)21.
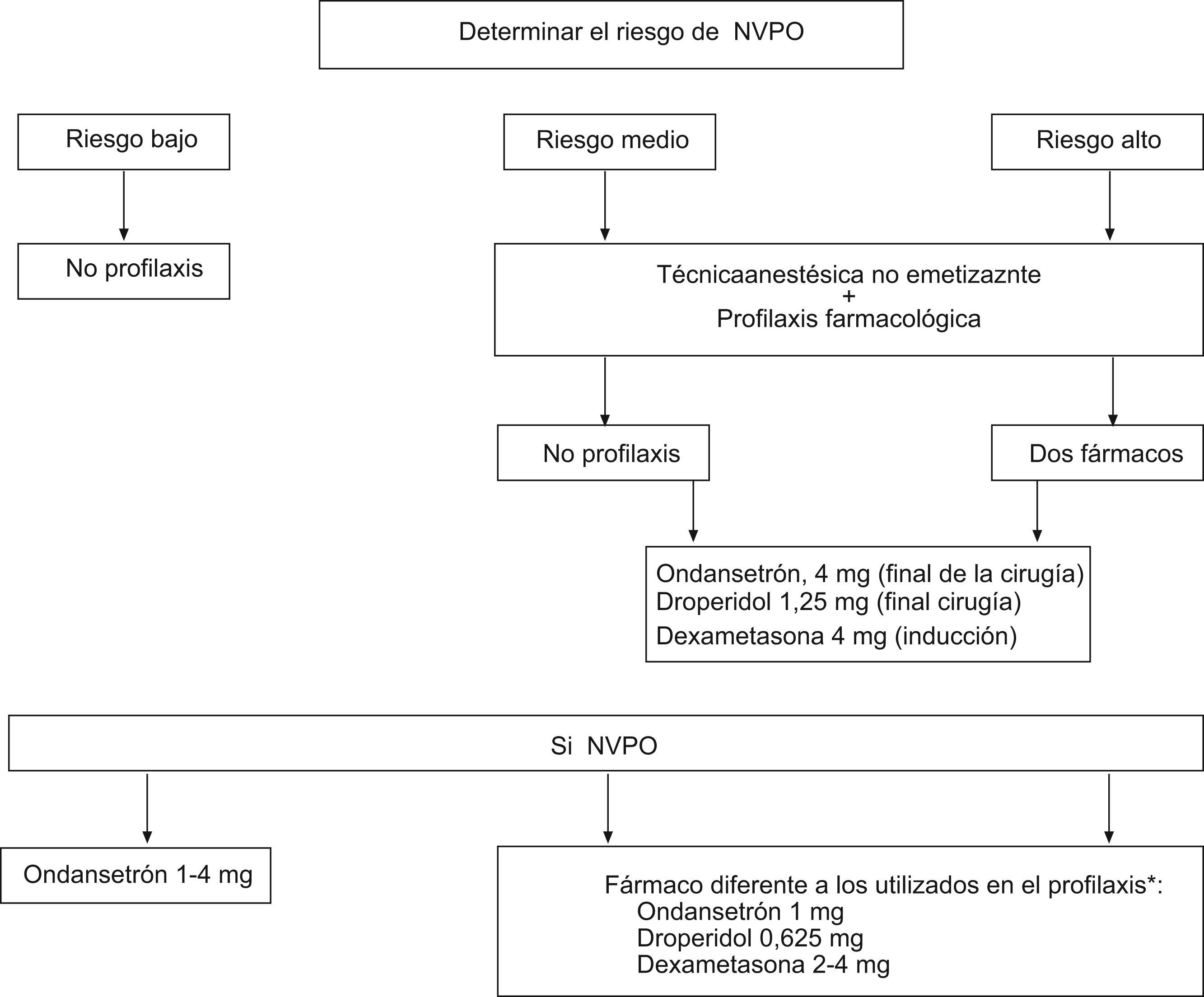
Para finalizar, mostramos gráficamente la estrategia aquí establecida, mediante un algoritmo (fig. 1).
ConclusiónConcluimos que el manejo de las NVPO puede resultar eficaz, si se estratifica adecuadamente el riesgo y se actúa en consecuencia. Conviene no olvidar que, una vez establecidas las NVPO, los recursos terapéuticos son limitados, por lo que debemos apelar al amplio abanico de opciones profilácticas disponibles, principalmente relacionadas con la anestesia, amén del oportuno tratamiento antiemético. Una estrategia sencilla podría consistir en emplear tales medidas, acompañadas de droperidol, dexametasona o ambas, si el riesgo lo requiere, reservando el ondasetrón para el tratamiento de rescate.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.