Descubrir una masa intracardiaca en pediatría obliga a hacer un diagnóstico diferencial entre tumores (primarios/secundarios) y trombos, todos ellos infrecuentes en niños. Presentamos nuestra experiencia quirúrgica pediátrica de resección de masas intracardiacas.
MétodosIndicamos exéresis de la masa intracardiaca cuando causa síntomas o tiene repercusión hemodinámica por obstruir el flujo sanguíneo. Estudiamos retrospectivamente a 12 niños operados entre 2011-2022. Análisis estadístico: SPSS® v. 20.0.
ResultadosEdad media: 7,1±6 años (rango: 1 mes-15 años), 67% mujeres. Dos niños tenían cardiopatía congénita operada y 5 enfermedad oncológica; 2 presentaban coagulación alterada. Mayoritariamente (67%) asintomáticos y un 33% sintomáticos. Se realizó ecocardiograma en el 100% y resonancia cardiaca en el 50%: la masa obstructiva estaba localizada en la aurícula derecha en 6 pacientes, en la válvula tricúspide en 2, en el ventrículo derecho en 2 y en el ventrículo izquierdo en otros 2. Lesiones asociadas: foramen oval permeable (5), insuficiencia tricuspídea moderada (3) y estenosis pulmonar/subaórtica severa (2). Dos pacientes tenían tumor renal derecho con extensión intracardiaca por la cava inferior. Se realizó cirugía por esternotomía (11) o toracotomía (uno), con circulación extracorpórea (4 sin pinzar aorta), lográndose extirpar la masa completa (11) o parcialmente (uno). Tiempos medios de circulación extracorpórea y pinzado aórtico: 72±44 y 34±33min, respectivamente. Intubación media 7±7h y estancia postoperatoria 11±6 días. Dos pacientes presentaron complicaciones postoperatorias (ascitis y derrame pericárdico). Anatomía patológica de las masas explantadas: 4 trombos, 2 fibromas, 2 nefroblastomas, un mixoma, un rabdomioma, un fibroelastoma papilar y un pseudotumor inflamatorio. Sin mortalidad hospitalaria ni tardía. No hubo reoperaciones posteriores. Seguimiento medio 4,8±3,7 años (máximo 10 años).
ConclusionesRecomendamos extirpar cualquier masa intracardiaca que obstruya significativamente el flujo sanguíneo o cause síntomas, para mejorar la clínica y filiar etiológicamente la masa. Nuestros resultados quirúrgicos son buenos, sin mortalidad ni reintervención en el seguimiento posterior.
Discovering an intracardiac mass in pediatrics needs a differential diagnosis between tumours (primary/secondary) and thrombi, all being uncommon in children. We present our surgical experience resecting intracardiac masses in children.
MethodsWe indicate intracardiac mass excision when it causes symptoms or has hemodynamic consequences by obstructing blood flow. Retrospective study: 12 children operated from 2011 to 2022. Statistical analysis: SPSS® v. 20.0.
ResultsMean age: 7,1±6 years, 67% female. Two children had previous congenital heart disease repair and 5 oncologic pathology; 2 had anomalous coagulation test. Asymptomatic 67% and symptomatic 33%. Echocardiogram was performed in 100% and magnetic resonance in 50%: Obstructive mass located in the right atrium in 6 patients, tricuspid valve in 2, right ventricle in 2 and left ventricle in other 2. Associated lesions: patent foramen ovale (5), moderate tricuspid regurgitation (3) and severe pulmonary/subaortic stenosis (2). Two patients had a right renal tumor with intracardiac extension through the inferior vena cava. Surgery performed by sternotomy (11) or thoracotomy (one), with extracorporeal circulation (4 with beating heart), achieving removal of the whole mass (11) or partial (one). Mean extracorporeal circulation and aortic clamp times: 72±44 and 34±33min, respectively. Mean intubation 7±7h and postoperative stay 11±6 days. Two patients presented postoperative complications (ascites and pericardial effusion). Pathological anatomy of the explanted masses: 4 thrombi, 2 fibromas, 2 nephroblastomas, one myxoma, one rhabdomyoma, one papillary fibroelastoma and one inflammatory pseudotumor. No hospital or late mortality. No subsequent reoperations. Mean follow-up 4.8±3.7 years (maximum 10 years).
ConclusionsWe recommend removing any intracardiac mass that significantly obstructs blood flow or causes symptoms, in order to improve clinically and determine the etiology of the mass. Our surgical results are good, without mortality or reintervention in subsequent follow-up.
El descubrimiento casual de una masa intracardiaca en un paciente pediátrico obliga a hacer un diagnóstico diferencial entre tumores, trombos y vegetaciones relacionadas con endocarditis, todos ellos infrecuentes en niños. Según sea su tamaño, movilidad y etiología, y dependiendo de la cavidad cardiaca que ocupen, las manifestaciones clínicas serán variadas, incluyendo desde pacientes asintomáticos a los que presentan diferentes grados de cansancio, disnea y arritmias, e incluso los hay que comienzan con un episodio de muerte súbita1.
Además de la valoración clínica de los pacientes, las pruebas de imagen cardiaca definen las dimensiones de la masa y su relación con las estructuras adyacentes, orientan hacia alguna posible etiología y cuantifican la función ventricular, así como el funcionamiento de las válvulas cardiacas, que puede verse alterado si la masa obstruye el flujo sanguíneo intracardiaco2.
La cirugía estará indicada en los casos que presenten síntomas relacionados con la masa intracardiaca o exista deterioro hemodinámico secundario a la obstrucción al flujo sanguíneo, con el objetivo de filiar la masa tras su estudio anatomopatológico, así como restaurar la anatomía y fisiología normales del corazón3.
Presentamos en este trabajo nuestra experiencia quirúrgica de resección de masas intracardiacas en pediatría.
MétodosNuestro hospital es un centro terciario de referencia nacional para el tratamiento quirúrgico de las cardiopatías congénitas. Revisamos nuestra base de datos quirúrgica seleccionando los pacientes de edad inferior a 18 años, operados con la indicación de resecar una masa intracardiaca. Indicamos la exéresis de dicha masa cuando esta causa síntomas o tiene repercusión hemodinámica por obstruir el flujo sanguíneo. Incluimos en este trabajo a 12 niños operados en el intervalo temporal desde el año 2011 hasta el 2022.
Estudiamos retrospectivamente sus historias clínicas, centrándonos en las características preoperatorias y el diagnóstico de imagen, las técnicas quirúrgicas empleadas, nuestros resultados a corto y medio plazo, para valorar su evolución posquirúrgica y comparar nuestra experiencia con la reportada por otros centros de referencia.
Definimos mortalidad hospitalaria (MH) como cualquier muerte acaecida durante los 30 días posteriores a la cirugía, o en cualquier momento mientras que el paciente siga hospitalizado tras la intervención quirúrgica. Mortalidad tardía es toda muerte que ocurre posteriormente.
Consideramos el fin del seguimiento en cada caso, si este fallece o está vivo en la última revisión.
El estudio estadístico se ha realizado con el paquete estadístico SPSS® v. 20.0 para Windows. Se presentan las variables cuantitativas como media±desviación estándar si la distribución es normal, o como mediana con rango intercuartílico si la distribución no es normal, y las variables cualitativas como porcentajes.
Consideraciones éticasTodos los padres y/o tutores legales de nuestros pacientes fueron informados acerca de la intervención y firmaron el consentimiento autorizando el uso de datos e imágenes con fines docentes y de investigación previamente aprobado por el Comité de Ética de nuestro hospital (código HULP PI-5305). Hicimos la recogida de datos de forma anónima, siguiendo los protocolos del hospital para la realización de estudios clínicos y respetando la ley de protección de datos actualmente vigente en nuestro país.
ResultadosLa resección de masas intracardiacas es una cirugía muy infrecuente en nuestro servicio. Estos 12 niños operados suponen el 0,7% del total de las extracorpóreas realizadas entre 2011 y 2022 en población pediátrica (edad menor de 18 años).
Nuestros pacientes tenían una edad media de 7,1±6 años (rango: 1 mes-15 años) y un peso medio de 25±18kg (rango: 4-55kg), siendo la mayoría del sexo femenino (67%).
Respecto a sus antecedentes personales (tabla 1), 2 niños tenían cardiopatía congénita operada y 5 enfermedad oncológica; 2 pacientes presentaban las pruebas de coagulación alterada (déficit del factor v de Leiden en una adolescente operada previamente de Fallot y microangiopatía trombótica en otra niña con enfermedad oncológica). Mayoritariamente se encontraban asintomáticos (67%), descubriéndose la masa en un estudio de imagen de manera casual. Los 4 pacientes (33%) que presentaron síntomas manifestaron astenia y cansancio; otro de ellos comenzó con un episodio de muerte súbita.
Características de los pacientes operados por una masa intracardiaca
| Edad(años) | Peso(kg) | Antecedentes personales | Localización de masa intracardiaca | Anatomía patológica |
|---|---|---|---|---|
| 3,33 | 14 | RC de CIA, CIV, DAP hace 2 años | VT | Trombo |
| 13 | 50 | RC de TOF hace 12,5 años | AD | Fibroelastoma papilar |
| 12 | 55 | Síndrome de Carney | AD | Mixoma |
| 2,33 | 14 | VI | Fibroma | |
| 0,25 | 5,0 | VD | Pseudotumor inflamatorio | |
| 0,08 | 4,0 | Esclerosis tuberosa | VI | Rabdomioma |
| 13 | 30 | Linfoma no Hodgkin | AD | Trombo |
| 4 | 13 | Leucemia mieloide aguda | VT | Trombo |
| 15 | 44 | Pseudoobstrucción intestinal crónica miógena | AD | Trombo |
| 12,16 | 44 | Tumor renal derecho | AD | Sarcoma renal de células claras estadio iii |
| 0,42 | 9 | VD | Fibroma | |
| 10 | 24 | Tumor renal derecho | AD | Nefroblastoma de riesgo intermedio |
AD: aurícula derecha; CIA: comunicación interauricular; CIV: comunicación interventricular; DAP: ductus arterioso persistente; RC: cirugía de reparación completa; TOF: tetralogía de Fallot; VD: ventrículo derecho; VI: ventrículo izquierdo; VT: válvula tricúspide.
Respecto al diagnóstico, solo una masa localizada en el ventrículo derecho se diagnosticó prenatalmente, observándose un crecimiento importante posnatal, por lo que se realizó cirugía a los 5 meses de vida (fig. 1). La masa intracardiaca se observó con ecocardiografía en todos los pacientes, y el estudio se completó con resonancia magnética (RM) cardiaca en la mitad de ellos (fig. 2). La masa intracardiaca obstructiva estaba localizada en las cavidades derechas cardiacas en la mayoría de los casos (aurícula derecha 6, válvula tricúspide 2, ventrículo derecho 2), y en los 2 niños restantes se encontraba en el ventrículo izquierdo (VI). Las lesiones asociadas halladas fueron foramen oval permeable (5), insuficiencia tricuspídea moderada (3), comunicación interventricular residual tipo Gerbode (uno), estenosis pulmonar severa (uno) y estenosis subaórtica severa (uno), estando las lesiones valvulares habitualmente relacionadas con la compresión por parte de la masa intracardiaca. Dos pacientes tenían un tumor renal derecho con extensión intracardiaca a través de la vena cava inferior (fig. 3).
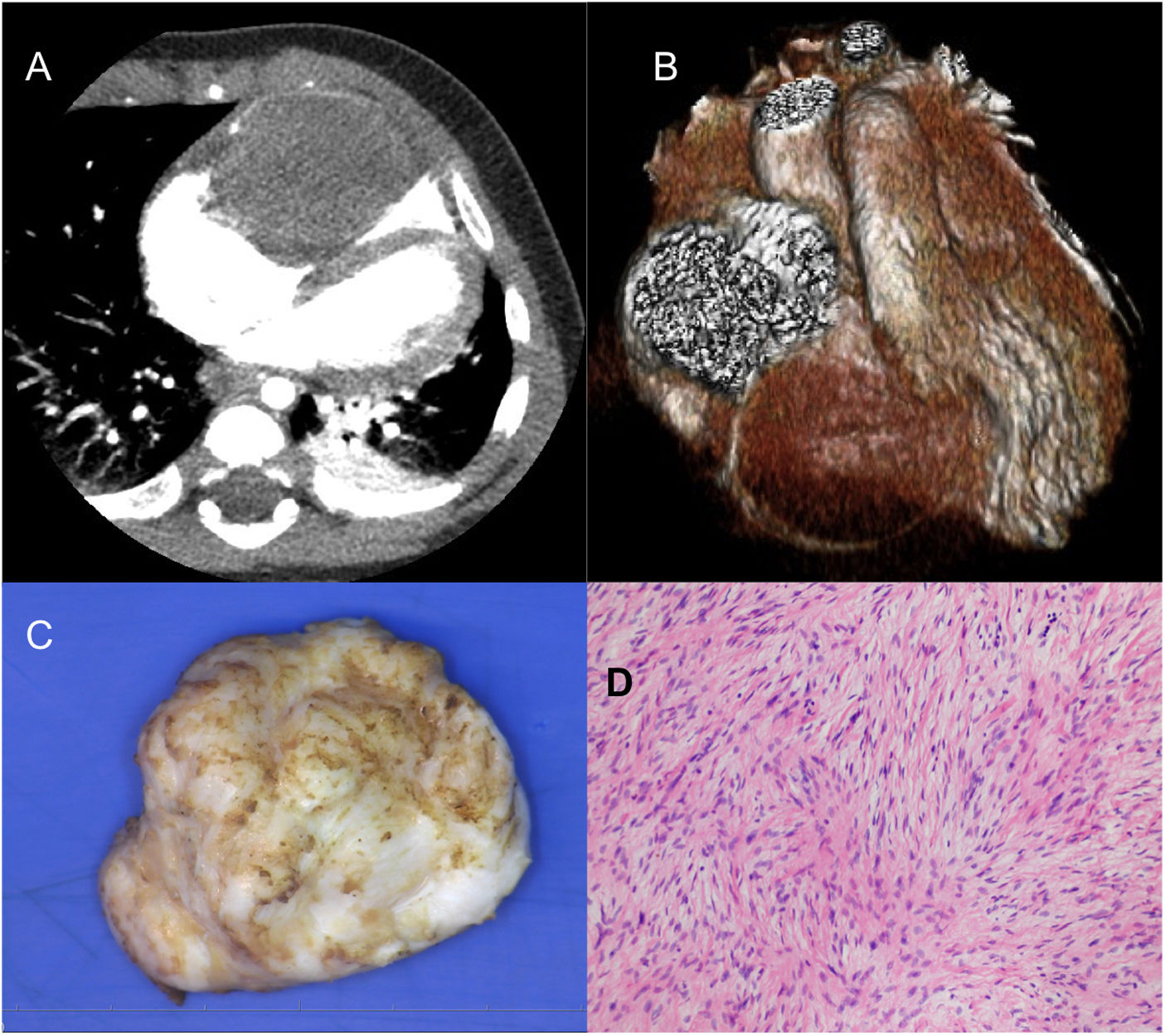
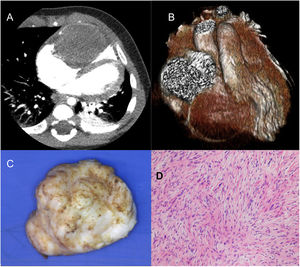
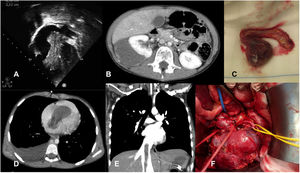
Lactante mujer de 5 meses y 9kg con fibroma gigante en ventrículo derecho (46×36×27mm). Corte transversal (A) y reconstrucción tridimensional (B) de tomografía computarizada cardiaca. Imagen macroscópica (C) nacarada del fibroma explantado en su totalidad. Imagen microscópica (D) con hematoxilina-eosina donde se observan fibroblastos en una densa matriz de colágeno y elastina compatibles con fibroma.
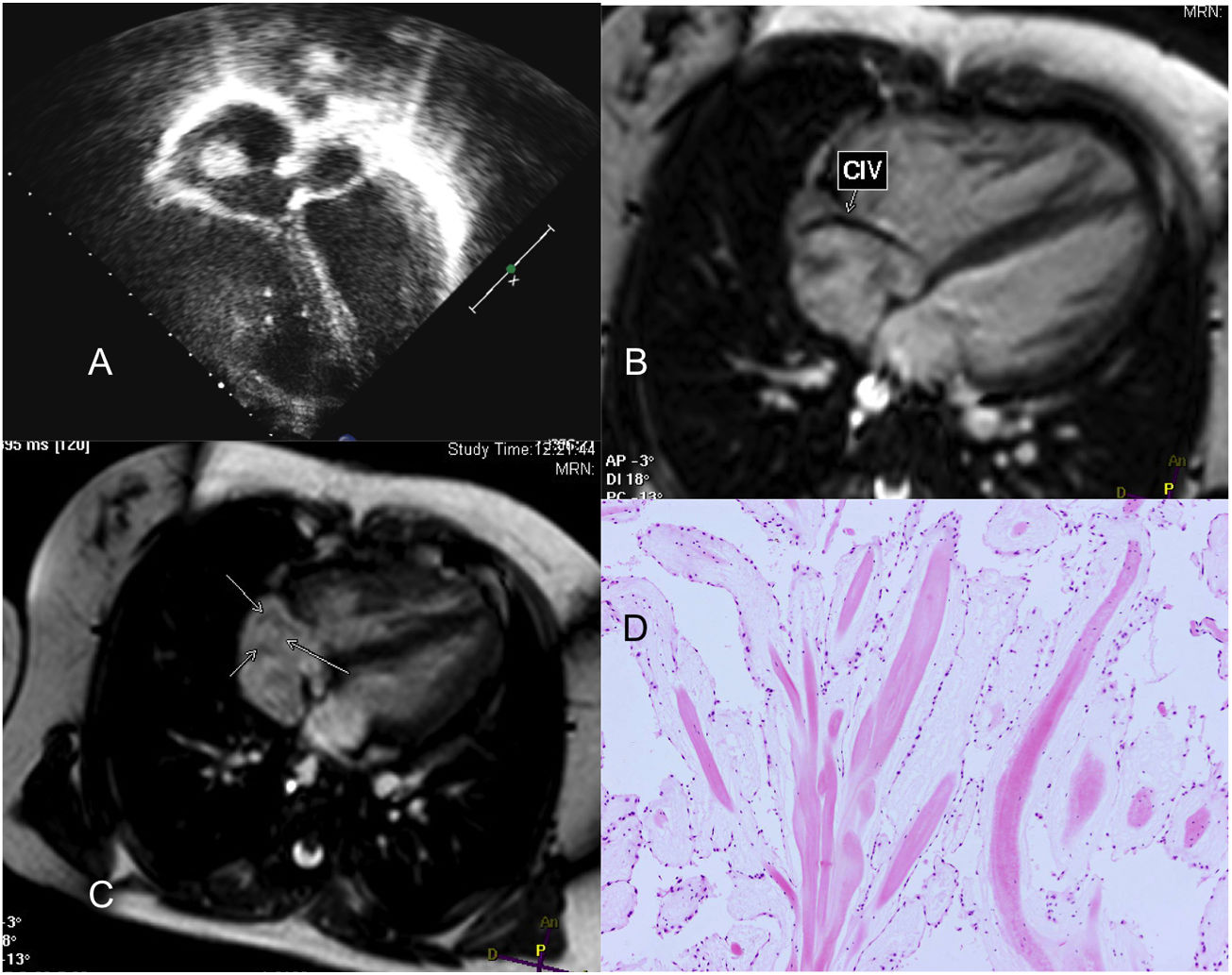
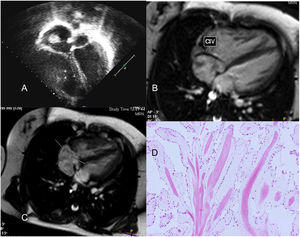
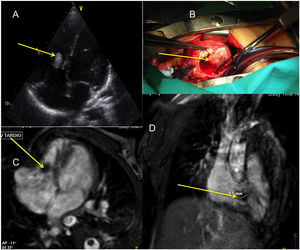
Niña de 13 años y 50kg operada de Fallot a los 5 meses. Diagnóstico en seguimiento ecocardiográfico (A), plano apical de 4 cámaras de masa hiperecogénica redondeada localizada en región posterior de la aurícula derecha. Cortes transversales de resonancia magnética donde observamos: flujo de comunicación interventricular (CIV) residual tipo Gerbode (B) y, señalada con flechas, la masa en aurícula derecha (C). Imagen microscópica (D) con hematoxilina-eosina del tumor constituido por papilas avasculares y mixoides revestidas por células endoteliales, compatible con fibroelastoma papilar.
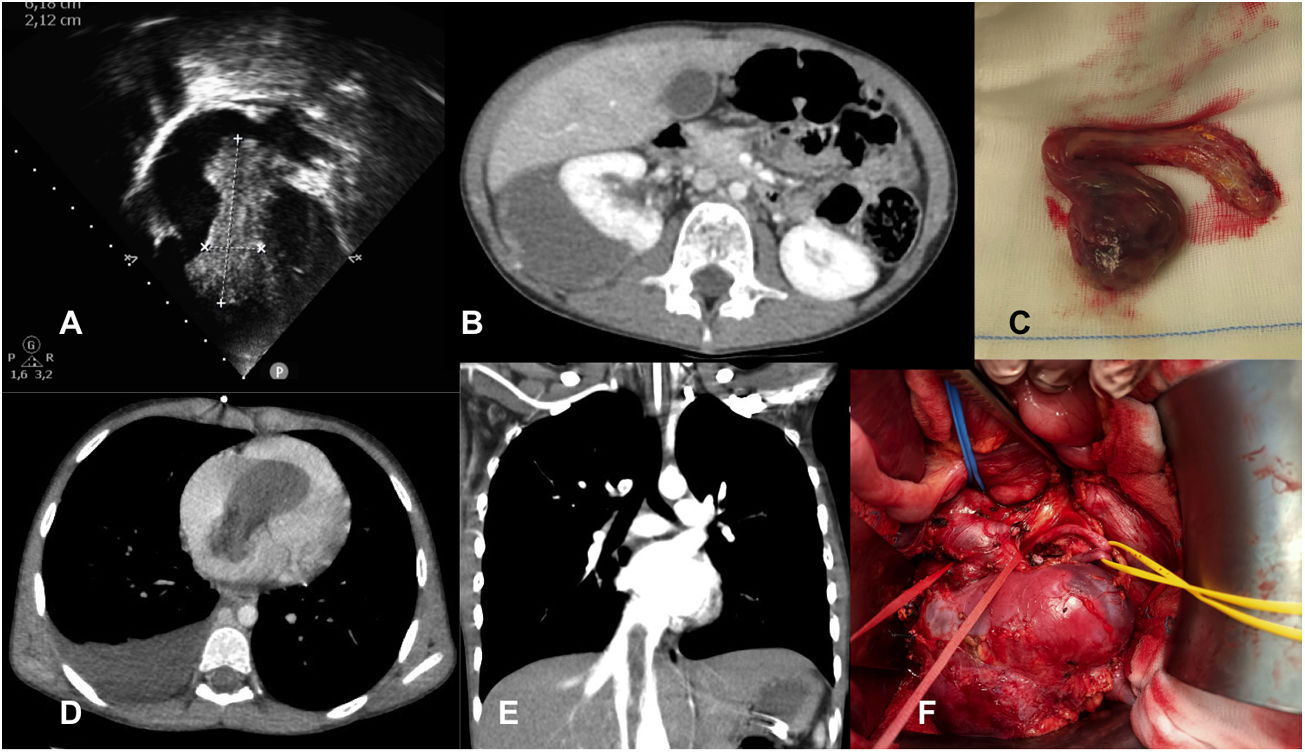
Niña de 10 años y 24kg que acude a Urgencias por disnea. Imagen ecocardiográfica (A) en plano apical de 4 cámaras donde se observa gran masa de 20×65mm que entra en la aurícula derecha desde la vena cava inferior e invade hasta el ventrículo derecho. B, D y E son imágenes de la angio-TC toracoabdominal donde se observa una gran masa abdominal dependiente del riñón derecho compatible con tumor de Wilms (B), que invade el corazón (D) a través de la vena cava inferior (E). Imágenes intraoperatorias de la disección del riñón derecho con el tumor adherido a su polo superior (F), y masa intracardiaca con la extensión desde la vena cava inferior explantadas (C).
Las cirugías se hicieron por esternotomía media (11) y un caso por toracotomía lateral derecha, canulando aorta ascendente y 2 cavas para entrar en circulación extracorpórea (fig. 4), con pinzado aórtico en 8 pacientes y evitándolo en 4 casos que operamos a corazón latiendo. Logramos extirpar la masa completa en 11 niños y parcial en un niño que tenía un fibroma en cara lateral de VI afectando a la válvula mitral y al surco auriculoventricular posterior. En todos los casos se mandó muestra de la masa explantada a Anatomía Patológica y Microbiología para completar el diagnóstico etiológico. Se realizó cirugía asociada en 5 pacientes consistente en cierre de foramen oval permeable (4), cierre de comunicación interventricular tipo Gerbode (uno) (fig. 5), ampliación transanular entre el ventrículo derecho y la arteria pulmonar (uno) y parche de pericardio autógeno en desgarro de vena cava inferior (uno). Los tiempos medios de circulación extracorpórea y de pinzado aórtico fueron 72±44 y 34±33min, respectivamente.
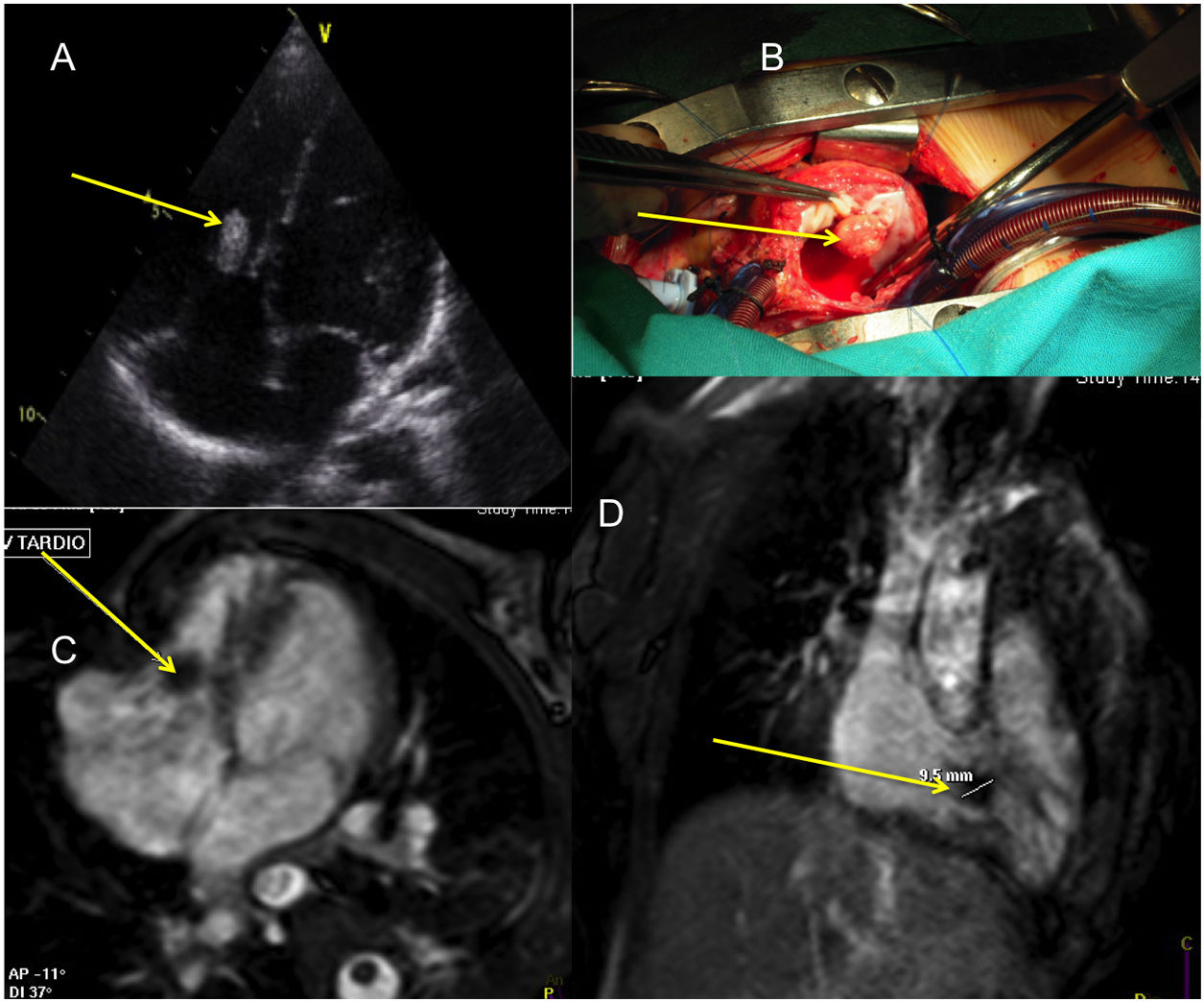
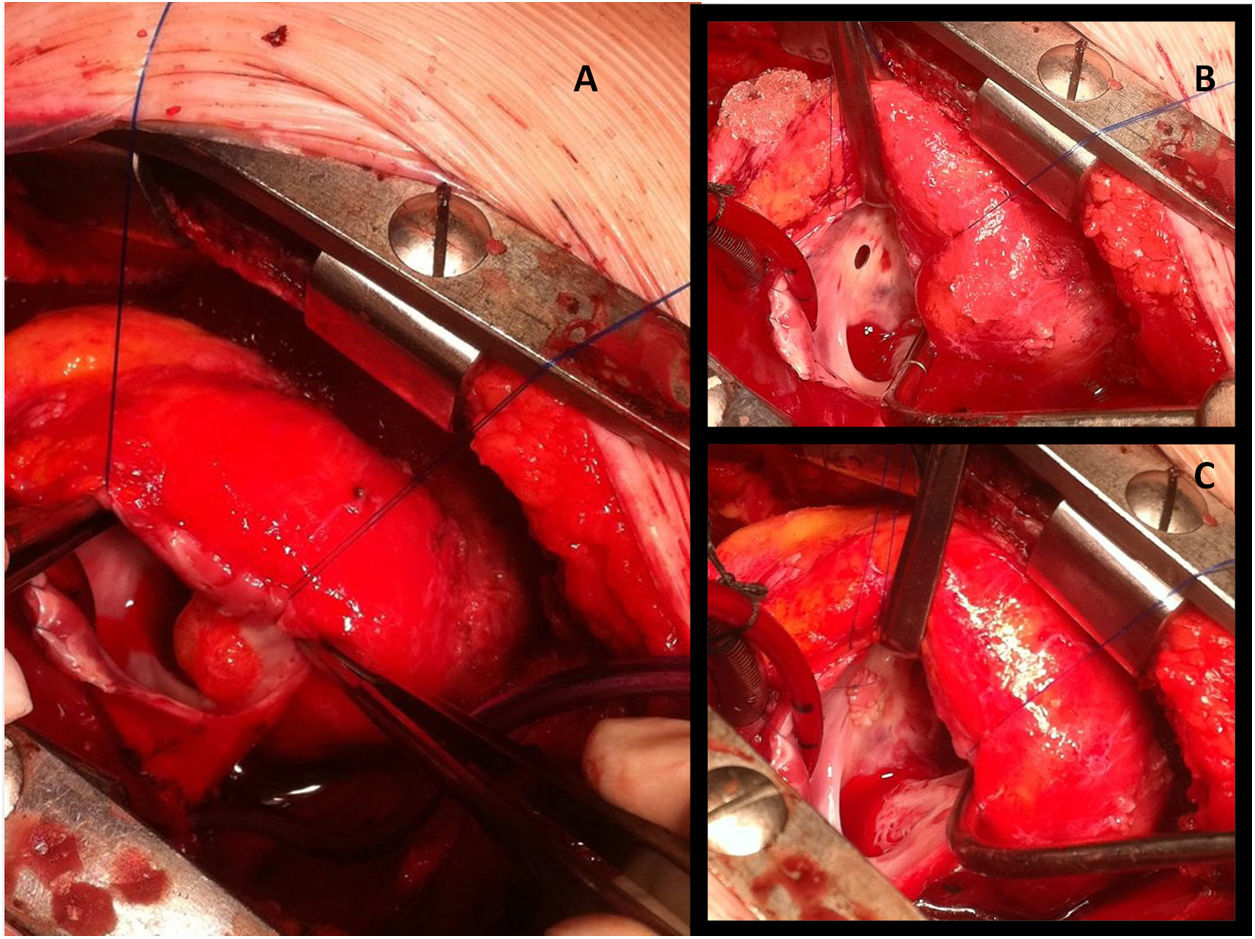
Imágenes diagnósticas de niña de 3 años con trombo en la válvula tricúspide señalado con una flecha amarilla. A: plano ecocardiográfico de 4 cámaras. C y D: imágenes de resonancia magnética transversal y sagital, respectivamente. B: imagen intraoperatoria con abordaje desde atriotomía derecha longitudinal, observándose el trombo adherido al velo anterior tricuspídeo.
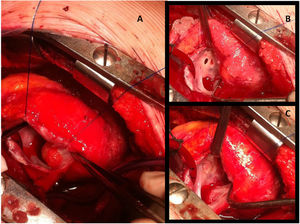
Imágenes intraoperatorias de la niña con el fibroelastoma papilar comentada en la figura 2. Tras atriotomía derecha longitudinal, el tumor de 2cm se ve adherido a la pared anterior de la aurícula derecha (A). En la imagen B se observa el Gerbode residual señalado con una flecha, y en C el mismo defecto cerrado con parche de pericardio heterólogo.
La anatomía patológica de las masas explantadas confirmó las siguientes etiologías: trombos (4), fibromas (2), mixoma (uno), rabdomioma (uno), fibroelastoma papilar (uno), pseudotumor inflamatorio o tumor miofibroblástico inflamatorio (uno), sarcoma de células claras de origen renal (uno) y nefroblastoma de riesgo intermedio (uno).
No falleció ningún paciente durante todo el tiempo de estudio, por lo que fueron nulas tanto la MH como la mortalidad tardía.
Respecto al postoperatorio inmediato, aparecieron complicaciones en 2 pacientes (16%): ascitis y derrame pericárdico. El tiempo medio de intubación fue de 7±7h y el de estancia hospitalaria postoperatoria de 11±6 días.
El seguimiento de los pacientes es completo, la media son 4,8±3,7 años (máximo 10 años). Durante este tiempo no han acontecido fallecimientos ni los pacientes han requerido nuevas reintervenciones de causa cardiaca.
DiscusiónLos tumores cardiacos son muy raros a cualquier edad, con una incidencia estimada del 0,02%, y en la población pediátrica son aún más infrecuentes4. Los tumores cardiacos primarios son menos frecuentes que los secundarios, que resultan de la extensión local o por vía hemática o linfática de otros tumores primarios de diferente localización. Los tumores cardiacos primarios generalmente son benignos; los mixomas son los más frecuentes en adultos y en niños son los rabdomiomas. Otras entidades también poco frecuentes con las que hay que hacer diagnóstico diferencial son los trombos que suelen asociarse a catéteres centrales, las vegetaciones en pacientes con clínica de endocarditis infecciosa y alguna que otra rareza como los quistes hidatídicos5.
Nuestra experiencia corrobora que la resección quirúrgica de masas intracardiacas es muy poco frecuente en la práctica diaria, suponiendo el 0,7% del total de extracorpóreas infantiles realizadas en los últimos 11 años. Un 50% de estas cirugías correspondieron a tumores cardiacos primarios de etiología benigna, un 33% a trombos intracavitarios y un 17% a tumores renales con extensión cardiaca a través de la vena cava inferior. La mayoría de las masas de nuestros pacientes estaban localizadas en el corazón derecho (83%), y el 17% restante se ubicaban en el VI.
Los rabdomiomas suelen diagnosticarse en el primer año de vida, generalmente son asintomáticos, se asocian con esclerosis tuberosa hasta el 50% de los casos, suelen ser múltiples, se localizan en el VI y habitualmente remiten de forma espontánea con el tiempo. Nuestro caso de rabdomiomas múltiples fue un niño de un mes con diagnóstico posnatal y obstrucción severa a nivel del tracto de salida del VI por uno de los rabdomiomas, que requirió cirugía, similar a lo reportado por otros grupos6.
Los fibromas son el segundo tipo de tumor primario más frecuente en pediatría, después de los rabdomiomas. Generalmente también aparecen en lactantes, suelen ser solitarios, localizados en ventrículos y causan arritmias ventriculares7. A veces se calcifican y esa característica orienta hacia su diagnóstico con las técnicas de imagen. En la RM se identifican como una masa encapsulada y sin vascularización que se realza tardíamente con gadolinio.
El fibroelastoma papilar suele ser pediculado y móvil, se relaciona con las válvulas cardiacas, es un tumor de adultos8 y cuando aparece en la edad pediátrica suele ser en la adolescencia.
Los mixomas son más frecuentes en adultos que en niños, predominan en mujeres y se localizan preferentemente en la aurícula izquierda, adheridos al septo interauricular. Un 5% de ellos se asocian al síndrome de Carney, que es una entidad autosómica dominante asociada a lentiginosis cutánea y alteraciones endocrinas.
Los trombos intracavitarios pueden aparecer en pacientes con anomalías de la coagulación, como por ejemplo nuestra paciente que tenía déficit del factor v de Leiden, o con situaciones protrombóticas, como nuestros pacientes oncológicos con catéteres centrales de larga evolución.
El tumor de Wilms es el tumor renal más frecuente en niños. Generalmente responde bien a la quimioterapia y a la resección quirúrgica, con supervivencias superiores al 90% a los 5 años. Es poco frecuente que tengan invasión intracardiaca a través de la vena cava inferior, dato que ensombrece el pronóstico respecto a los que están localizados en el riñón9.
Aunque las masas intracardiacas tengan etiología benigna en su mayoría, la clínica estará relacionada con su tamaño y localización, que puede alterar el flujo sanguíneo cardiaco y causar importante morbimortalidad. Los pacientes pueden estar asintomáticos y descubrirse el tumor de forma incidental en una prueba de imagen, que en nuestra experiencia es la presentación más habitual. También pueden referir síntomas inespecíficos como fiebre, artralgias, pérdida de peso o fatiga. Otras veces dan clínica cardiaca por su obstrucción al flujo sanguíneo, como arritmias, estenosis o insuficiencias valvulares por la interferencia del tumor, derrame pericárdico, o pueden causar embolia pulmonar o sistémica si se fragmenta o desprende la masa.
El diagnóstico actualmente es multimodal con las diferentes técnicas de imagen disponibles10. La ecocardiografía habitualmente proporciona la sospecha diagnóstica inicial incluso desde el período prenatal, define el tamaño, la movilidad y la localización de la masa, su relación con las cámaras cardiacas y el pericardio, y valora la repercusión funcional de la masa en la hemodinámica del paciente. La RM cardiaca complementa la ecocardiografía, y actualmente es el patrón oro para hacer diagnóstico diferencial de las masas intracardiacas. La RM afina el diagnóstico histopatológico según sean las imágenes en T1-T2 y la captación tardía de gadolinio, y también permite valorar las estructuras extracardiacas. La tomografía computarizada cardiaca ayuda a definir las masas que tienen localización cercana a las arterias coronarias y también permite estudiar los órganos torácicos y abdominales para descartar un tumor primario en esas localizaciones. El cateterismo no se debe realizar para minimizar el riesgo de embolia asociada a fragmentación tumoral durante el procedimiento.
El tratamiento ha de ser individualizado en cada caso. Hay consenso internacional en que la resección quirúrgica está indicada si la masa intracardiaca produce síntomas de compromiso hemodinámico o respiratorio, arritmias severas o existe riesgo de embolismo sistémico. El objetivo de la cirugía será la resección completa de la masa, y si esto no es posible, hacer resección parcial para restaurar la anatomía y fisiología normales del corazón11. Las lesiones intracardiacas se abordan con circulación extracorpórea; si se localizan en el lado derecho del corazón y no asocian defecto septal se realizan con el corazón latiendo evitando la parada cardiaca. Generalmente, como la mayoría de las masas son benignas, se podrán respetar o, si es necesario, reparar las válvulas cardiacas afectadas. En nuestra experiencia, el explante de la masa se pudo hacer completo en el 92% de los casos, sin mortalidad y con un excelente resultado quirúrgico a corto y medio plazo.
En general, la MH tras la resección de masas de etiología benigna es muy baja, a diferencia de los tumores malignos, que asocian una elevada MH12. El seguimiento tras la resección de masas intracardiacas de etiología benigna es favorable, con bajas tasas de recidiva posterior y buena situación clínica de los pacientes13.
ConclusionesLas masas intracardiacas diagnosticadas en niños que requieren explante quirúrgico son muy poco frecuentes.
Recomendamos extirpar cualquier masa intracardiaca que obstruya significativamente el flujo sanguíneo o cause síntomas, para mejorar la clínica y filiar etiológicamente la misma. Nuestros resultados quirúrgicos son muy buenos, sin mortalidad ni reintervención en el seguimiento posterior.
FinanciaciónEste manuscrito no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.