Introducción y objetivos. Comparar la resección cuadrangular frente al uso de neocuerdas para el tratamiento del prolapso del componente P2 del velo posterior mitral en términos de evolución clínica, durabilidad y parámetros ecocardiográficos.
Métodos. Estudio de seguimiento longitudinal prospectivo que compara ambas técnicas. se analizaron los resultados clínicos (evento combinado [EC]: reintervención, accidente cerebrovascular, reingreso o muerte de causa cardiológica) y ecocardiográficos.
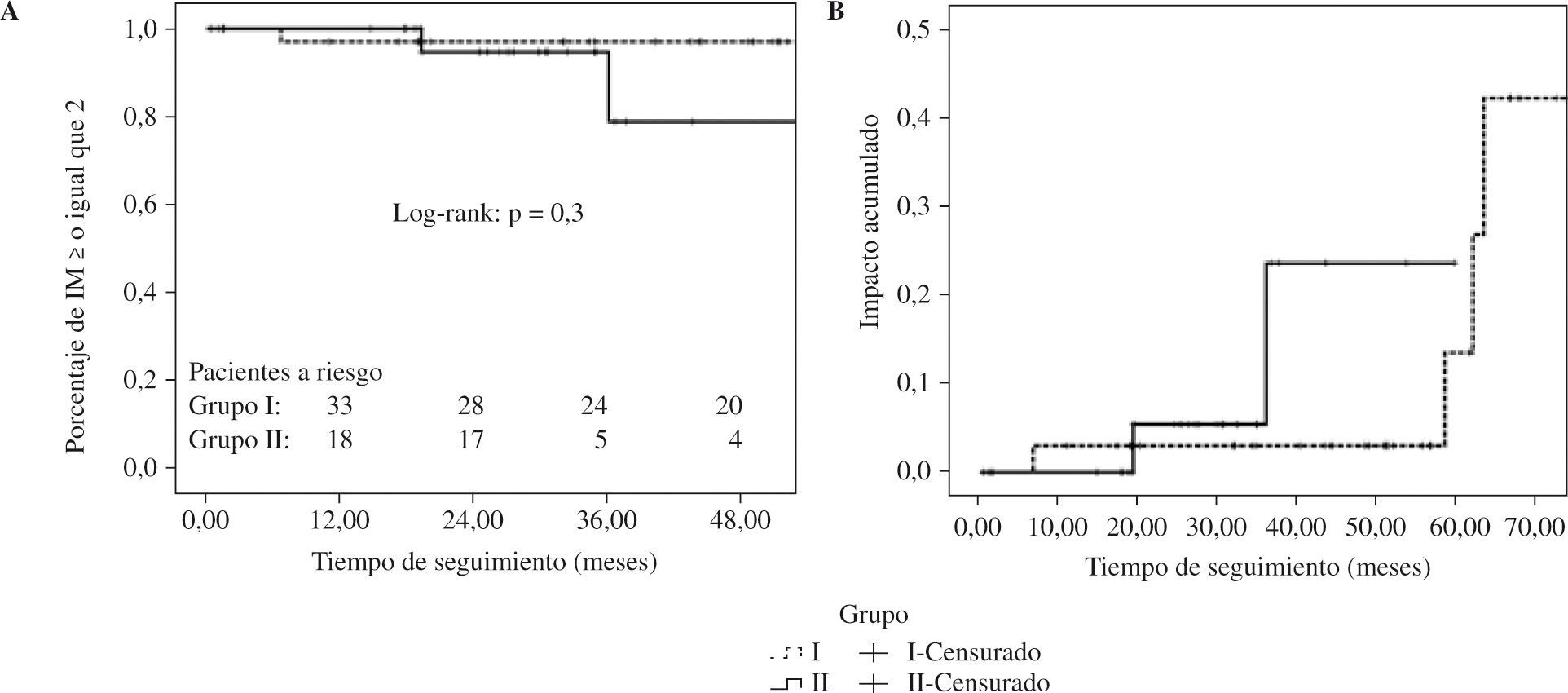
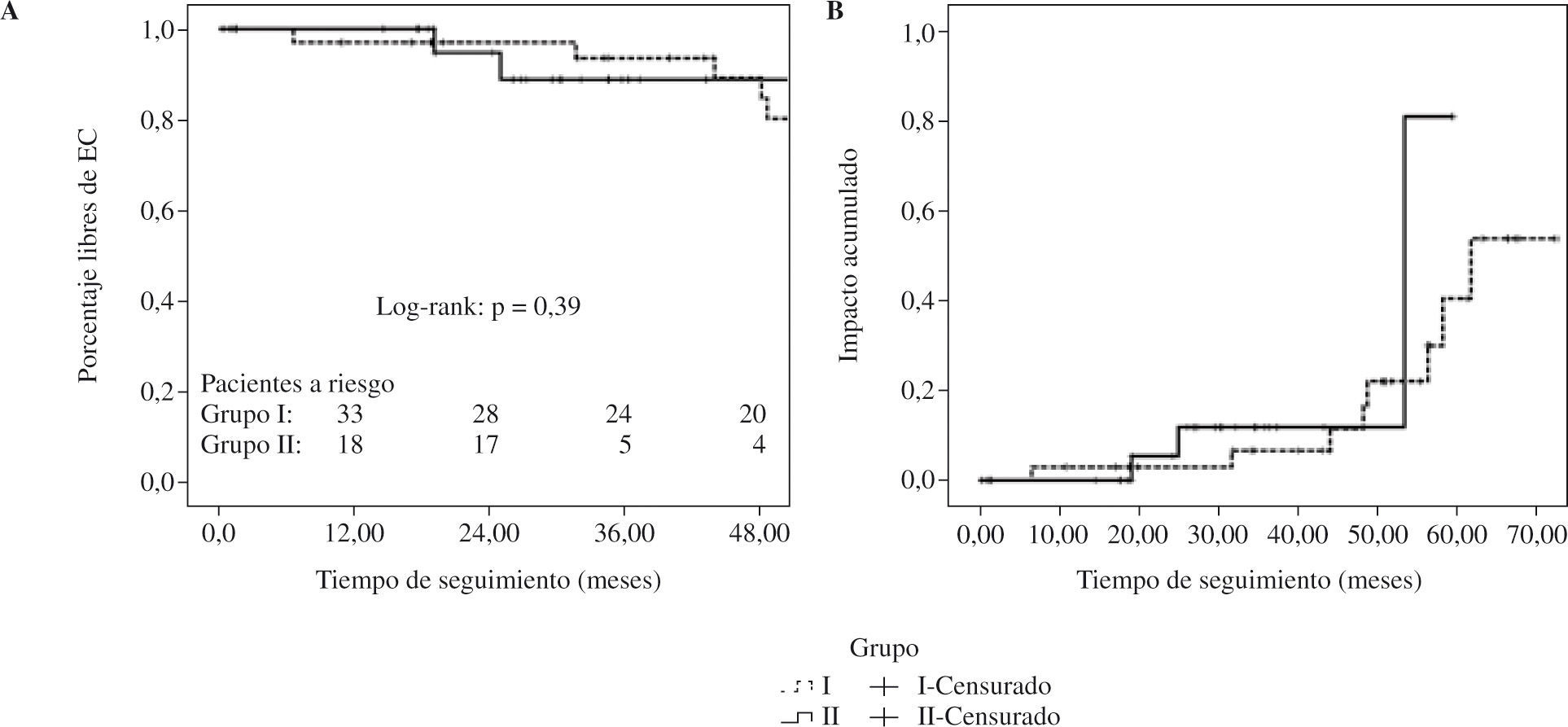
Resultados. Durante un periodo de 5 años y medio fueron intervenidos 63 pacientes por prolapso aislado de P2, con una edad media de 64,1 (desviación estándar [DE]: 13) años, 18 mujeres (27,1%). En 35 pacientes (55,5%) se realizó resección cuadrangular (grupo I) y en 28 (44,5%) se utilizaron neocuerdas (grupo II). Se observó una distribución homogénea del riesgo preoperatorio, EuroSCORE grupo I 2,5 (rango intercuartílico [RIQ]: 5,1) frente al grupo II 3,3 (RIQ: 4,4) (p=0,67). No hubo diferencias en la mortalidad ni en los tiempos de estancia postoperatoria. La supervivencia libre de insuficiencia mitral (IM) mayor o igual a 2 a los 12 y 36 meses fue de 97,1±0,06% y 87,4±1,9% en el grupo i frente a 94,7±0,1% y 89±0,3% en el grupo ii (log-rank: p=0,3). No hubo diferencias en los demás parámetros ecocardiográficos durante el seguimiento. La supervivencia libre de EC a los 12 y 36 meses fue similar en ambos grupos (grupo I: 97,1±0,06% y 93,6±0,08% vs grupo II: 94,7±0,1% y 89±0,15%; log-rank: p=0,39)
Conclusiones. En nuestra experiencia, la resección cuadrangular y el uso de neocuerdas mues-tran resultados similares a medio plazo en lo referente a durabilidad, evolución clínica y parámetros ecocardiográficos.
Background and objectives. To compare quadrangular resection with neochordae replacement for the repair of isolated P2 prolapse of the posterior mitral leaflet in terms of clinical progress, durability and echocardiography.
Patients and methods. In this longitudinal prospective study we compare both techniques. Outcome measures analysed during follow-up were clinical (combined event: redo surgery, neurological damage, readmission or death of cardiological cause) and echocardiographic data.
Results. Sixty-three patients underwent surgery for isolated P2 prolapse over a 5 and 1/2-year period. mean patient age was 64.1 (SD: 13) years, and 18 patients were women (27.1%). In 35 patients (55.5%) the procedure was quadrangular resection (group I) and in 28 (44.5%) neochordae were inserted (group II). Preoperative risk using the EuroSCORE was similar in group I 2.5 (IQR: 5.1) and group II 3.3 (IQR: 4.4) (p=0.67). No differences were recorded in mortality or postoperative hospital stay. The percentages of patients free of mitral regurgitation greater or equal to 2 at 12 and 36 months were 97.1±0.06% and 87.4±1.9% in group I vs. 94.7±0.1% and 89±0.3% in group II (log-rank: p=0.3). The remaining echocardiographic variables were similar in the two groups during follow-up. Patients free of a combined event at 12 and 36 months were similar in the two groups (group I: 97.1±0.06% and 93.6±0.08% vs. group II: 94.7± 0.1% and 89±0.15%; log-rank: p=0.39).
Conclusions. Both techniques, quadrangular resection and the use of neochordae provided similar midterm results in terms of durability, clinical progress and echocardiography.
La reparación valvular mitral es la técnica de elección para el tratamiento de la IM de origen degenerativo con unos resultados de supervivencia y durabilidad ampliamente contrastados1–4. El prolapso del velo posterior por cambios degenerativos que afectan al tejido valvular y/o cuerdas tendinosas constituye el hallazgo más frecuente en esta patología. La resección cuadrangular es la técnica más utilizada para el tratamiento de este subgrupo de enfermos con unos excelentes resultados clínicos y de durabilidad a largo plazo1–6.
Como técnica alternativa a la resección cuadrangular para el tratamiento del prolapso del velo posterior se ha desarrollado en los últimos años el uso de neocuerdas de politetrafluoroetileno expandido (PTFE). Este procedimiento trata de conservar una mayor cantidad de tejido valvular y ha demostrado ser reproducible y duradero, por lo que en la actualidad se está extendiendo su uso entre numerosos grupos quirúrgicos7–13.
El objetivo del presente estudio es comparar ambas técnicas para el tratamiento del prolapso del festón P2 del velo posterior mitral en lo referente a la evolución clínica, durabilidad y parámetros ecocardiográficos. Como hipótesis de trabajo tratamos de analizar las diferencias en la evolución clínica y de los valores ecocardiográficos a medio plazo entre ambas técnicas en una serie prospec-tiva de pacientes intervenidos en nuestro centro.
Material y métodoseDiseño y población a estudioEstudio de seguimiento longitudinal prospectivo sobre una serie consecutiva de pacientes intervenidos de cirugía reparadora mitral por prolapso aislado del festón P2 del velo posterior mitral, definido según los hallazgos ecocardiográficos preoperatorios e intraoperatorios. Los pacientes fueron intervenidos entre enero de 2005 y junio de 2010. Sobre esta serie fueron analizados los resultados quirúrgicos y de seguimiento de forma comparativa entre el grupo de pacientes tratados mediante resección cuadrangular (grupo I) y el grupo en el que se utilizó neocuerdas de PTFE (grupo II). Las intervenciones fueron realizadas por cirujanos con una experiencia previa de más de 30 reparaciones mitrales, y el único criterio para la elección de la técnica fue exclusivamen-te la preferencia del cirujano.
Se recogieron de forma prospectiva las variables clínicas preoperatorias (clase funcional de New York Heart Association [NYHA], presencia de ritmo sinusal en el electrocardiograma (ECG) de doce derivaciones, índice de masa corporal (IMC) y variables del EuroSCORE), intraoperatorias (tipo de cirugía, diámetro del anillo implantado, procedimientos asociados, tiempo de circulación extracorpórea [CEC] e isquemia miocárdica). Se recogieron a su vez los datos de evolución postoperatoria: mortalidad y tiempos de estancia en unidad de vigilancia intensiva (UVI) y hospitalaria.
Técnica quirúrgicaTodos los pacientes fueron intervenidos mediante esternotomía media, el uso de CEC con canulación bicava, cardioplejía hemática fría e hipotermia moderada (32 °C). Se accedió a la aurícula izquierda a través del surco interauricular, y tras la exposición y análisis de los diferentes segmentos valvulares, según la clasificación de Carpentier5,6, se realizaron las distintas técnicas repara-doras. La resección cuadrangular se llevó a cabo según la técnica habitual previamente descrita5,6. Para el uso de neocuerdas se empleó sutura de PTFE de cinco ceros (Goretex CV™, Flagstaff, Arizona, USA). Tras un punto de doble pasada en lazo sobre la cabeza del músculo papilar se hace pasar por el borde libre del velo desde la cara ventricular a la auricular, se anuda con tres nudos y desde la cara auricular del velo se pasa nuevamente para su anudado definitivo en la cara ventricular. En todos los pacientes se implantó un anillo Physio Carpentier-Edwards (Edwards Life-Sciences™, Irving, California, USA).
Estudio ecocardiográfico y seguimientoTodos los pacientes fueron estudiados mediante ecocardiograma transesofágico y transtorácico preoperatorio, transesofágico intraoperatorio y transtorácico al alta, al mes de la cirugía y de forma anual durante el seguimiento.
Los estudios de eco-Doppler fueron realizados con un equipo Philips IE-338 (Philips Medical Systems, DA Best, Netherland). Las mediciones se realizaron siguiendo las recomendaciones de la Sociedad Europea de Ecocardiografía (Recommendations for chamber quantification)14,15. La proyección en el eje parasternal largo en modo M se utilizó para medir los diámetros auricular izquierdo, telesistólico (DTSVI) y telediastólico (DTDVI) ventriculares izquierdos. La fracción de eyección se calculó por el método biplano de Simpson, empleando las proyecciones bidimensionales de dos y cuatro cámaras. La presión sistólica de la arteria pulmonar se calculó añadiendo la presión estimada de la aurícula derecha al gradiente entre el ventrículo derecho y aurícula derecha, obtenido a través de la regurgitación tricuspídea según la ecuación simplificada de Bernouilli.
La IM se cuantificó en cinco grados (0=sin IM, 1=IM ligera, 2=IM leve-moderada, 3=IM moderada-grave, 4=IM grave), según el tamaño de la vena contracta, el método proximal isovelocity surface area (PISA) y otros parámetros semicuantitativos14,15.
Los pacientes fueron seguidos en consultas externas al mes de la cirugía y posteriormente de forma anual. Durante el seguimiento se recogió la situación clínica (clase funcional de NYHA), el ritmo de base mediante ECG de 12 derivaciones, la historia de reingreso hospitalario por causa cardiológica (arritmia o insuficiencia cardíaca), la necesidad de reintervención y la presencia de accidente cerebrovascular. Se definió EC cuando el paciente presentó durante el seguimiento al menos una de las siguientes complicaciones: reingreso de causa cardiológica, reintervención por nueva IM, accidente cerebrovascular o muerte de causa cardíaca. Respecto a los parámetros ecocardiográficos, fueron analizados aquellos obtenidos en el último ecocardiograma realizado.
Análisis estadísticoSe utilizó el programa SPSS versión 17.0 (SPSS™, Chicago, Illinois, USA) para realizar el análisis estadístico. Las variables categóricas son presentadas en n (%) y las continuas como la media con la DE o la mediana con el rango intercuartílico (RIQ) si no siguen una distribución normal. Se comprobó el supuesto de normalidad con las pruebas de Kolmogorov-Smirnof y la homogeneidad de las varianzas.
Se utilizó la prueba de x2 (prueba exacta de Fisher si alguna de las frecuencias esperadas era < 5) para comparar las variables categóricas entre ambos grupos, y la prueba t de Student para las variables continuas (prueba de U de Mann-Whitney si no seguían una distribución normal). La medida de asociación se calculó mediante el riesgo relativo (RR) o la diferencia entre las medias (DM) con su intervalo de confianza (IC) del 95%. Para la comparación de las medidas de cambio intrasujeto se utilizó la prueba t de Student para datos emparejados (prueba de t de Wilcoxon si no existía una distribución normal)16.
Posteriormente, se construyeron mediante el método de Kaplan-Meier las curvas de tiempo libre de IM igual o superior a 2 y EC. Las diferencias entre ambos grupos se analizaron con la prueba de log-rank. Se consideró la significación estadística para p inferior a 0,05 (bilateral).
ResultadosCaracterísticas de la poblaciónDurante el periodo comprendido entre enero de 2005 y junio de 2010 (5 años y medio) se realizaron en nuestro servicio 202 reparaciones de la válvula mitral, de las cuales, 63 (31,2%) presentaban un prolapso aislado del festón P2 de la valva posterior mitral. En 35 (55,5%) enfermos se realizó resección cuadrangular como técnica reparadora (grupo I) y en los 28 (44,5%) restantes se implantaron neocuerdas de PTFE (grupo II). La edad media de la serie fue 64,1 (DE: 13) años, con 18 mujeres (27,1%) y una clase funcional NYHA media preoperatoria de 2,3 (DE: 0,8). El grado de IM preoperatoria era de 3,9 (DE: 0,36) y la mediana del EuroSCORE logístico en el grupo total fue 3 (RIQ: 4,6).
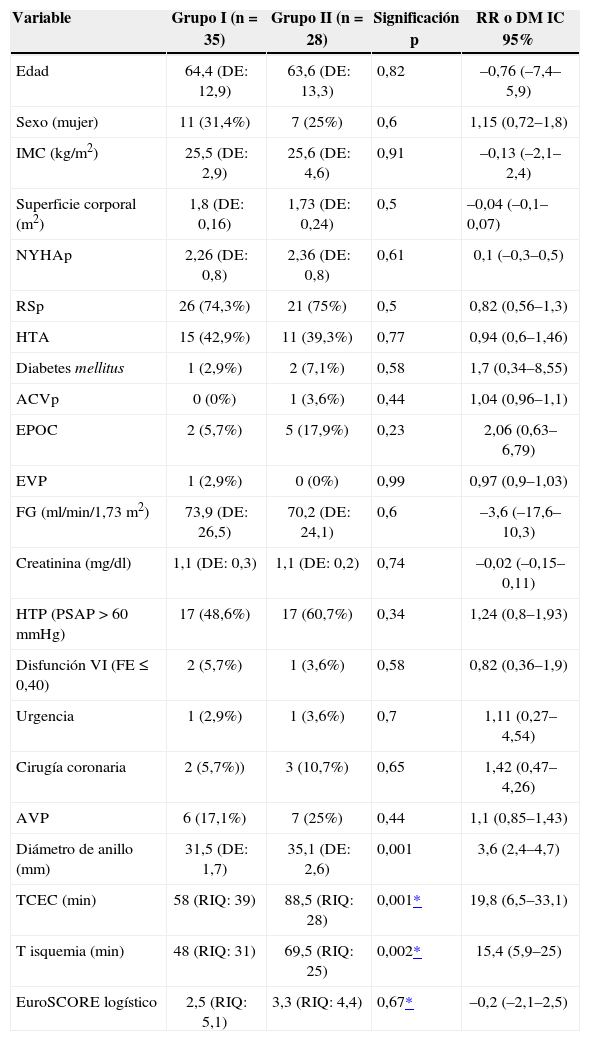
Resultados preoperatorios e intraoperatorios comparativos entre ambos grupos>Las tablas I y II muestran los datos comparativos de las variables preoperatorias, intraoperatorias y los parámetros ecocardiográficos prequirúrgicos entre los grupos I y II. Se observa una distribución homogénea de las variables preoperatorias, lo cual se traduce en un EuroS-CORE similar en ambos grupos; grupo I: 2,5 (RIQ: 5,1) frente a grupo II: 3,3 (RIQ: 4,4) (p=0,67; DM: –0,2 [–2,1–2,5]). En cuanto a las variables intraoperatorias se observan unos tiempos de CEC e isquemia más prolon-gados en el grupo II; tiempo CEC grupo I: 58 (RIQ: 39) min frente al grupo II: 88,5 (RIQ: 28) min (p=0,001; DM: 19,8 [6,5–33,1]); tiempo de isquemia grupo I: 48 (RIQ: 31) min frente al grupo II: 69,5 (RIQ: 25) min (p=0,002; DM: 15,4 [5,9–25]). Por otra parte, es de destacar como fueron implantados anillos de mayor diá-metro en el grupo II; media de anillo en el grupo I: 31,5 (DE: 1,7) mm frente al grupo II: 35,1 (DE: 2,6) mm (p = 0,001; DM: 3,6 [2,4–4,7]).
Distribución entre ambos grupos de las variables preoperatorias e intraoperatorias. grupo i: resección cuadrangular vs grupo II: Uso de neocuerdas
| Variable | Grupo I (n=35) | Grupo II (n=28) | Significación p | RR o DM IC 95% |
| Edad | 64,4 (DE: 12,9) | 63,6 (DE: 13,3) | 0,82 | –0,76 (–7,4–5,9) |
| Sexo (mujer) | 11 (31,4%) | 7 (25%) | 0,6 | 1,15 (0,72–1,8) |
| IMC (kg/m2) | 25,5 (DE: 2,9) | 25,6 (DE: 4,6) | 0,91 | –0,13 (–2,1–2,4) |
| Superficie corporal (m2) | 1,8 (DE: 0,16) | 1,73 (DE: 0,24) | 0,5 | –0,04 (–0,1–0,07) |
| NYHAp | 2,26 (DE: 0,8) | 2,36 (DE: 0,8) | 0,61 | 0,1 (–0,3–0,5) |
| RSp | 26 (74,3%) | 21 (75%) | 0,5 | 0,82 (0,56–1,3) |
| HTA | 15 (42,9%) | 11 (39,3%) | 0,77 | 0,94 (0,6–1,46) |
| Diabetes mellitus | 1 (2,9%) | 2 (7,1%) | 0,58 | 1,7 (0,34–8,55) |
| ACVp | 0 (0%) | 1 (3,6%) | 0,44 | 1,04 (0,96–1,1) |
| EPOC | 2 (5,7%) | 5 (17,9%) | 0,23 | 2,06 (0,63–6,79) |
| EVP | 1 (2,9%) | 0 (0%) | 0,99 | 0,97 (0,9–1,03) |
| FG (ml/min/1,73m2) | 73,9 (DE: 26,5) | 70,2 (DE: 24,1) | 0,6 | –3,6 (–17,6–10,3) |
| Creatinina (mg/dl) | 1,1 (DE: 0,3) | 1,1 (DE: 0,2) | 0,74 | –0,02 (–0,15–0,11) |
| HTP (PSAP > 60mmHg) | 17 (48,6%) | 17 (60,7%) | 0,34 | 1,24 (0,8–1,93) |
| Disfunción VI (FE ≤ 0,40) | 2 (5,7%) | 1 (3,6%) | 0,58 | 0,82 (0,36–1,9) |
| Urgencia | 1 (2,9%) | 1 (3,6%) | 0,7 | 1,11 (0,27–4,54) |
| Cirugía coronaria | 2 (5,7%)) | 3 (10,7%) | 0,65 | 1,42 (0,47–4,26) |
| AVP | 6 (17,1%) | 7 (25%) | 0,44 | 1,1 (0,85–1,43) |
| Diámetro de anillo (mm) | 31,5 (DE: 1,7) | 35,1 (DE: 2,6) | 0,001 | 3,6 (2,4–4,7) |
| TCEC (min) | 58 (RIQ: 39) | 88,5 (RIQ: 28) | 0,001* | 19,8 (6,5–33,1) |
| T isquemia (min) | 48 (RIQ: 31) | 69,5 (RIQ: 25) | 0,002* | 15,4 (5,9–25) |
| EuroSCORE logístico | 2,5 (RIQ: 5,1) | 3,3 (RIQ: 4,4) | 0,67* | –0,2 (–2,1–2,5) |
NYHAp: clase NYHA preoperatoria; RSp: ritmo sinusal preoperatorio; HTA: hipertensión arterial; ACVp: accidente cerebrovascular agudo preoperatorio; EVP: enfermedad vascular periférica; FG: filtrado glomerular estimado con la fórmula modification of diet in renal disease (MDRD-4); HTP: hipertensión pulmonar; PSAP: presión sistólica de arteria pulmonar; VI: ventrículo izquierdo; FE: fracción de eyección; AVP: ablación de venas pulmonares; TCEC: tiempo circulación extracorpórea; T isquemia: tiempo de isquemia miocárdica.
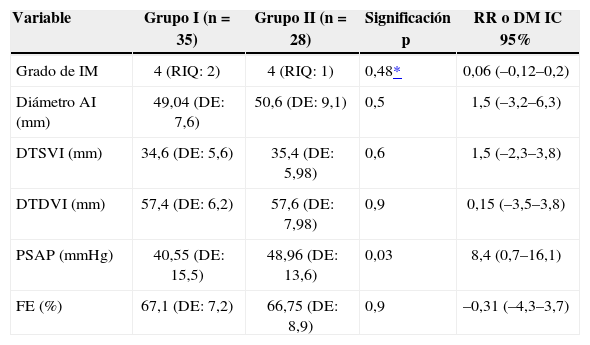
En lo referente a los parámetros ecocardiográficos preoperatorios, el grupo II presentó una presión sistólica de arteria pulmonar media mayor que el grupo I: grupo I: 40,55 (DE: 15,5) mmHg frente al grupo II: 48,96 (DE: 13,6) mmHg (p=0,03; DM: 8,4 [0,7–16,1]) y no se observaron diferencias significativas en el resto de los parámetros (Tabla II).
Distribución entre ambos grupos de los parámetros ecocardiográficos preoperatorios. grupo i: resección cuadrangular vs grupo II: Uso de neocuerdas
| Variable | Grupo I (n=35) | Grupo II (n=28) | Significación p | RR o DM IC 95% |
| Grado de IM | 4 (RIQ: 2) | 4 (RIQ: 1) | 0,48* | 0,06 (–0,12–0,2) |
| Diámetro AI (mm) | 49,04 (DE: 7,6) | 50,6 (DE: 9,1) | 0,5 | 1,5 (–3,2–6,3) |
| DTSVI (mm) | 34,6 (DE: 5,6) | 35,4 (DE: 5,98) | 0,6 | 1,5 (–2,3–3,8) |
| DTDVI (mm) | 57,4 (DE: 6,2) | 57,6 (DE: 7,98) | 0,9 | 0,15 (–3,5–3,8) |
| PSAP (mmHg) | 40,55 (DE: 15,5) | 48,96 (DE: 13,6) | 0,03 | 8,4 (0,7–16,1) |
| FE (%) | 67,1 (DE: 7,2) | 66,75 (DE: 8,9) | 0,9 | –0,31 (–4,3–3,7) |
AI: aurícula izquierda (mm); FE: fracción de eyección; PSAP: presión sistólica de arteria pulmonar.
Una paciente perteneciente al grupo II falleció en el postoperatorio inmediato por daño neurológico grave, sin que se observaran diferencias significativas entre ambos grupos respecto a la mortalidad. No hubo diferencias en las estancias en UVI y postoperatoria: la media de estancia postoperatoria en el grupo I fue 9,4 días (DE: 4,1) frente a 11,2 días (DE: 5,9) en el grupo II (p=0,44; DM: 1,8 [–2,8–6,5]), mientras que la mediana de estancia en unidad de cuidados intensivos (UCI) en el grupo I fue 1 (RIQ: 2) día frente a 1 (RIQ: 21) día en el grupo II (p=0,72; DM: 1,23 [–2,1–2,9]).
Seguimiento clínico y ecocardiográficoSe completó el seguimiento clínico y ecocardiográfico en 62 pacientes (98,4%), de los cuales 55 (87,4%) completaron el seguimiento al menos 1 año, con una media y mediana de seguimiento de 37,1 (DE: 19,7) y 34,6 (RIQ: 34,7) meses, respectivamente.
La clase funcional NYHA durante el seguimiento fue similar entre ambos grupos (grupo I: 1,3 [DE: 0,52] vs grupo II: 1,1 [DE: 0,57]; p=0,24), mientras que el 74,4% (26/35) de los pacientes del grupo I y el 82,14% (23/28) del grupo II permanecían en ritmo sinusal (p=0,46).
En el grupo total se observó una reducción de todos los valores de los parámetros ecocardiográficos respecto a los valores preoperatorios, salvo en la fracción de eyección: diámetro aurícula izquierda (pre: 50,4mm vs post: 46,4mm; p=0,009), DTSVI (pre: 35,2mm vs post: 31,3mm; p=0,0001), DTDVI (pre: 57,6mm vs post: 49,4mm; p=0,0001), presión sistólica de arteria pulmonar (pre: 45,2mmHg vs post: 33,6mmHg; p=0,0001), fracción de eyección (pre: 66,7 vs post: 65,5; p=0,31) y grado de IM (pre: 3,9 vs post: 1,03; p=0,0001).
Al comparar estos valores ecocardiográficos durante el seguimiento entre los grupos I y II no se observaron diferen-cias significativas (Tabla III). La figura 1 muestra los resultados comparativos entre el grupo I y II de la IM residual durante el seguimiento. IM grupo I: 1 (RIQ: 3) frente a grupo II: 1 (RIQ: 2) (p=0,37; DM: 0,23 [–0,28–0,74]). En esta figura se observa cómo cuatro pacientes en el grupo I y uno en el grupo II presentaban una IM grado III o I V.
Distribución entre ambos grupos de los parámetros ecocardiográficos durante el seguimiento. grupo i: resección cuadrangular vs grupo II: Uso de neocuerdas
| Variable | Grupo I (n=35) | Grupo II (n=28) | significación p | RR o DM IC 95% |
| Grado de IM | 1 (RIQ: 3) | 1 (RIQ: 2) | 0,37* | 0,23 (–0,28–0,74) |
| Diámetro AI (mm) | 47,4 (DE: 9,3) | 45,9 (DE: 90,1) | 0,54 | 1,6 (–3,6–6,7) |
| DTSVI (mm) | 31,8 (DE: 7) | 31 (DE: 6,97) | 0,7 | 0,8 (–3,1–4,8) |
| DTDVI (mm) | 49,3 (DE: 6,4) | 49,7 (DE: 5,8) | 0,8 | –0,44 (–3,7–2,9) |
| PSAP (mmHg) | 31,7 (DE: 10,2) | 34,9 (DE: 8,6) | 0,24 | –3,2 (–8,6–2,2) |
| FE (%) | 66,2 (DE: 9,2) | 64,7 (DE: 12,3) | 0,61 | 1,45 (–4,2–7,1) |
AI: aurícula izquierda (mm); FE: fracción de eyección; PSAP: presión sistólica de arteria pulmonar.
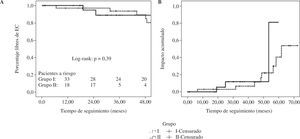
Durante el seguimiento 6 pacientes (17,1%) en el grupo I y 2 pacientes (7,1%) en el grupo II presentaban IM igual o superior a 2. La figura 2 muestra las estimaciones comparativas entre ambos grupos del porcentaje libre de IM igual o superior a 2 así como la función de riesgo. El porcentaje estimado de pacientes libres de IM igual o superior a 2 a los 12 y 36 meses en el grupo I fue del 97,1±0,06% y 87,4±1,9% frente al 94,7±0,1% y 89±0,3% en el grupo II (p=0,3) (Fig. 2).
Por otra parte, se computaron 12 EC durante el se-guimiento, 9 (25,7%) pacientes en el grupo I y 3 (10,7%) pacientes en el grupo II. El porcentaje libre estimado de EC a los 12 y 36 meses en el grupo I fue del 97,1±0,06% y 93,6±0,08% frente al 94,7±0,1% y 89±0,15%, respectivamente (p=0,39) (Fig. 3). Durante este seguimiento fueron reintervenidos 3 pacientes (8,6%) en el grupo I y uno (3,6%) en el grupo II, estimándo-se una supervivencia libre de reintervención a los 12 y 36 meses del 97,1±0,06% y 93,6±0,09% en el grupo I frente a 94,7±0,9% y 92,1±0,6% en el grupo II (p=0,95). Las causas que llevaron a la reintervención fueron retracción del velo posterior en todos los casos del grupo I y desarrollo de prolapso del velo anterior en el caso del grupo II.
DiscusiónLa resección cuadrangular del velo posterior ha sido considerada durante muchos años la técnica de elección para el tratamiento del prolapso del festón P2 del velo posterior mitral, motivado por unos excelentes resultados de durabilidad a largo plazo y por ser una técnica relativamente sencilla y reproducible1–6. Sin embargo, esta técnica basada en una plicatura del anillo mitral y en la reaproximación de los bordes del velo convierte a la válvula mitral en una válvula prácticamente monocúspide en la que el velo queda rígido sin apenas movilidad, y en la que el diámetro del anillo mitral queda sensiblemente reducido con una disminución del área efectiva10. Por este motivo, se han desarrollado técnicas que tratan de preservar la movilidad del velo posterior como la resec-ción triangular o el uso de neocuerdas de PTFE7,8,10,17. El uso de neocuerdas de PTFE fue introducido en el año 1985 para el tratamiento del prolapso del velo anterior, y posteriormente se extendió su uso al velo posterior7. Basado en la filosofía «respetar más que resecar», el uso de neocuerdas trata de preservar la mayor cantidad de tejido valvular para así conseguir una mayor superficie de coaptación y una mayor área efectiva, parámetros que han demostrado ser predictores de la durabilidad a largo plazo de la reparación8,10,18. Otra posible ventaja de esta técnica es la extensión de su uso para el trata-miento de la patología de la valva anterior o de ambos velos, en las cuales las técnicas clásicas como la transposición de cuerdas tendinosas o la técnica de deslizamiento son menos reproducibles. Perier, et al. publican en 2005 los resultados a largo plazo de una serie de 225 pacientes intervenidos por prolapso del velo posterior mediante el uso de neocuerdas, comunicando una excelente durabilidad de la técnica a largo plazo (88% de los pacientes con IM < 2 a los 10 años)19.
En este trabajo hemos tratado de comparar los resultados de ambas técnicas para el tratamiento del prolapso aislado del festón P2 del velo posterior mitral y determinar si existen diferencias en la durabilidad y en la evolución clínica o ecocardiográfica. Seleccio-namos pacientes con el prolapso aislado del festón P2 con el objeto de comparar grupos homogéneos respecto a las características anatómicas, evitando incluir pacientes con afectación de otros segmentos valvulares en los que fuera preciso modificar la técnica quirúrgica.
El hallazgo fundamental de este estudio es que no encontramos diferencias en lo referente a evolución clínica (presencia de eventos cardiológicos) ni en los valores ecocardiográficos durante el seguimiento (grado de IM residual).
Los estudios que han tratado de comparar ambas técnicas han obtenido resultados similares. Falk, et al., sobre una serie de 129 enfermos, no encontraron diferencias entre ambas técnicas en los resultados intrahospitalarios ni en los parámetros ecocardiográficos durante el seguimiento9. Únicamente los tiempos de CEC e isquemia miocárdica fueron superiores en el grupo en los que se utilizó neocuerdas, hecho que coincide con los resultados del presente estudio. Pertenecien-te a este mismo grupo quirúrgico, Seeburguer, et al. publican 2 años después los resultados comparativos entre ambas técnicas en una serie de 670 pacientes12. En este estudio se observó en el postoperatorio inmedia-to una mayor área mitral efectiva y una mayor superficie de coaptación en el grupo de neocuerdas, así como una menor tasa de reintervención durante el seguimiento a medio plazo. Sin embargo, tras realizar un análisis multivariante con el método de Cox, la técnica empleada no fue un predictor independiente de reintervención. En nuestra serie observamos una tendencia no significativa a partir de los 60 meses en el tiempo libre de IM igual o superior a 2 a favor del uso de neocuerdas. Quizás el tamaño muestral reducido de este trabajo pueda explicar estos hallazgos. Por lo tanto, queda por determinar con claridad el impacto de la mayor superficie de coaptación y área efectiva conseguidas con el uso de neocuerdas en la durabilidad a largo plazo de la reparación.
Por último, Lange, et al. publican una serie consecutiva de 397 pacientes intervenidos por prolapso del velo posterior mitral mediante ambas técnicas13. No se obser-varon diferencias en la evolución intrahospitalaria ni en el seguimiento, a excepción de una media de diámetro del anillo implantado superior en el grupo de neocuerdas y una tendencia a menor tasa de reintervención en grupo de resección cuadrangular, hallazgos que coinciden con el presente estudio.
En resumen, en nuestra experiencia, el uso de neocuerdas de PTFE para el tratamiento del prolapso aislado del festón P2 del velo posterior mitral ofrece unos resultados a medio plazo similares a la resección cuadrangular en cuanto a la evolución clínica y pará-metros ecocardiográficos. Queda por determinar si el uso de neocuerdas pudiera ofrecer una mayor durabilidad de la reparación a largo plazo cuando las series recojan mayor número de pacientes y mayor tiempo de seguimiento.
Limitaciones del estudioComo limitación del presente estudio se observa un número de pacientes reducido que genera una disminución de la potencia creando un posible error estadístico tipo II. Por otra parte, aunque se trate de un estudio de seguimiento prospectivo, la no aleatorización pudiera motivar la existencia de un sesgo de selección. Sin embargo, debido a la consistencia en los resultados con otros estudios que obtienen datos similares, creemos que las conclusiones obtenidas son válidas.