La fístula atrioesofágica (FAE) es una complicación infrecuente pero mortal de la ablación por radiofrecuencia (ARF) utilizada para tratar la fibrilación auricular (FA), con una incidencia estimada del 0,03-0,08%. En la bibliografía publicada hasta la fecha, la mortalidad es cercana al 100%, sin tratamiento quirúrgico. Presentamos el caso de un varón de 72 años con antecedentes de FA crónica que desarrolló FAE al mes de la ARF, desarrollando ictus embólico bilateral. Dado el elevado riesgo quirúrgico, tras discusión multidisciplinar del caso, se abordó de manera conservadora con la colocación de una prótesis esofágica (PE) bajo control radiológico y tratamiento antibiótico, logrando una evolución favorable. Aunque la cirugía es el tratamiento de elección, en nuestro caso, la intervención conservadora resultó exitosa, evitando la necesidad de circulación extracorpórea y reduciendo el riesgo de complicaciones neurológicas. Este caso resalta la importancia del diagnóstico temprano y el enfoque multidisciplinar en los pacientes con riesgo quirúrgico elevado.
Atrial-esophageal fistula (AEF) is a rare but life-threatening complication of radiofrequency ablation (RFA) for atrial fibrillation (AF), with an estimated incidence of 0,03 - 0,08%. In the literature published, mortality is close to 100% without surgical treatment. We report the case of a 72-year-old man with chronic AF who developed an AEF 30 days post-RFA and with bilateral stroke. A conservative approach was taken, involving the placement of an esophageal stent under radiological guidance and antibiotic therapy, resulting in a favorable outcome. Although surgery is the treatment of choice, in our case, the conservative intervention was successful, avoiding the need for extracorporeal circulation and reducing the risk of neurological complications. This case highlights the importance of early diagnosis and multidisciplinary options in patients with high surgical risk.
La fístula atrioesofágica (FAE) es una complicación infrecuente de la ablación por radiofrecuencia (ARF) utilizada para el tratamiento de la fibrilación auricular (FA)1. Se estima que tiene una incidencia entre el 0,03% y el 0,08%, pero podría estar subestimada debido a una notificación insuficiente o a un diagnóstico erróneo2. La FAE se presenta usualmente entre los días 3 y 60 del posprocedimiento3. El cuadro clínico incluye fiebre, disfagia, hemorragia gastrointestinal (GI), sepsis por un microorganismo de origen gastrointestinal y accidente cerebrovascular (ACV) embólico en un paciente con antecedente de ARF4. No existe un consenso definido sobre el manejo de esta complicación, pero la cirugía emergente se considera una piedra angular de su tratamiento, reportándose mortalidades próximas al 100% en los pacientes no intervenidos. Esta mortalidad suele ser secundaria a un ACV por embolia séptica o aérea. En este documento reportamos un caso de FAE por ARF tratado exitosamente de manera conservadora.
Caso clínicoVarón de 72 años, con antecedente de obesidad, FA crónica anticoagulada con edoxabán, diabetes mellitus tipo 2 (DM2) e hipertensión arterial (HTA). Acude a urgencias por fiebre termometrada de 3 días de evolución, con tiritona, escalofríos, cefalea intensa, molestias epigástricas inespecíficas y vómitos. Inicialmente se catalogó como probable colangitis y fue ingresado como síndrome febril para estudio e inicio de tratamiento antibiótico dirigido.
A la exploración física el paciente presentaba una frecuencia cardiaca de 70lpm, tensión arterial 160/60, temperatura 36,7°C y saturación arterial del 97%. El examen físico no reveló ninguna otra alteración significativa.
En la analítica destacaba presencia de leucocitosis (24.900 leucocitos/mm3) con proteína C reactiva (PCR) 143,8mg/l y procalcitonina (PCT) 8,48ng/ml. El ECG demostró que el paciente se encontraba en ritmo sinusal. La radiografía de tórax mostraba una leve cardiomegalia y una TC craneal, solicitado por cefalea intensa, que no mostraba alteraciones significativas.
El paciente presentaba el antecedente de haber sido intervenido 30 días antes del episodio actual de una ARF de venas pulmonares por fibrilo-flutter auricular. El procedimiento de ablación se había realizado bajo anestesia general, con catéter Orbiter® de 24 polos que a través de punción femoral se avanzó hasta aurícula derecha-seno coronario. Mediante punción transeptal se progresó a la aurícula izquierda catéter de mapeo Hd-Grid y catéter de ablación irrigado. Con sistema NavX® se realizó mapa de activación en taquicardia de aurícula izquierda compatible con reentrada auricular en las 2 venas pulmonares derechas. La aplicación puntual de radiofrecuencia a 25-35W en vena superior derecha interrumpió el flutter. El procedimiento transcurrió sin complicaciones inmediatas. En las semanas siguientes el paciente presentó dolor torácico inespecífico, que fue atribuido a probable pericarditis posprocedimiento, por el cual no recibió ningún tratamiento específico.
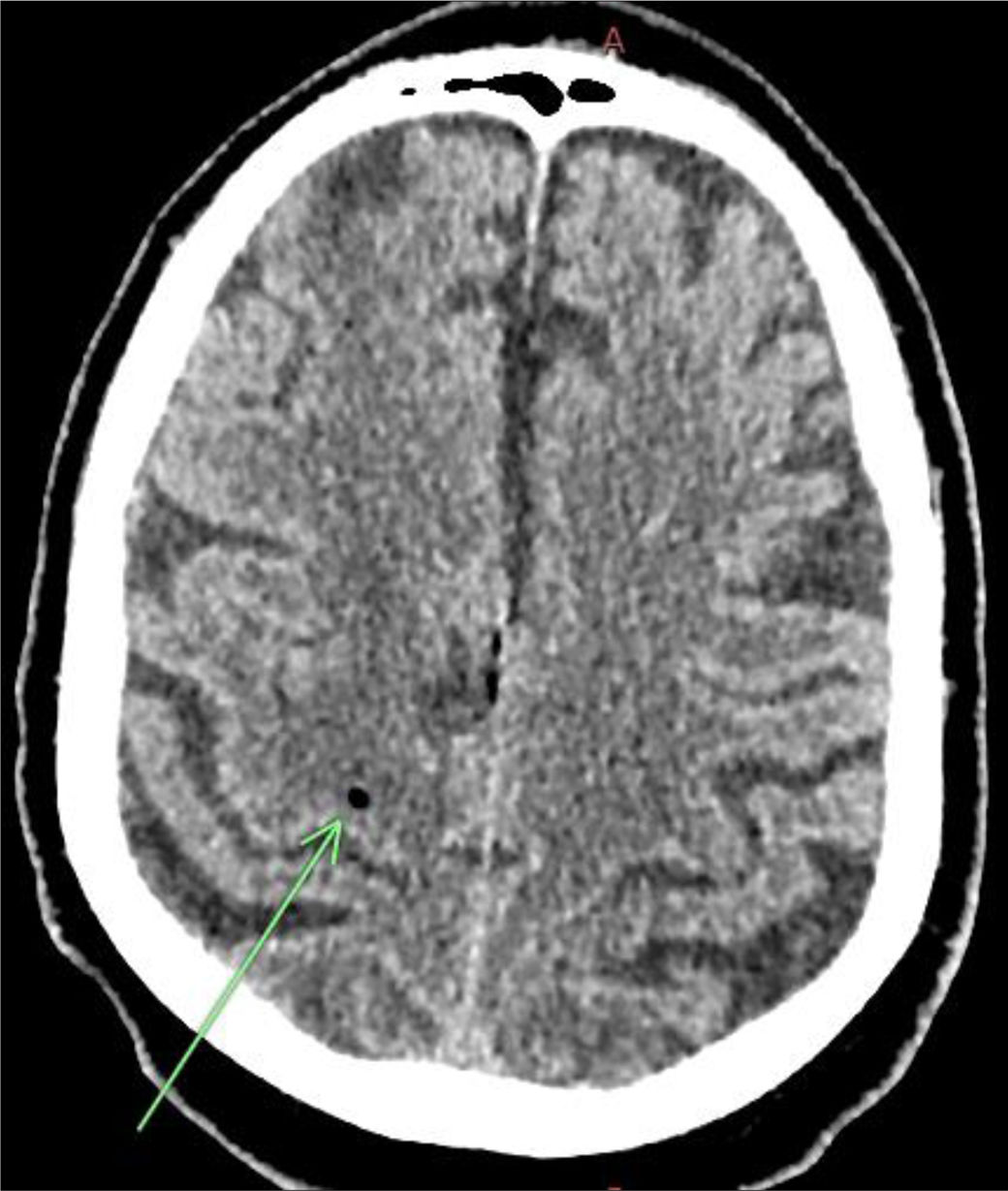
A las 24h del ingreso presentó de manera súbita una alteración progresiva del nivel de conciencia y desaturación. El examen físico evidenció un Glasgow (GCS) de 10 (O:1V:4M:5) y hemiplejia izquierda. Persistía hemodinámicamente estable y en ritmo sinusal. Se solicitó una nueva TC craneal, que demostró la existencia de infarto isquémico agudo establecido en territorio frontoparietal derecho con gas en su interior, lo que se informó como microembolismos gaseosos de origen desconocido (fig. 1).
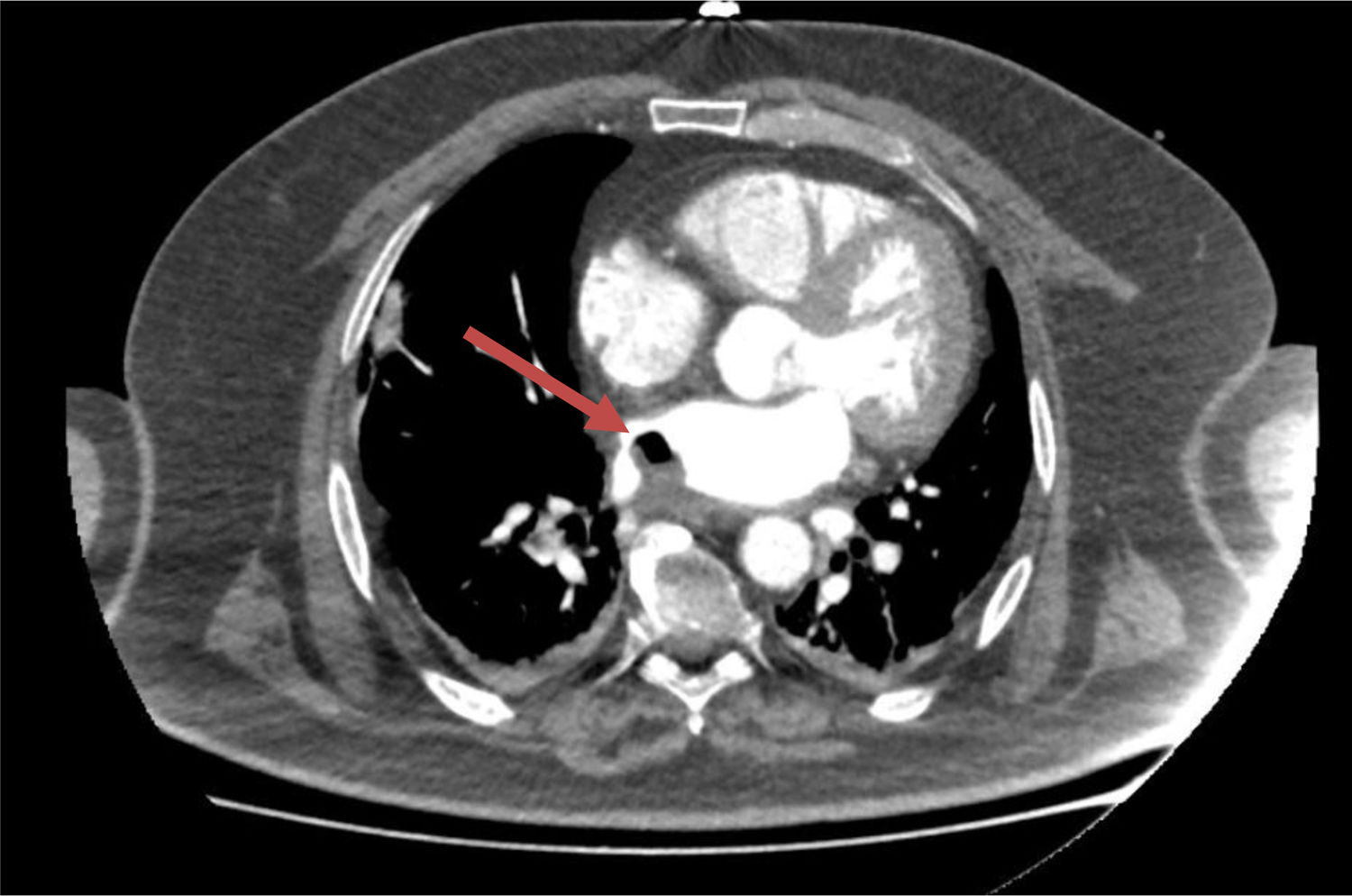
Debido al deterioro del nivel de consciencia se decidió intubación orotraqueal e ingreso en la UVI. Para tratar de identificar el origen del embolismo aéreo se realizó una angio-TC de tórax (fig. 2) donde se evidenció un defecto de repleción adyacente a la cara posterior de la aurícula izquierda de 22×14mm, con contenido aéreo en posición antideclive, todo ello sugestivo de trombo. En la imagen se describió también una difícil delimitación del esófago sin observarse plano graso de separación esófago-cardíaco. La presencia de aire en la aurícula izquierda junto a la clínica y los antecedentes del paciente (ablación de venas pulmonares) resultaron altamente sugestivos del diagnóstico de FAE como causa probable de embolia aérea descrita en la TC craneal.
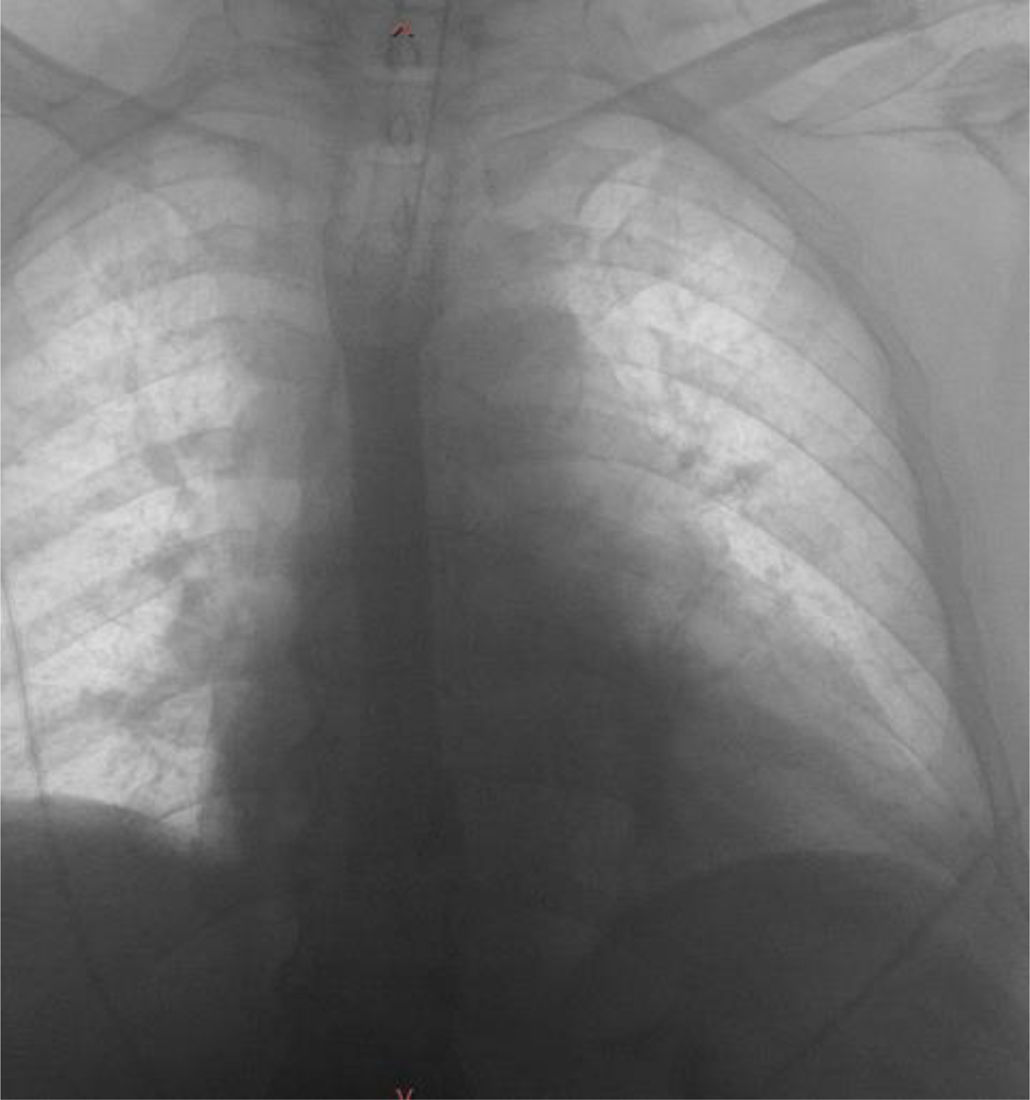
Se discutió el caso en sesión multidisciplinar con equipo de cirugía cardiovascular, cirugía general y gastroenterología. Se planteó cirugía emergente para reparación quirúrgica de la fístula atrio-esofágica. Dicho procedimiento implicaba el uso de circulación extracorpórea (CEC) con la necesidad de anticoagulación con heparina en dosis altas para poder realizar una reparación exitosa. En el contexto de ACV isquémico reciente, el uso de CEC representaba un muy alto riesgo de trasformación hemorrágica por lo que se optó por plantear otras posibilidades. La reparación directa del esófago con abordaje endoscópico por parte de cirugía general implicaba alto riesgo de embolismo aéreo por la insuflación de CO2 y probabilidad de sangrado por la estrecha relación con la aurícula izquierda. Por el prohibitivo riesgo de complicaciones y la situación neurológica descrita se desestimó los tratamientos planteados. En vista de ello, se decidió la colocación de prótesis esofágica (PE) por parte de gastroenterología, sin uso de escopia y únicamente con guía radiológica, para cerrar la comunicación atrioesofágica y con ello evitar la recidiva de embolismos aéreos (fig. 3).
Se localiza la unión esófago-gástrica con la ayuda del balón y con inyección de contraste intraluminal. No se observa salida de contraste por fuera de la luz esofágica. Se coloca prótesis esofágica autoexpandible totalmente recubierta de 10×25×120mm (Evolution LOT C2064237), dejando el extremo distal de la prótesis por encima de la unión esófago-gástrica y el extremo proximal por encima de la silueta cardíaca.
El implante de PE se realizó únicamente con control radiológico y guía con inyección de contraste para evitar el riesgo de aumentar la presión intraluminal y producir nuevos embolismos aéreos. Se colocó prótesis esofágica autoexpandible totalmente recubierta de 10×25×120mm (Evolution LOT C2064237), dejando el extremo distal de la prótesis por encima de la unión esofagogástrica y el extremo proximal por encima de la silueta cardíaca.
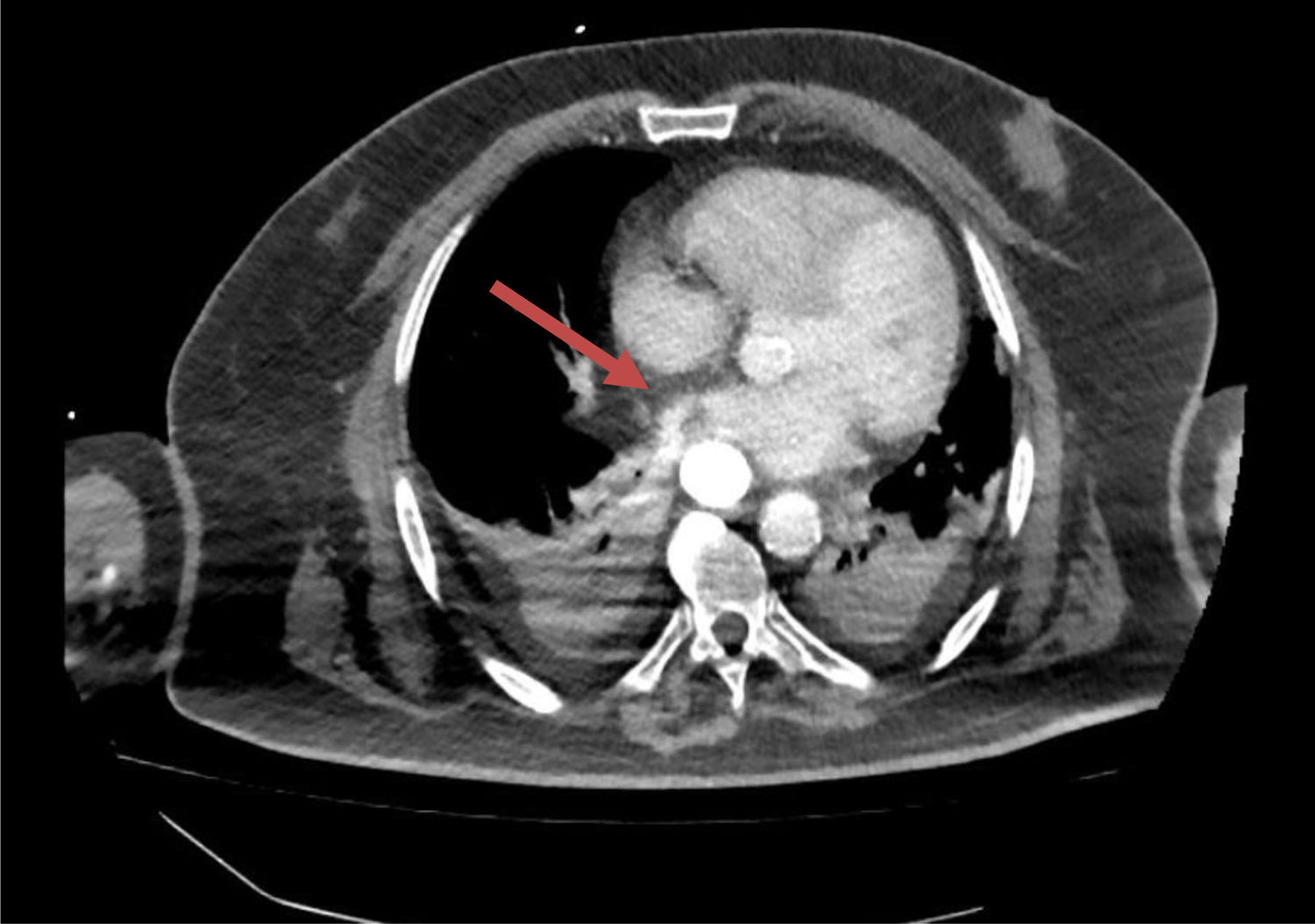
Tras la colocación de la PE presentó una progresiva mejoría radiológica de las imágenes observadas en la angio-TC en la aurícula izquierda, con resolución gradual de cavidad aérea intraauricular, hasta resolverse por completo (fig. 4), y normalización de valores de analítica sérica. Se retiró la PE luego de 21 días, que es el tiempo aproximado que se debe mantener para asegurar la cicatrización definitiva del esófago (entre 3 a 4 semanas).
El paciente evolucionó favorablemente desde el punto de vista respiratorio e infeccioso con la PE y antibióticos (meropenem+linezolid) que se suspendieron luego de 21 días al haber normalizado reactantes de fase aguda y ausencia de signos clínicos de infección. Se logró extubación 10 días después de ingreso en la UVI, y se colocó traqueostomía percutánea para destete respiratorio progresivo debido a secuela neurológica que condicionaba mal manejo de secreciones. Se logró decanular un mes después.
Tras el alta de la UVI, el paciente fue trasladado a planta de neurología para continuar tratamiento y rehabilitación, donde se mantuvo clínicamente estable, sin presentar nuevas complicaciones vasculares. En el momento del alta, el paciente mantenía bradipsiquia, con disartria leve, tetraparesia con afectación de extremidades derechas de predominio braquiocrural e hipoestesia de extremidades izquierdas en probable relación con infarto establecido por evento cardioembólico al ingreso.
Seis meses después del alta, presentaba menor limitación funcional, persistiendo con hemiparesia de hemicuerpo izquierdo, sin embargo, es independiente para las actividades de la vida diaria. Camina, sube y baja escaleras por sus propios medios.
DiscusiónEste caso clínico se presenta la posibilidad de considerar un manejo no quirúrgico de la FAE. En nuestro caso, el manejo conservador con la colocación de una PE bajo control radiológico y antibióticos ha conseguido un resultado satisfactorio, en contra de lo publicado en la literatura revisada donde, según una cohorte de casos publicada en la Heart Rythm Society, se reportó mortalidades del 100% en pacientes no intervenidos5.
La FAE es una complicación rara y muy grave de la ARF. Se asume que es consecuencia de ulceración esofágica a causa de un daño térmico que conduce a la formación de una fístula unidireccional desde el esófago hacia la aurícula izquierda6. Los métodos de protección esofágica, como los inhibidores de la bomba de protones antes del procedimiento o el desplazamiento mecánico del esófago no evidencia la reducción de lesiones esofágicas. La ecocardiografía y la monitorización de la temperatura son métodos que pueden reducir la probabilidad de lesión esofágica, pero existen datos limitados que no respaldan el uso de un método sobre el otro. La única variable conocida que confiere protección esofágica es minimizar la energía del catéter durante la ablación, sin embargo, esta conducta puede reducir la eficacia del ARF. También se ha demostrado que una mayor energía del catéter, pero una duración más corta, es más protectora que una duración más larga con una menor energía del catéter7.
Más del 70% de los pacientes con FAE desarrollaron síntomas infecciosos. En cambio, en los pacientes cuyo debut cursa con síntomas neurológicos es un reto, debido al difícil diagnóstico diferencial con el ictus tromboembólico riesgo inherente de los pacientes con FA8. Por otro lado, en los casos en los que aparece hemorragia gastrointestinal superior u odinofagia/disfagia después de la ablación de FA, se debe sospechar de inmediato en FAE, lo cual es particularmente importante debido a la alta mortalidad asociada con esta presentación clínica.
En los pacientes con diagnóstico establecido de FAE se debe evitar la esofagogastroduodenoscopia debido al riesgo de embolia gaseosa durante la insuflación de aire para la visualización endoscópica. De hecho, cualquier paciente que se haya sometido a una ablación debe evitar toda insuflación, incluidas la broncoscopia, la gastroscopia y la intubación esofágica involuntaria dentro de las cinco semanas posteriores a la ablación, debido al riesgo de FAE.
Debido a que es una complicación rara y se presenta inicialmente como sepsis, el diagnóstico precoz puede ser un desafío. Por lo tanto, una necesidad crucial es que el médico mantenga un alto índice de sospecha de esta complicación mortal en todos los pacientes con ablaciones recientes que presentan síntomas infecciosos, incluso si no hay fiebre. Nuestro paciente presentó síntomas infecciosos y síntomas neurológicos de rápido desarrollo, presumiblemente por fenómenos embólicos, lo que motivó una alta sospecha de FAE, consiguiéndose diagnosticar a las pocas horas del debut clínico.
Las opciones de tratamiento descritas para la FAE incluyen enfoques conservadores como antibióticos intravenosos, colocación de stent esofágico endoscópico e intervención quirúrgica, siendo esta última el único tratamiento que ha demostrado aumentar la supervivencia. Según una revisión sistemática publicada en el AHA Journal en noviembre del 2017, de una serie de 85 artículos, se encontró que el manejo conservador (colocación de PE o antibióticos) tiene un pronóstico ominoso, ya que solo un paciente que no recibió intervención quirúrgica sobrevivió, pero tuvo déficit neurológico significativo9.
Nuestro paciente no presentó signos de sangrado activo ó hematemesis con compromiso hemodinámico. La clínica neurológica, condicionada por el ictus cardioembólico extenso, fue el factor determinante para desestimar el tratamiento quirúrgico emergente debido al mal pronóstico asociado a cirugía con necesidad de CEC. Por lo expuesto, se planteó manejo conservador con prótesis esofágica que se colocó con radioscopia para evitar la insuflación esofágica y con ello el riesgo de embolia aérea. Aunque el pronóstico inicial era muy grave, la decisión terapéutica permitió la supervivencia del paciente.
En conclusión, la naturaleza variable de las presentaciones clínicas de la FAE puede provocar potencialmente un retraso en el diagnóstico, lo que puede acarrear un pronóstico fatal. Los síntomas predominantes de fiebre, cambios neurológicos o cambios gastrointestinales pueden hacer que los pacientes sean tratados inicialmente por diversas especialidades médicas distintas a la cirugía cardiovascular, por lo que es fundamental conocer el antecedente epidemiológico de ablación por FA y el riesgo de desarrollo de esta enfermedad. El diagnóstico temprano de esta afección puede permitir intervenciones antes de que el paciente desarrolle un compromiso circulatorio significativo o secuelas neurológicas irreversibles.
ConclusionesLa ablación con catéter de la FA se asocia con lesiones térmicas esofágicas relativamente frecuentes, pero con un riesgo mínimo de fístula auriculoesofágica, la cual es una complicación catastrófica y a menudo letal. A parte de disminuir empíricamente la energía10 y la duración del procedimiento, no existen otros enfoques válidos para minimizar esta complicación excepcionalmente rara. No obstante, su diagnóstico precoz es esencial para permitir estrategias terapéuticas inmediatas que minimicen la elevada morbilidad y mortalidad asociada a esta afección.
Se debe considerar este diagnóstico en todo paciente que presente clínica compatible y haya sido sometido a ARF en las 6 semanas previas.
Aunque la cirugía es la piedra angular del tratamiento, es posible considerar el manejo conservador (prótesis esofágica, antibióticos de amplio espectro) en los pacientes cuya presentación clínica sea neurológica o infecciosa en ausencia de sangrado activo.
Consideraciones éticasSe obtuvo el consentimiento informado por escrito del familiar directo para la publicación del artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.