La reparación de la válvula mitral con neocuerdas de politetrafluoroetileno constituye actualmente la piedra angular del tratamiento basado en el principio respetar antes que resecar. Se han desarrollado diferentes técnicas para medir la longitud exacta de las neocuerdas que resultan desafiantes y complicadas. Nuestro objetivo es describir la técnica de asa (loop technique) con una medida estándar en reparación mitral.
Materiales y métodosSe realizó un estudio descriptivo, en una cohorte retrospectiva de 34 pacientes consecutivos, desde enero de 2011 hasta octubre de 2017. A todos los pacientes se les realizó implante de neocuerdas con técnica de asa fabricadas en casa. La longitud de las neocuerdas fue preestablecida en 15mm para la valva posterior y 25mm para la anterior, basadas en mediciones ecocardiográficas de otros autores. Se evaluó la competencia valvular a la salida de circulación extracorpórea con ecocardiografía transesofágica y se realizó seguimiento temprano con ecocardiografía transtorácica.
ResultadosEl abordaje por minitoracotomía videoasistida se realizó en el 70,5% (24/34) y por esternotomía convencional en el 29,4% de los casos (10/34). Se reparó la valva anterior en el 26,4% (9/34), la posterior en el 61,7% (21/34) y ambas en el 11,7% (4/34). Se realizó anuloplastia con anillo rígido en el 79,4% y semirrígido en el 20,5% de los casos. El tamaño promedio del anillo fue 29,9±2,0. El ecocardiograma intraoperatorio no reveló ningún grado de insuficiencia en el 82,3% (28/34) y mostró insuficiencia trivial en el 17,6% (6/34). Ningún paciente llevado a cirugía mínimamente invasiva requirió conversión. El tiempo de circulación extracorpórea fue de 158±38 min y de pinzamiento de 116±31 min. Ningún paciente requirió resección o ajuste de la medida de las neocuerdas ni conversión a reemplazo. Se presentaron 2casos de mortalidad hospitalaria: el primero por choque hipovolémico y el segundo por choque séptico de origen pulmonar. En el seguimiento temprano con una media de 8 meses (1-40), el 82,3%(28/34) no presentó insuficiencia mitral y el 17,6% (6 /34) presentó insuficiencia de grado I.
ConclusiónLa técnica propuesta con asas preformadas de neocuerdas de politetrafluoroetileno con medida estandarizada mostró resultados preliminares satisfactorios. Son necesarios estudios con seguimiento a largo plazo.
Mitral valve repair with polytetrafluoroethylene neochord is currently the gold standard of treatment, based on the respect rather than resect approach. Different challenging and complicated techniques have been developed to measure the exact length of the neochord. Our objective is to describe the loop technique with a standard measurement in mitral repair.
Materials and methodsA descriptive study was conducted on a retrospective cohort of 34 consecutive patients, from January 2011 to October 2017. All patients underwent the implanting of a neochord using an in-house loop technique. The length of the neochord was pre-measured with 15mm for the posterior leaflet and 25mm for the anterior leaflet, based on the echocardiographic measurements of other authors. An evaluation was made of valvular competence at the weaning of extracorporeal circulation using transoesophageal echocardiography was evaluated, with an early follow-up with transthoracic echocardiography.
ResultsThe video-assisted mini-thoracotomy approach was performed in 70.5% (24/34) of cases, and by conventional sternotomy in 29.4% (10/34). The anterior leaflet was repaired in 26.4% (9/34), the posterior in 61.7% (21/34), and both in 11.7% (4/34). Annuloplasty was performed with a rigid ring in 79.4%, and semi-rigid in 20% of cases. The mean ring size was 29.9±2.0. The intraoperative echocardiogram did not show any grade of failure in 82.3% (28/34), and mild insufficiency in 17.6% (6/34). No patient undergoing minimally invasive surgery required conversion. The extracorporeal circulation time was 158±38minutes and clamping 116±31min. No patient required resection or adjustment of the neochord measurement or conversion to replacement. There were 2cases of hospital mortality; the first due to hypovolaemic shock and the second due to septic shock of pulmonary origin. In the early follow-up with a mean of 8 months (1-40), 82.3% (28/34) did not present with mitral regurgitation, and 17.6% (6/34) had grade I insufficiency.
ConclusionThe proposed technique with preformed loops of polytetrafluoroethylene neochord with standardised measurement showed reliable preliminary results. Studies with long-term follow-up would be necessary.
En 1990 se establecieron los beneficios de la cirugía de reconstrucción valvular que, sumados al desarrollo de técnicas para el tratamiento de la fibrilación auricular, desarrollan el concepto de cirugía valvular no trombogénica1. La reparación de la válvula mitral se ha convertido en el procedimiento de elección en la mayoría de los casos de insuficiencia mitral, en especial para la de origen degenerativo2.
El aparato valvular mitral es complejo y está formado por varios componentes diferentes: el denominado anillo mitral, las valvas anterior y posterior, las cuerdas tendinosas, los músculos papilares y el ventrículo izquierdo3. La afectación de cualquiera de ellos resulta en la insuficiencia de la válvula. Actualmente se clasifican en 2grupos según el mecanismo causante: primaria (orgánica) y secundaria (funcional). Para la reparación de la válvula mitral, esencialmente para la enfermedad degenerativa, se deben cumplir 3principios básicos: preservar la movilidad de las válvulas, crear una amplia superficie de coaptación y remodelar el anillo1.
En la insuficiencia degenerativa un segmento se prolapsa por elongación o rotura de las cuerdas tendinosas. Anteriormente, el abordaje consistía en la resección del segmento prolapsado y la anuloplastia. Muchas de estas técnicas parecían complejas y resultaron en el abandono de los cirujanos, quienes preferían el reemplazo valvular. En el centro cardiovascular de Leipzig se desarrolló la técnica que es el pilar de nuestra estrategia de reparación: consiste en fabricar asas de neocuerdas de politetrafluoroetileno (PTFE) que se anclan al músculo papilar correcto y al segmento valvular afectado y corrigen así el prolapso (tipo II de Carpentier)4. El desarrollo de esta técnica no les simplificó la vida a los cirujanos: surgieron dificultades para lograr una adecuada longitud de la neocuerda, por lo que no se logró una aplicación clínica generalizada. Algunos grupos se basan en mediciones ecocardiográficas preoperatorias para preformar las cuerdas de PTFE. Sus resultados arrojan medidas estándar tanto para la valva anterior como para la posterior, que se utilizaron para respaldar nuestra técnica, formando las asas con una medida invariable para todos los casos. El número de asas y el lugar de implantación fue decidido con el análisis de cada caso.
Nuestro objetivo es describir la técnica con una medida estándar en la reparación mitral y los resultados tempranos del seguimiento.
Materiales y métodosSe revisaron las bases de datos y se realizó un estudio descriptivo, en una cohorte retrospectiva de 34 pacientes consecutivos llevados a reparación de la válvula mitral con técnica de asa estandarizada en nuestra institución en el periodo comprendido entre enero de 2011 y octubre de 2017.
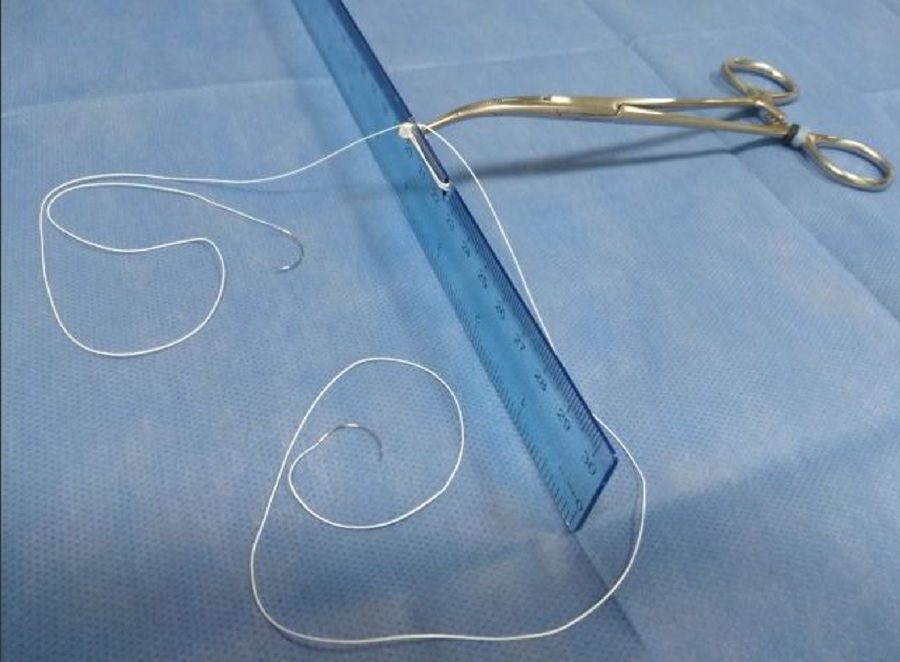
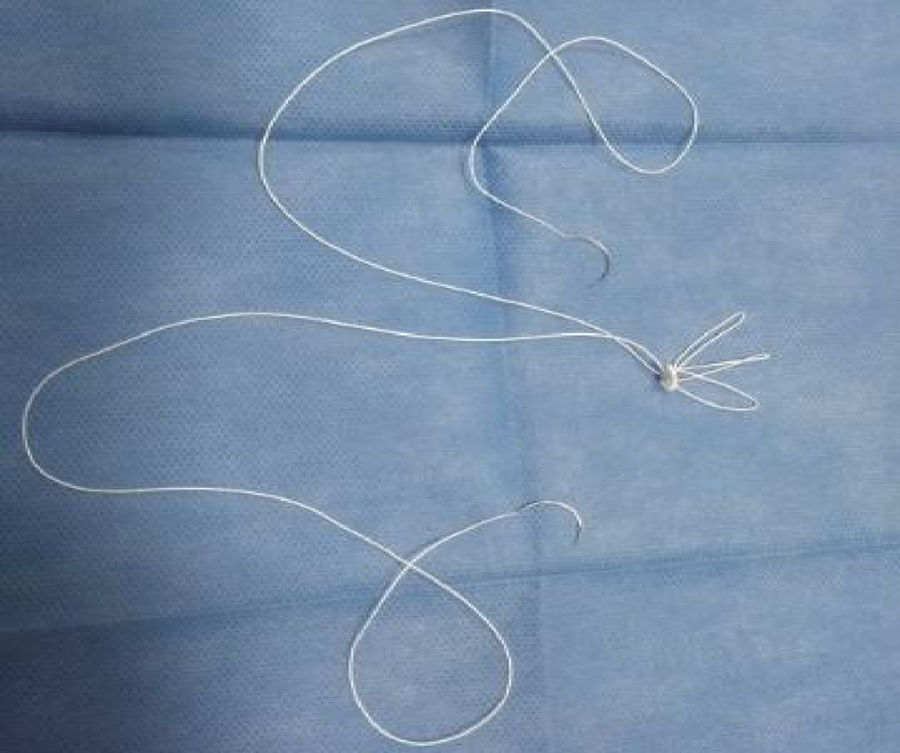
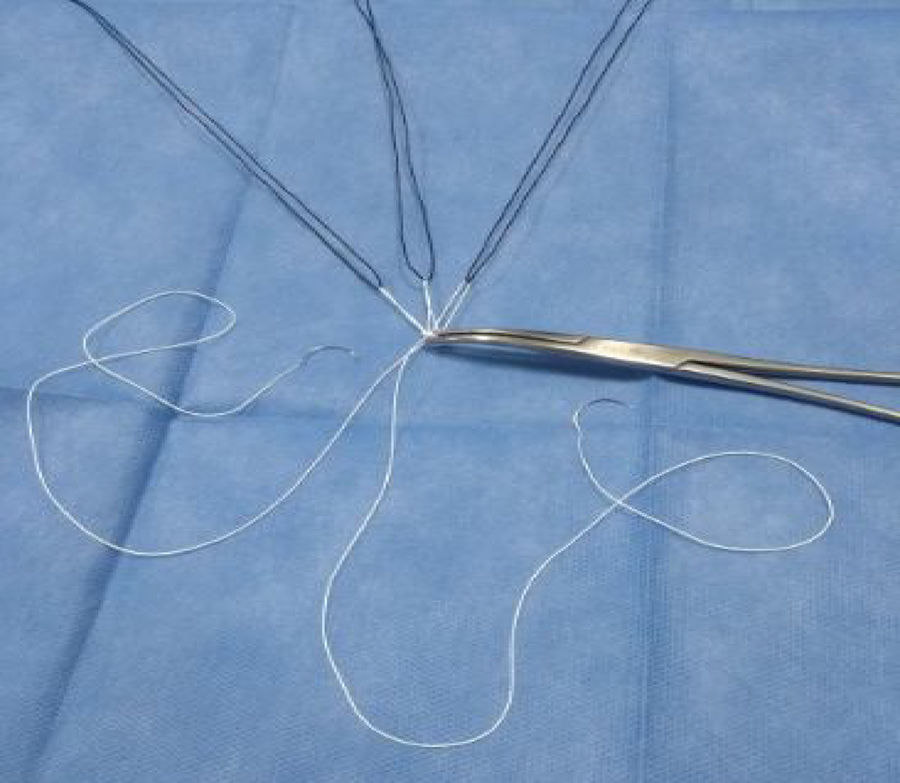
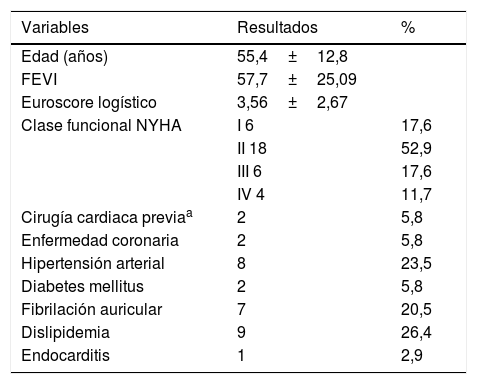
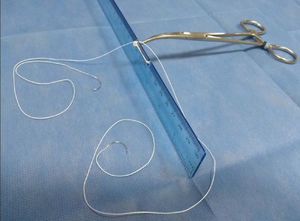
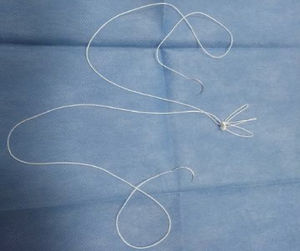
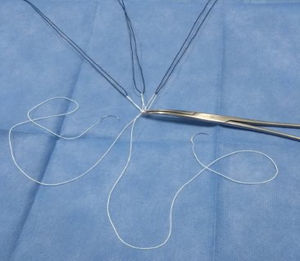
Técnica de asaLas asas se confeccionan con única sutura de PTFE (Gore-Tex) 4-0 con una felpa central con 3 asas. La medida se estandariza con una regla que se modifica con una hendidura para 15mm y otra en 25mm (fig. 1). Las agujas que salen de la felpa, tras formar las asas, atraviesan la porción fibrosa de la cabeza del músculo papilar y se anudan sobre una felpa secundaria (fig. 2). Cada una de las asas se repara con una seda y son anudadas de forma individual con una sutura accesoria de Gore-Tex 4-0 o 5-0 en el segmento de la válvula prolapsada (fig. 3). El asa preformada se coloca entre el músculo papilar y el segmento prolapsado correspondiente, teniendo en cuenta no sobrepasar la línea media. Si el segmento prolapsado es A1 o P1, corresponde al músculo papilar anterolateral; si el segmento prolapsado es A3 o P3 el músculo papilar corresponde al posteromedial y si se trata de A2 o P2, depende de hacia qué lado queda mejor funcional y anatómicamente sin sobrepasar la línea media. Se realiza prueba neumática para verificar la competencia valvular. Se culmina la reparación valvular con anuloplastia.
Se realiza un ecocardiograma transesofágico intraoperatorio para evaluar el resultado de la reparación valvular. Se determinó de acuerdo con lo publicado en las guías5 en los siguientes grados de insuficiencia: 0 o ninguna; I trivial o leve; II moderada; III de moderada a severa y IV severa.
ResultadosLas características de los pacientes se resumen en la tabla 1. La mayoría de los pacientes tenían una buena función ventricular y un riesgo operatorio bajo. El 70,5% (24/34) de los pacientes se abordaron por cirugía mínimamente invasiva a través de minitoracotomía lateral derecha videoasistida, en el resto se realizó esternotomía convencional 29,4% (10/34). Se realizaron procedimientos combinados que incluyeron plastia tricúspidea (2,9%; 2/34), procedimiento de Cox Maze (20,5%; 7/34), revascularización miocárdica (5,8%; 2/34) y cierre de comunicación interauricular (5,8%; 2/34).
Características preoperatorias de los pacientes
| Variables | Resultados | % |
|---|---|---|
| Edad (años) | 55,4±12,8 | |
| FEVI | 57,7±25,09 | |
| Euroscore logístico | 3,56±2,67 | |
| Clase funcional NYHA | I 6 | 17,6 |
| II 18 | 52,9 | |
| III 6 | 17,6 | |
| IV 4 | 11,7 | |
| Cirugía cardiaca previaa | 2 | 5,8 |
| Enfermedad coronaria | 2 | 5,8 |
| Hipertensión arterial | 8 | 23,5 |
| Diabetes mellitus | 2 | 5,8 |
| Fibrilación auricular | 7 | 20,5 |
| Dislipidemia | 9 | 26,4 |
| Endocarditis | 1 | 2,9 |
Se realizó la técnica de asas estandarizadas con medida de 25mm para la valva anterior y de 15mm para la posterior. Se hizo reparación en forma aislada de la valva anterior en el 26,4% (9/34), de la posterior en el 61,7% (21/34) y de ambas valvas en el 11,7% (4/34). Ningún paciente requirió resección de las valvas o ajuste de la medida de las neocuerdas. Adicionalmente fue necesario realizar plicatura comisural en el 11,7% (4/34) y cierre de hendidura (cleft) en el 23,5% (8/34). Se realizó anuloplastia con anillo rígido en silla de montar (St. Jude Medical) en el 79,4% y semirrígido en el 20,5% (CG Future-Medtronic). El tamaño promedio del anillo fue 29,7±2,0.
Se realizó ecocardiograma transesofágico intraoperatorio; se evaluó la competencia valvular a la salida de circulación extracorpórea. El 100% de los pacientes quedó libre de insuficiencia residual o con insuficiencia trivial. El 82,3% (28/34) quedó sin ningún grado de insuficiencia y el 17,6 (6/34) con insuficiencia de grado I.
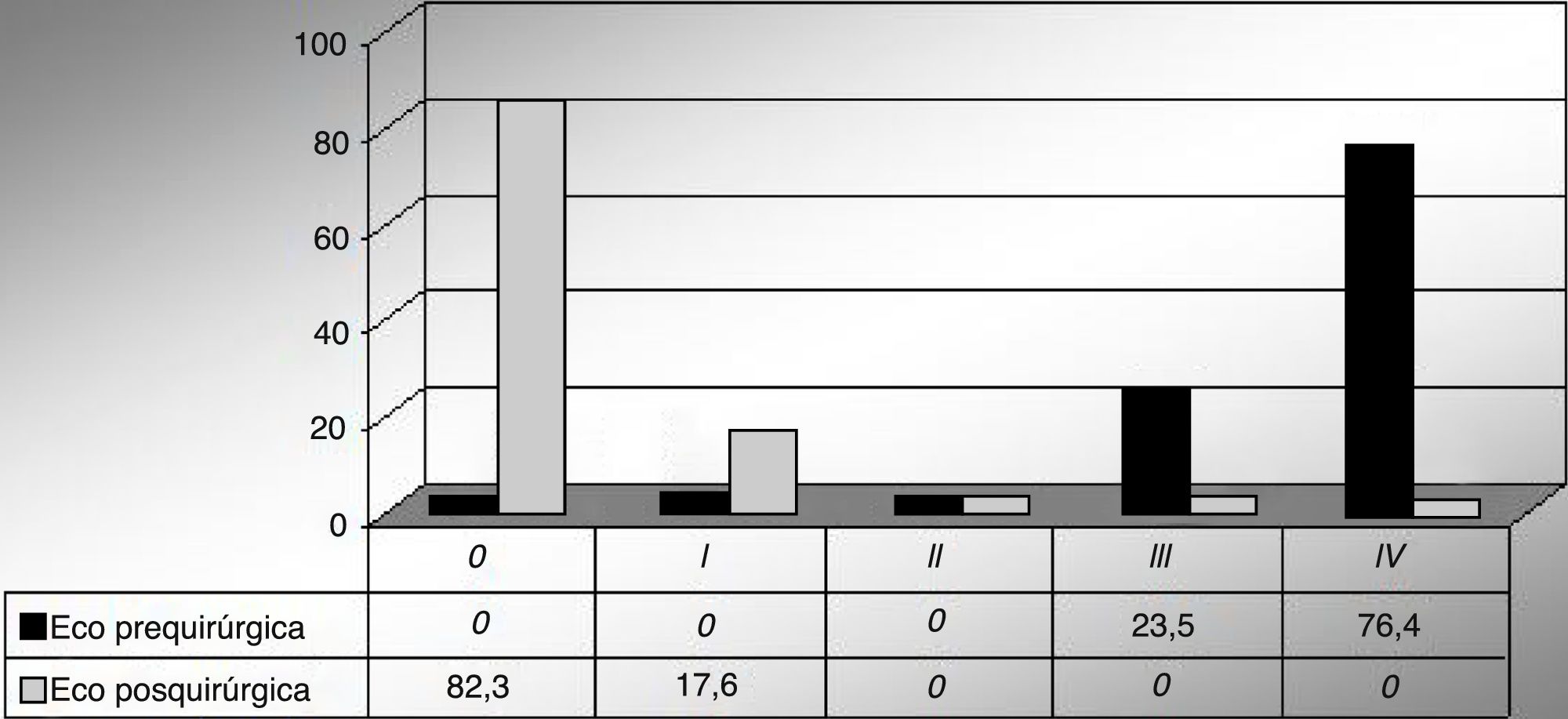
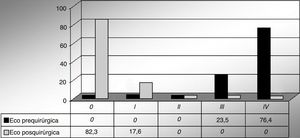
Se realizó un seguimiento posquirúrgico con una media de 8 meses (1-40) libres de reoperación por falla en la reparación valvular. La figura 4 muestra la severidad de la insuficiencia pre- y posquirúrgica medidas por ecocardiografía.
Un total de 6 pacientes presentaron complicaciones. El 5,8% (2/34) desarrolló infecciones pulmonares que requirieron drenaje y posterior decorticación. Uno de los casos con insuficiencia mitral severa de origen mixomatoso asociada a hipertensión pulmonar suprasistémica precisó abordaje por minitoracotomía derecha. Tuvo difícil manejo en el postoperatorio con intubación prolongada, desarrolló cuadro neumónico, derrame pleural complicado con empiema y requirió decorticación temprana. Tuvo una evolución tórpida: sepsis, disfunción multiorgánica y muerte a los 47 días posquirúrgicos.
El segundo caso se trató de una insuficiencia mitral severa secundaria a rotura de cuerda tendinosa de la valva posterior. Tuvo abordaje por minitoracotomía derecha. Presentó derrame pleural tabicado, se realizó drenaje pleural y posterior decorticación por videotoracoscopia, con evolución satisfactoria. Egresó a los 19 días posquirúrgicos.
El 2,9% (1/34) presentó falla renal aguda sin requerimiento de diálisis. La creatinina fue de 1,16 mg/dl y la tasa de filtración glomerular prequirúrgica fue de 55,3 ml/min.
El 5,8% (2/34) presentó delirio hiperactivo que se resolvió satisfactoriamente.
El 2,9% (1/34) requirió reoperación por sangrado. Se trataba de un paciente con insuficiencia mitral severa mixomatosa, con abordaje mínimamente invasivo, sangrado postoperatorio y hemotórax masivo. En la reintervención se encontró sangrado difuso, coagulopatía, politransfusión y disfunción multiorgánica. Se produjo la muerte al segundo día posquirúrgico.
DiscusiónRealizar una medida estandarizada de la longitud de la neocuerda nos simplifica la técnica y nos permite reparar prolapsos en una o ambas valvas. Consideramos que puede ser reproducible; no es aleatoria y está basada en estudios ecocardiográficos de grandes series. Nuestro trabajo permite demostrar que ningún paciente corregido con la técnica de asa estandarizada requirió reemplazo, tampoco se presentaron dificultades como el movimiento anterior sistólico, ni hubo necesidad de reajustar la medida o realizar resecciones. La clave está en analizar cuidadosamente la válvula para decidir el lugar de implantación del asa.
El comportamiento de las neocuerdas de PTFE ha sido objetivo de estudio de algunos autores. Se demostró que en pocos meses se produce un recubrimiento por una vaina fibrosa y sin calcificaciones, con aspecto macroscópico muy similar al de las cuerdas nativas6. El principal problema con el implante de las neocuerdas es la medición adecuada de la longitud del PTFE, la mayoría de los cirujanos se sienten más seguros al realizar el reemplazo valvular que al arriesgarse a una medición inexacta con el fallo de la plastia mitral. Existen varias formas de estimar esta longitud. Habitualmente se hace en el intraoperatorio midiendo la longitud desde el músculo papilar hasta el borde libre de una porción no prolapsada de la VM (válvula mitral) con un caliper. La desventaja de este método se basa en que la medición se hace con el corazón parado y el ventrículo vacío. Uno de las técnicas más antiguas consiste en llenar el ventrículo izquierdo con solución salina o prolongar la neocuerda hasta la superficie de coaptación7,8: todos subjetivos y estimados a ojo por el operador. Algunos grupos como el de Chu et al. comenzaron a realizar ecocardiografía transesofágica preoperatoria para la evaluación integral de la válvula mitral y la determinación de la longitud adecuada de la neocuerda.
Estos encontraron que la longitud media para la valva anterior fue de 24,7±2,7 y 14,6±2,4mm para la posterior; el 100% de los pacientes tuvieron una reparación exitosa libre de conversión al reemplazo9. Otros grupos como el de Melnitchouk también realizaron medidas preoperatorias usando el eje largo de 2 cámaras y concluyeron, a su vez, que la medida en la mayoría de los pacientes correspondía a rangos de 10-16mm para la valva posterior y de 20-26mm para la anterior10. Dado que la medida estándar fue 15mm para la valva posterior y 25 para la anterior, se confeccionó una regla para preformar las asas de neocuerdas (1 set de 3 asas) que, utilizadas en todos los pacientes, resultaron exitosas.
Existen 2 grupos que también describieron esta técnica con medida estandarizada: Lamelas en Miami11 e Hysi et al. en Lens (Francia)12 con resultados óptimos y aplicables en su experiencia a todos los casos.
Nuestras limitaciones incluyen que son resultados de un solo centro, con un solo operador; además de las propias de un estudio retrospectivo, la pérdida en el seguimiento de algunos pacientes por tratarse de planes internacionales que regresan a su lugar de origen o que por su seguridad social no asisten al control.
ConclusiónEn nuestra experiencia la técnica con asas preformadas de neocuerdas de PTFE con medida estandarizada constituye un método confiable y reproducible para la reparación de la válvula mitral con prolapso de una o ambas valvas. Se obtienen resultados óptimos con abordaje convencional o mínimamente invasivo. La duración a largo plazo debe ser comprobada, por lo que se necesitan más estudios al respecto, sin embargo, los hallazgos iniciales señalan que es segura y duradera.
Conflicto de interesesLos autores declaran no tener conflictos de interés para la realización de este artículo.