Actualmente existe controversia respecto a los beneficios y riesgos de la revascularización coronaria con injertos arteriales múltiples.
ObjetivosAnalizar la supervivencia a medio plazo entre pacientes sometidos a cirugía coronaria aislada sin circulación extracorpórea (CEC) según recibiesen, o no, más de un injerto arterial. Evaluar el objetivo primario en una muestra ajustada mediante puntuación de propensión.
Material y métodosRevisión retrospectiva de pacientes sometidos a cirugía coronaria sin CEC entre 2005 y 2017. Con el propósito de limitar sesgos, se realizó un análisis de supervivencia tras ajustar la muestra mediante puntuación de propensión (1:1; nearest neighbor) y un análisis de riesgos proporcionados de Cox para identificar variables asociadas al evento primario.
ResultadosSe incluyeron 1.875 pacientes. En la cohorte total, los pacientes con solo un injerto arterial presentaron edad media más avanzada (70,3 vs 60,4años; p<0,00), más comorbilidades y riesgo quirúrgico (EuroScoreI: 6,2 vs 3,1; p<0,00). Tras ajustar la muestra (n=654) los grupos no presentaron diferencias significativas en características preoperatorias (EuroScoreI: 2,1% vs 1,9%; p=0,49). A 7años, tanto en la cohorte total como en la ajustada observamos una mayor supervivencia en el grupo sometido a revascularización arterial múltiple (88,7% vs 80%; p=0,021), siendo esta estrategia de revascularización un predictor independiente de mayor supervivencia a medio plazo (HR: 0,67; IC95%: 0,51-0,89; p=0,005).
ConclusionesLa revascularización arterial múltiple se asocia a una mayor supervivencia en comparación con el uso aislado de un solo injerto arterial a medio plazo.
Currently, there is controversy regarding outcomes between the use of multiple or single arterial grafts for coronary artery revascularization.
ObjectivesMid-term survival analysis of patients undergoing off-pump coronary artery revascularization with multiple or single arterial grafts. Analysis of the primary outcome in a propensity score-matched cohort.
Material and methodsRetrospective analysis of patients who underwent off-pump coronary artery revascularization between 2005 and 2017. In order to reduce bias, an analysis was performed in a propensity score matched sample (1:1; nearest neighbor) and a Cox proportional hazard model was developed to identify variables associated with the primary outcome.
ResultsA total of 1,875 patients included. In the total cohort, patients with single arterial graft were older (70.3 vs 60.4 years; P<.00) had more comorbidities and higher surgical risk (EuroScoreI: 6.2 vs 3.1; P<.00). After adjustment, both groups were balanced and had similar perioperative risk. At 7-year follow up, patients with multiple arterial grafts had better survival than patients with single arterial graft, this result was consistent in the total and adjusted cohorts (88.7% vs 80%; P=.021). This revascularization strategy was an independent predictor for better mid-term survival (HR: 0.67; 95%CI: 0.51-0.89; P=.005).
ConclusionsMultiple arterial graft revascularization is associated with better mid-term survival than single arterial graft revascularization.
En 2018, más de 5.000 pacientes en España fueron sometidos a cirugía de revascularización coronaria1. La práctica más común es el uso del injerto de arteria mamaria interna izquierda a la arteria descendente anterior y de la vena safena para realizar derivaciones coronarias adicionales. La durabilidad de los injertos utilizados es uno de los principales determinantes en los resultados a largo plazo de esta intervención, y en los últimos años se ha acumulado evidencia a favor de que el uso de injertos arteriales múltiples (revascularización arterial múltiple [MAG]) mejora los resultados en comparación con el uso de injertos venosos2-7; actualmente el uso de un segundo injerto arterial es una indicación con claseIIa8. No obstante, ensayos clínicos aleatorizados no son concluyentes a la hora de demostrar los beneficios de la MAG9,10, por lo que aún existe controversia respecto a la mejor estrategia11-16. El propósito de este estudio es comparar la supervivencia a medio plazo de pacientes sometidos a cirugía de revascularización con MAG o con solo un injerto arterial (revascularización arterial única [SAG]).
Material y métodosPacientesRealizamos una revisión retrospectiva de la base de datos SICCS (Biomenco, Barcelona, España) de nuestro centro para identificar pacientes sometidos a cirugía coronaria aislada sin circulación extracorpórea. Fueron excluidos pacientes con cirugía cardiaca previa, pacientes sin injertos arteriales y con una única derivación coronaria.
La recogida de las características perioperatorias se realizó de manera prospectiva. Los datos acerca de la supervivencia fueron obtenidos del registro del Instituto Nacional de Defunciones y de informes clínicos de los centros hospitalarios del Servicio Madrileño de Salud.
El presente estudio se realizó de acuerdo con las recomendaciones para la investigación en humanos de la 18.ª Asamblea Médica Mundial, Helsinki, Finlandia, 1964. Todos los datos de los pacientes fueron tratados de acuerdo con la Ley de Protección de datos en España (LOPD 3/2018). Dado el diseño del estudio, no fue necesario el consentimiento informado.
IntervenciónTodas las intervenciones fueron realizadas con anestesia general y sin circulación extracorpórea. La arteria mamaria interna izquierda fue el injerto de elección para revascularizar la arteria descendente anterior. Los injertos utilizados para revascularizar el resto de los vasos fueron elegidos por el cirujano, tras previa valoración de la edad, comorbilidades del paciente y calidad de los vasos epicárdicos.
En nuestra institución la extracción de las arterias mamarias se realiza de manera esqueletonizada, con una disección por planos y hemostasia. El injerto de arteria radial se obtiene de manera pediculada, acompañado de la grasa perivascular y las venas radiales; este injerto se obtiene del antebrazo no dominante previa valoración con test de Allen y pulsioximetría. La extracción de la vena safena se realizó de manera abierta, mediante disección cuidadosa de planos, ligando ramas y evitando la manipulación directa de la vena.
Las anastomosis coronarias se realizaron con el sistema Cor-Vasc (CoroNeo, Montreal, Canadá), utilizando sutura continua de polipropileno7/0 para anastomosis distales y proximales en caso de injertos arteriales; se utilizó polipropileno6/0 para anastomosis proximales de injertos venosos.
Durante la intervención se administró heparina no fraccionada en una dosis de 1,5mg/kg, para alcanzar un tiempo de coagulación activado >250s. Una vez finalizada la revascularización y tras comprobar los injertos mediante flujometría por tiempo de tránsito, la heparina fue revertida con protamina en una proporción 1:1.
ObjetivosEl objetivo primario fue conocer y comparar la supervivencia a medio plazo entre pacientes sometidos a cirugía coronaria aislada según recibiesen, o no, más de un injerto arterial. Además de un análisis de este objetivo en una muestra ajustada mediante puntuación de propensión.
Los objetivos secundarios incluyeron el análisis en la cohorte total y ajustada de eventos adversos cardiovasculares mayores (muerte, infarto agudo de miocardio, ictus) de manera perioperatoria (30días) y otros eventos perioperatorios como mediastinitis, reintervención por sangrado, tiempo de intubación orotraqueal >24h, tiempo de estancia en UCI y fracaso renal agudo con necesidad de hemodiálisis o hemofiltración.
El infarto perioperatorio fue definido como una elevación de troponinaI >20ng/ml con o sin nuevas alteraciones electrocardiográficas o ecocardiográficas.
Análisis estadísticoLa normalidad de las variables cuantitativas fue analizada mediante el test de Shapiro-Wilk. Las comparaciones entre grupos se realizaron mediante los tests de chi-cuadrado, test de Fisher y t de Student o Wilcoxon, según el tipo de variable y su distribución.
La supervivencia fue estimada con el método de Kaplan Meier y se utilizó el test de riesgos proporcionados de Cox para calcular y comparar la razón de tasas (HR) para las dos estrategias de revascularización.
Con la finalidad de identificar variables asociadas con el evento primario, construimos un modelo predictivo a partir de todas las posibles ecuaciones utilizando el modelo de Cox; las variables asociadas a la supervivencia (p<0,2) en el análisis univariante fueron incluidas en el modelo multivariante; de los distintos modelos generados, se eligió el más parsimonioso y con el mejor índice de Aikake y C de Harrel. Los supuestos del modelo fueron evaluados mediante análisis estratificado y el análisis del coeficiente del predictor lineal al cuadrado.
Con el propósito de limitar sesgos que pudiesen afectar a la relación entre MAG y eventos, realizamos un análisis del evento primario ajustado mediante puntuación de propensión. Identificamos variables con distribución desigual entre grupos (p<0,2) que posteriormente fueron incluidos en un modelo no saturado para estimar una puntación de propensión. Los pacientes fueron apareados en una proporción 1:1 con el método nearest neighbor; el caliper fue seleccionado tras estimar 0,25 de la desviación estándar del logit de la puntuación de propensión.
Todas las pruebas de contraste de hipótesis fueron de dos colas, con un nivel de significación estadística de p<0,05. El análisis estadístico fue realizado con STATA14 (StataCorp. 2105. College Station, TX, EE.UU.).
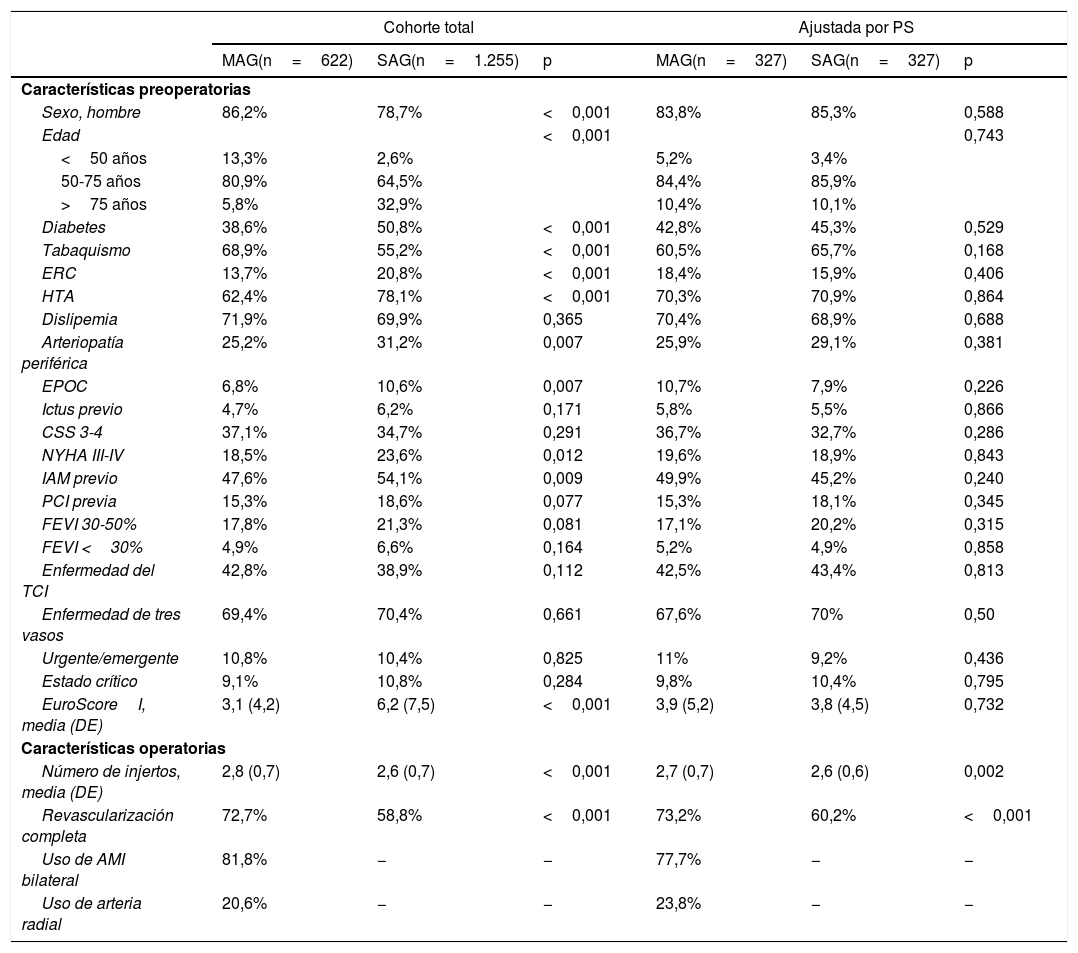
ResultadosDe enero de 2005 a diciembre de 2017, 1.877 pacientes fueron incluidos en el estudio, de los cuales 622 (33,1%) recibieron MAG. Los pacientes con SAG presentaron edad media más avanzada (70,3 vs 60,4años, p<0,001) y mayor comorbilidad, respectivamente (hipertensión arterial: 78% vs 62,4%, p<0,001; arteriopatía periférica: 31,2% vs 25,2%, p=0,007; EPOC: 10,6% vs 6,7%, p=0,007; diabetes: 50,8% vs 38,5%, p<0,001; enfermedad renal crónica: 20,8% vs 13,6%, p<0,001; EuroScoreI: 6,2 vs 3,1, p<0,001). Las características preoperatorias y operatorias se representan en la tabla 1.
Características preoperatorias y operatorias en la cohorte total y en la ajustada mediante puntuación de propensión (PS)
| Cohorte total | Ajustada por PS | |||||
|---|---|---|---|---|---|---|
| MAG(n=622) | SAG(n=1.255) | p | MAG(n=327) | SAG(n=327) | p | |
| Características preoperatorias | ||||||
| Sexo, hombre | 86,2% | 78,7% | <0,001 | 83,8% | 85,3% | 0,588 |
| Edad | <0,001 | 0,743 | ||||
| <50 años | 13,3% | 2,6% | 5,2% | 3,4% | ||
| 50-75 años | 80,9% | 64,5% | 84,4% | 85,9% | ||
| >75 años | 5,8% | 32,9% | 10,4% | 10,1% | ||
| Diabetes | 38,6% | 50,8% | <0,001 | 42,8% | 45,3% | 0,529 |
| Tabaquismo | 68,9% | 55,2% | <0,001 | 60,5% | 65,7% | 0,168 |
| ERC | 13,7% | 20,8% | <0,001 | 18,4% | 15,9% | 0,406 |
| HTA | 62,4% | 78,1% | <0,001 | 70,3% | 70,9% | 0,864 |
| Dislipemia | 71,9% | 69,9% | 0,365 | 70,4% | 68,9% | 0,688 |
| Arteriopatía periférica | 25,2% | 31,2% | 0,007 | 25,9% | 29,1% | 0,381 |
| EPOC | 6,8% | 10,6% | 0,007 | 10,7% | 7,9% | 0,226 |
| Ictus previo | 4,7% | 6,2% | 0,171 | 5,8% | 5,5% | 0,866 |
| CSS 3-4 | 37,1% | 34,7% | 0,291 | 36,7% | 32,7% | 0,286 |
| NYHA III-IV | 18,5% | 23,6% | 0,012 | 19,6% | 18,9% | 0,843 |
| IAM previo | 47,6% | 54,1% | 0,009 | 49,9% | 45,2% | 0,240 |
| PCI previa | 15,3% | 18,6% | 0,077 | 15,3% | 18,1% | 0,345 |
| FEVI 30-50% | 17,8% | 21,3% | 0,081 | 17,1% | 20,2% | 0,315 |
| FEVI <30% | 4,9% | 6,6% | 0,164 | 5,2% | 4,9% | 0,858 |
| Enfermedad del TCI | 42,8% | 38,9% | 0,112 | 42,5% | 43,4% | 0,813 |
| Enfermedad de tres vasos | 69,4% | 70,4% | 0,661 | 67,6% | 70% | 0,50 |
| Urgente/emergente | 10,8% | 10,4% | 0,825 | 11% | 9,2% | 0,436 |
| Estado crítico | 9,1% | 10,8% | 0,284 | 9,8% | 10,4% | 0,795 |
| EuroScoreI, media (DE) | 3,1 (4,2) | 6,2 (7,5) | <0,001 | 3,9 (5,2) | 3,8 (4,5) | 0,732 |
| Características operatorias | ||||||
| Número de injertos, media (DE) | 2,8 (0,7) | 2,6 (0,7) | <0,001 | 2,7 (0,7) | 2,6 (0,6) | 0,002 |
| Revascularización completa | 72,7% | 58,8% | <0,001 | 73,2% | 60,2% | <0,001 |
| Uso de AMI bilateral | 81,8% | − | − | 77,7% | − | − |
| Uso de arteria radial | 20,6% | − | − | 23,8% | − | − |
AMI: arteria mamaria izquierda; CSS: clasificación de la intensidad de angina según la Canadian Cardiovascular Society; EPOC: enfermedad pulmonar obstructiva crónica; ERC: enfermedad renal crónica; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; IAM: infarto de miocardio; MAG: revascularización arterial múltiple; NYHA: clase funcional según la New York Heart Association; PCI: intervención coronaria percutánea; SAG: revascularización arterial única; TCI: tronco coronario izquierdo.
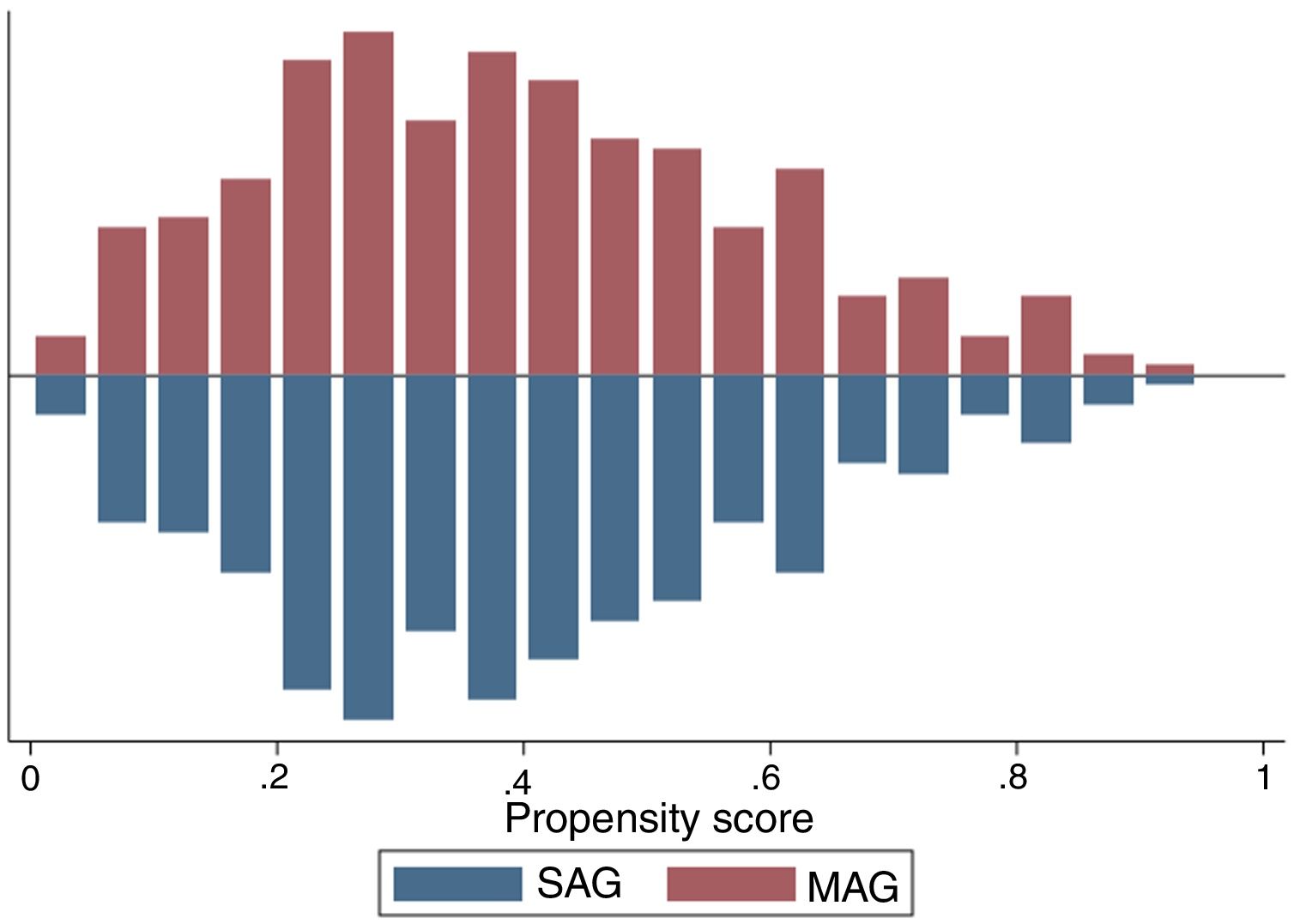
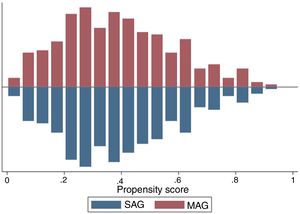
La eficacia del apareamiento por escore de propensión fue analizada con histogramas de la puntuación de propensión según la estrategia de revascularización (MAG/SAG) (fig. 1), mediante el análisis de la diferencia estandarizada y comparación de medias, sin observar diferencias significativas en las características preoperatorias de ambos grupos.
La arteria mamaria interna izquierda fue el injerto de elección para revascularizar la arteria descendente anterior. La media de injertos realizados fue de 2,8 vs 2,6 (p<0,001) y en el 72,7% vs 58,8% (p<0,001) se consiguió una revascularización completa en el grupo de MAG vs SAG, respectivamente.
En el grupo MAG la arteria mamaria interna derecha fue el segundo injerto arterial de elección (81,8%), seguido de la arteria radial (18,2%). No se utilizó la arteria gastroepiploica. En el 51,4% se realizó una revascularización arterial completa.
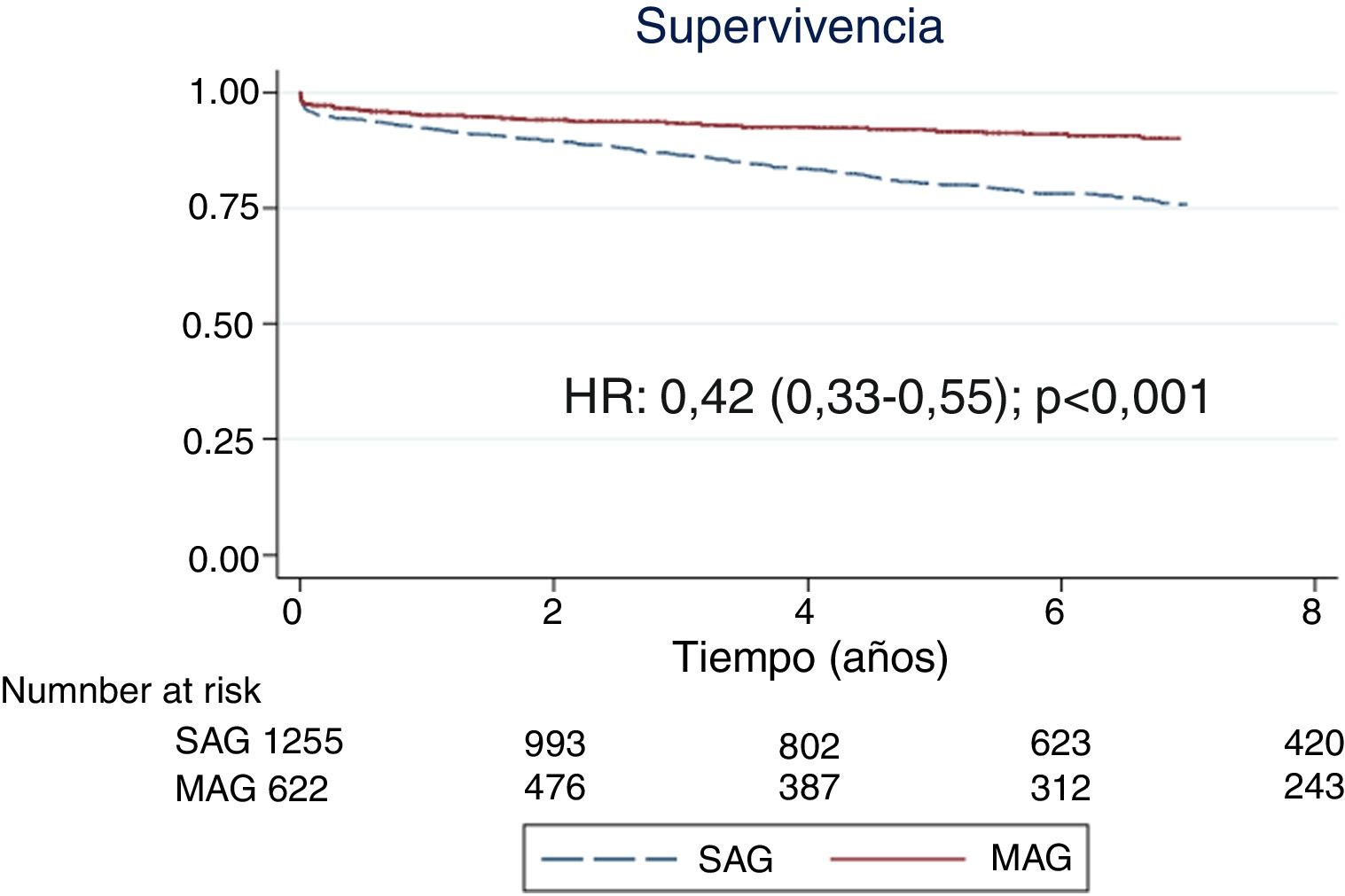
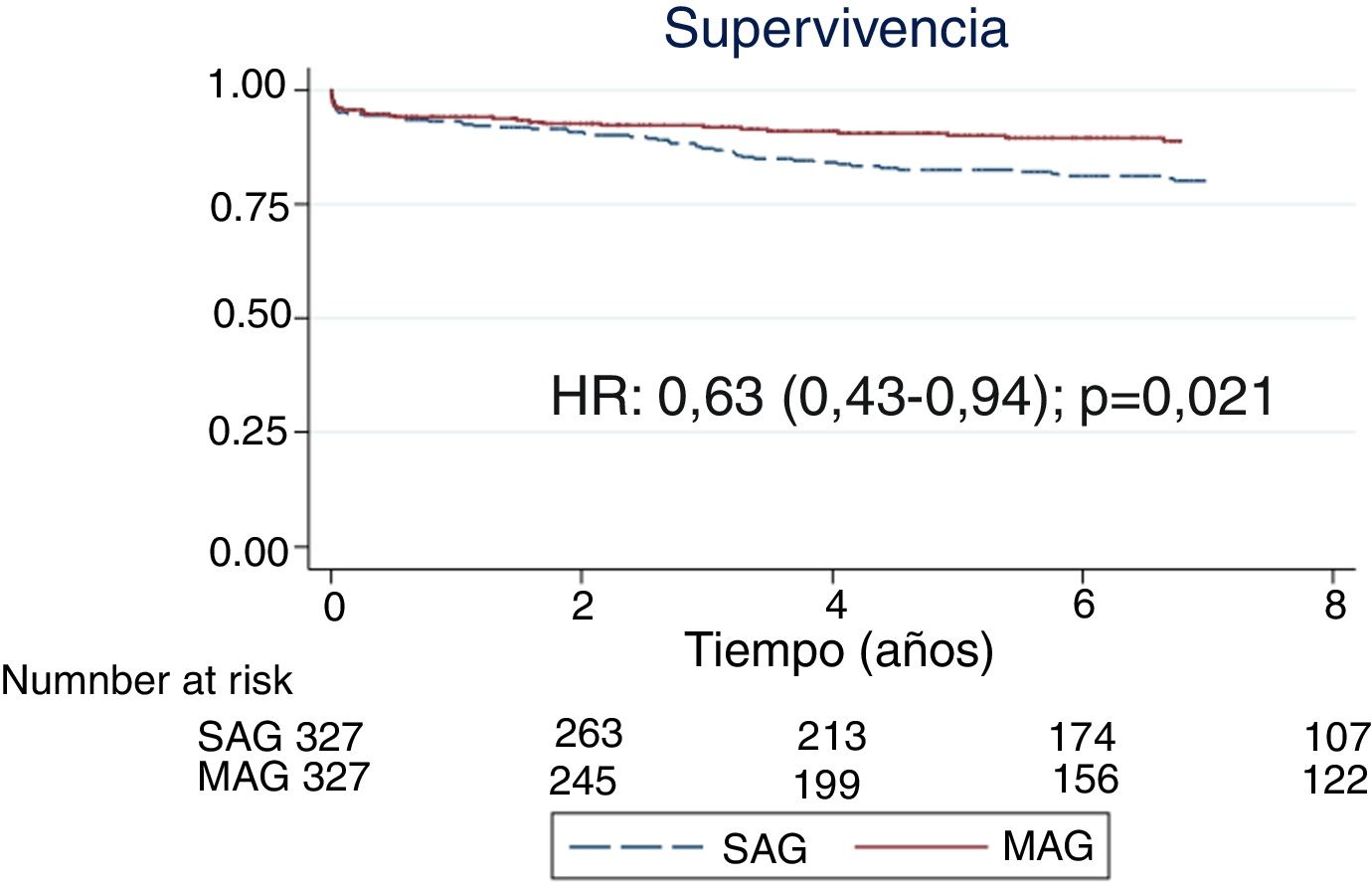
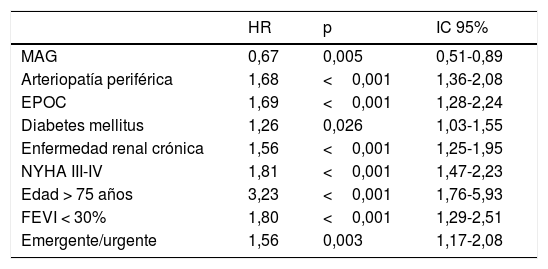
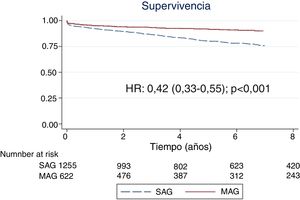
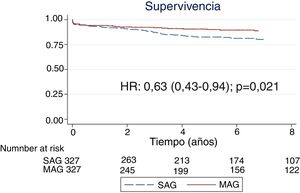
La mediana de seguimiento fue de 5,9años (IQR: 2,4-9,2). Ningún paciente fue perdido en el seguimiento. La supervivencia a 3, 5 y 7años para MAG y SAG fue de 93,2% vs 86,3%, de 91,7% vs 80,1% y de 89,9% vs 75,8%, respectivamente (HR: 0,42; IC95%: 0,33-0,55; p<0,001) (fig. 2). Tras el ajuste mediante puntuación de propensión observamos una supervivencia entre MAG y SAG a 3, 5 y 7años del 91,6% vs 87,1%, del 89,8% vs 82,4% y del 88,7% vs 80% (HR: 0,63; IC95%: 0,43-0,93; p=0,021) (fig. 3). En el análisis de riesgos proporcionados de Cox para la cohorte total, el uso de MAG fue un factor independiente asociado a mayor supervivencia (HR: 0,67; IC95%: 0,51-0,89; p=0,005). Identificamos como factores de riesgo significativos para menor supervivencia la arteriopatía periférica (HR: 1,68; IC95%: 1,36-2,08; p<0,001), la enfermedad pulmonar obstructiva crónica (HR: 1,69; IC95%: 1,28-2,24; p<0,001), la diabetes mellitus (HR: 1,26; IC95%: 1,03-1,55; p=0,026); la enfermedad renal crónica (HR: 1,56; IC95%: 1,25-1,95; p<0,001), una clase funcional NYHAIII-IV (HR: 1,81; IC95%: 1,47-2,23; p<0,001), edad >75años (HR: 3,23; IC95%: 1,76-5,93; p<0,001), fracción de eyección <30% (HR: 1,80; IC95%: 1,29-2,51; p<0,001) y el carácter urgente o emergente de la intervención (HR: 1,56; IC95%: 1,17-2,08; p=0,003) (tabla 2).
Predictores del evento primario mediante análisis de riesgo proporcionados de Cox en la cohorte total
| HR | p | IC 95% | |
|---|---|---|---|
| MAG | 0,67 | 0,005 | 0,51-0,89 |
| Arteriopatía periférica | 1,68 | <0,001 | 1,36-2,08 |
| EPOC | 1,69 | <0,001 | 1,28-2,24 |
| Diabetes mellitus | 1,26 | 0,026 | 1,03-1,55 |
| Enfermedad renal crónica | 1,56 | <0,001 | 1,25-1,95 |
| NYHA III-IV | 1,81 | <0,001 | 1,47-2,23 |
| Edad > 75 años | 3,23 | <0,001 | 1,76-5,93 |
| FEVI < 30% | 1,80 | <0,001 | 1,29-2,51 |
| Emergente/urgente | 1,56 | 0,003 | 1,17-2,08 |
EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; HR: razón de tasas; IC: intervalo de confianza; MAG: revascularización arterial múltiple; NYHA: clase funcional según la New York Heart Association.
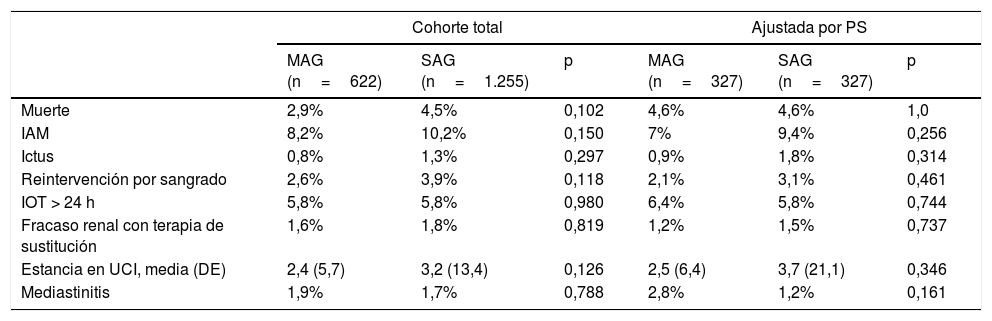
De manera perioperatoria no se observaron diferencias significativas en eventos adversos cardiovasculares mayores entre MAG y SAG tanto en la cohorte total como en la ajustada: muerte (n=18) 2,9% vs (n=56) 4,5% (p=0,10); ictus 0,8% vs 1,3% (p=0,29); infarto de miocardio (IAM) 8,2% vs 10,2% (p=0,15). Tampoco observamos diferencias significativas en otros eventos evaluados entre MAG y SAG, como mediastinitis (1,9% vs 1,7%; p=0,78), reintervención por sangrado (2,6% vs 3,4%; p=0,12), fracaso renal con requerimiento de terapia de sustitución renal (1,6% vs 1,7%; p=0,82), entre otros (tabla 3).
Resultados perioperatorios en la cohorte total y tras ajuste mediante puntuación de propensión (PS)
| Cohorte total | Ajustada por PS | |||||
|---|---|---|---|---|---|---|
| MAG (n=622) | SAG (n=1.255) | p | MAG (n=327) | SAG (n=327) | p | |
| Muerte | 2,9% | 4,5% | 0,102 | 4,6% | 4,6% | 1,0 |
| IAM | 8,2% | 10,2% | 0,150 | 7% | 9,4% | 0,256 |
| Ictus | 0,8% | 1,3% | 0,297 | 0,9% | 1,8% | 0,314 |
| Reintervención por sangrado | 2,6% | 3,9% | 0,118 | 2,1% | 3,1% | 0,461 |
| IOT > 24 h | 5,8% | 5,8% | 0,980 | 6,4% | 5,8% | 0,744 |
| Fracaso renal con terapia de sustitución | 1,6% | 1,8% | 0,819 | 1,2% | 1,5% | 0,737 |
| Estancia en UCI, media (DE) | 2,4 (5,7) | 3,2 (13,4) | 0,126 | 2,5 (6,4) | 3,7 (21,1) | 0,346 |
| Mediastinitis | 1,9% | 1,7% | 0,788 | 2,8% | 1,2% | 0,161 |
DE: desviación estándar; IAM: infarto de miocardio; IOT: intubación orotraqueal; MAG: revascularización arterial múltiple; SAG: revascularización arterial única; UCI: unidad de cuidados intensivos.
Hace ya 20 años que Lytle et al.2 publicaron su estudio seminal observando los beneficios de la MAG. Desde ese entonces y hasta la actualidad se ha generado una gran cantidad de evidencia que respalda el uso de MAG, pero, a pesar de esto, el uso de esta estrategia de revascularización no ha sido adoptada de manera generalizada, con gran variabilidad entre registros nacionales: desde un 43,8% en España1 hasta menos del 10% en Estados Unidos13.
Existe la constante en diversos estudios observacionales2,5,7 del uso de MAG preferentemente en pacientes jóvenes y con menor comorbilidad en comparación con pacientes que reciben SAG, y debido a esta heterogeneidad entre los dos grupos, la mayoría de estos estudios utilizan alguna técnica de ajuste estadístico para minimizar sesgos. En nuestro estudio las características del grupo SAG son las de un grupo de alto riesgo quirúrgico (EuroScoreI 6,2%), que tras el ajuste estadístico permitió una comparación con mayor control de sesgos. Las características de nuestra cohorte ajustada son similares a lo publicado, con una edad media de 64años y riesgo quirúrgico moderado.
No observamos diferencias significativas en la mortalidad perioperatoria en la cohorte total (p=0,10) y tras ajuste por puntación de propensión (p=1,0). La incidencia de este evento es similar a lo reportado en otros estudios observacionales2,4,13. Estos resultados nos indican que las dos estrategias de revascularización son seguras y que el uso de MAG no posee mayor riesgo respecto al estándar actual para cirugía de revascularización. Creemos que la baja incidencia de ictus en nuestra cohorte se debe principalmente a que las intervenciones se realizaron sin circulación extracorpórea y con manipulación de la aorta ascendente de manera parcial o nula, evitando el desprendimiento de placas de ateroma y disminuyendo la probabilidad de eventos adversos neurológicos, como ya se ha reportado previamente17. La incidencia de IAM es mayor a la reportada en diversas series, lo cual se encuentra en relación con la definición de IAM perioperatorio utilizada en nuestra institución. Varios autores han reportado la variabilidad en la incidencia de IAM perioperatorio según la definición empleada, y con ello el impacto de este evento en los resultados a largo plazo18,19. Finalmente, la incidencia de mediastinitis fue baja en ambos grupos, sin observar diferencias significativas (p=0,161). Existe variabilidad en este evento en las diversas series reportadas. En nuestra serie, la baja incidencia de mediastinitis puede ser explicada en parte por la técnica quirúrgica empleada para la extracción de los injertos (esqueletonizada), la cual se asocia a menor incidencia de esta complicación20-22.
A 7 años observamos mayor supervivencia, de manera significativa, a favor del uso de MAG, tanto en la cohorte total como en la ajustada (89,9% vs 75,8%, p<0,001, y 88% vs 80%, p=0,021, respectivamente) e identificamos la MAG como un predictor independiente para mayor supervivencia (HR: 0,67; IC95%: 0,51-0,89). En el metaanálisis de 38 estudios (174.204 pacientes) publicado por Gaudino et al.23 comparando el uso de arteria mamaria interna unilateral o bilateral y una media de seguimiento de 7,2años, se observó una supervivencia del 60% vs 72% (p<0,001), respectivamente, mientras que en el registro del estado de Nueva York (21.656 pacientes)7, comparando MAG/SAG con una media de seguimiento de 6,5años y una supervivencia del 87,3% vs 85,7% (p<0,001), respectivamente. El Arterial Revascularization Trial (ART)9 fue un ensayo clínico (3.000 pacientes) donde se comparó el uso de arteria mamaria unilateral o bilateral y que en 2019 publicó sus resultados a 10años, sin observar diferencias significativas entre ambas estrategias de revascularización (HR: 0,96; IC95%: 0,82-1,12). No obstante, el uso de la arteria radial como segundo injerto fue identificado como factor de confusión, y en un análisis a posteriori entre MAG y SAG se observaron diferencias significativas a favor de la MAG (HR: 0,81; IC95%: 0,68-0,95)9,10. En nuestra cohorte, creemos que dos causas confluyen de manera importante para explicar estos resultados. Primero, la proporción de revascularización completa fue mayor en el grupo MAG (73,2% vs 60,2%, p<0,001), la cual se ha asociado previamente a una mayor supervivencia24. Segundo, los injertos arteriales, debido a su resistencia a la aterosclerosis y a su mejor adaptabilidad al flujo coronario, tienen mayor durabilidad que los injertos venosos8,11,25. El ensayo ROMA26, que se encuentra en desarrollo actualmente, evaluará estas dos estrategias de revascularización y ofrecerá evidencia robusta en este ámbito de la cirugía cardiovascular.
LimitacionesSe trata de un estudio retrospectivo y unicéntrico, con una cohorte limitada; además, a pesar del uso de técnicas estadísticas para obtener muestras similares, pueden existir sesgos no controlados que influyan en nuestros resultados, por lo que estos deben interpretarse con cautela y como generadores de hipótesis.
ConclusionesLa revascularización arterial múltiple se asocia a una mayor supervivencia en comparación con el uso aislado de un solo injerto arterial a medio plazo. Ambas técnicas son seguras y poseen una baja incidencia de complicaciones perioperatorias.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.