El uso extensivo y precoz del ácido acetilsalicílico (AAS) está ampliamente aceptado en el postoperatorio de cirugía de derivación coronaria (CDC); sin embargo, su aplicación combinada en doble terapia antiagregante (DTA) es aún hoy controvertida. La DTA podría favorecer la protección de la permeabilidad de los injertos coronarios por una menor vulnerabilidad/desprotección frente a resistencias antiagregantes constitutiva y/o transitoria, así como por efectos pleiotrópicos de limitación de la progresión de la hiperplasia intimal. No obstante, la dosificación y duración del tratamiento no están completamente establecidas.
MetodologíaBúsqueda bibliográfica en Medline sobre la base de combinaciones de 3 grupos de palabras clave y selección de trabajos en pasos sucesivos.
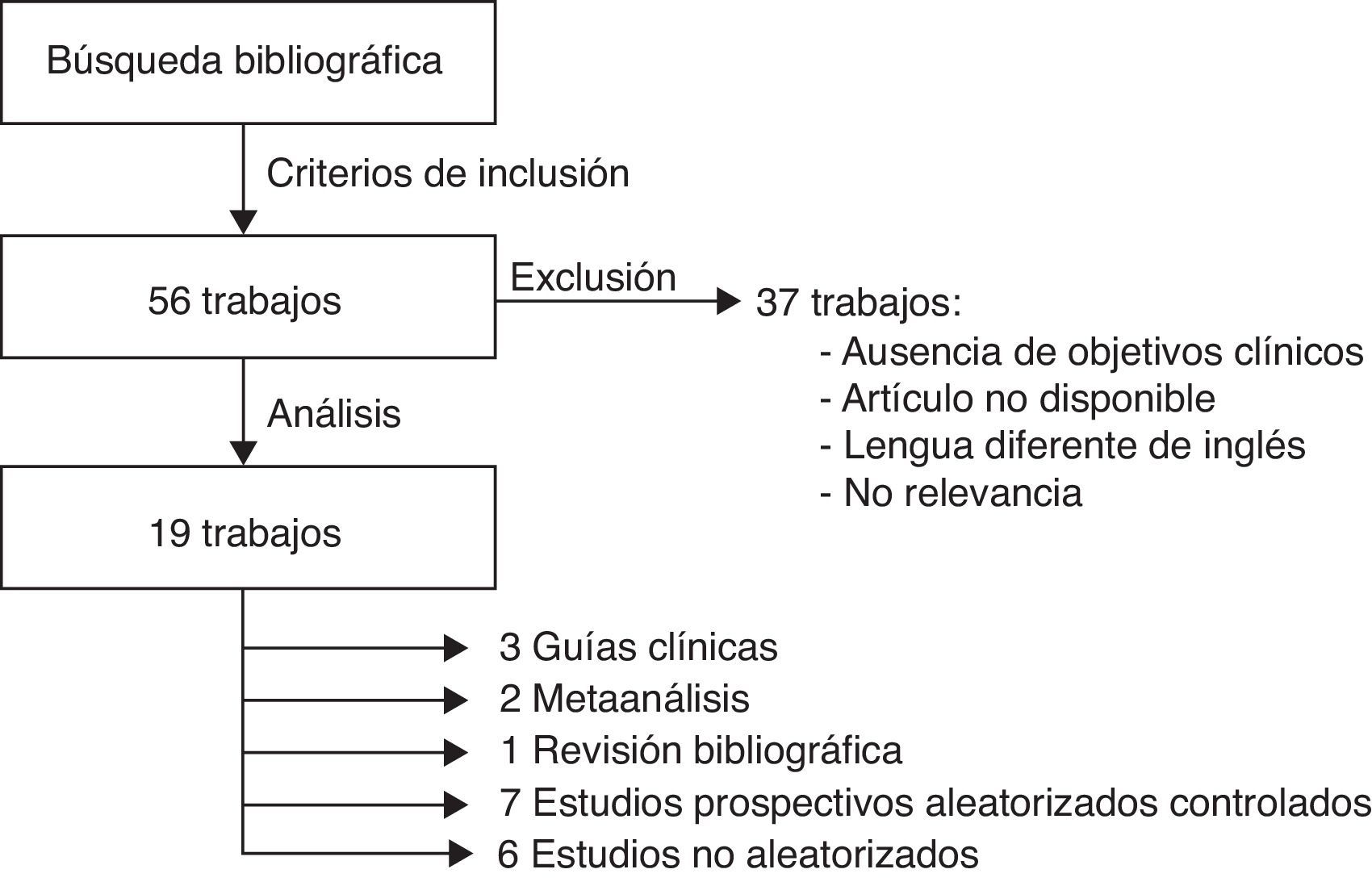
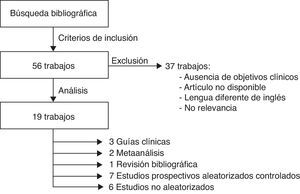
ResultadosSe obtuvieron 56 estudios preliminarmente, siendo 19 seleccionados para análisis: 7 prospectivos aleatorizados controlados, 2 metaanálisis, una revisión bibliográfica, 3 guías clínicas y 6 no aleatorizados. Todos ellos fueron analizados individualmente y clasificados según su resultado favorable o no a la DTA.
ConclusionesNo existe evidencia para apoyar extensivamente el uso de DTA en el postoperatorio de CDC aunque, podría ofrecer beneficios en contextos clínicos como la CDC tras síndrome coronario agudo reciente, la utilización extensiva de injertos de vena safena o la CDC sin CEC. Los beneficios mostrados en los estudios favorables para la mejoría de la permeabilidad de los injertos coronarios en el corto-medio plazo no se tradujeron en diferencias en la incidencia de eventos cardiovasculares mayores. No existieron tampoco diferencias en términos de seguridad frente a eventos hemorrágicos, tanto en el postoperatorio inmediato como en el seguimiento.
Extensive and early use of acetyl-salicylic acid (ASA) is widely accepted in the post-operative period after coronary artery bypass grafting surgery (CABG), however, its combination in double antiplatelet therapy (DAT) is still controversial. DAT may improve coronary graft patency due to a lower vulnerability against constitutive and/or transient antiplatelet therapy resistance, and due to potential pleiotropic effects against intimal hyperplasia. Nevertheless, dosage and duration of the treatment are not completely established.
MethodsSystematic bibliographic review in Medline combining 3 clusters of key words and stepwise selection of articles obtained.
ResultsOut of a total of 56 preliminary studies found, 19 were chosen for analysis, of which 7 were randomised controlled trials, 2 meta-analyses, 1 literature review, 3 clinical guidelines, and 6 non-randomised studies. All of them were individually analysed and classified as favourable or not to DAT.
ConclusionsThere is not enough evidence to warrant extensive use of DAT after CABG. However, DAT could show a benefit in certain clinical scenarios, such as CABG after prior coronary acute syndrome, extensive use of venous grafts, or CABG off-pump. The benefits shown in studies favourable to DAT on the improvement of coronary graft patency in the short-midterm did not lead to differences in the incidence of major cardiovascular events. Neither of the groups showed differences in terms of safety related to haemorrhagic events, nor in the immediate postoperative or follow-up period
La terapia antiagregante constituye una de las principales medidas en el manejo clínico de los pacientes sometidos a cirugía de derivación coronaria (CDC). Siendo ampliamente aceptada la introducción del ácido acetilsalicílico (AAS) desde fases precoces del postoperatorio en pacientes estables, la aplicación de doble terapia antiagregante (DTA), fundamentalmente como combinación de AAS y un agente antagonista del receptor P2Y12, aún hoy es controvertida1.
Recientes estudios de farmacodinámica de los agentes antiagregantes han demostrado marcada variabilidad de respuesta interindividual para las dosis habitualmente utilizadas en la práctica clínica, tanto en in vivo como in vitro2-4. Así, la falta de respuesta biológica o resistencia ha sido establecida con una prevalencia del 0,4-57% (media 24-27%) para AAS2 y del 4-30% en el caso del clopidogrel3. En la mayoría de los casos, esta resistencia es de origen multifactorial (véase la tabla 1), pudiendo presentar variaciones intraindividuales en diferentes circunstancias clínicas a lo largo del tiempo. En el contexto del postoperatorio inmediato de la CDC ha sido reportado el desarrollo de resistencia aproximadamente en un tercio de los pacientes intervenidos, presentando un carácter transitorio durante 1-3 meses y recuperando los pacientes su respuesta basal de no presentar nuevos eventos cardiovasculares mayores (ECVM)5. Otros escenarios clínicos que también pueden incrementar la resistencia intraindividual a antiagregantes son los síndromes coronarios agudos, estableciendo de antemano una condición adversa para el perioperatorio de CDC posterior. La asociación de diferentes agentes antiagregantes con mecanismos de acción complementarios podría proponerse como una alternativa frente a la desprotección en casos de presencia de resistencia farmacológica, superior a la continuación de monoterapia con dosis intensificada, ya que apenas conseguiría alcanzar el efecto farmacológico deseado incrementando el riesgo de eventos adversos (particularmente en el caso del AAS). Aunque no existe una clara correlación de las determinaciones analíticas con el riesgo de desarrollo de ECVM, la presencia de desprotección por resistencia al tratamiento con AAS y/o clopidogrel ha sido reportada como factor de riesgo independiente de desarrollo de los mismos2.
Factores relacionados con la resistencia a antiagregantes plaquetarios en el perioperatorio de cirugía de derivación coronaria
| Resistencia a AAS | Resistencia a clopidogrel | |
|---|---|---|
| Clínicos | Sexo femenino, edad, dislipidemia, obesidad, diabetes mellitus tipo 1 y 2, catecolaminas, insuficiencia cardiaca, enfermedad coronaria extensa y/o aguda/reagudizada | |
| Biodisponibilidadlimitada | Incumplimiento terapéuticoCompr. gastrorresistentes | Incumplimiento terapéuticoMalabsorciónInteracción en 1.er paso hepáticoPolimorfismos CYP450 3A4 |
| Farmacodinámicos | Competencia por la COX-1 y otros AINEPolimorfismos de COX-1 | Polimorfismos de P2Y12 |
| Mecanismos de escape/rebote | Síntesis alternativa de TXA2Reducción de la síntesis de PGI2Cambios en el sustrato/estímulo proagreganteAumento del turnover plaquetario (post-CEC) | Incremento de niveles de ADPCambios en el sustrato/estímulo proagreganteAumento del turnover plaquetario (post-CEC) |
AAS: ácido acetilsalicílico; ADP: adenosín difosfato; CEC: circulación extracorpórea; COX: enzima ciclooxigenasa; CYP450: citocromo P450; PGI2: prostaciclina; TXA2: tromboxano A2.
La utilización de la terapia antiagregante en el postoperatorio de la CDC, además de constituir parte del tratamiento farmacológico básico de la cardiopatía isquémica, pretende proteger los injertos coronarios de fallo, especialmente en el corto y medio plazo. Múltiples son los factores relacionados con dicho fallo (véase la tabla 2), entre los que la terapia antiagregante postoperatoria solo constituye un variable más5-8. Por ello, a priori, la posibilidad de extraer conclusiones en estudios individuales, unicéntricos y con muestras limitadas puede verse comprometida o sesgada incluso a pesar de la aleatorización en la selección de los grupos de estudio. A este hecho se suma que, a pesar de que la mayoría de los trabajos comparan AAS frente a DTA compuesta por AAS+clopidogrel, no existe clara homogeneidad en lo referente a la dosificación (particularmente de AAS) y timing de administración (inicio y tiempo de mantenimiento en el postoperatorio de la DTA). No obstante, el fallo de los injertos coronarios, en especial los de vena safena invertida, que continúan siendo los más utilizados en la práctica tanto de nuestro medio, como del europeo o americano, se estima entre el 10,9-26,4% (según series) en el primer año, con el 1-4% en los años subsiguientes, dando como resultado, a 10 años, aproximadamente un 40% de los injertos ocluidos y, del 60% restante, un 50% aproximadamente con estenosis angiográficamente significativas8. El fallo de los injertos coronarios ha sido también descrito como predictor independiente de desarrollo de nuevos ECVM8.
Factores relacionados con la permeabilidad de los injertos coronarios
| Factores técnicos | Extracción de injertosLesionesNon-touchEndoscopia vs. abiertaPediculado vs. esqueletizadoDilatación injerto VSBaño de injertosEstrategia de revascularizaciónAnatómica vs. funcional% estenosis vs. FFTTécnica anastomóticaCon/sin CECSitio de anastomosisSutura polipropileno 6-7-8/0Injertos libres vs. secuencialesErrores técnicosTorsiónAcodamientoInjerto largo/cortoExo-stents |
| Factores farmacológicos/postoperatorios | Bajo gasto/hipotensión postoperatoriaVasoconstrictores, transfusión pool plaquetas postoperatoriosCalcioantagonistas a largo plazo en arteria radialTerapia antiagreganteControl de factores de riesgo cardiovascularTerapias adyuvantes |
| Factores anatómicos/hemodinámicos | Injerto venoso vs. arterial (y qué arteria/s)Discrepancia calibre injerto-coronariaCalidad intrínseca del injertoAteromatosisColateralesLongitudRun offLecho coronarioAnastomosis secuencialesFlujo competitivo |
CEC: circulación extracorpórea; FFT: reserva fraccional de flujo; VS: vena safena.
En algunos estudios ha sido descrito un efecto pleiotrópico del clopidogrel como inhibidor del desarrollo de hiperplasia intimal9. Este fenómeno es el principal responsable de fallo de los injertos de vena safena a medio plazo por lo que la utilización de este fármaco podría ser de gran interés en el contexto de la CDC durante los primeros 3-6 meses de postoperatorio. Aunque los resultados in vitro han sido prometedores, no ha podido refrendarse tan claramente su papel in vivo a nivel de los injertos10, aunque sí en la progresión de las lesiones preexistentes, el desarrollo de nuevas lesiones o deterioro del lecho coronario nativo distal a las anastomosis11.
A pesar del potencial beneficio expuesto para la DTA, el contexto del postoperatorio de cirugía cardiaca6,7, particularmente en sus primeros días/semanas, constituye un escenario con riesgo hemorrágico incrementado. Además, el riesgo de complicaciones hemorrágicas, fundamentalmente a nivel digestivo y neurológico, está asimismo incrementado en pacientes bajo tratamiento crónico con 2 fármacos antiagregantes, aspecto que puede comprometer el potencial beneficio clínico de la DTA.
La siguiente revisión sistemática tratará de actualizar la evidencia comunicada en la literatura sobre el papel de la DTA en el postoperatorio de CDC en términos de beneficio clínico: ECVM (muerte, infarto agudo de miocardio, nueva revascularización), permeabilidad de injertos y seguridad frente a eventos hemorrágicos.
MetodologíaSe llevó a cabo una búsqueda bibliográfica en MedLine® por palabras clave, combinando un término de cada uno de los 3 grupos siguientes en todas las combinaciones posibles:
- 1.
Grupo 1: clopidogrel, dual/double antiaggregation, dual/double antiplatelet therapy.
- 2.
Grupo 2: CABG postoperative, coronary bypass postoperative.
- 3.
Grupo 3: randomized controlled trial, RCT.
Incluyendo asimismo citaciones relacionadas de los trabajos seleccionados.
Para la selección de los trabajos se realizó un análisis de la calidad metodológica y se siguió el criterio de best evidence topic, particularmente en el caso de los trabajos no aleatorizados, para ser incluidos en la revisión. El objetivo de la revisión se centró en la respuesta a la pregunta: ¿existe beneficio clínico de la terapia con doble antiagregación plaquetaria en el postoperatorio de la cirugía de derivación coronaria? (fig. 1).
Fueron seleccionados todos los estudios prospectivos aleatorizados publicados hasta mayo del 2015, así como una selección de los estudios no aleatorizados publicados en los últimos 5 años desde la fecha de corte establecida, según los criterios anteriores. Se consideraron asimismo revisiones bibliográficas y metaanálisis publicados en los últimos 3 años y los apartados específicos en lo referente a la DTA en el postoperatorio de CDC de la última versión las guías clínicas específicas de la American College of Cardiology/American Heart Association (ACC/AHA), la European Association for Cardiothoracic Surgery/European Society of Cardiology (EACTS/ESC) y la Canadian Cardiovascular Society (CCS).
Fueron excluidos todos los trabajos no realizados en humanos, que no contuvieran objetivos clínicos (permeabilidad de injertos, eventos cardiovasculares), así como aquellas editoriales, opiniones de expertos o escritos en idioma diferente de la lengua inglesa.
ResultadosResultados de la búsqueda bibliográficaSe obtuvieron 56 artículos preliminarmente sobre la base de los criterios anteriormente expuestos. De estos, 19 estudios10-28 fueron seleccionados para el análisis sobre la base de criterios de metodología y calidad de evidencia: 7 estudios prospectivos aleatorizados controlados10,11,14,15,18-20, 2 metaanálisis26,27, una revisión bibliográfica28, 3 guías clínicas12,13,17 y 6 estudios no aleatorizados16,21-25. Los estudios prospectivos aleatorizados controlados en el estudio se desglosan con detalle de sus diseños y principales conclusiones en la tabla 3.
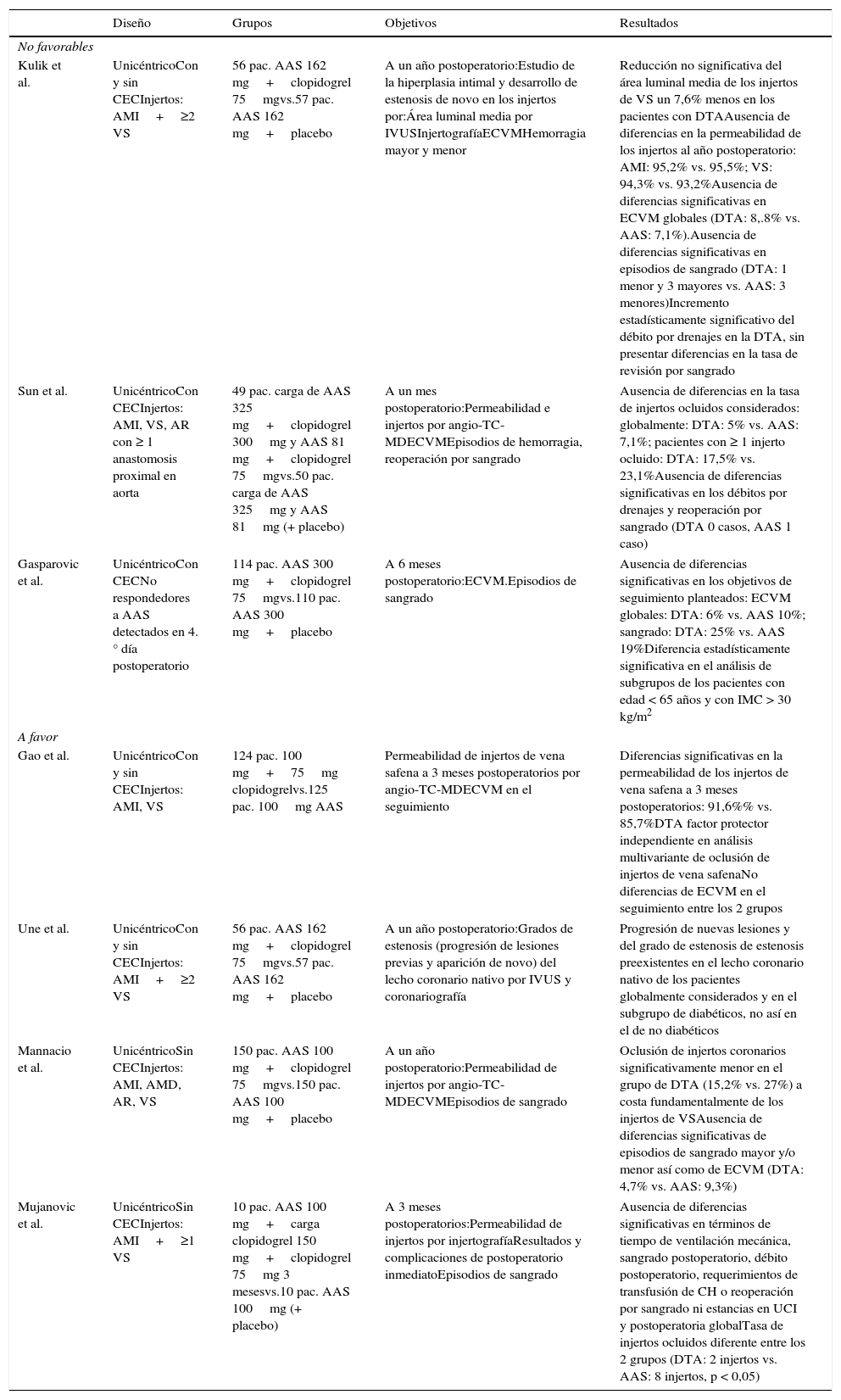
Resumen de diseños y resultados de estudios prospectivos aleatorizados controlados
| Diseño | Grupos | Objetivos | Resultados | |
|---|---|---|---|---|
| No favorables | ||||
| Kulik et al. | UnicéntricoCon y sin CECInjertos: AMI+≥2 VS | 56 pac. AAS 162 mg+clopidogrel 75mgvs.57 pac. AAS 162 mg+placebo | A un año postoperatorio:Estudio de la hiperplasia intimal y desarrollo de estenosis de novo en los injertos por:Área luminal media por IVUSInjertografíaECVMHemorragia mayor y menor | Reducción no significativa del área luminal media de los injertos de VS un 7,6% menos en los pacientes con DTAAusencia de diferencias en la permeabilidad de los injertos al año postoperatorio: AMI: 95,2% vs. 95,5%; VS: 94,3% vs. 93,2%Ausencia de diferencias significativas en ECVM globales (DTA: 8,.8% vs. AAS: 7,1%).Ausencia de diferencias significativas en episodios de sangrado (DTA: 1 menor y 3 mayores vs. AAS: 3 menores)Incremento estadísticamente significativo del débito por drenajes en la DTA, sin presentar diferencias en la tasa de revisión por sangrado |
| Sun et al. | UnicéntricoCon CECInjertos: AMI, VS, AR con ≥ 1 anastomosis proximal en aorta | 49 pac. carga de AAS 325 mg+clopidogrel 300mg y AAS 81 mg+clopidogrel 75mgvs.50 pac. carga de AAS 325mg y AAS 81mg (+ placebo) | A un mes postoperatorio:Permeabilidad e injertos por angio-TC-MDECVMEpisodios de hemorragia, reoperación por sangrado | Ausencia de diferencias en la tasa de injertos ocluidos considerados: globalmente: DTA: 5% vs. AAS: 7,1%; pacientes con ≥ 1 injerto ocluido: DTA: 17,5% vs. 23,1%Ausencia de diferencias significativas en los débitos por drenajes y reoperación por sangrado (DTA 0 casos, AAS 1 caso) |
| Gasparovic et al. | UnicéntricoCon CECNo respondedores a AAS detectados en 4.° día postoperatorio | 114 pac. AAS 300 mg+clopidogrel 75mgvs.110 pac. AAS 300 mg+placebo | A 6 meses postoperatorio:ECVM.Episodios de sangrado | Ausencia de diferencias significativas en los objetivos de seguimiento planteados: ECVM globales: DTA: 6% vs. AAS 10%; sangrado: DTA: 25% vs. AAS 19%Diferencia estadísticamente significativa en el análisis de subgrupos de los pacientes con edad < 65 años y con IMC > 30 kg/m2 |
| A favor | ||||
| Gao et al. | UnicéntricoCon y sin CECInjertos: AMI, VS | 124 pac. 100 mg+75mg clopidogrelvs.125 pac. 100mg AAS | Permeabilidad de injertos de vena safena a 3 meses postoperatorios por angio-TC-MDECVM en el seguimiento | Diferencias significativas en la permeabilidad de los injertos de vena safena a 3 meses postoperatorios: 91,6%% vs. 85,7%DTA factor protector independiente en análisis multivariante de oclusión de injertos de vena safenaNo diferencias de ECVM en el seguimiento entre los 2 grupos |
| Une et al. | UnicéntricoCon y sin CECInjertos: AMI+≥2 VS | 56 pac. AAS 162 mg+clopidogrel 75mgvs.57 pac. AAS 162 mg+placebo | A un año postoperatorio:Grados de estenosis (progresión de lesiones previas y aparición de novo) del lecho coronario nativo por IVUS y coronariografía | Progresión de nuevas lesiones y del grado de estenosis de estenosis preexistentes en el lecho coronario nativo de los pacientes globalmente considerados y en el subgrupo de diabéticos, no así en el de no diabéticos |
| Mannacio et al. | UnicéntricoSin CECInjertos: AMI, AMD, AR, VS | 150 pac. AAS 100 mg+clopidogrel 75mgvs.150 pac. AAS 100 mg+placebo | A un año postoperatorio:Permeabilidad de injertos por angio-TC-MDECVMEpisodios de sangrado | Oclusión de injertos coronarios significativamente menor en el grupo de DTA (15,2% vs. 27%) a costa fundamentalmente de los injertos de VSAusencia de diferencias significativas de episodios de sangrado mayor y/o menor así como de ECVM (DTA: 4,7% vs. AAS: 9,3%) |
| Mujanovic et al. | UnicéntricoSin CECInjertos: AMI+≥1 VS | 10 pac. AAS 100 mg+carga clopidogrel 150 mg+clopidogrel 75mg 3 mesesvs.10 pac. AAS 100mg (+ placebo) | A 3 meses postoperatorios:Permeabilidad de injertos por injertografíaResultados y complicaciones de postoperatorio inmediatoEpisodios de sangrado | Ausencia de diferencias significativas en términos de tiempo de ventilación mecánica, sangrado postoperatorio, débito postoperatorio, requerimientos de transfusión de CH o reoperación por sangrado ni estancias en UCI y postoperatoria globalTasa de injertos ocluidos diferente entre los 2 grupos (DTA: 2 injertos vs. AAS: 8 injertos, p < 0,05) |
AR: arteria radial; AAS: ácido acetilsalicílico; AMI: arteria mamaria interna; CEC: circulación extracorpórea; DTA: doble terapia antiagregante; ECVM: eventos cardiovasculares mayores; VS: vena safena.
Ninguno de los trabajos incluidos (3 estudios prospectivos aleatorizados controlados10,14,15, 2 guías clínicas12,13 y un estudio no aleatorizado16) demuestra que la DTA de AAS y clopidogrel frente a la monoterapia antiagregante con AAS no presenta clara superioridad significativa en términos de permeabilidad de injertos o prevención de ECVM en el postoperatorio, independientemente del diseño. Asimismo tampoco se reporta un incremento significativo de eventos adversos, predominantemente de tipo hemorrágico, tanto en el postoperatorio inmediato o en el seguimiento.
Guías clínicasLas guías de la ACC/AHA de 201112 no contemplan alguna indicación formal para la DTA. Las sociedades europeas EACTS/ESC en las guías clínicas de 201413 especifican que «debería ser considerado el reinicio de clopidogrel, ticagrelor o prasugrel tras CDC tan pronto como se considere seguro» (clase iia nivel C), estableciéndose una aproximación a la DTA en el postoperatorio de CDC pero que solo sería aplicada en aquellos pacientes que ya la seguían preoperatoriamente en relación con diferentes contextos clínicos. No obstante, no se trata de una indicación expresa de inicio de DTA tras CDC.
Estudios prospectivos aleatorizados controladosTres de los 3 estudios prospectivos aleatorizados controlados incluidos10,14,15 analizan la permeabilidad de los injertos coronarios mediante angio-TC coronario o mediante injertografía, en uno de ellos a un año postoperatorio y en los otros a uno y 6 meses. A pesar de la heterogeneidad de la técnica quirúrgica (con/sin circulación extracorpórea, tipo de injertos utilizados) y de la pauta de tratamiento antiagregante seguido (diferentes dosis, duración de la DTA, aplicación o no de dosis de carga), no se apreciaron diferencias significativas en la permeabilidad de los injertos tanto de vena como arteriales. En el estudio de Sun et al.14 (estudio PAPA-CABG) es llamativa la limitada permeabilidad de los injertos de arteria radial tanto en el grupo de AAS (43,8%) como de DTA (10%) a un año (p < 0,05), siendo reconocido en el análisis como una posible limitación de la técnica de extracción y manejo intraoperatorio del injerto en la discusión del trabajo. Adicionalmente, el estudio de Kulik et al.10 (estudio CASCADE) realiza un análisis con IVUS de los injertos para comprobar la limitación de la progresión de la hiperplasia intimal a un año postoperatorio como efecto pleiotrópico del tratamiento con clopidogrel, obteniéndose limitada diferencia (7,6%; p > 0,05) en el área luminal media entre los 2 grupos de tratamiento. En los 4 trabajos se incluye análisis de eventos adversos de la terapia antiagregante en el postoperatorio inmediato y en el seguimiento. Ninguno de los trabajos demostró un incremento significativo de las estancias postoperatorias en UCI y global, requerimientos transfusionales, necesidad de revisión quirúrgica por sangrado o episodios hemorrágicos en el seguimiento. Solo el trabajo de Kulik et al.10 demostró un incremento en la mediana del débito postoperatorio sin otra repercusión clínica. Análogamente, tampoco se demostró globalmente diferencia alguna en la incidencia de ECVM en el seguimiento en los estudios analizados. No obstante, Gasparovic et al.15 reportan diferencias significativas en la incidencia de ECVM en el análisis de subgrupos de pacientes con edad < 65 años e índice de masa corporal > 30 kg/m2, siendo propuestos como predictores de resistencia a la terapia antiagregante.
Estudios no aleatorizadosEl principal trabajo fue realizado por Ebrahimi et al.16 como reanálisis de los datos del estudio ROOBY. El estudio es el más extenso en la muestra de pacientes incluida (n=953), constituyendo el 43% de la muestra original del estudio ROOBY, de la cual hubo disponibilidad de conocimiento de la terapia antiagregante seguida y de control de permeabilidad de los injertos coronarios al año postoperatorio por angiografía. A pesar de tratarse de un estudio multicéntrico, incorpora ciertas deficiencias de diseño que pueden comprometer los resultados obtenidos. Así, la dosis de AAS que siguieron los pacientes de los grupos de monoterapia y DTA fueron variables según centros, no se aplicó enmascaramiento con placebo del grupo de monoterapia y existieron diferencias significativas en las variables preoperatorias de los grupos de tratamiento en términos de la distribución de razas, el seguimiento de terapia antiagregante preoperatoria, así como la tasa de pacientes intervenidos con/sin circulación extracorpórea (CEC) o el porcentaje de extracción de vena safena interna por vía endoscópica. No existieron diferencias significativas en términos de la permeabilidad de los injertos coronarios tanto globalmente considerados (86,5% vs. 85,3%) como particularmente los de vena safena (82,6% vs. 80,3%). El análisis de subgrupos por la realización la CDC con o sin CEC reprodujo los resultados, sin diferencias significativas entre grupos, aunque sí con una marcada tendencia clínica desfavorable a la CDC sin CEC y bajo régimen de monoterapia (permeabilidad de injertos de vena safena a una año postoperatorio: con CEC: DTA 84,5%, AAS 82,6%; sin CEC: DTA 81,3%, AAS 77,4%; p > 0,05).
Trabajos a favor de la doble terapia antiagreganteLos trabajos analizados (4 estudios prospectivos aleatorizados controlados11,18-20, una guía clínica17 y 5 estudios no aleatorizados21-25) muestran beneficio en la mejoría de la permeabilidad de los injertos coronarios para la DTA frente a la monoterapia con AAS. Este beneficio no queda tan claramente traducido en la prevención de ECVM en el seguimiento, así como tampoco se demuestra un incremento significativo de eventos adversos hemorrágicos.
Guías clínicasLa guía de 2009 de la CCS17 especifica que en «aquellos pacientes que recibieron clopidogrel pre-CDC por un síndrome coronario agudo (SCA) reciente debe ser reinstaurado tras la cirugía para reducir el riesgo de SCA recurrente». Esta indicación, aunque con similitudes respecto de las anteriores guías, hace hincapié expreso en el beneficio de la DTA en el manejo perioperatorio de los pacientes afectados de SCA, tanto en el preoperatorio (detallándose criterios para guiar la suspensión preoperatoria del clopidogrel) como en el postoperatorio. Se distingue así al subgrupo de pacientes sometidos a revascularización quirúrgica urgente como de alto riesgo dentro del espectro de la CDC. No obstante, estas guías no extienden formalmente la indicación de DTA a otros escenarios clínicos de la revascularización quirúrgica.
Estudios prospectivos aleatorizados controladosSe analizaron 4 trabajos11,18-20 con objetivos centrados en el análisis de permeabilidad de injertos coronarios por injertografía (2 trabajos) o angio-TC coronaria (2 trabajos), así como de la incidencia de eventos adversos en el postoperatorio inmediato y en el seguimiento tanto ECVM como de tipo hemorrágico. Gao et al.18 demuestran una permeabilidad marcadamente más limitada de los injertos de vena safena en un plazo de 3 meses, sin presentar traducción clínica en incremento de ECVM, aunque la DTA se mostró como un factor protector independiente de la oclusión de injertos de vena safena. El estudio de Une et al.11 constituye un reanálisis de la muestra del estudio CASCADE de Kulik et al.10, donde, en la misma muestra, el estudio de IVUS de la progresión de la hiperplasia intimal en los injertos coronarios también fue aplicado al lecho nativo para determinar la aparición de lesiones de novo o progresión de lesiones previamente conocidas. Globalmente, fue identificada una protección del lecho nativo en el caso de los pacientes sometidos a DTA, fue debida al efecto protector de esta terapia en el subgrupo de pacientes diabéticos, determinado en un subanálisis de subgrupos. El subgrupo de pacientes no diabéticos no presentó diferencias en la progresión de enfermedad coronaria en el lecho nativo, independientemente de la estrategia de tratamiento antiagregante. Mannacio et al.19 (estudio CRYSSA) constituyen el trabajo con diseño prospectivo aleatorizado controlado con mayor tamaño muestral (n=300), que evidencia una reducción de la tasa de oclusión de los injertos coronarios a un año postoperatorio a costa fundamentalmente de los injertos de vena safena. No obstante, este hecho no presenta traducción en una incidencia significativamente mayor de ECVM en el seguimiento, aunque esta es prácticamente el doble en el grupo de AAS frente al de DTA. No se evidenciaron diferencias estadísticamente significativas en términos de episodios hemorrágicos entre los grupos. El estudio CRYSSA incluye una línea de análisis paralela en la muestra original determinando la resistencia a AAS y clopidogrel al 5.° día postoperatorio. Las tasas de resistencia fueron de aproximadamente un tercio de los casos para cada uno de los fármacos, quedando por tanto desprotegidos 49 de 150 en el grupo de monoterapia y 19 de 150 en el caso de la DTA. El estudio de Mujanovic et al.20 es el más débil de los trabajos prospectivos aleatorizados controlados, con una muestra de solo 20 enfermos. No se evidenciaron diferencias en términos de seguridad en el postoperatorio inmediato ni en el seguimiento. La tasa de oclusión de injertos coronarios a 3 meses fue estadísticamente significativa, aunque debe ser interpretado con cautela ante las limitaciones del diseño (injertos totales ocluidos: DTA 2 vs. AAS 8).
Estudios no aleatorizadosLos 5 trabajos no aleatorizados21-25 presentan objetivos y diseños heterogéneos, con una conclusión común que permite apoyar la asociación de DTA en el postoperatorio de CDC sobre la base de algún beneficio clínico. Engoren et al.21 describen una serie de pacientes sometidos a DTA con AAS+ketorolaco pautado con objetivos de adyuvancia en la analgesia, siendo el antiagregante un efecto colateral. Demuestran un retardo en la necesidad de nueva coronariografía, así como en la oclusión de injertos coronarios respecto de los pacientes con AAS en monoterapia, ajustando los grupos por metodología de propensity score. Ibrahim et al.22 demuestran, en una serie retrospectiva, una menor tasa de oclusión de los injertos de vena safena en aquellos pacientes de DTA vs. AAS. El análisis se apoya en un diseño retrospectivo observacional y la realización de los cateterismos de control, aunque electivamente no siguió una pauta temporal protocolizada (media 185±92 días). Shenibb et al.23 plantean un estudio prospectivo descriptivo de la tasa de eventos adversos de la DTA, requiriendo menos del 10% del tratamiento con clopidogrel asociado, siendo en la mitad de los casos debido al inicio de terapia anticoagulante y solo presentando un episodio de hemorragia digestiva entre 135 pacientes. La tasa de ECVM también fue asimismo favorable, con un 2,22% de accidentes cerebrovasculares y un 5% de infartos de miocardio, todos ellos con injertos permeables. Gurbuz et al.24 profundizan en la cuestión del timing de aplicación de la DTA en el postoperatorio de CDC, estableciendo 3 grupos de estudio: DTA un mes y posteriormente AAS en monoterapia, DTA crónica y un tercero como control de AAS en monoterapia exclusiva. El análisis multivariante identificó recibir tratamiento con clopidogrel como factor predictor independiente de ECVM globalmente y particularmente de recurrencia de angina de pecho. No existieron, sin embargo, diferencias significativas entre los grupos de DTA con diferente timing en términos de ECVM o recurrencia de angina de pecho. Los eventos hemorrágicos fueron limitados y sin diferencias significativas, tanto en los grupos de DTA como de monoterapia. Kayacioglu et al.25 estudian el papel de la trombocitosis reactiva tras la CDC en la permeabilidad de los injertos coronarios y el papel protector de la terapia antiagregante. Establecen un estudio prospectivo en 6 meses seleccionando pacientes con trombocitosis reactiva sometidos a monoterapia y DTA. El grupo de monoterapia presentó mayor tasa de ergometrías positivas, así como una mayor tasa de oclusión de injertos.
Metaanálisis y revisiones bibliográficasLa revisión de de Leon y Jackevicius28 constituye la revisión bibliográfica más extensa de los últimos 5 años, incluyendo 9 estudios, 4 de ellos prospectivos aleatorizados controlados. Concluyen que la evidencia para apoyar la DTA en el postoperatorio de CDC está limitada a los hallazgos de análisis de subgrupos en estudios observacionales. La mayoría de los estudios prospectivos aleatorizados controlados no han permitido demostrar una mejoría en la permeabilidad de los injertos coronarios que asimismo se traduzca en beneficio clínico, por lo que la evidencia revisada es considerada insuficiente para apoyar la DTA.
Por otro lado, los metaanálisis de Nocerino et al.26 y Deo et al.27 agregan los hallazgos de la mayoría de los estudios analizados con anterioridad, permitiendo un análisis con mayor potencia estadística en términos de conservación de la permeabilidad de los injertos coronarios, ECVM y fenómenos de sangrado. Cabe destacar que, en ambos trabajos, una amplia mayoría de estudios incluidos en el metaanálisis para cada objetivo analizado podrían ser clasificados como no favorables para apoyar la DTA, siguiendo la clasificación planteada con anterioridad. Sin embargo, en lo que respecta a la permeabilidad de los injertos, ambos metaanálisis muestran un claro beneficio de la DTA en la preservación de los injertos de vena safena (RR 0,59), no siendo significativo sin embargo este beneficio en el caso de los injertos arteriales o considerados globalmente; estos 2 últimos supuestos solo contemplados en el metaanálisis de Nocerino et al. No se demostró una reducción significativa de los ECVM con la DTA en el estudio de Deo et al.27, aunque sí una clara tendencia clínica favorable; sin embargo, específicamente la mortalidad postoperatoria fue menor en el caso de la DTA (RR 0,31-1,14 y 0,25-0,57, respectivamente). Ninguno de los 2 metaanálisis demostró un incremento significativo de los eventos hemorrágicos (RR 1,00-1,37).
DiscusiónA la vista de la evidencia recogida en los trabajos analizados en la presente revisión, no puede apoyarse extensivamente la aplicación de DTA en el postoperatorio de CDC. Sin embargo, múltiples factores orientan hacia una tendencia favorable respecto de la aplicación de terapia antiagregante intensificada frente a la monoterapia.
Los diferentes estudios comparativos de las 2 alternativas no han mostrado un claro efecto pernicioso de la DTA en términos de incremento de eventos adversos postoperatorios de tipo hemorrágico. Si bien en algunos estudios se aprecia un incremento en el débito postoperatorio o en el número de episodios de sangrado, estos no han presentado traducción en relevancia clínica (transfusión de hemoderivados, reoperación por sangrado, mortalidad). La agregación de casuística en metaanálisis26 refrenda asimismo los hallazgos de los estudios individuales.
La mayoría de los estudios incluidos, tanto si vierten un resultado favorable como no favorable a la DTA, presentan una potencia estadística limitada, fundamentalmente en relación con una inclusión de pacientes limitada. Asimismo, existe una marcada heterogeneidad de diseños, particularmente en el timing y la dosificación de AAS y clopidogrel, así como en la técnica quirúrgica (tipo de injertos, CDC con/sin CEC, extracción endoscópica o no de injertos). Este hecho no solo limita la obtención de conclusiones acerca del manejo clínico óptimo, sino que en cierta medida compromete la posibilidad de agregar los casos para incrementar la potencia estadística. No obstante, los metaanálisis26,27 incluidos son favorables a la DTA en términos de permeabilidad de injertos venosos y de protección frente a ECVM, advirtiéndose que en su diseño incluyen en ocasiones una mayoría de estudios que, analizados individualmente, fueron clasificados como no favorables a la DTA. A la vista de los múltiples factores que pueden influir en la permeabilidad de los injertos coronarios y en el curso clínico de los pacientes revascularizados quirúrgicamente1-8, probablemente sea necesaria mayor potencia estadística y diseños que permitan contrarrestar los múltiples factores de confusión para permitir aislar el verdadero papel de la DTA en el postoperatorio de DTA. Igualmente, todos los seguimientos realizados (≤ 1 año) son probablemente limitados para evaluar un fenómeno clínico con presentación más frecuentemente a medio-largo plazo8.
Aunque no ha sido un objetivo primario del análisis, numerosos estudios fundamentados en análisis bioquímicos y de agregometría advierten de las importantes tasas de resistencia a la terapia antiagregante, de base en la población y su incremento en contextos post-SCA y/o CDC. Independientemente de factores técnicos o anatómicos/hemodinámicos, la posibilidad de iniciar la terapia antiagregante precozmente tras la CDC junto a la terapia con estatinas constituyen los principales factores protectores de la permeabilidad de los injertos coronarios. Por ello, la desprotección que supone la resistencia a la terapia antiagregante puede ser un argumento de peso para apoyar la DTA como Mannacio et al.19.
Finalmente, aunque no ha sido contemplado en las guías clínicas de la ACC/AHA y de la EACTS/ESC, las guías de la CCS recomiendan el manejo clínico completo de los pacientes afectados por SCA con DTA, especialmente si son sometidos a CDC. Podrían ser definidos además otros nichos de tratamiento en relación con diferentes factores perioperatorios como el empleo extensivo de injertos de vena safena8,18, presencia de lechos distales a las anastomosis con enfermedad y/o calibre límite, resultados de flujometría y/o índices de pulsatilidad de los injertos en la medición intraoperatoria subóptimos, CDC sin CEC29 o presencia de trombocitosis reactiva postoperatoria25. Es por ello que consideramos, a la vista de la evidencia disponible, que la terapia antiagregante debe aún hoy ser individualizada según la práctica institucional como medida más eficiente y segura. La monitorización o la identificación de pacientes con resistencia a terapia antiagregante no está recomendada de forma sistemática y la aplicación individualizada de la terapia antiagregante podría comportar una falta de homogeneidad en el manejo terapéutico que comportase fallos en el ajuste terapéutico y un potencial incremento de los eventos adversos.
ConclusionesA la vista de la evidencia analizada, no puede apoyarse la aplicación sistemática de DTA en el postoperatorio de CDC. No obstante, la agregación de resultados en metaanálisis puede orientar favorablemente hacia la utilización de terapia antiagregante intensificada en el postoperatorio de CDC, pudiendo ser particularmente beneficiosa en el contexto post-SCA. Es necesaria mayor investigación con potencia estadística suficiente para determinar el papel de la DTA frente a la monoterapia con AAS en el postoperatorio de CDC, así como para determinar su prescripción óptima. En el momento actual, la individualización de la terapia antiagregante debe ser una práctica homogeneizada institucionalmente de acuerdo con el mejor balance riesgo/beneficio de cada práctica clínica particular.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.