La enfermedad de la válvula tricúspide (VT) y las consecuencias sobre la función ventricular derecha son determinantes en la morbilidad y mortalidad de gran número de pacientes con enfermedad cardiovascular. Sin embargo, ni los métodos diagnósticos ni las estrategias terapéuticas están tan desarrollados y validados como en las enfermedades del corazón izquierdo. Un motivo para esto es su menor prevalencia, que condiciona series con escaso número de pacientes, pocos estudios aleatorizados y resultados contradictorios. Por otro lado, es frecuente la insuficiencia tricuspídea (IT) «funcional» o «secundaria», consecuencia de una valvulopatía izquierda o de una miocardiopatía avanzada, en los que estos procesos primarios ocupan la mayor parte del esfuerzo diagnóstico y terapéutico. Tampoco la indicación quirúrgica de la IT está bien definida. Hay consenso en intervenir la IT grave durante la cirugía de valvulopatías izquierdas. Sin embargo, existe controversia cuando el grado de insuficiencia es menor o el anillo tricuspídeo está dilatado. La reparación valvular es la técnica de elección en la IT funcional. La implantación de un anillo tricuspídeo parece ofrecer los mejores resultados quirúrgicos. En la valvulopatía tricuspídea primaria la sustitución valvular con prótesis biológica o metálica es a menudo necesaria. Ésta se asocia a un alto riesgo quirúrgico, determinado por la alta tasa de reoperaciones y por la disfunción ventricular derecha. En esta revisión abordaremos los métodos ecocardiográficos para la evaluación de la VT, las indicaciones quirúrgicas de la valvulopatía tricuspídea y los resultados de las series publicadas más importantes.
Tricuspid valve disease and its impact on the right ventricular function determine the morbidity and mortality in many patients with cardiovascular disease. However, the diagnostic methods and therapeutic strategies are not so developed and validated as in the left heart disease. A reason for that is that its lesser prevalence determines series with low number of patients, few randomized studies and contradictory results. On the other hand, the “functional” or secondary tricuspid regurgitation (TR), consequence of a left valve disease or an advanced cardiomyopathy is a common finding. In these cases, the primary disease focuses the diagnostic and therapeutic effort. The indication of TR surgery is not well established. Consensus exists in the intervention during surgery for left heart disease if TR is severe. However, there is controversy when the TR is less than severe or the tricuspid annulus is dilated. Valve repair is of choice in functional TR. The tricuspid ring seems to offer the best surgical results. Valve replacement with biological or mechanical prostheses is often necessary in the primary tricuspid disease. It is a high risk surgery, determined by the high reoperations number and the right ventricular function. In this review we examine the echocardiographic methods for an appropriate tricuspid valve evaluation, the indications for tricuspid surgery and the results of the most important studies.
La ecocardiografía, en sus distintas modalidades (transtorácica [ETT], transesofágica [ETE] y tridimensional [E3D]), permite caracterizar de manera precisa la anatomía tricúspide y su disfunción, cuantificar el grado de afectación y distinguir entre enfermedad primaria o secundaria. Además, ofrece herramientas para la valoración del ventrículo derecho (VD) y para la estimación de la presión sistólica de arteria pulmonar (PSAP)1,2.
Valoración de la morfología valvularLa válvula tricúspide la constituyen tres valvas, el anillo tricuspídeo (AT), las cuerdas tendinosas, los músculos papilares y parte del miocardio de la aurícula derecha (AD) y VD. Tiene forma de paracaídas, con un anillo fibroso de forma elíptica muy dinámico, con capacidad de cambiar marcadamente según las condiciones hemodinámicas.
La valva anterior es la de mayor tamaño. Se extiende desde el infundíbulo hasta la pared inferolateral del VD. La valva septal se origina en el septo interventricular (apical a la inserción de la válvula mitral) y se extiende hasta la pared posterior del VD. La valva posterior discurre por el margen posterior del anillo desde el septo hasta la pared inferolateral.
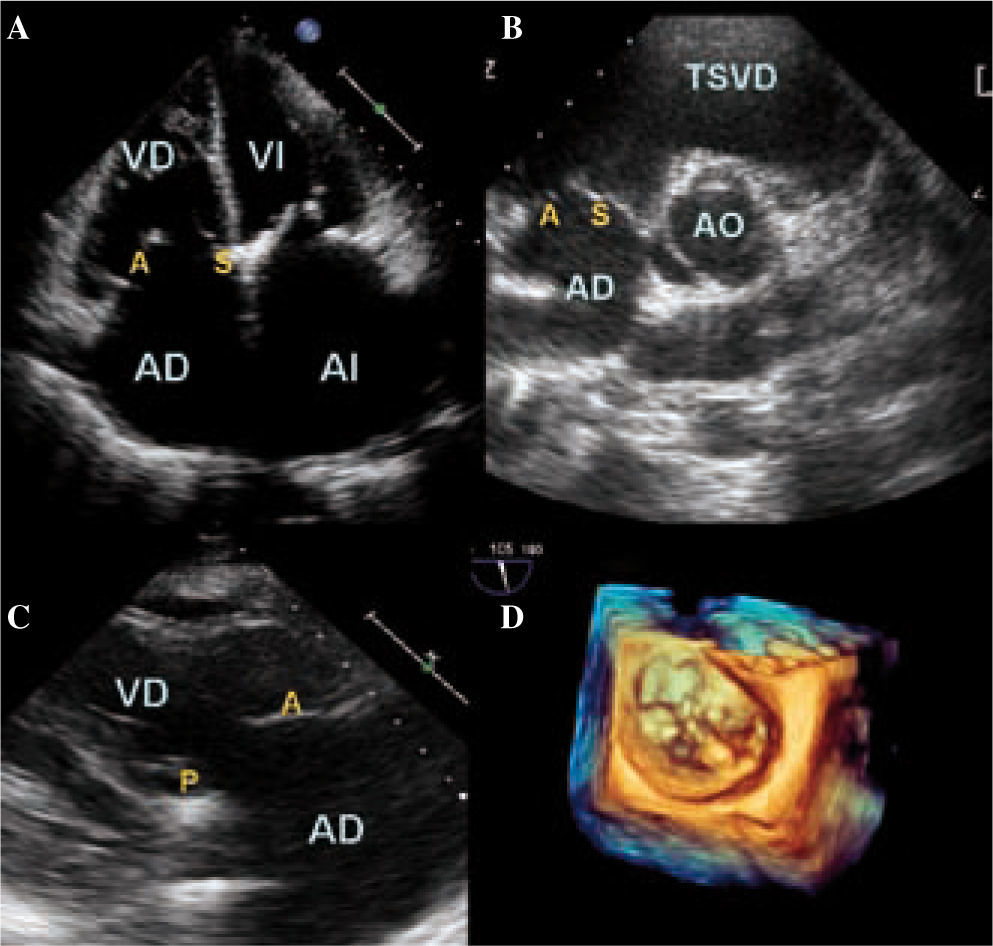
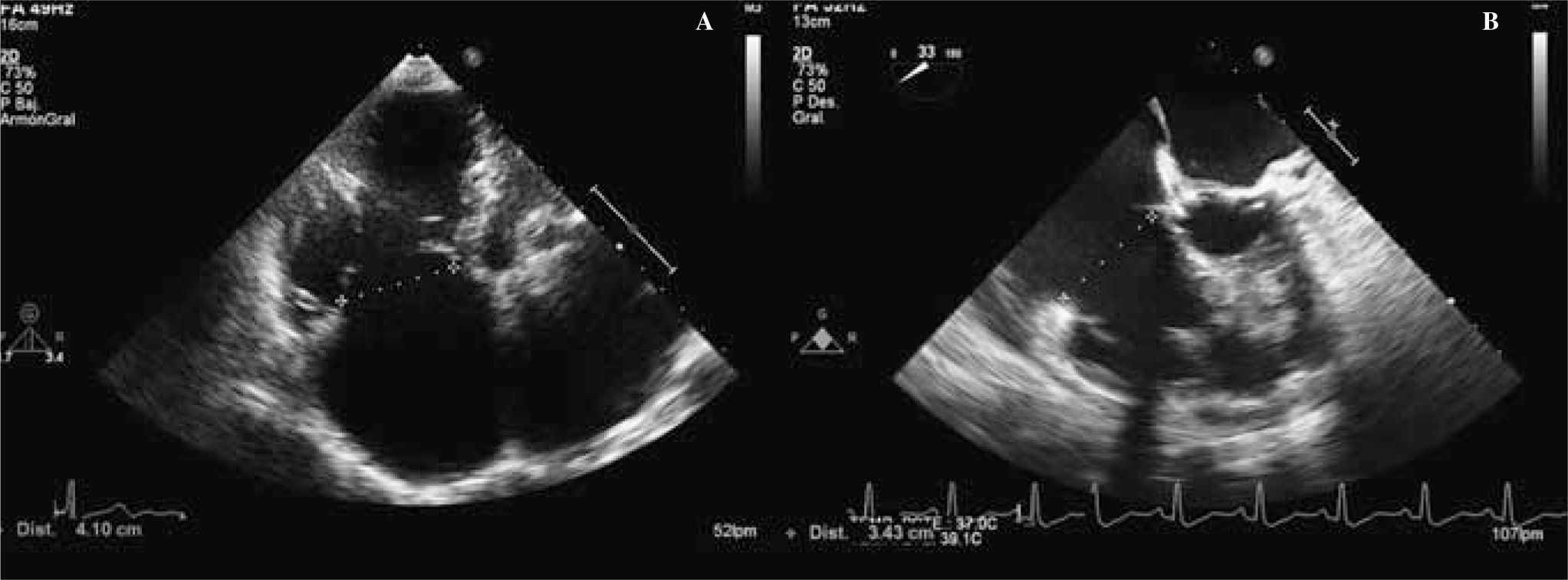
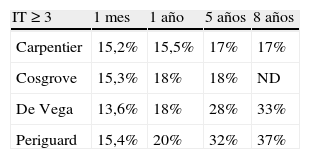
La ETT utiliza clásicamente tres planos para la evaluación de las valvas. Sólo el E3D permite valorar en un mismo plano las tres valvas y el AT (Fig. 1). Otro aspecto fundamental en la caracterización anatómica es la medición del AT. Esta medida se ha mostrado de gran utilidad a la hora de establecer la indicación quirúrgica en la IT funcional y planificar la intervención6. El AT posee una forma elíptica con la porción anteroseptal más alta y su porción posteroseptal más baja. Cuando éste se dilata adopta una forma circular y plana. La medición más aproximada en ETT se realiza en el plano de cuatro cámaras en telediástole (Fig. 2). Sin embargo, dada la forma oval del AT, esta medida suele estar infraestimada respecto a la E3D. El rango de la normalidad en adultos es de 28 ± 5mm. Se considera dilatado si el diámetro diastólico supera los 35mm o los 21mm/m2. La dilatación anular se ha correlacionado con el grado de insuficiencia valvular.
Planos ecocardiográficos para la valoración de la válvula tricúspide. a: apical cuatro cámaras. B: paraesternal eje corto a nivel de la aorta. C: paraesternal eje largo derecho. D: plano valvular en 3D. VD: ventrículo derecho; AD: aurícula derecha; VI: ventrículo izquierdo; AI: aurícula izquierda; TSVD: tracto de salida de ventrículo derecho; AO: aorta; A: valva anterior; S: valva septal; P: valva posterior.
Los músculos papilares (anterior, posterior y septal) son variables en tamaño. El anterior y el septal son los mayores, mientras que el posterior es el más pequeño o incluso está ausente. De cada valva emergen cuerdas tendinosas hacia uno o varios músculos papilares. El músculo papilar anterior provee cuerdas a las valvas anterior y posterior, el posterior a las valvas posterior y septal, y el septal a la anterior y septal. Además, pueden existir cuerdas tendinosas accesorias hacia la pared libre del VD o hacia la banda moderadora.
La evaluación anatómica es especialmente importante para distinguir entre la enfermedad tricuspídea primaria u orgánica, en la que la VT es anormal (25% de los casos) y la enfermedad tricuspídea secundaria (75% de los casos), en la que la válvula no está afectada y la insuficiencia valvular es consecuencia de miocardiopatías o valvulopatías izquierdas avanzadas, dilatación o afectación primaria de VD por afectación miocárdica (displasia, infarto…), o hipertensión pulmonar de cualquier origen (Tabla I). En la mayoría de estos casos el proceso primario condiciona un aumento de la PSAP, que conduce a la dilatación de las cavidades derechas y del AT, lo que deriva finalmente en una IT de distinta gravedad.
Etiología de la valvulopatía tricuspídea
| Causas primarias (25%) |
| - Enfermedad reumática |
| - Degenerativa |
| - Congénita |
| • Cleft valvular |
| • Enfermedad de Ebstein |
| • Estenosis tricuspídea congénita |
| • Atresia tricúspide |
| - Endocarditis |
| - Síndrome carcinoide |
| - Toxina: fenfluramina-fentermina, metisergida |
| - Tumores |
| - Yatrogénica: electrodo marcapasos, biopsia |
| - Traumática |
| Causas secundarias (75%) |
| - Valvulopatía o miocardiopatía izquierda |
| - HTP de cualquier origen |
| - Disfunción VD (isquemia, miocardiopatía) |
| - Dilatación VD |
HTP: hipertensión pulmonar
La estenosis tricuspídea es una entidad menos frecuente que se asocia a enfermedad orgánica de la válvula (generalmente reumática) y suele estar asociada a la presencia de IT.
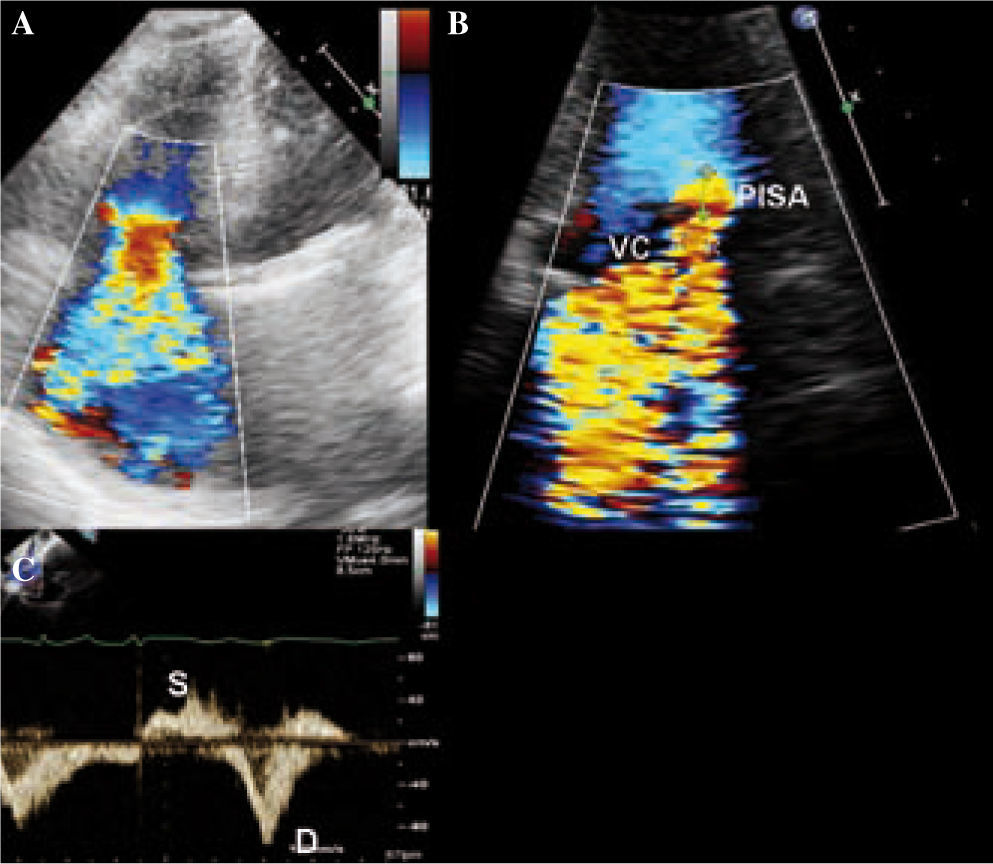
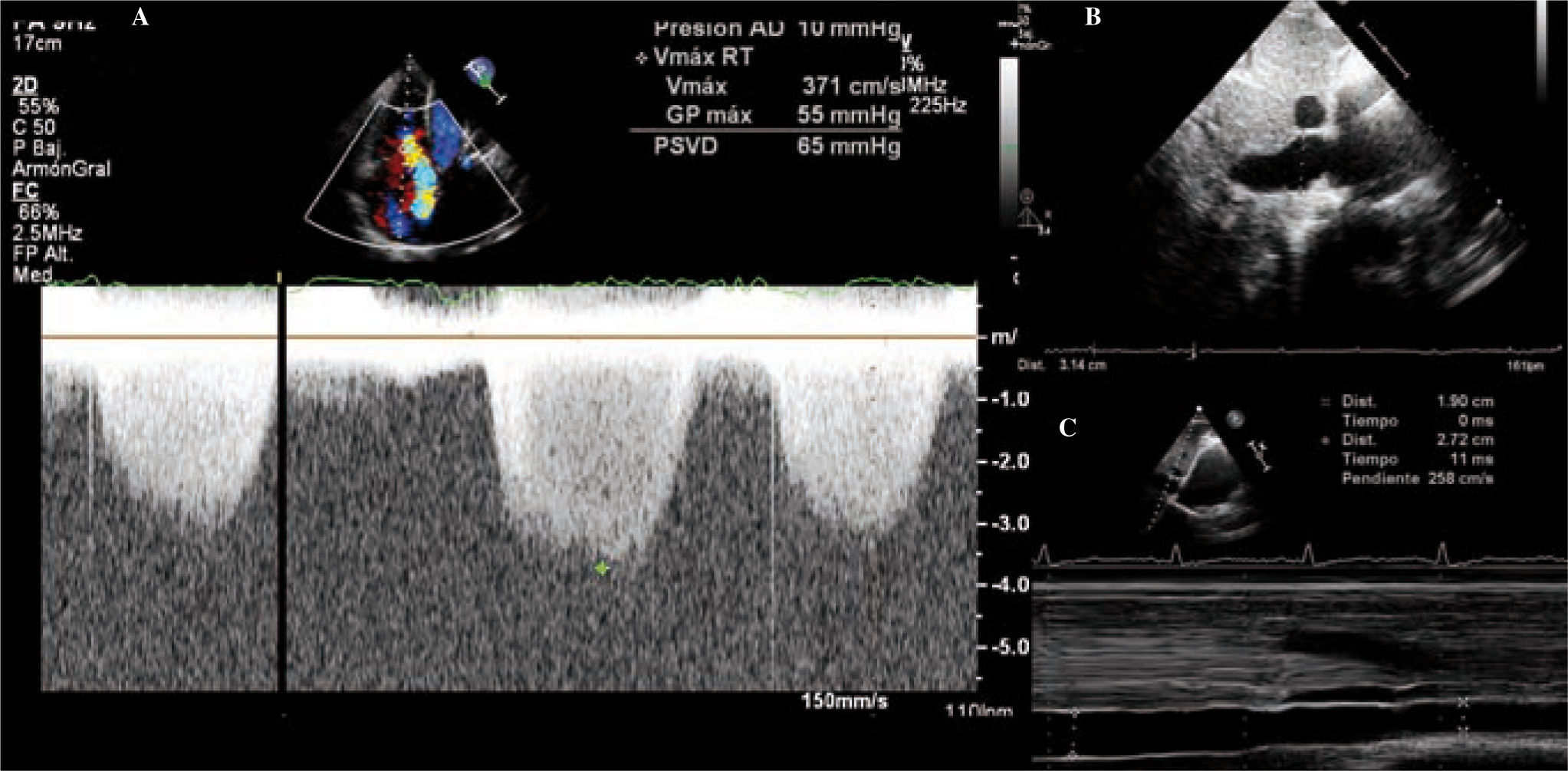
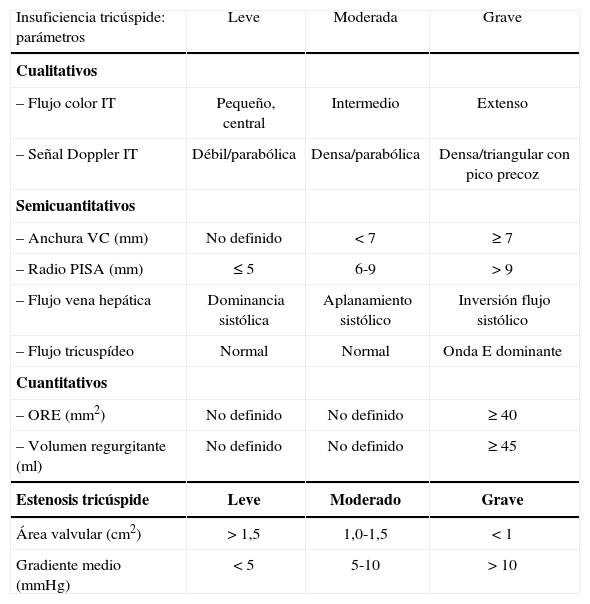
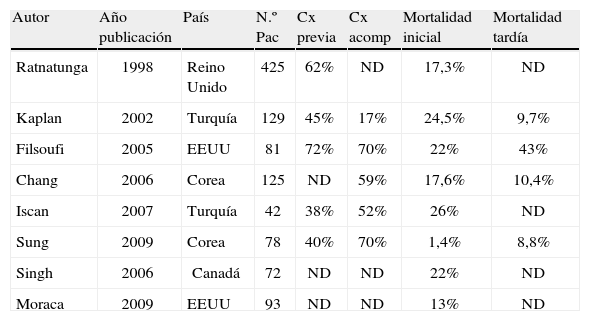
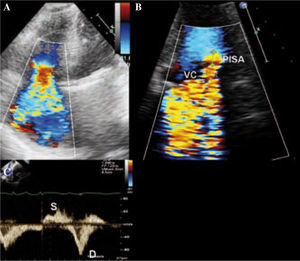
Cuantificaón de la valvulopatía tricuspideaLa caracterización de la IT en leve, moderada o grave depende de la valoración de varios parámetros ecocardiográficos (Tabla II). Aunque el flujo color es útil para establecer la presencia de IT, tiene importantes limitaciones a la hora de valorar la gravedad de ésta. Por lo tanto, para una estimación más exacta se deben utilizar medidas semicuantitativas como la anchura de la vena contracta, y cuantitativas como el orificio regurgitante efectivo. Ambas se realizan en el plano apical de cuatro cámaras o en el paraesternal eje largo (Fig. 3).
Valoración ecocarafigráfica de la severidad de la valvulopatía tricúspide
| Insuficiencia tricúspide: parámetros | Leve | Moderada | Grave |
| Cualitativos | |||
| – Flujo color IT | Pequeño, central | Intermedio | Extenso |
| – Señal Doppler IT | Débil/parabólica | Densa/parabólica | Densa/triangular con pico precoz |
| Semicuantitativos | |||
| – Anchura VC (mm) | No definido | < 7 | ≥ 7 |
| – Radio PISA (mm) | ≤ 5 | 6-9 | > 9 |
| – Flujo vena hepática | Dominancia sistólica | Aplanamiento sistólico | Inversión flujo sistólico |
| – Flujo tricuspídeo | Normal | Normal | Onda E dominante |
| Cuantitativos | |||
| – ORE (mm2) | No definido | No definido | ≥ 40 |
| – Volumen regurgitante (ml) | No definido | No definido | ≥ 45 |
| Estenosis tricúspide | Leve | Moderado | Grave |
| Área valvular (cm2) | > 1,5 | 1,0-1,5 | < 1 |
| Gradiente medio (mmHg) | < 5 | 5-10 | > 10 |
VC: vena contracta; PISA: área de isovelocidad proximal; ORE: orificio de regurgitación efectivo (modificado de Rudsky, et al.)1
La vena contracta es la parte más estrecha del flujo regurgitante inmediatamente distal al orificio de regurgitación. Un diámetro igual o superior a 7mm orienta a IT grave.
El orificio regurgitante efectivo (ORE) se obtiene a través de la fórmula: ORE = 2πr2V/VPF, donde V es la velocidad del límite Nyquist, la velocidad de permeabilidad vascular (VPF) es la velocidad pico de la IT, y «r» es el radio de la hemiesfera proximal al plano tricuspídeo (área de velocidad isoproximal [PISA]) (Fig. 3). El Doppler color basal debe desplazarse en la dirección de la regurgitación para obtener una velocidad aproximada de 30 cm/s. Este método se basa en el análisis de la convergencia del flujo proximal al orificio de la regurgitación. Cuanto mayor es la insuficiencia, la convergencia del flujo proximal y, por lo tanto, el PISA y el ORE serán mayores. Aunque menos validado que en la insuficiencia mitral y con limitaciones, un ORE superior a 40mm2 o un radio PISA mayor de 9mm indican IT grave.
El grado de dilatación de la vena cava inferior y el flujo de la vena hepática son otras herramientas indirectas para la cuantificación de la IT. La presencia de flujo sistólico reverso por Doppler pulsado orienta a IT grave (Fig. 3), así como la dilatación de la vena cava inferior que no colapsa con la inspiración.
La estenosis tricuspídea suele asociarse a IT. Por ecocardiografía se detecta inicialmente por la afectación de la morfología valvular y por el Doppler color, que muestra un núcleo central de chorro de alta velocidad. La estimación de la gravedad se realiza con el registro del flujo tricuspídeo por Doppler continuo en el plano de cuatro cámaras, mediante la medición del gradiente medio y el área obtenida a través del tiempo de hemipresión (Tabla II). Es importante evitar el cálculo con frecuencias cardíacas altas y utilizar un promedio de cinco o más latidos en caso de fibrilación auricular.
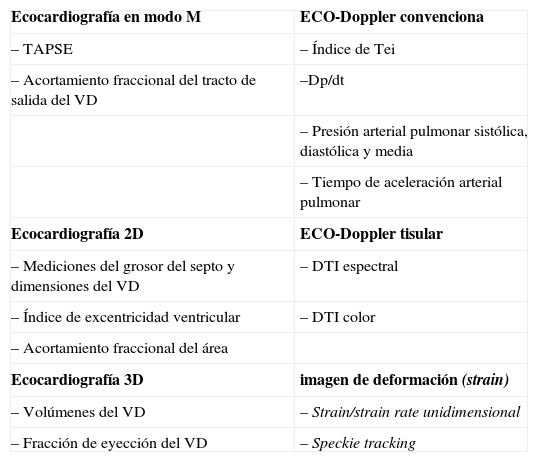
Valoración del ventrículo derecho y de la presión sistólica arteria pulmonarLa disfunción ventricular derecha desempeña un importante papel en la morbilidad y mortalidad cardiovascular. Sin embargo, en la práctica diaria no es común su evaluación ecocardiográfica sistemática. Esto se debe a varias causas. Por un lado, su forma anatómica, más compleja, hace difícil la determinación de sus volúmenes y de la fracción de eyección. Por otro lado, los métodos ecocardiográficos descritos no están tan validados como los utilizados en el corazón izquierdo. Esto hace que los datos disponibles no sean suficientes para clasificar las categorías de disfunción en leve, moderado y grave. Existen varios métodos ecocardiográficos que han demostrado utilidad en el estudio del VD (Tabla III).
Métodos ecocardiográficos para la valoración del ventriculo derecho
| Ecocardiografía en modo M | ECO-Doppler convenciona |
| – TAPSE | – Índice de Tei |
| – Acortamiento fraccional del tracto de salida del VD | –Dp/dt |
| – Presión arterial pulmonar sistólica, diastólica y media | |
| – Tiempo de aceleración arterial pulmonar | |
| Ecocardiografía 2D | ECO-Doppler tisular |
| – Mediciones del grosor del septo y dimensiones del VD | – DTI espectral |
| – Índice de excentricidad ventricular | – DTI color |
| – Acortamiento fraccional del área | |
| Ecocardiografía 3D | imagen de deformación (strain) |
| – Volúmenes del VD | – Strain/strain rate unidimensional |
| – Fracción de eyección del VD | – Speckie tracking |
La Sociedad Europea de Ecocardiografía2 recomienda el uso de múltiples ventanas ecocardiográficas para la correcta valoración del VD. Esta valoración debe incluir: la medición del VD y la AD, la estimación de la PSAP y la determinación de la función sistólica del VD mediante al menos una de las siguientes medidas: el acortamiento fraccional del área, la velocidad del anillo lateral tricuspídeo por Doppler tisular («S») o la medición de la excursión sistólica del anillo tricuspídeo (TAPSE) en modo M. El cálculo del índice de función miocárdica (TEI) es opcional.
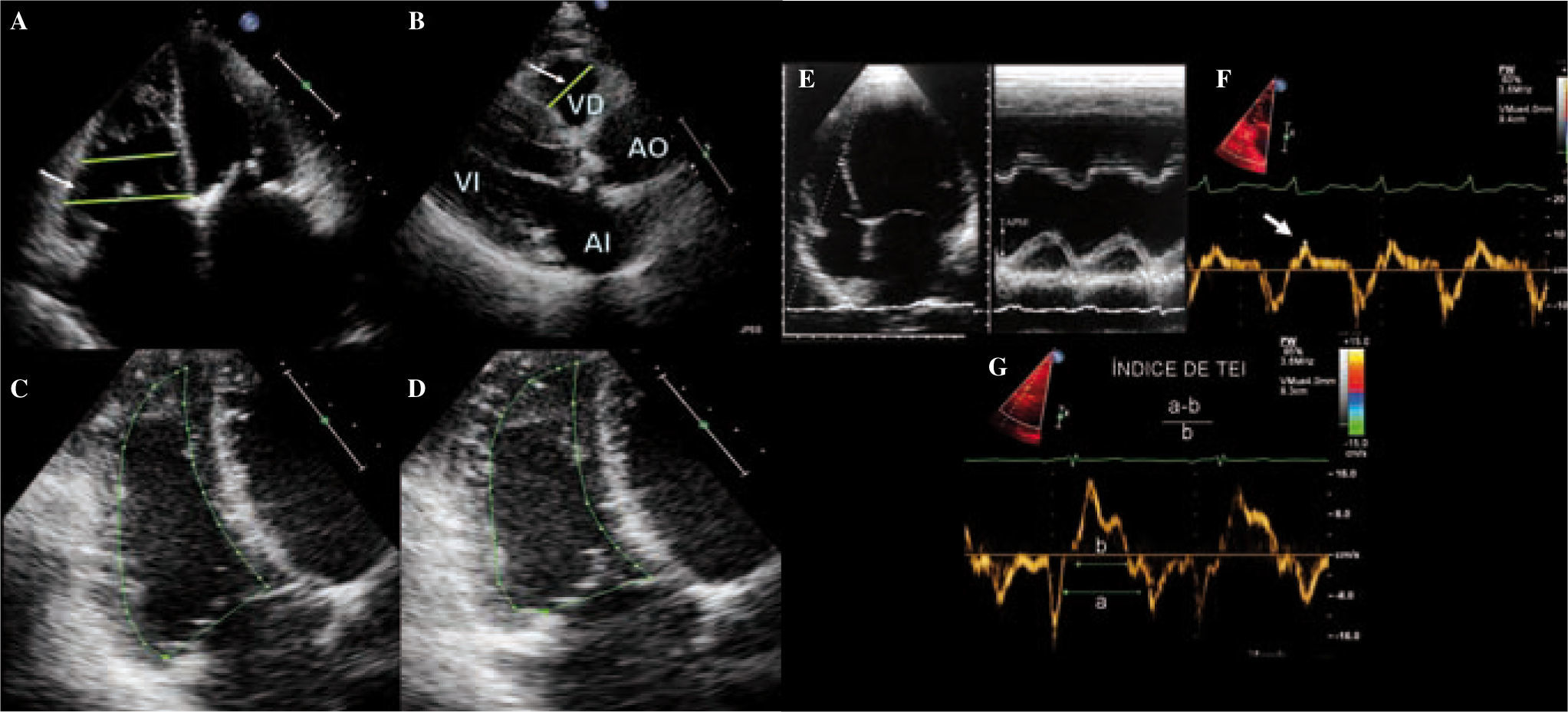
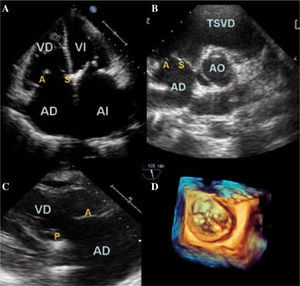
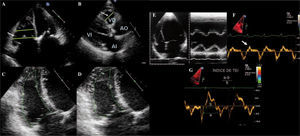
Medición del ventrículo derechoLa dilatación del VD y del AT pueden ser el origen de la IT o bien el resultado de una valvulopatía tricuspídea primaria grave. La medición del VD se realiza en telediástole en el plano apical de cuatro cámaras (Fig. 4). Es importante evitar la rotación del transductor y obtener un buen plano, con el fin de no sobrestimar o infraestimar la medida. El VD está dilatado si su diámetro es mayor de 42mm en la base, 35mm en su parte media, o su dimensión longitudinal es mayor de 86mm. El tracto de salida de VD puede medirse en el paraesternal eje largo o eje corto a nivel del anillo pulmonar (más reproducible). Es patológico un diámetro mayor de 27mm en el eje largo o 33mm en el eje corto.
Valoración del VD (véase texto). A: diámetro del VD en el plano de cuatro cámaras a nivel basal y medio (flechas); B: diámetro del TSVD en el paraesternal eje largo (flecha); C y D: cálculo acortamiento fraccional del área a través de la estimación del área del VD en sístole y diástole; E: medición del TAPSE; F: velocidad de la onda sistólica del VD por Doppler tisular (flecha); G: cálculo del índice de TEI por Doppler tisular.
Los métodos descritos anteriormente son los más validados para el estudio del VD en ETT. Sin embargo, la fracción de eyección por E3D parece ser la medida más fiable y con menos errores de reproducción, aunque todavía son necesarios estudios con mayor número de pacientes. Indican disfunción ventricular derecha un acortamiento fraccional del área inferior a 35%, un TAPSE inferior a 16mm, un índice de TEI superior a 0,55 por Doppler tisular o superior a 0,40 por Doppler continuo o una velocidad de S’ inferior a 10.
Acortamiento fraccional del áreaEl acortamiento fraccional del área (AFA) viene determinado por la fórmula: [(área telediastólica del VD- área telesistólica del VD)/área telediastólica del VD] × 100. Su cálculo se realiza en el plano apical de cuatro cámaras, con la estimación del área del VD mediante el trazado del borde endocárdico del VD en sístole y diástole. Es importante la inclusión de todo el VD, con visualización del ápex y de la pared lateral, así como la exclusión de las trabeculaciones (Fig. 4). La determinación de la fracción de eyección no está recomendada dada la complejidad anatómica del VD y la heterogeneidad de los métodos descritos.
Excursión sistólica del anillo tricuspídeoEl TAPSE es una medida fácil y reproducible que se correlaciona con la función del VD. Corresponde a la distancia medida en modo M de la excursión sistólica de la base de la pared libre del VD en el plano apical de cuatro cámaras (Fig. 4). A mayor distancia, mejor función del VD. Su principal limitación es asumir que el desplazamiento de un solo segmento representa la función de todo el VD, por lo que no es útil cuando existen alteraciones segmentarias de la contractilidad.
Velocidad del anillo lateral tricuspídeo por Doppler tisular («S»)Esta medida se realiza en el plano apical de cuatro cámaras mediante Doppler tisular (Fig. 4), con la estimación de la velocidad sistólica a nivel lateral del AT o en la parte media de la pared libre del VD. Una S’ inferior a 10 cm/s orienta a disfunción ventricular derecha. Al igual que el TAPSE, es fácilmente reproducible pero carece de utilidad cuando el VD no se contrae de manera homogénea.
Índice de función miocárdicaEste índice estima la función sistólica y diastólica del VD. Se basa en la relación entre la contracción y la relajación del VD, mediante la fórmula: (tiempo de cierre de la VT - tiempo de eyección)/tiempo de eyección (Fig. 4). El tiempo de cierre de la VT incluye el tiempo de contracción isovolumétrica, el tiempo de eyección y el tiempo de relajación isovolumétrica del VD. Estos parámetros pueden obtenerse mediante Doppler tisular a nivel del anillo tricuspídeo o mediante Doppler continuo estimando la duración de la regurgitación a nivel del flujo tricuspídeo y el tiempo de eyección del VD a nivel de la válvula pulmonar. Una importante limitación es la variabilidad ante la presencia de frecuencias irregulares. Este método no debe utilizarse como única medida para la evaluación del VD.
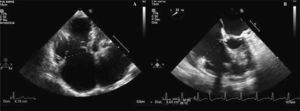
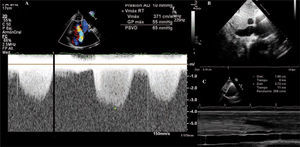
Estimación de la presión sistólica de arteria pulmonarLa presión sistólica del VD (PSVD) se estima mediante la ecuación simplificada de Bernoulli a partir de la velocidad de la IT por Doppler continuo (V) y la presión estimada de la AD: PSVD: 4(V)2 + presión AD. En ausencia de obstrucción al tracto de salida del VD, este valor coincide con la PSAP. La presión de la AD se estima según el grado de dilatación de la vena cava inferior (VCI) y su colapso durante la inspiración. La VCI debe medirse en el plano subcostal al final de la espiración, inmediatamente proximal a la entrada de las venas suprahepáticas (Fig. 5). Si la VCI está dilatada (> 21mm) y colapsa menos del 50% durante la inspiración se suman 15mmHg (rango: 10-20mmHg). Si está dilatada pero colapsa más del 50%, o no está dilatada pero no se produce este colapso, se añaden 8mmHg (rango: 5-10mmHg). Por último, si no está dilatada y colapsa adecuadamente se suman 3mmHg (rango: 0-5mmHg). Una velocidad de la IT superior a 2,8-2,9 m/s, que corresponde a una PSAP aproximada de 36mmHg asumiendo una presión arterial diastólica (PAD) de 3-5mmHg, indica un aumento de la presión de la arteria pulmonar.
Resultados e indicaciones de la cirugía de la válvula tricúspideLa presencia de IT significativa se asocia a una alta morbimortalidad en un gran número de pacientes. La indicación quirúrgica de la IT viene determinada por una serie de cuestiones. Esta intervención:
- –
¿Mejora los síntomas y la supervivencia de los pacientes?
- –
¿Cuándo está indicada?
- –
¿Qué factores predicen el desarrollo de IT posquirúrgica tras la cirugía mitral?
- –
¿Qué tipo de técnica quirúrgica ofrece mejores resultados, reparación, reemplazo o anillo valvular?
Hasta en el 25-30% de los pacientes que se someten a cirugía de la válvula mitral existe también una IT «funcional» al menos moderada. Históricamente, la reparación valvular concomitante de la VT no ha sido una práctica común por la creencia de que la IT revertía tras la cirugía mitral. Sin embargo, dado que la dilatación anular y la alteración geométrica del VD no son procesos reversibles, hasta en el 14-25% de los pacientes la IT no desaparece. La IT no corregida se asocia además a peor supervivencia y clase funcional.
Por otro lado, estas alteraciones anatómicas evolucionan con el tiempo, incluso años después de la cirugía mitral. La progresión de la IT es variable e impredecible, y oscila entre el 17-74%. En la serie de 124 pacientes de Matsunaga, et al.3 que se sometieron a cirugía mitral, la prevalencia de IT moderada se incrementó de un 25% el primer año, a un 53% entre el primer y el tercer año, y un 74% a partir del tercer año.
Song, et al.4 analizaron en su serie los factores asociados al desarrollo de IT tardía cuando el grado de IT inicial era igual o inferior a 2. De los 638 pacientes que se sometieron a cirugía aórtica o mitral, casi el 10% (7,7%) desarrolló IT tardía significativa, lo que condicionó una disminución significativa de la supervivencia libre de eventos a los 8 años (76 vs 91%; p < 0,001). Los factores asociados a la progresión de la IT fueron la etiología reumática, la presencia de fibrilación auricular, la hipertensión pulmonar, la edad avanzada y el sexo femenino. Sin embargo, a diferencia de lo publicado por el grupo de Dreyfus, la dilatación anular no se relacionó con el desarrollo de IT tardía.
Por otro lado, Chan, et al.5 describen una serie de 624 pacientes intervenidos de sustitución valvular mitral desde 1990-2005. De los 231 que tenían IT moderada-grave, en 125 se realizó reparación tricuspídea y 106 se dejaron evolucionar de manera natural. Se demostró que una IT preoperatoria superior a 2 se traducía en un incremento de la mortalidad tardía del 53%. Aunque no se produjeron diferencias significativas en la supervivencia, la reparación valvular mejoró los síntomas de insuficiencia cardíaca y disminuyó la progresión de la IT (8 vs 17%; p < 0,05). En este trabajo, el tamaño del anillo tampoco predijo la progresión de la IT en ausencia de IT grave (p > 0,5).
La dilatación anular sin IT significativa ha sido evaluada en otros estudios con resultados opuestos. Dreyfus, et al.6 analizaron 311 pacientes en los que se realizó reparación valvular mitral, tenían IT inferior a 2 y el AT dilatado (> 70mm intraoperatorio, equivalente a 40mm por ecocardiografía). De éstos, a 163 pacientes sólo se les realizó reparación valvular mitral (RVM) y al resto (148) se les implantó además un anillo tricuspídeo. Aunque tampoco se encontraron diferencias en la mortalidad (1,8 vs 0,7%), en el grupo de pacientes del anillo tricuspídeo mejoró significativamente la clase funcional y la falta de progresión de la IT (2 vs 48%; p < 0,001) tras un seguimiento medio de 5 años.
Por lo tanto, la cirugía de la IT funcional está encaminada fundamentalmente al alivio de los síntomas de insuficiencia cardíaca. Existe cierto acuerdo en intervenir la IT durante la cirugía mitral o aórtica cuando ésta es grave. La evidencia es menor en el caso de IT no grave o dilatación anular sin IT significativa. Ciertos factores que predicen el desarrollo de IT tardía pueden apoyar la cirugía en casos determinados. Las últimas recomendaciones de la Sociedad Europea7 y Americana8 de Cardiología se exponen en las tablas IV y V.
Guías europeas del 2007 sobre el manejo de la enfermedad valvular cardiaca. indicación quirúrgica de la valvulopatía tricuspídea
| Clase IC | – IC o ET.a grave en pacientes que se someten a cirugía valvular izquierda |
| – IT grave primaria sintomática a pesar de tratamiento médico en ausencia de disfunción VD grave | |
| – Estenosis tricuspídea severa (± IT) sintomática a pesar de tratamiento médico | |
| Clase IIaC | – IT moderada orgánica en pacientes que se somenten a cirugía valvular izquierda |
| – IT moderada secundaria en pacientes con dilatación del anillo tricuspídeo (> 40mm) que se someten a cirugía valvular izquierda | |
| – IT grave sintomática tras cirugía valvular izquierda, en ausencia de enfermedad valvular izquierda, disfunción del VD o HTP grave (> 60mmHg) | |
| Clase IIbC | – IT grave aislada asintomática o levemente sintomática y dilatación o disfunción del VD |
HTP: hipertensión pulmonar; IT: insuficiencia tricuspídea; VD: ventrículo derecho; a: la intervención percutánea puede ser la primera opción en la ET aislada (modificado de Vahanian et al.)7
Update del 2008 de las guías de la acc/aha del 2006 sobre el manejo de pacientes con enfermedad valvular cardiaca. indicación quirúrgica de la valvulopatía tricuspídea
| Clase IB | – La reparación valvular es beneficiosa en la IT grave en pacientes que se someten a cirugía valvular izquierda |
| Clase IIaC | – El reemplazo valvular o la anuloplastia es razonable en la IT primaria grave sintomática |
| – El reemplazo valvular es razonable en la IT grave orgánica no susceptible de reparación o anulopastia | |
| Clase IIbC | – La anuloplastia puede considerarse en la IT no grave en pacientes que se someten a cirugía valvular mitral cuando existe HTP o dilatación anular |
| Clase IIIC | – El reemplazo valvular o la anuloplastia no están indicadas en pacientes asintomáticos con IT sin HTP en presencia de una válvula mitral normal |
| – El reemplazo valvular o la anuloplastia no están indicadas en pacientes con IT primaria leve |
HTP: hipertensión pulmonar; IT: insuficiencia tricuspídea (modificado de Bonow, et al.)8.
En ambas está recomendada como clase I (evidencia C y B) la reparación valvular de la IT grave funcional en pacientes que se someten a cirugía valvular izquierda. Las guías Europeas apoyan también la reparación de la VT en pacientes que se someten a cirugía valvular izquierda y presentan IT moderada y dilatación del AT (IIa). También está recomendada la intervención quirúrgica (clase I y IIa, respectivamente) en caso de IT orgánica sintomática a pesar de tratamiento médico y en ausencia de disfunción VD o hipertension pulmonar (HTP).
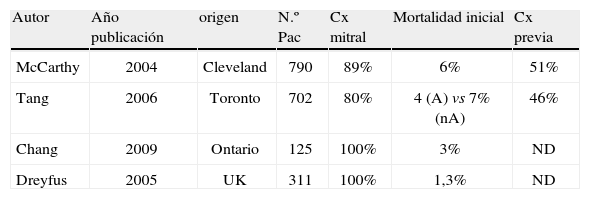
¿Cómo?Varios trabajos han evaluado las distintas técnicas de reparación en la IT funcional (Tabla VI). Al contrario que en el caso del reemplazo valvular, y a pesar del gran número de reoperaciones y de cirugía valvular mitral asociada, la mortalidad inicial comunicada no supera el 6-7%4–6,9.
Resultados de la reparación valvular tricuspídea en la it funcional
| Autor | Año publicación | origen | N.º Pac | Cx mitral | Mortalidad inicial | Cx previa |
| McCarthy | 2004 | Cleveland | 790 | 89% | 6% | 51% |
| Tang | 2006 | Toronto | 702 | 80% | 4 (A) vs 7% (nA) | 46% |
| Chang | 2009 | Ontario | 125 | 100% | 3% | ND |
| Dreyfus | 2005 | UK | 311 | 100% | 1,3% | ND |
A: anillo tricúspide, nA: no anillo
Las técnicas clásicas de reparación son las técnicas de sutura (fundamentalmente la reparación en bolsa de tabaco de De Vega y la plicatura con sutura de la valva posterior) y las técnicas de anuloplastia (anuloplastia de Periguard, anuloplastia de borde a borde, anillo semirrígido de Carpentier, anillo flexible de Duran y las bandas o anillos incompletos). De éstas, el anillo tricuspídeo ha demostrado en varios trabajos menor progresión de la IT y mejor supervivencia global y libre de eventos.
McCarthy, et al.9 analizaron en su serie las distintas técnicas de reparación y los factores implicados en su fracaso. En los 790 pacientes las técnicas quirúrgicas empleadas fueron: el anillo semirrígido de Carpentier-Edwards, la banda flexible de Cosgrove-Edwards, la plastia de De Vega y la anuloplastia de Periguard. Al mes de la cirugía, 14% de los pacientes tenían una IT igual o superior a 3. Sin embargo, mientras la IT se mantenía estable en el tiempo con las dos primeras técnicas, ésta se incrementaba cuando la técnica utilizada era la plastia de De Vega o la anuloplastia de Periguard (Tabla VII). Los factores relacionados con el desarrollo de IT tardía fueron el grado de IT preoperatoria, la fracción de eyección, la presencia de cable de marcapasos y la reparación distinta a la implantación de un anillo.
Por otro lado, Tang, et al.10 compararon los resultados de 702 pacientes con IT funcional. En 209 se implantó un anillo tricuspídeo y en 493 se realizó la técnica de De Vega. La implantación del anillo fue un predictor independiente de la supervivencia a largo plazo (hazard ratio [HR]: 0,7; intervalo de confianza [IC]: 0,5-1,0; p = 0,03) y la supervivencia libre de eventos (HR: 0,8; IC: 0,6-1,0; p = 0,04).
Por lo tanto, la reparación valvular es una técnica con baja mortalidad inicial. Sin embargo, la progresión de la IT es frecuente. La implantación de un anillo tricuspídeo parece ofrecer mejores resultados a medio y largo plazo.
Aunque la reparación es la técnica de elección, la sustitución valvular es a menudo necesaria cuando existe una afectación orgánica de las valvas. La cirugía aislada de la VT está asociada a una alta mortalidad inicial (de hasta el 37%), baja supervivencia a largo plazo y ausencia de mejoría clínica significativa en muchos pacientes (Tabla VIII)11–18. Los resultados tienden a ser mejores cuando no existe disfunción ventricular derecha en el momento de la cirugía. Algunos trabajos han comparado la reparación y la sustitución en la IT orgánica con resultados variables:
Resultados del reemplazo valvular tricuspídeo en la valvulopatía tricuspídea
| Autor | Año publicación | País | N.º Pac | Cx previa | Cx acomp | Mortalidad inicial | Mortalidad tardía |
| Ratnatunga | 1998 | Reino Unido | 425 | 62% | ND | 17,3% | ND |
| Kaplan | 2002 | Turquía | 129 | 45% | 17% | 24,5% | 9,7% |
| Filsoufi | 2005 | EEUU | 81 | 72% | 70% | 22% | 43% |
| Chang | 2006 | Corea | 125 | ND | 59% | 17,6% | 10,4% |
| Iscan | 2007 | Turquía | 42 | 38% | 52% | 26% | ND |
| Sung | 2009 | Corea | 78 | 40% | 70% | 1,4% | 8,8% |
| Singh | 2006 | Canadá | 72 | ND | ND | 22% | ND |
| Moraca | 2009 | EEUU | 93 | ND | ND | 13% | ND |
Adaptado11-18
Singh, et al.17 objetivaron que la sustitución valvular era un predictor independiente de la mortalidad a medio plazo (HR: 5,1; IC: 2,9-9,1; p < 0,001). Aunque la progresión de la IT fue mayor con la reparación valvular (38 vs 5%; p < 0,001), esto no se tradujo en la clase funcional o en la tasa de reoperación. Por el contrario, Moraca, et al.18 no encontraron diferencias en la mortalidad inicial o en la supervivencia a medio o largo plazo entre ambas técnicas.
A la hora de seleccionar el tipo de prótesis es preciso valorar los riesgos y beneficios asociados a cada grupo. El metaanálisis de Rizzoli, et al.19, que incluyó 1.160 prótesis, comparó ambos tipos. No se evidenciaron diferencias significativas en la supervivencia o en la tasa de reoperación, aunque sí se objetivó una tendencia a mayor trombosis de la prótesis metálica, y una tendencia a mayor reoperación en el caso de la prótesis biológica. Por lo tanto, es recomendable individualizar la decisión según las características del paciente.
ConclusionesLa valvulopatía tricuspídea grave es responsable de una importante morbilidad y disminución de la supervivencia en gran número de pacientes. La progresión de la IT «funcional» tras la cirugía mitral es frecuente e impredecible, incluso años después de ésta. Las técnicas de reparación valvular tricuspídea durante la cirugía mitral, especialmente el anillo tricuspídeo, han demostrado buenos resultados, sin incrementar de manera significativa el tiempo quirúrgico ni la morbimortalidad inicial. Sin embargo, la mortalidad descrita en la reoperación aislada de la VT es muy elevada.
Todo ello hace razonable valorar la reparación tricus-pídea cuando la IT no es grave, pero existen factores que parecen contribuir al desarrollo de IT tardía, como la dilatación del anillo tricuspídeo, la HTP, la fibrilación auricular o la etiología reumática.
La sustitución valvular tricuspídea, ya sea con prótesis mecánica o biológica, presenta una alta mortalidad inicial y baja supervivencia a largo plazo. Un motivo para ello es la avanzada clase funcional y la pobre función del VD en el momento de indicar la intervención. Aunque no hay recomendaciones establecidas acerca del momento idóneo para la sustitución valvular en los pacientes con IT grave, parece muy importante el seguimiento de la función ventricular derecha de éstos para evitar que el deterioro del VD aumente el riesgo quirúrgico o contraindique la cirugía. El continuo desarrollo de la ecocardiografía y de la resonancia magnética contribuirán a este fin.