En este capítulo, se realizará una revisión general sobre esta cardiopatía compleja, incidiendo en las sucesivas etapas de manejo con diferentes técnicas quirúrgicas y la difícil toma de decisiones hacia una vía uni o biventricular.
A systematic review will be done in this chapter about general aspects in this complex defect, discussing the initial and subsequent management, surgical techniques, and the difficult decision making towards a uni or biventricular endpoint.
La atresia pulmonar (estenosis pulmonar crítica) con septo íntegro es una cardiopatía rara. El rango de presentación es variable, en función del grado de hipoplasia de las estructuras derechas.
De manera genérica, no existe (o de forma escasa) paso anterógrado de sangre del ventrículo derecho a la arteria pulmonar, creando una presión suprasistémica. La sangre desaturada pasa de la aurícula derecha a la izquierda a través de una CIA, generando cianosis. Por otro lado, el flujo a las ramas pulmonares proviene desde el ductus. Encontramos, pues, un cortocircuito derecha-izquierda (CIA) junto con otro cortocircuito izquierda-derecha (ductus).
Anatómicamente, la válvula pulmonar es estenótica o displásica (estando sustituida en algunos casos por una membrana fibrosa imperforada) y el ventrículo derecho está reducido de tamaño. Se asocia una estenosis infundibular (secundaria a la hipertrofia concéntrica del ventrículo derecho, responsable junto a la válvula de la poscarga elevada). El diámetro tricuspídeo es normal en la mitad de los casos, aproximadamente. En este contexto, encontramos habitualmente el tronco pulmonar, así como su bifurcación de tamaño normal.
Un 10% de los pacientes presentan anomalías coronarias, tales como fístulas, estenosis o sinusoides. En algunas situaciones, la perfusión coronaria depende de la presión elevada en el ventrículo derecho (quedando comprometida ante maniobras que descompriman dicha cavidad).
¿Por dónde llega la sangre a las ramas pulmonares en la atresia pulmonar? Lógicamente, a través del ductus. Por tal motivo, es necesaria la administración de prostaglandinas para mantener su permeabilidad en neonatos.
¿Qué factores pronósticos definimos a medio-largo plazo? El tamaño y la función del ventrículo derecho determinarán el pronóstico de esta cardiopatía. La válvula tricúspide, como indicador del ventrículo derecho (Z score) nos servirá para tomar decisiones sobre la actitud futura.
Tratamiento en un primer tiempo quirúrgicoEl objetivo es garantizar el aporte de sangre a las ramas pulmonares, previo manejo con prostaglandinas (circulación pulmonar dependiente del ductus).
Históricamente, se han descrito diversas técnicas quirúrgicas, con o sin circulación extracorpórea, promoviendo el flujo anterógrado o retrógrado, etc. Desde los años 90, y con el advenimiento de la cardiología intervencionista, han proliferado los abordajes en hemodinámica (tabla 1).
Promover tratamientos que mejoren el flujo anterógrado (apertura de la válvula pulmonar) facilita el crecimiento del ventrículo derecho y disminuye la presión suprasistémica del ventrículo derecho. Son, teóricamente, los adecuados. Por el contrario, las técnicas que mantienen la circulación pulmonar por vía retrógrada no promueven el crecimiento del ventrículo derecho («no flow, no growth») ni disminuyen la presión suprasistémica (sin embargo, resultan interesantes en los raros casos que asocian anomalías coronarias en los que no hay que «descomprimir» el ventrículo derecho, dada la dependencia de la perfusión coronaria de este).
El empleo de cada una de estas técnicas (quirúrgicas o percutáneas) va a depender de la presentación clínica inicial del paciente. De esta forma, en el neonato sintomático se realizarán inicialmente técnicas paliativas con el objetivo de mantener un flujo pulmonar adecuado, para poder plantear una reparación «definitiva» en un segundo tiempo, tal como describimos posteriormente.
Valvulotomía pulmonar quirúrgicaConsiste en la ampliación del orificio pulmonar a través del infundíbulo (Brock) o de la arteria pulmonar (mediante la oclusión de cavas o «inflow occlusion technique»). Son procedimientos sin circulación extracorpórea, que consiguen incidir (valvulotomía) o extirpar (valvulectomía) la válvula pulmonar. No se manipulan el ductus ni la comunicación interauricular (CIA), que sirven de rescate si el procedimiento no resulta eficaz. Aunque se amplía el diámetro de la válvula, no se actúa sobre el infundíbulo.
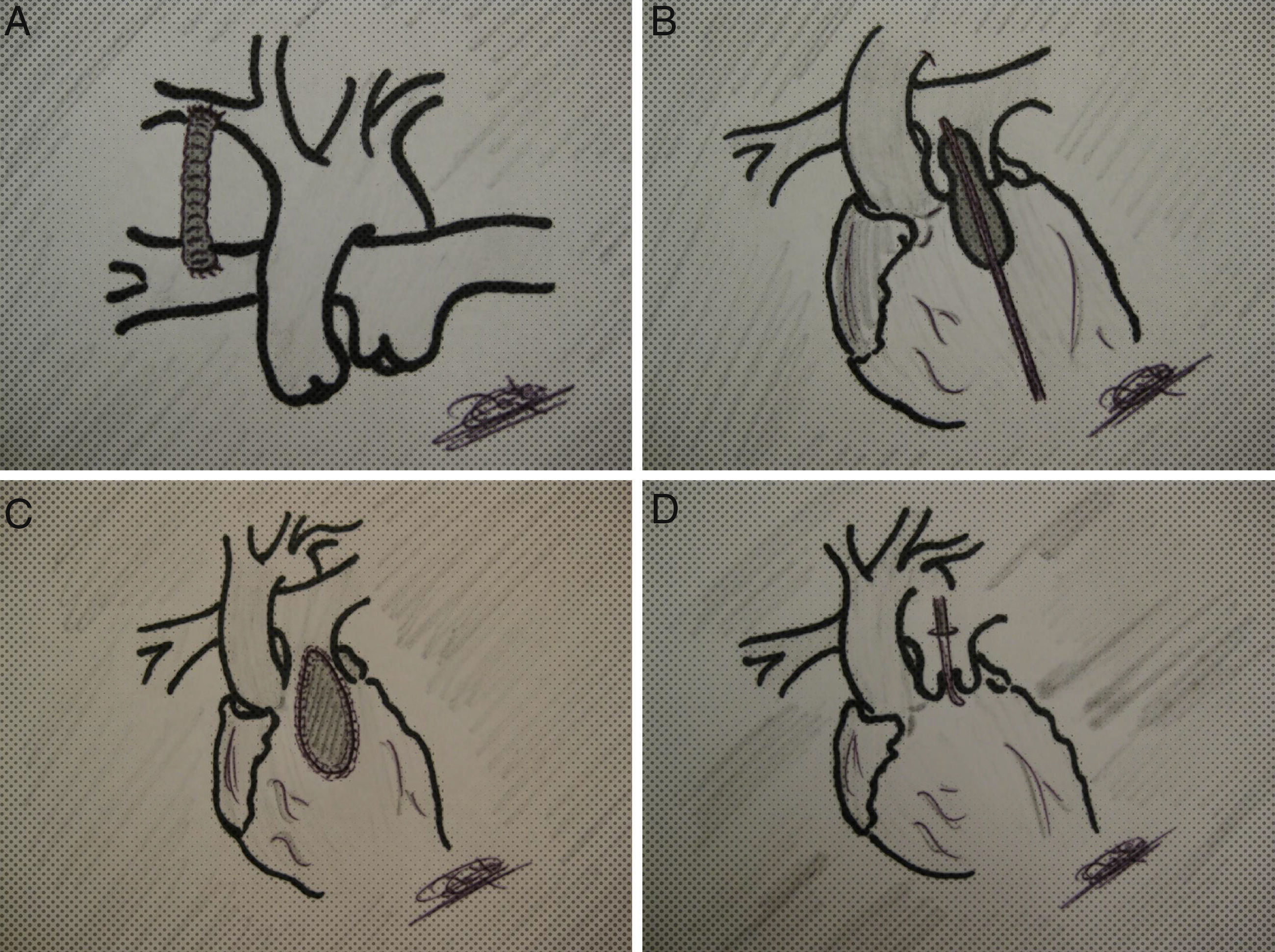
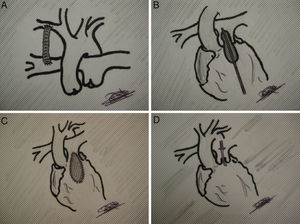
Parche transanularEn circulación extracorpórea, y de manera similar a la corrección en un Fallot, se amplían la arteria, el anillo y el infundíbulo para cubrirlos posteriormente con un parche (fig. 1). Al aliviar eficazmente el infundíbulo, disminuye la poscarga y se promueve el crecimiento del ventrículo derecho (a expensas de una insuficiencia pulmonar libre).
Fístula sistémico-pulmonarBlalock-Taussig modificado (con tubo de goretex). Bien por toracotomía (habitualmente derecha) o esternotomía. En este último caso, si se prevé asociarlo a otra técnica.
Procedimientos percutáneosPueden facilitar el flujo anterógrado, como la valvuloplastia pulmonar (el más habitual) o la implantación de un stent en el infundíbulo, o bien mantener la circulación dependiente del ductus con stents ductales. No es infrecuente la asociación de varios procedimientos en una misma sesión.
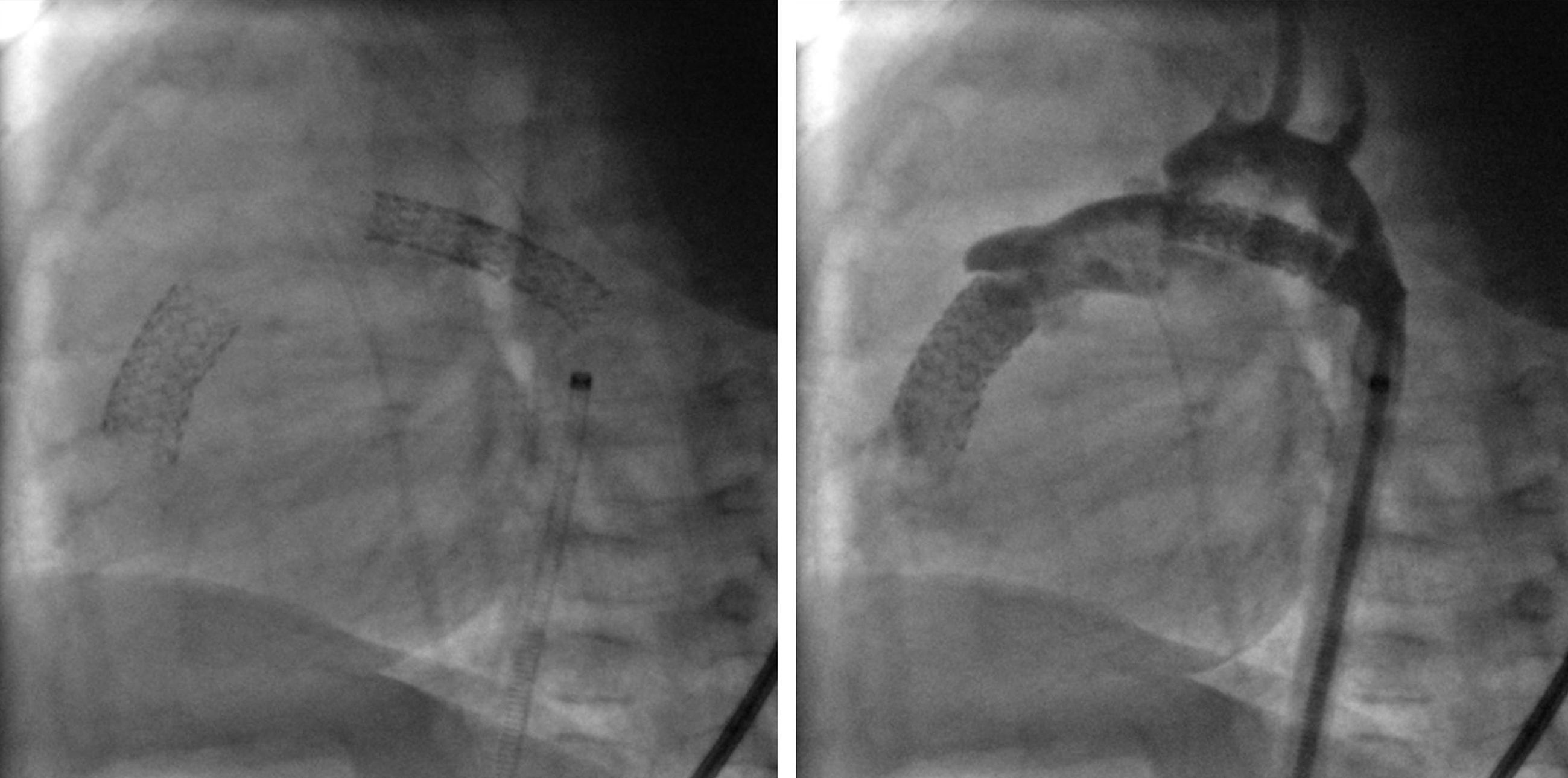
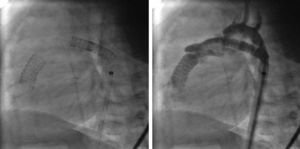
En ocasiones, una sola técnica no es suficiente para resolver el problema. La fisiopatología del ventrículo derecho con poscarga elevada, una vez que resulta descomprimido, presenta disfunción diastólica en grado variable. No es raro que, a pesar de una correcta técnica, se precise asociar otro procedimiento al inicial. Así nos podemos encontrar con niños que requieren una valvulotomía quirúrgica más fístula, o un stent ductal más stent infundibular (fig. 2), etc. El terreno está abonado para la colaboración entre cirugía y hemodinámica en uno o varios tiempos, incluyendo procedimientos híbridos.
Tratamiento en un segundo tiempo quirúrgicoSi el pronóstico depende del crecimiento del ventrículo derecho, la estrategia se basa en el valor del anillo tricúspide (Z score).
- –
La morfología del ventrículo derecho puede ser uni, bi o tripartita (si ha desarrollado correctamente tracto de entrada, ápex y tracto de salida).
- –
El tamaño de la tricúspide, medido por el Z score, actúa como parámetro del tamaño ventricular.
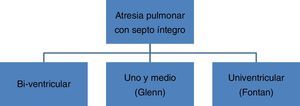
Un ventrículo derecho correctamente formado (tripartito), con un Z score normal, puede soportar una fisiología biventricular. Por el contrario, ventrículos pequeños (uni o bipartitos), con valores Z muy reducidos (menores de –4) o con circulación coronaria dependiente del ventrículo derecho se orientan hacia fisiología univentricular o incluso al trasplante en casos de alto riesgo.
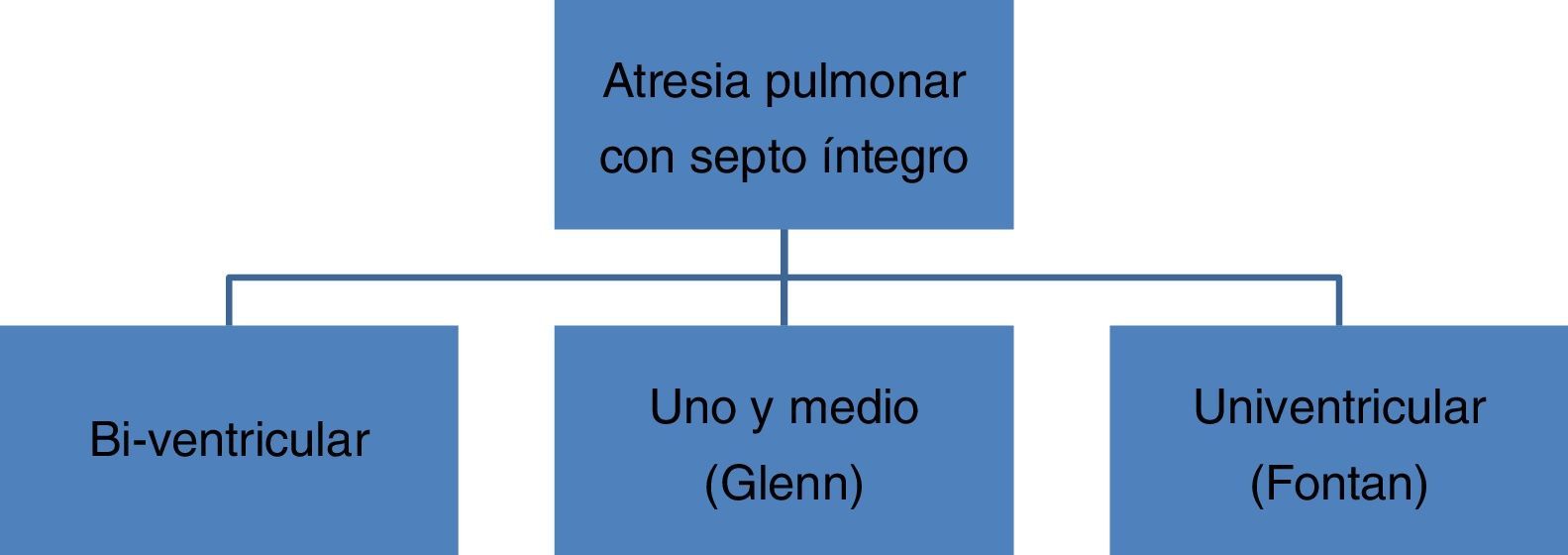
Cabe preguntarse por aquellos casos intermedios, con ventrículos de tamaño moderadamente reducido (no hipoplásicos, realmente) y valores Z intermedios (entre –1 y –4). En esta situación, se plantea una solución intermedia denominada uno-y-medio, realizando un Glenn bidireccional, de manera que el ventrículo pequeño maneje menor precarga. En cualquier caso, se trata del mismo paso que en la vía hacia Fontan (fig. 3).
En función del procedimiento paliativo inicial, es necesario asociar otras técnicas a la hora de realizar el Glenn bidireccional: desmontaje de fístula, ligadura de stent en ductus, retirada de stent en tracto de salida derecho, reconstrucción de infundíbulo, etc.
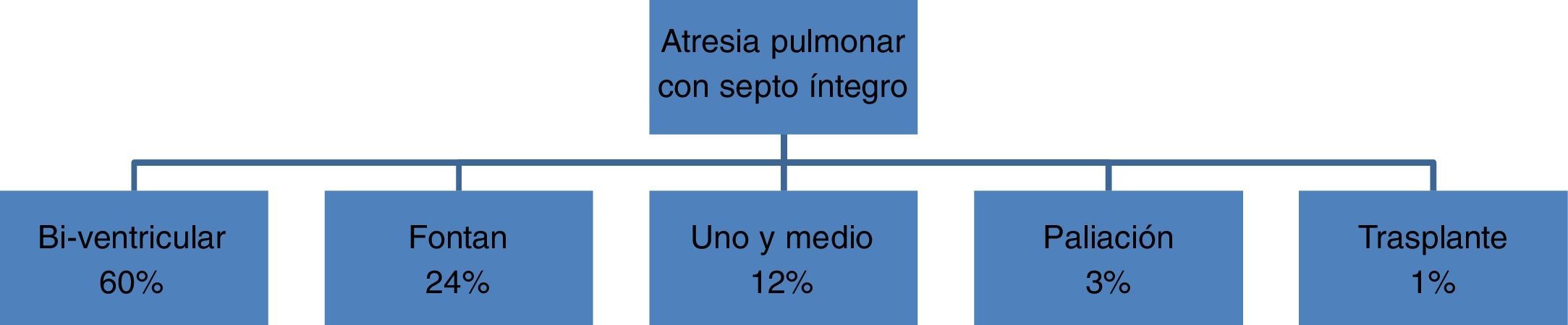
Un estudio multicéntrico reciente muestra el porcentaje de casos que finalmente alcanza la corrección biventricular. La cifra llega al 60%, frente un 24% que terminan en Fontan y un 12% como uno-y-medio. El 4% restante (probablemente, casos con anomalías coronarias) queda en una situación intermedia de paliación o termina en trasplante (fig. 4).
Aunque la tendencia actual favorece la corrección biventricular en la atresia pulmonar con septo íntegro, debemos evitar este sesgo en casos límite (Z score entre –1 y –4). Cabe el riesgo de comprometer la clase funcional y la tolerancia al ejercicio si forzamos la vía biventricular en dichas situaciones, en las que parece sensato optar por el uno-y-medio o incluso Fontan, finalmente. La posibilidad de crecimiento del ventrículo derecho debe ser valorada comparando el Z score del nacimiento (paliación inicial) con el de la cirugía posterior. En otras palabras, el Z score inicial nos orienta sobre el procedimiento inicial, pero no es determinante sobre el futuro del paciente.
Conclusiones- 1
La atresia pulmonar con septo íntegro presenta un amplio espectro, definido principalmente por los tamaños del ventrículo derecho y la válvula tricúspide.
- 2
En el periodo neonatal, debemos garantizar el flujo pulmonar, bien de manera anterógrada o retrógrada, por vía percutánea o quirúrgica.
- 3
Los parámetros de crecimiento ventricular y Z score tricúspide marcarán el tipo de corrección futura, preferiblemente biventricular. En casos límite, es preferible la solución univentricular o uno-y-medio.
Los autores declaran no tener ningún conflicto de intereses.