El recuperador celular es una alternativa a las transfusiones sanguíneas según la evidencia existente. Sin embargo no existe evidencia a la cual determinen el momento de la reinfusión de glóbulos rojos en consonancia con las transfusiones. Nuestro objetivo fue analizar las pruebas sobre la eficacia del recuperador celular para reducir las transfusiones sanguíneas.
MétodosEnsayo clínico aleatorizado con 91 pacientes en grupo no expuesto (donde la reinfusión de sangre autóloga con el recuperador celular se realizó al finalizar la cirugía) y 80 pacientes del grupo expuesto (donde la reinfusión de sangre autóloga se realizó de forma continua durante la cirugía). Se recogieron variables en tres momentos (preoperatorio, intraoperatorio y postoperatorio).
ResultadosTanto la hemoglobina como el hematocrito fueron inferiores en el grupo no expuesto al ser comparados con el grupo expuesto, tanto durante como después de la cirugía (p = 0,011 y 0,018, respectivamente). Así mismo, las transfusiones sanguíneas fueron mayores en el grupo no expuesto tanto durante, como después de la cirugía (p = 0,001).
ConclusionesCon el fin de reducir al máximo la tasa transfusional de los pacientes cardíacos, el momento óptimo donde reinfundir sangre autóloga procedente del recuperador celular debería ser durante la cirugía, según un protocolo de reinfusión continua.
The cell saver is an alternative to blood transfusions according to the existing evidence. However, there is no evidence to determine the time of reinfusion of red blood cells in line with transfusions. Our objective was to analyze the evidence on the effectiveness of the cell saver to reduce blood transfusions.
MethodsRandomized clinical trial with 91 patients in a non-exposed group (reinfusion of autologous blood with the cell saver was performed at the end of surgery) and 80 patients exposed group (reinfusion of autologous blood was performed continuously during surgery). Variables were collected at three moments (preoperative, intraoperative and postoperative).
ResultsBoth haemoglobin and haematocrit were lower in the unexposed group when compared to the exposed group, both during after surgery (p=.011 and.018, respectively), and blood transfusions were higher in the unexposed group both during, and after surgery (p=.001).
ConclusionsIn order to reduce the transfusion rate of cardiac patients as much as possible, the optimal time to reinfuse autologous blood from the cell saver should be during the surgery, according to a continuous reinfusion protocol.
La cirugía cardíaca se asocia con un alto consumo de productos sanguíneos homólogos y debido a los riesgos conocidos de estos productos existe interés en usar alternativas a las transfusiones sanguíneas1, como el recuperador celular (RC) un dispositivo electrónico que recupera pérdidas sanguíneas del campo operatorio para su posterior reinfusión en el paciente. La evidencia científica sostiene los beneficios de utilizar el RC2, pero las guías de administración de sangre recientemente publicadas no dan una dirección inequívoca sobre su uso3 ya que las tasas de transfusiones sanguíneas en cirugía cardíaca siguen siendo altas a pesar de los avances del RC. Varios estudios exponen que el RC carece de orientación clara y falta de evidencia de alta calidad sobre su uso4,5. Las variaciones en los detalles de cómo se usa el RC, incluyendo el equipo específico elegido y el consenso sobre el enfoque óptimo para el rescate celular sería útil3. La reinfusión de sangre autóloga procedente del RC puede realizarse durante o después (mayormente realizado) de la cirugía según necesidad6, aunque los datos disponibles difieren en determinar el momento adecuado para su reinfusión a tenor de los resultados expuestos7. La reinfusión de sangre autóloga al finalizar la intervención quirúrgica no ha demostrado ser beneficiosa para reducir los requerimientos de transfusión sanguínea8. En otras cirugías, informan de la decisión de no reinfundir sangre recolectada con el RC durante la intervención debido al aumento de la falciformes tras el procesamiento de la sangre9. Sin embargo, un reciente metaanálisis indica que los ensayos en torno al RC presentan déficit metodológico al no estar cegado, el ocultamiento de la asignación al tratamiento fue inadecuado y las prácticas de transfusión pueden haber estado influidas por el conocimiento del estado del tratamiento del paciente, lo que puede sesgar los resultados y favorecer el RC6. Por ello, nos marcamos como objetivo analizar las pruebas sobre la eficacia del recuperador celular para reducir las transfusiones sanguíneas. Se planteó la hipótesis de que reinfundir sangre autóloga con el recuperador celular en el periodo intraoperatorio en el paciente de cirugía cardíaca, disminuye las tasas de transfusiones sanguíneas.
MétodosEnsayo clínico aleatorizado con la participación de pacientes programados para cualquier procedimiento de cirugía cardíaca (válvula aórtica, mitral, tricúspide y coronaria) con uso del circuito extracorpóreo y del recuperador celular Continuos Autologous Autotransfusion System, Fresenius (C.A.T.S®) (en periodo comprendido del 1 de enero a 1 de julio del año 2017.
PacientesLa asignación de la muestra fue de forma intencionada mediante un muestreo aleatorizado sistematizado, donde el primer paciente se asignó al grupo «A», denominado grupo no expuesto, donde se recuperaba las pérdidas sanguíneas con el RC del campo operatorio y que, tras el procesamiento, los glóbulos rojos obtenidos se reinfundían al paciente al finalizar la cirugía, mientras que el segundo paciente se asignó al grupo «B», denominado grupo expuesto, donde se recuperaba las pérdidas sanguíneas con el RC del campo operatorio y que, tras el procesamiento, los glóbulos rojos obtenidos se reinfundían al paciente de forma continua durante la cirugía. La secuencia aleatoria, reclusión y asignación de los pacientes en ambos grupos fue realizado por el investigador principal. Se incluyeron a los pacientes con edad igual o superior a 18 años, programados para cirugía cardíaca bajo un circuito extracorpóreo donde los procedimientos y controles realizados en los pacientes se llevaron a cabo después de recibir su consentimiento informado. Por el contrario, se excluyeron aquellos pacientes con transfusiones sanguíneas doce h prevías a la cirugía y con trastornos de la sangre (anemia o alteraciones de coagulación, entre otros) que requieran transfusiones sanguíneas previo al comienzo de la cirugía porque podrían provocar sesgo en la recogida de datos y enmascarar los resultados. Además, de pacientes incapaces de comunicarse en lengua española e inglesa o que no hayan firmado el consentimiento informado. Todos los datos se recogieron en el servicio de cirugía cardíaca y unidad de cuidados intensivos (UCI) del hospital. En todo momento se informó al paciente de forma verbal y por escrito de las características propias del estudio que tras aclaración de las dudas que pudieran surgir aceptaron y firmando el consentimiento informado. El tratamiento, comunicación y cesión de los datos del paciente se realizó conforme a lo dispuesto por la Ley Orgánica 15/1999, de 13 de diciembre, de protección de datos de carácter personal, además de obtener el informe favorable para la realización del estudio por el Comité de Ética de la Investigación del hospital. En ambos grupos se realizó una preparación quirúrgica de forma convencional bajo el mismo régimen estandarizado de anestesia general (inducción, mantenimiento y recuperación) con similares fármacos intravenosos adecuado a su peso y características propias de cada paciente. El abordaje quirúrgico fue similar en todos los casos, a través de esternotomía media longitudinal se accede al corazón que tras administrar dosis de heparina sódica en aurícula derecha (2mg/kg) y con tiempos de coagulación activada superior a 200 segundos se procedió a canular los grandes vasos para establecer la derivación cardiopulmonar con la máquina extracorpórea. Se indujo un paro cardiopléjico no hemático por agentes farmacológicos y suero frío para detener los movimientos del corazón donde poder realizar el procedimiento quirúrgico programado. La preservación miocárdica inducida se utilizó con solución cristaloide hiperkalémica (cardioplejía) de duración intermitente cuya ruta de infusión fue de forma anterógrada o retrógada a juicio del propio cirujano principal. Para la salida de la derivación cardiopulmonar se revirtió los efectos anticoagulantes de la heparina con sulfato de protamina a razón de 1:1. La recuperación de pérdidas sanguíneas del campo operatorio se realizó en el periodo intraoperatorio de forma similar, mediante el aspirador seno de la máquina extracorpórea (durante la derivación cardiopulmonar) cuyo volumen retornaba a la máquina y se reinfundía a través de las canulaciones. Aspirador de calle conectado a un sistema de vacío bajo presión negativa de 20cm H2O cuyo volumen se desechaba, y aspirador de doble luz del RC (atendiendo a los grupos seleccionados).
La preparación y uso del RC fue homogéneo en todos los pacientes de ambos grupos. Para el cebado y purgado del circuito se utilizó 3000ml de solución salina al 0,9% mezclado con 30.000 UI de heparina sódica. El aspirador de doble luz recuperó las pérdidas sanguíneas del campo operatorio mediante un vacío aspirativo regulable a –20cm H2O donde pasaron por un filtro de 25μm hacia un reservorio. Tras una orden manual se realizó el procesamiento de la sangre recuperada (separar los hematíes de los demás elementos formes de la sangre) a razón de 2000rpm bajo el programa de lavado de alta calidad. Tras el procesamiento se obtuvo en una bolsa de reinfusión solo los glóbulos rojos que se reinfundieron en el grupo no expuesto, al final de la cirugía. Y en el grupo expuesto durante la cirugía de forma continua.
Tras comprobar la hemostasia de las suturas intracardíacas y grandes vasos se procedió al cierre esternal con monofilamento de acero inoxidable y se procedió a la extubación del paciente para su posterior traslado a UCI con los pertinentes dispositivos de traslado. Durante el postoperatorio se administró en ambos grupos el mismo protocolo de transfusión sanguínea estandarizado para nuestro servicio. Quien realizó los procedimientos quirúrgicos durante el periodo de nuestro estudio fueron los mismos cirujanos cardiovasculares (dos) y el mismo médico residente cardiovascular (uno), con los mismos preparativos e idénticas técnicas quirúrgicas empleadas. Quien realizó la práctica del cebado del RC fue la misma enfermera perfusionista para todos los pacientes.
Las variables de estudios se distribuyeron en tres periodos: preoperatorio, sexo (género), edad (años), peso total (kg), procedimiento quirúrgico programado (valvular aórtico, tricúspide, mitral y coronario), antedecentes patológicos previos (hematológicos, respiratorio, digestivos, traumatológicos, torácico, psiquiátrico, ginecológicos, entre dos y tres patologías previas, entre cuatro y cinco patologías previas, más de cinco patologías previas. Todas ellas están descrita en los antecedentes patológicos previos) y cifras de hemoglobina (g/dl), hematocrito (%), plaquetas (103/uL) y proteínas totales (g/dl) antes de entrar el paciente en quirófano a través de su historia clínica digitalizada. Intraoperatorio, tiempo de cirugía (minutos), hemoglobina (g/dl), hematocrito (%), plaquetas (103/uL), proteínas totales (g/dl), transfusiones sanguíneas (sangre homóloga, plaquetas, factores de coagulación y plasma). Variables del recuperador celular tales como volumen en reservorio (ml), volumen de hematíes (ml), volumen de desecho (ml) y tiempo de procesado (minutos). Todas las variables en este periodo se recogieron al finalizar la cirugía programada y antes de reinfundir los hematíes procedentes del recuperador celular (excepto en el grupo expuesto) mediante la hoja de datos ad hoc. Postoperatorio, hemoglobina (g/dl), hematocrito (%), plaquetas (103/uL), proteínas totales (g/dl), transfusiones sanguíneas (sangre homóloga, plaquetas, factores de coagulación y plasma) además de hemorragias (respuesta dicotómica) durante las primeras 24 h del postoperatorio, teniendo como referencia la definición de hemorragia como la pérdida hemática del paciente en una hora > 400ml de sangre, en 2-3 h > 300ml/h, o en 4 h > 200ml/h10. Todas las variables del postoperatorio se recogieron a través de la historia clínica digitalizada.
Para la estimación del cálculo muestral se realizó un estudio piloto porque la escasa evidencia bibliográfica sobre el momento de uso del RC presenta deficiencia metodológica, pudiendo interferir en los resultados6. Del estudio previo se desprendió que los pacientes fueron transfundidos «durante» y «después» del uso del RC, por lo que la exposición se consideró un factor de riesgo, si al menos presentaba una transfusión sanguínea (riesgo relativo) con un nivel de significación del 5% y una potencia estadística de al menos el 80%. Usando una razón de un expuesto por cada no expuesto. Se usó el programa Epidat para poder calcular la «n» de cada grupo.
Los análisis estadísticos utilizados se expresaron mediante frecuencia absolutas o relativas, porcentaje (%), medias de tendencia central (media) y desviación estándar (DE), según correspondiera. Las variables categóricas fueron comparadas mediante el test de Chi-cuadrado y las continuas mediante el test t de Student. Se consideró significativo un valor p inferior a 0,05.
ResultadosDe los 237 pacientes programados para cirugía cardíaca bajo un circuito extracorpóreo, se incluyó a 171 pacientes (72,1%). Los 66 pacientes (27,9%) excluidos lo hicieron por razones diversas: a 15 pacientes (6,3%) se les trasfundió durante las doce h previas a la cirugía, 21 pacientes (8,9%) presentaban trastornos de coagulación y 30 pacientes (12,7%) no firmaron el consentimiento informado.
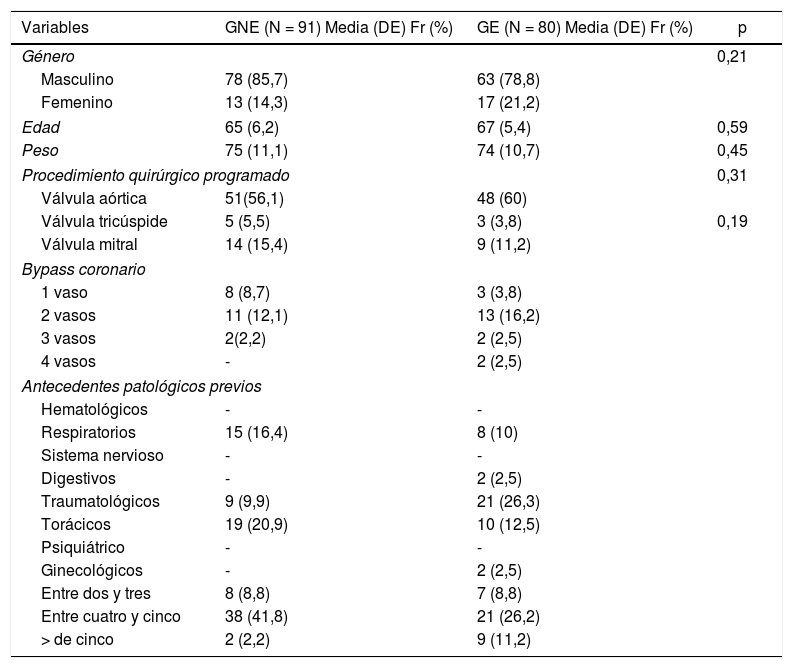
El grupo no expuesto con 91 pacientes (38,4%) se reinfundió sangre autóloga con el RC al finalizar la cirugía, mientras que al grupo expuesto con 80 pacientes (33,7%) se le reinfundió de forma continua durante la cirugía. En ambos grupos presentaron la siguiente caracterización conforme a la tabla 1.
Caracterización de los pacientes incluidos en el estudio
| Variables | GNE (N = 91) Media (DE) Fr (%) | GE (N = 80) Media (DE) Fr (%) | p |
|---|---|---|---|
| Género | 0,21 | ||
| Masculino | 78 (85,7) | 63 (78,8) | |
| Femenino | 13 (14,3) | 17 (21,2) | |
| Edad | 65 (6,2) | 67 (5,4) | 0,59 |
| Peso | 75 (11,1) | 74 (10,7) | 0,45 |
| Procedimiento quirúrgico programado | 0,31 | ||
| Válvula aórtica | 51(56,1) | 48 (60) | |
| Válvula tricúspide | 5 (5,5) | 3 (3,8) | 0,19 |
| Válvula mitral | 14 (15,4) | 9 (11,2) | |
| Bypass coronario | |||
| 1 vaso | 8 (8,7) | 3 (3,8) | |
| 2 vasos | 11 (12,1) | 13 (16,2) | |
| 3 vasos | 2(2,2) | 2 (2,5) | |
| 4 vasos | - | 2 (2,5) | |
| Antecedentes patológicos previos | |||
| Hematológicos | - | - | |
| Respiratorios | 15 (16,4) | 8 (10) | |
| Sistema nervioso | - | - | |
| Digestivos | - | 2 (2,5) | |
| Traumatológicos | 9 (9,9) | 21 (26,3) | |
| Torácicos | 19 (20,9) | 10 (12,5) | |
| Psiquiátrico | - | - | |
| Ginecológicos | - | 2 (2,5) | |
| Entre dos y tres | 8 (8,8) | 7 (8,8) | |
| Entre cuatro y cinco | 38 (41,8) | 21 (26,2) | |
| > de cinco | 2 (2,2) | 9 (11,2) | |
Fr (%): frecuencias absolutas (porcentajes); GE: grupo expuesto; GNE: grupo no expuesto; Media (DE): media de tendencia central (desviación estándar).
Existen diferencias estadísticamente significativas entre los grupos con valores de p < 0,05.
La media del tiempo de cirugía en el grupo no expuesto (aórtico 61 ± 30 min, mitral 81 ± 41 min, tricúspide 82 ± 29 min, coronario 101 ± 39 min) y el grupo expuesto (aórtico 58 ± 28 min, mitral 78 ± 49 min, tricúspide 77 ± 25 min, coronario 105 ± 27 min) fueron similares (p=0,46). Así mismo, la media de los datos en el recuperador celular fueron semejantes tanto en el grupo no expuesto (volumen en reservorio 1248ml, volumen de hematíes 530ml, volumen de desecho 5631ml y tiempo de procesado 18 min) como en el grupo expuesto (volumen en reservorio 1359ml, volumen de hematíes 581ml, volumen de desecho 5816ml y tiempo de procesado 23 min) (p=0,21).
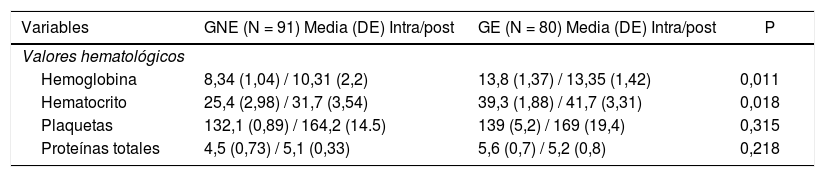
Respecto a la media de los valores hematológicos en el periodo preoperatorio, no presentaron diferencias estadísticamente significativas entre el grupo expuesto y grupo no expuesto respectivamente. Hb: 12,9 g/dl- 12,2 g/dl (p = 0,213), Htco: 38,5% - 37,8% (p = 0,173), plaquetas: 214 103/uL-210 103/uL (p = 0,261), proteína totales: 7,6 g/DL – 7,1 g/DL (p = 0,272).
Sin embargo, en el grupo expuesto presentó mayores cifras de hemoglobina y hematocrito a la finalización de la cirugía (13,8 g/dl – 39,3%) y durante las primeras 24 h del postoperatorio (13,35 g/dl – 41,7%) respecto al grupo no expuesto conforme a la tabla 2.
Valores hematológicos de los pacientes incluidos en el estudio
| Variables | GNE (N = 91) Media (DE) Intra/post | GE (N = 80) Media (DE) Intra/post | P |
|---|---|---|---|
| Valores hematológicos | |||
| Hemoglobina | 8,34 (1,04) / 10,31 (2,2) | 13,8 (1,37) / 13,35 (1,42) | 0,011 |
| Hematocrito | 25,4 (2,98) / 31,7 (3,54) | 39,3 (1,88) / 41,7 (3,31) | 0,018 |
| Plaquetas | 132,1 (0,89) / 164,2 (14.5) | 139 (5,2) / 169 (19,4) | 0,315 |
| Proteínas totales | 4,5 (0,73) / 5,1 (0,33) | 5,6 (0,7) / 5,2 (0,8) | 0,218 |
GE: grupo expuesto; GNE: grupo no expuesto; Intra: intraquirúrgica (a la finalización de la cirugía programada); Media (DE): media aritmética (desviación estándar); Post: postoperatorio (24 h después de la cirugía).
Existieron diferencias estadísticamente significativas entre los grupos con valores de p < 0,05.
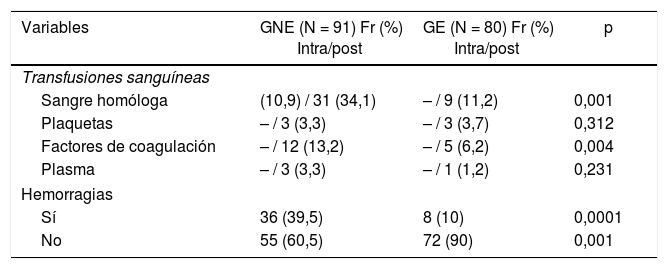
En cuanto a las transfusiones sanguíneas el grupo no expuesto presentaron mayores porcentajes de pacientes transfundidos, existiendo diferencias estadísticamente significativas de la sangre homóloga (grupo no expuesto 34,1% - grupo expuesto 11,2%) y de los factores de coagulación (grupo no expuesto 13,2% - grupo expuesto 6,2%). Además, los episodios de hemorragias fueron mayores en el grupo no expuesto (39,5%) que en el grupo expuesto (10%) conforme a la tabla 3.
Transfusiones sanguíneas y hemorragias de los pacientes incluidos en el estudio
| Variables | GNE (N = 91) Fr (%) Intra/post | GE (N = 80) Fr (%) Intra/post | p |
|---|---|---|---|
| Transfusiones sanguíneas | |||
| Sangre homóloga | (10,9) / 31 (34,1) | – / 9 (11,2) | 0,001 |
| Plaquetas | – / 3 (3,3) | – / 3 (3,7) | 0,312 |
| Factores de coagulación | – / 12 (13,2) | – / 5 (6,2) | 0,004 |
| Plasma | – / 3 (3,3) | – / 1 (1,2) | 0,231 |
| Hemorragias | |||
| Sí | 36 (39,5) | 8 (10) | 0,0001 |
| No | 55 (60,5) | 72 (90) | 0,001 |
Fr(%): frecuencia (porcentajes); GE: grupo expuesto; GNE: grupo no expuesto; Hemorragias: hemorragias en el postoperatorio; Intra: intraquirúrgica (a la finalización de la cirugía programada); Post: postoperatorio (24 h después de la cirugía).
Existieron diferencias estadísticamente significativas entre los grupos con valores de p < 0,05.
Este estudio permite comparar el momento adecuado de reinfusión de sangre autóloga procedente del recuperador celular en respuesta a las transfusiones sanguíneas del paciente sometido a cirugía cardíaca, ya que existen estudios con déficit metodológico que la determinen6. Los resultados principales obtenidos ponen en relieve una considerable disminución de la tasa transfusional cuando la reinfusión se realiza durante la intervención quirúrgica. Su justificación se debe a la disposición continua de sangre autológa que compensa el descenso de hemoglobina y hematocrito que provoca la derivación cardiopulmonar y la cirugía en sí, evitando en la mayor parte de que se proceda a una transfusión sanguínea.
En las recientes Guías de práctica clínica para la conservación de sangre11 comparan los efectos clínicos de la infusión del RC durante y después de su uso, pero no informan de las tasas de transfusiones sanguíneas derivadas de su utilización.
Quien sí la informaron, en la Conferencia the International Society for Minimally Invasive Cardiothoracic Surgery (ISMICS)12 fueron quienes evaluaron pruebas de eficacia en la reducción de la transfusiones sanguíneas en el contexto de la cirugía cardíaca, donde recomiendan que el RC debe ser utilizado durante toda la operación (Clase IIa, Nivel A). Sin embargo, no exponen los resultados de la tasa transfusional en el caso de utilizarlo al finalizar la cirugía. El estudio de Rubens13 sugirió que el uso del RC dio lugar a una mayor tasa de transfusiones sanguíneas. Los mismos resultados exponen otros estudios14,15. Sin embargo, no aclararon el papel (momento) del uso del RC en los resultados de la transfusión. Cabe destacar, la existencia de estudios recientes como los de Xie16, quien concluye que el momento de la infusión de sangre autóloga es en el intraoperatorio, por la eficacia, seguridad y rentabilidad en los países desarrollados, pero no lo recomienda en su país natal, China, quien no reporta la justificación del mismo, tasas de respuestas sobre transfusiones sanguíneas ni tampoco comparación con la infusión al finalizar la cirugía.
Además, Vonk et al.17 implementaron el uso del RC en todas las cirugías cardíacas, recomendando su uso durante la intervención quirúrgica, ya que reduce la tasa transfusional. Pero no pudieron recomendar la infusión de la sangre autóloga al finalizar la cirugía porque no la estudiaron, por lo que las afirmaciones están fundadas en un momento concreto. El estudio de Teker18 destaca que la sangre del propio paciente se utiliza y el RC es una buena alternativa para la transfusión sanguínea, e incluso recomienda su uso en cirugías de urgencia al proporcionar comodidad y confianza al cirujano. Sin embargo, no determinan el momento óptimo de su uso en base a la tasa transfusional. Recientes datos recogidos en el International Consortium for Evidence Based Perfusion pilot Registry indican que todos los servicios de cirugía cardíaca deben usar el RC, sin embargo la variación entre los dispositivos y operadores introduce complejidad en la evaluación de la literatura sobre los beneficios y los riesgos del momento de uso3. Esto no siempre está claramente descrito en la bibliografía, pero los metaanálisis recientes sugieren que el momento en que se utiliza el rescate celular es importante para la utilidad de la técnica19. En vista a nuestros resultados, el momento óptimo de reinfundir sangre autóloga procedente del RC es durante la cirugía ya que se ha demostrado que disminuye sustancialmente las transfusiones sanguíneas. En este momento, al paciente de cirugía cardíaca se le realizan procedimientos secundarios (hemodilución normovolémica, administración de fármacos, entre otros) al cual hace que disminuya las cifras de hemoglobina y hematocrito (responsable para optar por una transfusión de sangre homóloga), y gracias a la reinfusión estas cifras aumentan permitiendo alargar los tiempos de transfusiones o en su defecto evitarlo.
No obstante, alertamos que nuestro estudio presenta limitaciones en cuanto al tipo de aleatorización asignado (grupo A-expuesto y grupo B-no expuesto) ya que algún paciente que no se quiera incluir en uno de los grupos simplemente no se incluyen, pero cierto es, que la disminución de la tasa transfusional está en consonancia con el momento del uso del RC, al establecer una comparativa con el grupo que lo utiliza al finalizar la cirugía, por lo que la disminución de la tasa transfusional está fuertemente ligada a los riesgos derivados del mismo. Otra limitación que presenta este estudio, fue el volumen que rescata el aspirador de calle (volumen desechable), al cual no se recogió dichas pérdidas sanguíneas por estar mezclado con suero fisiológico, líquido pericárdico u otros fluidos que se vierten en el campo operatorio, y por tanto podría ser fuente de sesgo del volumen total de pérdidas sanguíneas del paciente durante el periodo intraoperatorio. De nuestra investigación existen implicaciones prácticas y para la investigación tras el uso del RC, porque el hecho de no reinfundir la sangre autóloga durante la cirugía motivará hacer uso de transfusiones sanguíneas durante el postoperatorio, en base a la evidencia clínica aportada. No hay necesidad de ensayos controlados aleatorios pequeños adicionales de rescate celular en la cirugía cardíaca. La principal necesidad es la realización de grandes ensayos comparativos, metodológicamente rigurosos para evaluar la eficacia relativa, la seguridad y el costo efectividad del rescate celular en diferentes procedimientos quirúrgicos6. Finalmente concluimos que, con el fin de reducir al máximo la tasa transfusional de los pacientes cardíacos, el momento óptimo donde reinfundir sangre autóloga procedente del recuperador celular debería ser durante la cirugía, según un protocolo de reinfusión continua.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Al estadístico por su dedicación y paciencia ante nuestra insistencia de hacer un buen estudio. A todos los profesionales que nos ayudan a crecer como persona.